Chronische Hepatitis-B- und Hepatitis-D-Virusinfektionen
Autorin:
Dr. Lisa Sandmann
Klinik für Gastroenterologie, Hepatologie und Endokrinologie
Medizinische Hochschule Hannover
E-Mail: sandmann.lisa@mh-hannover.de
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Sowohl die Hepatitis-B- als auch die Hepatitis-B/D-Koinfektion spielen eine entscheidende Rolle bei chronischen Lebererkrankungen. Trotz der Verfügbarkeit einer Impfung, antiviralen Therapien und der ständigen Weiterentwicklung neuer Substanzen stellen diese viralen Infektionen noch immer ein erhebliches weltweites Gesundheitsproblem dar.
Keypoints
-
Die HBV-Infektion zählt zu einer der häufigsten Ursachen von Leberzirrhose und hepatozellulärem Karzinom.
-
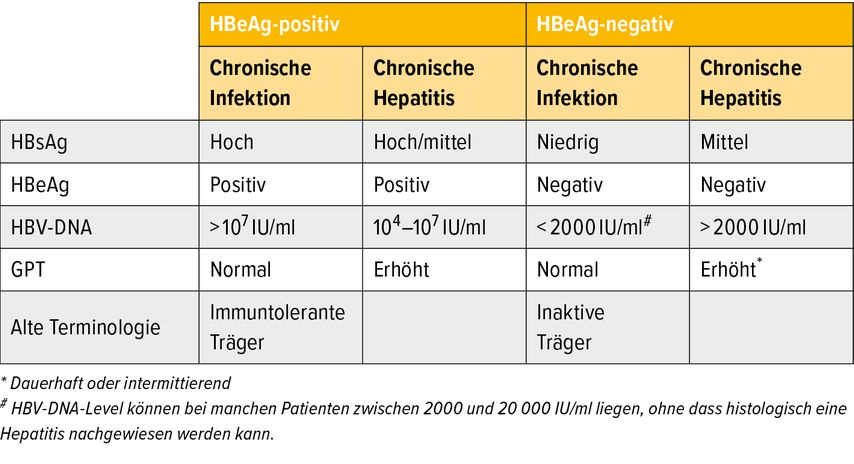
In der aktuellen Nomenklatur wird zwischen Infektion und Hepatitis sowie positivem oder negativem HBeAg-Nachweis unterschieden.
-
Therapieindikationen bestehen bei Patienten mit chronischer Hepatitis B (HBeAg- negativ und -positiv) und einer Viruslast >2000IU/ml, Patienten mit Leberzirrhose und nachweisbarer Viruslast sowie Patienten mit einem HCC und positiver HBV-DNA.
-
Das HCC-Risiko ist bei chronischer HBV-Infektion erhöht. Bei Patienten mit einem hohen HCC-Risiko sind HCC-Screenings alle 6 Monate erforderlich.
-
Vor Chemotherapie und immunsuppressiver Therapie muss eine HBV-Infektion ausgeschlossen werden. Eine Reaktivierung kann mittels antiviraler Prophylaxe verhindert werden.
-
Bei allen HBsAg-positiven Patienten sollte eine HDV-Koinfektion ausgeschlossen werden.
Die chronische Hepatitis-B-Virus(HBV)- Infektion undHBV/Hepatitis-D-Virus(HDV)-Koinfektion tragen wesentlich zur Morbidität und Mortalität chronischer Lebererkrankungen bei. Wichtig ist die Diagnose der Infektionen, insbesondere in Risikogruppen, sodass die Behandlungsindikation überprüft werden kann. Aktuelle Herausforderungen liegen in der Weiterentwicklung antiviraler Substanzen, sodass eine Heilung erreicht werden kann.
Chronische Hepatitis-B-Virusinfektion
Die chronische HBV-Infektion ist mit einer globalen Prävalenz von 250–340 Millionen trotz verfügbarer Impfung weiterhin ein weltweites Gesundheitsproblem und ist eine der häufigsten Ursachen von Leberzirrhose und hepatozellulärem Karzinom (HCC).1 Dieses Risiko kann durch den Einsatz antiviraler Medikamente reduziert werden, wobei hier entsprechend den aktuellen Leitlinienempfehlungen hochwirksame Substanzen mit hoher Resistenzbarriere eingesetzt werden sollen.2 Eine komplette Heilung ist aufgrund der in den Hepatozyten persistierenden HBV-cccDNA („covalently closed circular DNA“) sowie der in die hepatozelluläre DNA integrierten Virus-DNA mit den aktuell verfügbaren Therapien jedoch nicht möglich.
Terminologie und Therapieindikation
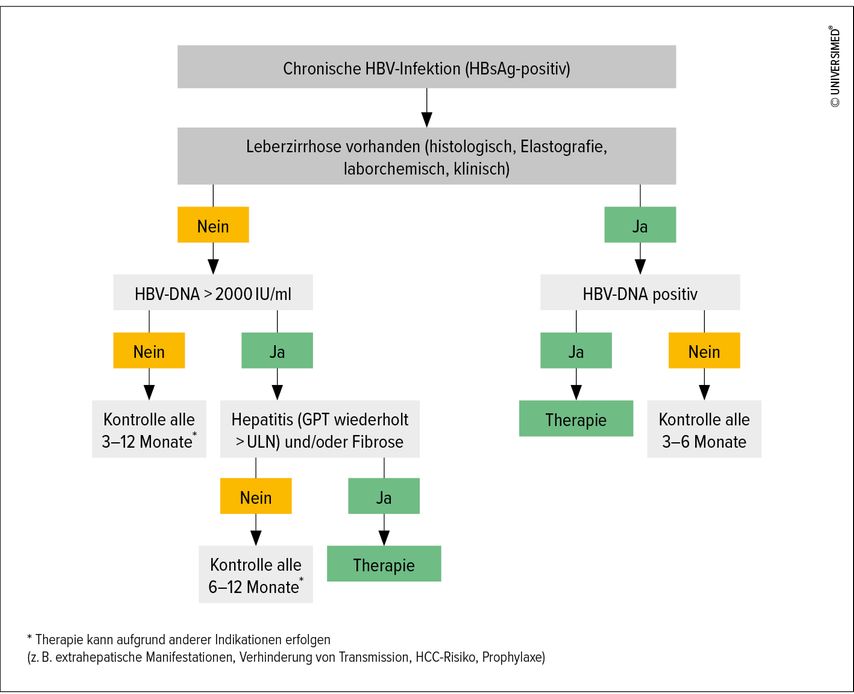
Aufgrund der Interaktion zwischen Virusreplikation und Immunsystem zeigt die chronische HBV-Infektion einen dynamischen Verlauf. Dieser lässt sich in verschiedene Phasen unterteilen, die sich nach HBeAg-Status, Viruslast, Transaminasenerhöhung und hepatischer Inflammation richten (Tab. 1).3 Die Einteilung ist relevant, da sich hieraus Therapieindikationen ableiten lassen. Diese beruhen auf der GPT-Aktivität im Serum, der Höhe der Viruslast und dem Entzündungs- und Fibrosestadium in der Elastografie oder Biopsie (Abb. 1). Sichere Therapieindikationen bestehen bei Patienten mit chronischer Hepatitis B (HBeAg-negativ und -positiv) und einer Viruslast >2000IU/ml, Patienten mit Leberzirrhose und nachweisbarer Viruslast sowie Patienten mit einem HCC und positiver HBV-DNA.2 Für weitere besondere Therapieindikationen verweisen wir auf die aktuellen Leitlinien der EASL sowie die deutsche Leitlinie der Deutschen Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS).2,3
Abb. 1: Therapieindikationen bei chronischer HBV-Infektion (modifiziert nach Cornberg M et al. 2021)2
Antivirale Therapie
Mit den aktuell verfügbaren Therapien können „partielle Heilung“ (HBsAg-Persistenz bei HBV-DNA-Suppression nach Ende der Therapie) und in seltenen Fällen „funktionelle Heilung“ (HBsAg-Verlust und HBV-DNA-Negativität nach Ende der Therapie) erreicht werden. Letztere geht gegenüber der partiellen Heilung mit einer Reduktion des HCC-Risikos einher. Zur antiviralen Behandlung stehen mit pegyliertem Interferon α (PEG-IFN-α) und Nukleos(t)id-Analoga (NA) aktuell zwei Substanzklassen zur Verfügung. Da es sich bei der Therapie mit pegyliertem IFN-α um eine zeitlich begrenzte Therapie von in der Regel 48 Wochen handelt, sollte laut aktuellen Leitlinien diese Therapiemöglichkeit bei Patienten überprüft werden. Prädiktive Faktoren für Therapieansprechen oder -versagen sollten vor und unter Therapie beachtet werden (s. aktuelle Leitlinie der DGVS). Bei Patienten mit dekompensierter Leberzirrhose ist diese Therapie kontraindiziert.
Bei der NA-Therapie sollen Entecavir (ETV), Tenofovirdisoproxilfumarat (TDF) oder Tenofoviralafenamid (TAF) aufgrund ihrer hohen Resistenzbarriere eingesetzt werden. Mit diesen Substanzen kann bei zuverlässiger und korrekter Einnahme in nahezu allen Fällen eine vollständige Virussuppression erreicht werden. Bei der Substanzauswahl sind Komorbiditäten und Vorbehandlungen zu beachten und Dosierungen müssen an die Nierenfunktion angepasst werden.2 Kontrovers wird weiterhin das möglicherweise unter ETV im Vergleich zu TDF erhöhte HCC-Risiko in bestimmten Subgruppen diskutiert.4–6 Unter bestimmten Voraussetzungen (anhaltender HBsAg-Verlust oder Serokonversion von HBeAg zu anti-HBe-Antikörper bei Patienten ohne Leberzirrhose nach einer Konsolidierungsphase von 12 Monaten) kann eine NA-Therapie beendet werden. Bei HBeAg-negativen Patienten ohne Leberzirrhose kann nach 3-jähriger HBV-DNA-Suppression auch bei fortbestehend nachweisbarem HBsAg ein Auslassversuch unternommen werden. Um eine Indikation zur Therapie-Wiederaufnahme im Falle eines Transaminasen- und HBV-DNA-Anstiegs nicht zu übersehen, sollten im ersten Jahr jedoch engmaschigere Kontrollen erfolgen.2,7Aufgrund des Risikos für eine hepatische Dekompensation im Falle einer Reaktivierung sollte bei Patienten mit Leberzirrhose ein Therapieauslass sehr kritisch hinterfragt werden und erst nach HBsAg-Verlust bzw. Serokonversion zu anti-HBs erfolgen.8
Neue Therapieansätze
Aktuell werden in mehreren Phase-I- und -II-Studien Substanzen mit unterschiedlichen Angriffspunkten im viralen Replikationszyklus untersucht. Ziel ist dabei das Erreichen einer „complete cure“ mit Verlust der HBV-cccDNA. Hierfür werden u.a. Eintrittsinhibitoren und HBsAg-Release-Inhibitoren, aber auch „small interfering(si)RNA“ und Nukleokapsid-Assembly-Modulatoren in aktuellen Studien untersucht. Mittels immunmodulatorischer Substanzen wird zudem die Wiederherstellung der HBV-spezifischen Immunantwort als Therapieansatz untersucht.9
Reaktivierung
Im Falle einer Immunsuppression ist bei positivem anti-HBc-Antikörpermit oder ohne nachweisbarem HBsAg eine potenziell lebensbedrohliche Reaktivierung möglich. Die Empfehlungen zur Prophylaxe sind dabei abhängig vom virologischen Status und Art der Immunsuppression und sind in der aktuellen Leitlinie aufgeführt.2 Wichtig ist, dass auch anti-HBc-positive, HBsAg-negative Patienten unter lokaler HCC-Therapie ein Reaktivierungsrisiko besitzen.10
Schwangerschaft
In der Schwangerschaft und Stillzeit ist eine antivirale Behandlung mit Tenofovir möglich. Um das Risiko für eine vertikale Transmission zu reduzieren und eine mögliche Therapieindikation zu erkennen, sollten alle Schwangeren rechtzeitig auf das Vorliegen einer HBV-Infektion untersucht werden. Eine Therapieindikation besteht bei einer Viruslast >200000IU/ml sowie entsprechend den generellen Empfehlungen zur antiviralen Behandlung (Abb.1). Das Übertragungsrisiko wird zudem durch die aktive und passive Immunisierung der Neugeborenen HBsAg-positiver Mütter innerhalb von 12 Stunden nach Geburt signifikant reduziert. Durch eine Sectio wird dieses Risiko bei einer mütterlichen Viruslast <200000IU/ml sowie der Durchführung der aktiven und passiven Immunisierung nicht weiter reduziert.11
Chronische Hepatitis-D-Virusinfektion
Eine HDV-Infektion kann nur gemeinsam mit einer HBV-Infektion (Simultan- oder Superinfektion) auftreten, da für die Synthese infektiöser Viruspartikel die Anwesenheit von HBsAg erforderlich ist. Die HBV/HDV-Koinfektion ist die schwerwiegendste aller chronischen Hepatitiden und mit einem deutlich höheren Risiko für die Entwicklung von Leberzirrhose und HCC assoziiert.12 Aufgrund des progredienten Verlaufs sollte die HDV-Diagnostik bei allen Patienten mit HBV-Infektion mindestens einmal erfolgen. Durch Migrationsbewegungen kann die HBV/HDV-Koinfektion auch in nichtendemischen Regionen wie Westeuropa vorkommen.
Antivirale Therapie
Die chronische HDV-Infektion kann bei kompensierter Lebererkrankung mittels PEG-IFN-α über einen Zeitraum von 48 Wochen behandelt werden. Ein virologisches Ansprechen tritt dabei bei weniger als einem Drittel der Patienten auf, jedoch können manche Patienten eine Serokonversion zu anti-HBsAg erreichen.13–15 NA haben keine Wirksamkeit gegen HDV, sollten bei nachweisbarer HBV-Replikation aber zur Behandlung der HBV-Infektion eingesetzt werden.
Mit dem kürzlich durch dieEuropäische Arzneimittelbehörde mit Einschränkungen zugelassenen Eintrittsinhibitor Bulevirtid steht eine neue Substanz zur Behandlung der chronischen HDV-Infektion zur Verfügung. Zum aktuellen Zeitpunkt ist die Behandlung auf Patienten mit kompensierter Lebererkrankung beschränkt und es ist von einer Dauertherapie auszugehen.16 Langzeitdaten sind noch ausstehend und die Phase-III-Studien zum aktuellen Zeitpunkt noch nicht abgeschlossen. Für Patienten mit dekompensierter Lebererkrankungen sind nach wie vor keine medikamentösen Therapien zugelassen, sodass diese Patienten in einem Lebertransplantationszentrum betreut werden sollten. Weitere Substanzen wie der Prenylierungsinhibitor Lonarfanib, Interferon lambda, siRNA-basierte Therapieansätze oder HBsAg-Release-Inhibitoren befinden sich in unterschiedlichen Stadien der klinischen Entwicklung.17
Fazit
In Deutschland und Österreich bestehen durch die Verfügbarkeit von Impfung und hochpotenter antiviraler Substanzen für die HBV-Infektion gute Präventions- und Behandlungsmöglichkeiten. Jedoch sind auch hier Risikogruppen mit erhöhtem Infektionsrisiko durch die vorhandenen Gesundheitsstrukturen teilweise nur schwer erreichbar, sodass Infektionen nicht erkannt, nicht behandelt und somit Übertragungsketten nicht unterbrochen werden können. Herausforderungen bestehen unverändert in der Weiterentwicklung antiviraler Therapien, sodass eine Heilung der HBV- und HBV/HDV-Koinfektion erreicht werden kann. Neue Therapien sind vielversprechend, allerdings müssen auch hier der weitere Verlauf und die Ergebnisse von Langzeitstudien abgewartet werden.
Literatur:
1 World Health Organization: Hepatitis B Fact Sheet. https://www.who.int/news-room/fact-sheets/detail/hepatitis-b ; zuletzt aufgerufen am 3.5.2022 2 Cornberg M et al.: S3-Leitlinie der Deutschen Gesellschaft für Gastroenterologie, Verdauungs- und Stoffwechselkrankheiten (DGVS) zur Prophylaxe, Diagnostik und Therapie der Hepatitis-B-Virusinfektion. AWMF-Register-Nr. 021-11. Z Gastroenterol 2021; 59: 641-3 3 EASL 2017: Clinical practice guidelines on the management of hepatitis B virus infection. J Hepatol 2017; 67: 370-98 4 Yip TCF et al.: Tenofovir is associated with lower risk of hepatocellular carcinoma than Entecavir in patients with chronic HBV infection in China. Gastroenterology 2020; 158: 215-25.e6 5 Papatheodoridis G V et al.: Similar risk of hepatocellular carcinoma during long-term entecavir or tenofovir therapy in Caucasian patients with chronic hepatitis B. J Hepatol 2020; 73: 1037-45 6 Yuan BH et al.: Lower risk of hepatocellular carcinoma with tenofovir than entecavir treatment in subsets of chronic hepatitis B patients: an updated meta-analysis. J Gastroenterol Hepatol 2022; doi: 10.1111/jgh.15783 7 Berg T, Lampertico P: The times they are a-changing - a refined proposal for finite HBV nucleos(t)ide analogue therapy. J Hepatol 2021; 75: 474-80 8 Jeng WJ et al.: Clinical relapse after cessation of Tenofovir therapy in Hepatitis B e antigen-negative patients. Clin Gastroenterol Hepatol 2016; 14: 1813-20.e1 9 Sandmann L, Cornberg M: Towards eradication of HBV: Treatment approaches and status of clinical trials. Curr Opin Pharmacol 2021; 60: 232-40 10 Papatheodoridi M et al.: Risk of HBV reactivation during therapies for HCC: a systematic review. Hepatology 2022; 75: 1257-74 11 Chen HL et al.: Vaginal delivery and HBV mother to child transmission risk after immunoprophylaxis: a systematic review and a meta-analysis. Midwifery 2019; 74: 116-25 12 Béguelin C et al.: Hepatitis delta-associated mortality in HIV/HBV-coinfected patients. J Hepatol 2017; 66: 297-303 13 Wedemeyer H et al.: Peginterferon plus adefovir versus either drug alone for hepatitis delta. N Engl J Med 2011; 364: 322-31 14 Wedemeyer H et al.: Peginterferon alfa-2a plus tenofovir disoproxil fumarate for hepatitis D (HIDIT-II): a randomised, placebo controlled, phase 2 trial. Lancet Infect Dis 2019; 19: 275-86 15 Heidrich B et al.: Late HDV RNA relapse after peginterferon alpha-based therapy of chronic hepatitis delta. Hepatology 2014; 60: 87-97 16 European Medicines Agency: https://www.ema.europa.eu/en/medicines/human/EPAR/hepcludex ; zuletzt aufgerufen am 3.5.2022 17 Sandmann L, Wedemeyer H: New treatments for chronic Hepatitis B virus/Hepatitis D virus infection. Clin Liver Dis 2021; 25: 831-9
Das könnte Sie auch interessieren:
Mit Alkoholverzicht zur Rekompensation von fortgeschrittener Leberzirrhose
Konsequenter und dauerhafter Alkoholverzicht kann selbst bei fortgeschrittener alkoholbedingter Leberzirrhose zu einer Rückbildung bereits bestehender leberbedingter Komplikationen ...
UEGW 2025: Neues aus der Hepatologie
In der Indikation metabolisch bedingte Lebersteatose bzw. Steatohepatitis scheiterten über viele Jahre zahlreiche Therapieversuche. Seit Kurzem stehen erstmals wirksame und zugelassene ...
Sonografie der Leber – aktuelle Entwicklungen, quantitative Verfahren und klinische Bedeutung
Der vorliegende Übersichtsartikel fasst aktuelle technische Entwicklungen sowie klinische Anwendungen und Limitationen der Lebersonografie zusammen und diskutiert deren Stellenwert im ...