Pillenmüdigkeit
Autor:
Prof. Dr. med. Thomas Steck
Ärztliche Partnerschaftsgesellschaft Kinderwunsch-Zentrum Mainz
Fort Malakoff Park, Mainz
E-Mail: prof.steck@kwz-mz.de
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Unter der Wortschöpfung «Pillenmüdigkeit» wird üblicherweise die Ablehnung oder mangelnde Bereitschaft einer Anwenderin verstanden, die Einnahme eines hormonellen Kontrazeptivums weiter fortzusetzen. In Deutschland war in den letzten 10–15 Jahren das Verordnungvolumen hormoneller empfängnisverhütender Mittel rückläufig. Dieser Trend ist möglicherweise bedingt durch das zunehmende Wissen um Nebenwirkungen und Risiken der «Antibabypille», das Vorhandensein zahlreicher Alternativen und die Sorge, dass durch eine jahrelange hormonelle Kontrazeption die Familienplanung in eine spätere Lebensphase mit reduzierter Fruchtbarkeit und erhöhtem Risiko für Spontanabort verschoben würde.
In den Jahren nach der Markteinführung der ersten «Antibabypille» in der BRD im Jahr 1961 (Anovlar, Hersteller Schering AG Berlin) und der ersten «Wunschkindpille» in der DDR im Jahr 1965 (Ovosiston, Hersteller VEB Jenapharm Jena) wurden hormonelle Kontrazeptiva nur von wenigen Frauenärzten vor allem an verheiratete Frauen und nach dem 30. Geburtstag verordnet. Die anfänglich restriktive Verordnung hatte zur Folge, dass etwa im Jahr 1966 in der BRD <2% der Frauen eines Geburtsjahrganges eine hormonelle Empfängnisverhütung anwendeten. In den 1970er- und 1980er-Jahren stiess die hormonelle Empfängnisverhütung in der BRD dann auf eine breite Akzeptanz und wurde zeitweilig von mehr als einem Drittel der Frauen in gebärfähigem Alter praktiziert, in bestimmten Altersgruppen sogar von mehr als der Hälfte. Indes war im wiedervereinigten Deutschland das Verordnungsvolumen hormoneller empfängnisverhütender Mittel in den letzten 10–15 Jahren wieder rückläufig. Gleichzeitig wird von zahlreichen praktisch tätigen Frauenärzten über eine zunehmend kritische Haltung vieler Anwenderinnen (und potenzieller Anwenderinnen) mit Betonung der unerwünschten Wirkungen und Risiken der hormonellen Kontrazeption berichtet. Der beobachtete Trend zu einem Rückgang in der jährlichen Verordnungsmenge hormoneller Kontrazeptiva hat bislang nicht zu einem Anstieg der Zahl an gemeldeten und nicht medizinisch indizierten Unterbrechungen einer Schwangerschaft geführt. Man kann daraus den Schluss ableiten, dass die Frauen im gebärfähigen Alter heute generell nicht «unvorsichtiger» geworden sind in ihrem sexuellen Verhalten und in der Anwendung einer Empfängnisverhütung als früher, bei gleichzeitig deutlicher Wahrnehmung der unerwünschten Wirkungen einer hormonellen Kontrazeption.
Gründe
Gesicherte Erkenntnisse über die Ursachen und Hintergründe der «Pillenmüdigkeit», die sich als kritische oder ablehnende Einstellung gegenüber jeglicher Form der hormonellen Antikonzeption manifestiert, gibt es nicht. Ein Teil der Anwenderinnen hat offensichtlich negative Erfahrungen gemacht oder Nebenwirkungen wie Depressivität, Stimmungsschwankungen, Appetitsteigerung mit Gewichtszunahme oder reduziertes sexuelles Verlangen erlebt. Andere Anwenderinnen (oder potenzielle Anwenderinnen) sind verständlicherweise besorgt über die beobachtete milde Erhöhung des Risikos für die Entstehung eines hormonrezeptorpositiven Mammakarzinoms unter der Einnahme kombinierter oraler Kontrazeptiva (COC) und kombinierter nicht oraler Kontrazeptiva (CNOC), besonders beim Vorliegen einer familiären Belastung,1 blenden bei dieser Betrachtung jedoch die gut dokumentierte Minderung des Risikos für andere Malignome (Ovarialkarzinom, Endometriumkarzinom und Kolonkarzinom) weitgehend aus. Auch die Angst vor dem Eintritt seltener, jedoch schwerwiegender Komplikationen, in erster Linie bedingt durch die langfristige Einnahme von Ethinylöstradiol (EE), das in der überwiegenden Zahl der COC und CNOC enthalten ist, wie thromboembolische Ereignisse, Myokardinfarkt und zerebrovaskuläre Apoplexie, ist nachvollziehbar.2 In der Tat ist unter langfristiger Einnahme von COC und CNOC eine milde Erhöhung des Risikos für arterielle und venöse thromboembolische Ereignisse zu beobachten, die in erster Linie auf die gerinnungsfördernde und blutdrucksteigernde Wirkung von EE zurückzuführen ist. Zwar beobachtet man auch unter der Einnahme bestimmter Gestagene (Desogestrel, Gestoden, Drospirenon) eine Verdoppelung des Risiko für venöse Thromboembolie, jedoch ist das altersabhängige Basisrisiko (2–10 pro 10000 Frauen und Jahr) gering. Im Gegensatz dazu fällt die Erhöhung des Risikos für venöse thromboembolische Ereignisse (um den Faktor 4–8 gegenüber einer Nichtanwenderin) aufgrund der langfristigen Einnahme von EE weitaus mehr ins Gewicht. Die berichtete Erhöhung des Risikos für Myokardinfarkt und zerebrovaskuläre Apoplexie ist zahlenmässig gering (relatives Risiko=1,6–1,7), jedoch handelt es sich hierbei um schwerwiegende Komplikationen.2
Ein wesentlicher Faktor, der die häufig zu beobachtende «Pillenmüdigkeit» begründet, ist die Furcht vor einer unerwünschten Verschiebung der Familienplanung in ein Lebensalter mit reduzierter Fruchtbarkeit und erhöhtem Risiko für Spontanabort. Beträgt die Rate spontaner Konzeptionen pro Jahr, eine nicht eingeschränkte männliche Fertilität und das Fehlen fertilitätsrelevanter weiblicher Erkrankungen vorausgesetzt, in der Gruppe der 25- bis 30-jährigen sexuell aktiven Frauen noch etwa 70%, sinkt diese jährliche Rate auf gut 10% in der Gruppe der 40- bis 45-jährigen Frauen bei gleichzeitiger Zunahme des Risiko für Spontanabort, das im Alter von ≥40 Jahren bei der Frau mindestens 30–40% beträgt. Ging man in den Anfangsjahren der hormonellen Kontrazeption in Ermangelung anderer Erkenntnisse noch davon aus, dass nach der Beendigung einer mehrjährigen Periode einer fortgesetzten hormonellen Empfängnisverhütung die Wahrscheinlichkeit einer spontanen Konzeption ähnlich hoch sei wie zu Beginn der Einnahme der «Antibabypille», ist es heute allgemein akzeptiert, dass die Konzeptionsrate altersabhängig stark abfällt. Die Sorge der Anwenderin, dass sie womöglich durch eine Verschiebung der Familienplanung in ein Lebensalter mit geringer Konzeptionswahrscheinlichkeit und reduzierter ovarieller Reserve ihre eigene Unfruchtbarkeit selbst herbeiführt oder fördert, erscheint begründet, nicht nur unter ungünstigen Umständen wie einer bereits zum Zeitpunkt des Beginns der Einnahme reduzierten Ovarreserve mit dadurch bedingter Annahme der Vorverlegung des Eintrittes in das Klimakterium/die Perimenopause. Möglicherweise wird es in der Zukunft zu diskutieren sein, vor dem Beginn einer langfristigen hormonellen Antikonzeption einen Marker der ovariellen Reserve, wie den AMH-Wert, zu bestimmen, um die Bedenken der Anwenderin zu bestätigen oder zu zerstreuen. Der AMH-Wert wird durch die laufende Einnahme einer Antibabypille (wie auch bei Vaginalring und Pflaster) übrigens um etwa 20–25% gesenkt, bei einer Bestimmung während der hormonellen Verhütung kann dieser Effekt jedoch herausgerechnet werden.3
Beratung
Die Antikonzeptionsberatung bei einer umfangreich vorinformierten Anwenderin (oder potenziellen Anwenderin) kann erfahrungsgemäss zeitaufwendig sein. Es gilt zu erfragen, ob überhaupt die Bereitschaft zur Anwendung einer hormonellen Methode besteht, ob eine eher kurz- oder langfristige Kontrazeption gewünscht wird, ob eine therapeutische Amenorrhö akzeptabel ist oder ein regelmässiges Blutungsmuster favorisiert wird, welche Hintergrundinformationen und Ängste vorhanden sind, welche Begleitwirkungen (abgesehen von der Empfängnisverhütung) erwartet werden und vor allem, welche medizinischen Vorerkrankungen, familiären Belastungen und Risikofaktoren bekannt sind. Die Bestimmung von Laborparametern (AMH-Wert, Screening auf angeborene und erworbene Thrombophilie, basale Hormonanalyse oder Zyklusmonitoring) im Rahmen einer Antikonzeptionsberatung ist derzeit nicht etabliert, kann aber in besonderen Situationen erwogen werden. Bei Frauen im Alter ≥40 Jahren und bei vorbestehender arterieller Hypertonie oder beim Vorliegen von ≥2 Risikofaktoren für venöse Thromboembolie (Tab.1) sollte auf die Verordnung eines COC oder CNOC mit Östrogenanteil verzichtet werden. Andererseits gibt es eine Reihe günstiger extrakontrazeptiver Wirkungen über den empfängnisverhütenden Effekt hinaus, wie Linderung von Periodenschmerzen, Reduktion des menstruellen Blutverlustes und Besserung dermatologischer Probleme (Akne, Seborrhö), die in die therapeutische Empfehlung einfliessen. Den häufigen Beschwerden in der einnahmefreien Phase, die überwiegend auf dem Entzug der synthetischen Hormone beruhen, wie Kopfschmerzen, Unterbauchschmerzen und Stimmungsveränderungen, kann durch einen Präparatewechsel mit Verkürzung der einnahmefreien Woche oder Einnahme im «Langzyklus» begegnet werden.
Tab. 1: Liegen ein oder mehrere Risikofaktoren vor, sollte auf COC oder CNOC mit Östrogenanteil verzichtet werden
Abhilfe
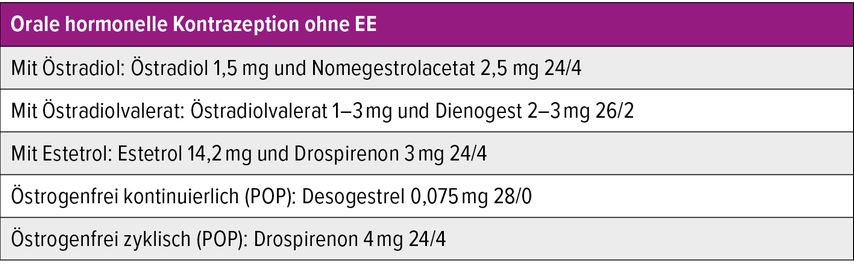
Das in der überwiegenden Zahl der aktuell auf dem Markt befindlichen COC und CNOC enthaltene EE weist im Vergleich zu Östradiol eine deutlich höhere orale Bioverfügbarkeit auf, bei gleichzeitig geringem hepatischem «First pass»-Effekt, sodass dessen östrogene Wirkung um ein Vielfaches höher ist als diejenige von Östradiol. Die schweren Nebenwirkungen der COC und CNOC, nämlich die milde Erhöhung des Risikos für venöse Thromboembolie, arterielle thromboembolische Ereignisse und hormonrezeptorpositives Mamma-Ca, sind in erster Linie bedingt durch den Gehalt an EE in den meisten gängigen Präparaten und nur in geringem Umfang durch die Gestagenkomponente. Es liegt daher nahe, entweder die tägliche Dosis von EE in den Präparaten zu reduzieren auf 15–20µg täglich (sog. «Mikropille») oder EE zu ersetzen durch andere Östrogene. In den letzten Jahren wurden mehrere COC entwickelt, die als östrogene Komponente entweder mikronisiertes Östradiol oder Östradiolvalerat enthalten, wobei Östradiolvalerat bereits bei der ersten Leberpassage in Östradiol umgewandelt wird und weitgehend identische pharmakologische Eigenschaften aufweist wie Östradiol, oder das in der fetalen Leber gebildete Estetrol (E4). Um irreguläre Blutungen zu vermeiden, werden mikronisiertes Östradiol und Östradiolvalerat mit Gestagenkomponenten kombiniert, die eine hohe endometriale Wirksamkeit aufweisen, wie Dienogest (DNG) und Nomegestrolacetat (NOMAC). Die kontrazeptive Sicherheit von COC mit natürlichen Östrogenen (statt mit EE) ist hoch und mit der von herkömmlichen Präparaten mit EE vergleichbar. Das thromboembolische Risiko der östradiolbasierten Präparate wurde im Jahr 2022 vom Bundesamt für Arzneimittel und Medizinprodukte in Berlin als vergleichbar mit dem der anderen COC bewertet. In Kohortenstudien zeigte sich jedoch teilweise ein signifikanter Trend in Richtung eines reduzierten thromboembolischen Risiko der COC mit Östradiol und Östradiolvalerat im Vergleich zu herkömmlichen COC mit EE und Levonorgestrel (LNG).4 Zur verlässlichen Einschätzung des thromboembolischen Risikos unter COC mit Estetrol sind weitere Daten aus Kohortenstudien notwendig, was erfahrungsgemäss mehrere Jahre in Anspruch nehmen wird. Klar ist andererseits, dass unter der Einnahme eines COC mit einem natürlichen Östrogen das thromboembolische Risiko auf jeden Fall höher liegt als beieiner Nichtanwenderin. Die Kombinationen mit natürlichen Östrogenen wirken sich, wenn überhaupt, nur geringfügig auf den Kohlenhydrat- und Lipidstoffwechsel aus und beeinflussen die Gerinnungsparameter weniger stark als COC mit EE und LNG. Verlässliche Daten zur Beeinflussung des Risikos für hormonrezeptorpositives Mammakarzinom unter und nach der Einnahme von COC mit natürlichen Östrogenen fehlen bislang, da hierfür eine Nachbeobachtung über viele Jahre und Jahrzehnte nach der Einnahme erforderlich wäre. Die Präparate mit natürlichen Östrogenen eignen sich ebenso zur Linderung von Dys- und Hypermenorrhö wie die Präparate mit EE, wobei sich die Verkürzung der einnahmefreien Phase in den Präparaten mit Östradiol, Östradiolvalerat und Estetrol (Einnahmeschema 24/4 oder 26/2 statt 21/7) günstig auswirkt.5 Die Verkürzung des hormonfreien Intervalls in den Präparaten mit natürlichen Östrogenen hat eine positive Wirkung auf hormonentzugsbedingte Kopf- und Unterbauchschmerzen zur Folge. Ein Wechsel auf ein COC mit natürlichen Östrogenen ist auch eine therapeutische Option für Frauen mit Beeinträchtigungen des sexuellen Erlebens unter anderen COC. Ein häufiges Problem unter der Einnahme von COC mit natürlichen Östrogenen liegt in dem gehäuften Vorkommen von unregelmässigen Blutungen. Aufgrund der kurzen Zeit seit der Markteinführung des bislang einzigen COC mit Estetrol und NOMAC gibt es bislang nur limitierte Erkenntnisse zu extrakontrazeptiven Wirkungen, Zufriedenheit und Compliance, in einer Kohortenstudie wurde allerdings über eine relativ hohe Nebenwirkungs- und Abbruchrate unter der Kombination aus Östradiol und NOMAC berichtet.6
Eine andere therapeutische Alternative zur hormonellen Antikonzeption bei einer sexuell aktiven Frau mit Pillenmüdigkeit (Tab. 2) besteht in der Gabe eines reinen Gestagenpräparates («Minipille» oder «progestogen only pill» – POP), beispielsweise als kontinuierliche Einnahme von Desogestrel (DG) oder zyklische Einnahme von Drospirenon (DRSP, Einnahmeschema 24/4). Dadurch werden sämtliche östrogenbedingten Nebenwirkungen vermieden, es ist allerdings mit einem gehäuften Vorkommen von Zwischen- und Schmierblutungen zu rechnen. Gleiches gilt für östrogenfreie Langzeitkontrazeptiva als intramuskuläre Injektion eines Depotgestagens («Dreimonatsspritze» mit Medroxyprogesteronacetat) oder als Implantat («Verhütungsstäbchen» mit Etonogestrel), bei denen zwar die empfängnisverhütende Wirkung extrem hoch und ein Einnahmefehler ausgeschlossen ist, jedoch lang anhaltende Zwischen- und Schmierblutungen auftreten können, bei hoher Frequenz gestagenbedingter Nebenwirkungen (Haarausfall, Gewichtszunahme, Stimmungsschwankungen und Libidoverlust). Aufgrund der fehlenden Reversibilität der Wirkung bei der «Dreimonatsspritze» und der möglichen Schwierigkeiten bei der Entfernung des subkutan implantierten «Hormonstäbchens» haben diese Methoden nur eine geringe Verbreitung erfahren.
Literatur:
1 Mørch LS et al.: Contemporary hormonal contraception and the risk of breast cancer. N Engl J Med 2017; 377(23): 2228-39 2 Roach REJ et al.: Combined oral contraceptives: the risk of myocardial infarction and ischemic stroke. Cochrane Database Syste Rev 2015; 2015(8): CD011054 3 Bernardi LA et al.: Duration, recency, and type of hormonal contraceptive use and antimüllerian hormone levels. Fertil Steril 2021; 116(1): 208-17 4 Dinger J et al.: Combined oral contraceptives containing dienogest and estradiol valerate may carry a lower risk of venous and arterial thromboembolism compared to conventional preparations: results from the extended INAS-SCORE study. Front Womens Health 2020; 5: 1-8 5 Nappi RE et al.: Noncontraceptive benefits of the estradiol valerate/dienogest combined oral contraceptive: a review of the literature. Int J Womens Health 2014; 6: 711-8 6 Ågren UM et al.: Effects of a monophasic combined oral contraceptive containing nomegestrol acetate and 17β-oestradiol compared with one containing levonorgestrel and ethinylestradiol on haemostasis, lipids and carbohydrate metabolism. Eur J Contracept Reprod Health Care 2011; 16(6): 444-57
Das könnte Sie auch interessieren:
Die Menopause aus evolutionärer Perspektive
Kann man die menopausale Transition überhaupt als pathologisches Geschehen interpretieren, wenn alle Frauen um das 50. Lebensjahr diese durchleben? Oder wurde das obligate irreversible ...
Sport und Krebserkrankungen
In den letzten Jahzehnten hat sich insgesamt ein Paradigmenwechsel in der Medizin vollzogen – von der körperlichen Schonung hin zur Aktivität und frühen Mobilisierung im Rahmen von ...
Hormonelle Gesundheit nach der Menopause
Frauen verbringen heute rund ein Drittel ihres Lebens in der Postmenopause. Diese Lebensphase ist mit einer hohen Symptomlast und langfristigen gesundheitlichen Risiken verbunden, was ...