Kann der Lifestyle eine IBD verhindern?
Bericht: Regina Scharf, MPH
Redaktorin
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Es gibt immer mehr Hinweise, dass die Entstehung und der Krankheitsverlauf von entzündlichen Darmerkrankungen durch Umwelt- und Lifestylefaktoren beeinflusst werden. Am 9. Postgraduate Course des IBDnet erhielten die Teilnehmenden eine Antwort auf die spannende Titelfrage, Updates zum Thema Lifestyle aus der SWISSIBD-Kohorte und praktische Tipps zur Abklärung von IBD-Patienten, die trotz Remission an anhaltenden Beschwerden leiden.
Noch vor einigen Jahren war der Enthusiasmus, dass sich das Risiko für das Auftreten von entzündlichen Darmerkrankungen («inflammatory bowel disease», IBD) durch die Genetik erklären liesse, gross. In der Zwischenzeit ist im Journal Nature eine Landmarkstudie erschienen. Diese kommt basierend auf der Analyse von mehr als 75000 genomweiten Assoziationsscans zu dem Schluss, dass die Genetik nur zu einem kleinen Teil das variierende Krankheitsrisiko für Morbus Crohn (MC) oder Colitis ulcerosa (CU) erklärt.1 Damit sind die Lebensstil- und Umweltfaktoren als Ursache in den Fokus gerückt.
Die von Prof. Dr. med. Luc Biedermann vom Universitätsspital Zürich vorgestellten Studien deuten auf einen Zusammenhang zwischen diesen Faktoren und dem IBD-Risiko hin. Eine dänische Kohortenstudie, die in den Jahren von 1977–2018 das Auftreten von MC und CU bei dänischen Staatsbürgern mit einem Migrationshintergrund untersuchte, zeigte, dass das IBD-Risiko bei Einwanderern der 1. Generation dem in ihrem Geburtsland entsprach und niedriger war als jenes von gebürtigen Dänen.2 Innerhalb eines Zeitraums von circa 20 Jahren glichen sich jedoch die Risiken an. Unter den Einwanderern der 2. Generation wiesen nur noch die Frauen ein niedrigeres IBD-Risiko auf.
Wie wichtig Umweltfaktoren bei der Entstehung von IBD sind, demonstrierten auch die Ergebnisse einer Studie aus Florida. Diese untersuchte, ob die Exposition gegenüber etablierten Umwelt-Risikofaktoren wie zum Beispiel eine Geburt via Kaiserschnitt in einem westlichen Land, häufiges Trinken aus Plastikflaschen etc. und das genetische Risiko einen Einfluss auf das Alter hatten, in dem eine IBD diagnostiziert wurde. Dabei konnte gezeigt werden, dass die Umwelt in Modellen, die sowohl den genetischen Risikoscore wie auch den Umweltrisikoscore berücksichtigten, der einzige signifikante Risikofaktor war, der in den jüngeren Altersgruppen mit einer IBD-Diagnose assoziiert war.3 Umweltfaktoren erklärten 21% der Altersvarianz bei der Diagnose eines MC und 39% der Altersvarianz bei der Diagnose einer CU.
Zu interessanten Ergebnissen kam auch eine Untersuchung der UK-Biobankkohorte. Diese zeigte, dass genetische Faktoren und Lifestylefaktoren unabhängig voneinander die Empfindlichkeit für einen MC und eine CU erhöhten. Personen mit einem hohen genetischen Risiko für eine IBD konnten dieses Risiko durch einen gesunden Lebensstil um fast 50% reduzieren.4 «Man kann also sagen, dass die Kombination von genetischen und Umweltfaktoren bei der Entwicklung von IBD eine Rolle spielt», sagte Biedermann. Und stellte gleich auch die Schlüsselfrage in diesem Kontext: «Ist es möglich, das Auftreten einer IBD zu verhindern?»
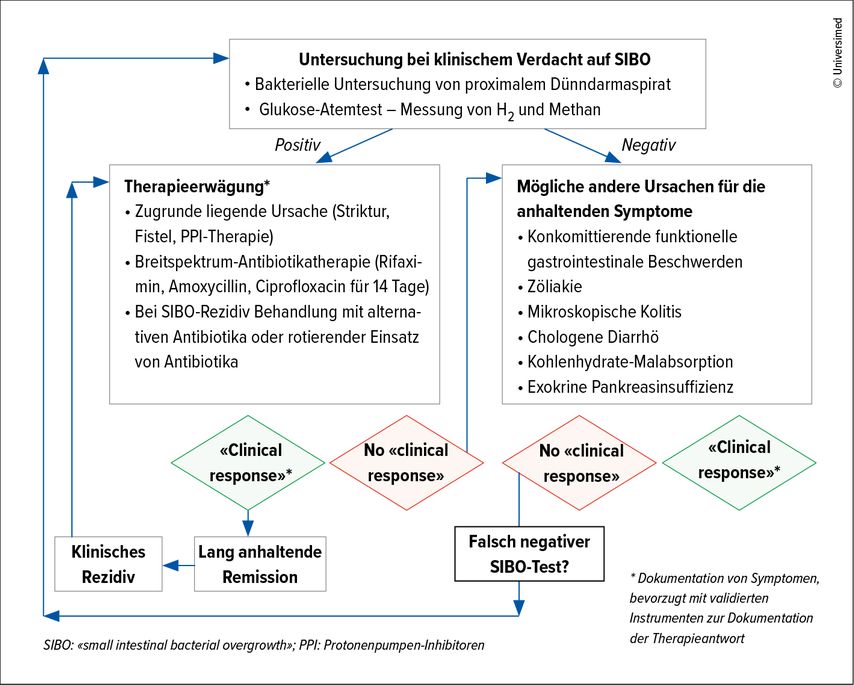
Abb. 1: Diagnostisches Vorgehen bei IBD-Patienten in Remission mit unklaren gastrointestinalen Symptomen und Verdacht auf SIBO (modifiziert nach Shah A et al. 2022)18
Lebensstil und Outcome
Eine Antwort auf diese Frage lieferten die Ergebnisse einer prospektiven Kohortenstudie mit Personen der Nurses-Health-Studien (NHS, NHSII) und der Health-Professionals-Follow-up-Studie (HPFS). Diese hatte die Inzidenz des MC und der CU in den Gruppen mit einem gesunden und ungesunden Lebensstil verglichen und das attributable Risiko berechnet. Den Ergebnissen zufolge hätten durch weniger Lifestyle-Risikofaktoren und eine höhere Adhärenz zu einem gesünderen Lebensstil ca. 42–61% der MC- und etwa 42–44% der CU-Fälle vermieden werden können.5 Eine andere auf den Daten der oben erwähnten Kohorten NHS, NHSII und HPFS basierende Untersuchung zeigte, dass sich selbst das Überleben der IBD-Patienten über den Lebensstil beeinflussen liess. So war die Gesamtmortalität bei den im Median mit 55 Jahren mit MC oder CU diagnostizierten Personen mit einem gesunden Lebensstil signifikant reduziert im Vergleich zu Personen mit einem ungesunden Lebensstil.6
Aktuelle Daten aus der SWISSIBD-Kohorte
Die anschliessend vorgestellten Daten aus der SWISSIBD-Kohortenstudie lieferten Informationen zum Impact der einzelnen Lifestylefaktoren auf den Krankheitsverlauf von MC und CU. Nachdem die Themen Ernährung und Diät lange Zeit vernachlässigt wurden, hat das Interesse daran in den letzten Jahren deutlich zugenommen. Eine Studie der SWISSIBD-Kohorte, die den Einfluss einer vegetarischen und einer glutenfreien Ernährung auf die Krankheitsaktivität untersuchte, konnte zwar keinen Unterschied zu einer omnivoren Ernährung feststellen.7 Interessanterweise fanden sich aber bei den Patienten, die eine strikte Diät einhielten, deutlich schwerere posttraumatische Stresssymptome. Patienten mit einer glutenfreien Diät wiesen zudem signifikant schwerere Angst- und Depressionssymptome auf. «Vermutlich handelt es sich dabei nicht um einen kausalen Zusammenhang», sagte Biedermann. Die strikte Adhärenz zu einer Diät sei aber möglicherweise mit bestimmten Persönlichkeitsmerkmalen verlinkt.
Ein weiterer Lifestylefaktor, der gemäss einer Untersuchung der SWISSIBD-Kohorte den Krankheitsverlauf negativ beeinflussen kann, ist die Adipositas. Wie die Ergebnisse einer Studie mit einem Follow-up von 6 Jahren zeigten, war ein BMI ≥30kg/m2 bei Patienten mit MC mit einer niedrigeren Wahrscheinlichkeit für eine Remission und mit einem erhöhten Risiko für Komplikationen assoziiert.8 Neue Daten gibt es auch zur MAFLD («metabolic-associated fatty liver disease») bei IBD. Die Prävalenz für eine MAFLD ist im Vergleich zur Normalbevölkerung bei Patienten mit IBD nur geringfügig höher. Eine aktuelle Untersuchung an zwei Universitätsspitälern in Spanien konnte jedoch zeigen, dass die Prävalenz für eine fortgeschrittene Leberfibrose bei IBD-Patienten mit einer MAFLD um das 4-Fache höher war als in der Normalbevölkerung.9 «Das müssen wir in den nächsten Jahren aufmerksam verfolgen», sagte der Referent.
IBD-IBS-Overlap
Bei Patienten mit IBD finden sich oftmals überlappende Symptome einer funktionellen Darmerkrankung («irritable bowel syndrome», IBS). Die Erkrankungen weisen viele Gemeinsamkeiten auf, darunter die multifaktorielle Pathogenese und ein breites Spektrum von vergleichbaren Symptomen.10,11 «Der grösste Unterschied zwischen den Erkrankungen ist, dass die Endoskopie bei einem IBS keine Läsionen zeigt, während bei Patienten mit IBD die Schleimhautentzündung, Stenosen oder Strikturen nachweisbar sind», sagte Prof. Dr. med. Elisabeth Schnoy vom Universitätsklinikum in Augsburg, Deutschland.
Wie Studien zeigten, leidet ein substanzieller Anteil von Patienten mit IBD in Remission weiterhin an Beschwerden wie Energielosigkeit, Krämpfen oder Stuhldrang etc.12 Gemäss einer Metaanalyse könnte die Ursache dafür ein IBS sein. Abhängig davon, ob Remission endoskopisch, histologisch oder klinisch definiert wurde, lag die Prävalenz für IBS-ähnliche Symptome bei 23,5%, 25,8% oder 33,6%. Besonders häufig betroffen waren Patienten mit MC.13
«Das hat enorme Folgen», sagte die Referentin und verwies auf eine Untersuchung, die zeigte, dass IBD-Patienten mit den Symptomen eines IBS häufiger hospitalisiert oder chirurgisch behandelt werden als Patienten mit IBD alleine. Zudem wiesen die Patienten deutlich häufiger Angststörungen und Depressionen auf. Auf der anderen Seite wird die Diagnose IBD bei gleichzeitigem Vorhandensein von IBS-Symptomen häufiger schon in einem jüngeren Alter gestellt.14
SIBO als Ursache anhaltender Symptome
Ob es sich bei den anhaltenden Symptomen bei IBD-Patienten in Remission tatsächlich um ein IBS handelt, lässt sich mithilfe eines Algorithmus evaluieren. Dabei werden schrittweise mögliche Faktoren für die Beschwerden wie eine aktive Entzündung, Infektionen oder unerwünschte Wirkungen einer bestehenden Medikation ausgeschlossen. Ein Grund für die persistierenden Abdominalschmerzen kann eine bakterielle Dünndarmfehlbesiedelung («small intestinal bacterial overgrowth», SIBO) sein. Diese tritt als Folge von strukturellen oder anatomischen Veränderungen auf, bei Störungen der Magen-Darm-Passage in Zusammenhang mit metabolischen Erkrankungen oder Organdysfunktionen etc. Ein typisches Beispiel ist das Fehlen der Ileozäkalklappe nach ileozäkaler Resektion bei Patienten mit MC. Aufgrund der fehlenden Barriere können die Bakterien ungehindert aus dem Kolon in den Dünndarm wandern und zahlreiche Beschwerden wie zum Beispiel Übelkeit und Bauchschmerzen, Völlegefühl, Blähungen, Appetitlosigkeit und Gewichtsverlust verursachen.15 Ein einfacher und praktischer Weg zur Abklärung bei Verdacht auf eine SIBO ist die Durchführung eines Wasserstoff(H2)-Atemtests. Vor dem Test müssen die Patienten für 12 Stunden nüchtern sein. Für den Test wird zunächst der basale H2-Gehalt in der Ausatemluft gemessen, anschliessend erhalten die Patienten eine definierte Menge Laktulose oder Glukose zum Trinken. Bei der Metabolisierung durch die Mikroorganismen im Darm entsteht H2, weshalb erneut eine Messung der H2-Konzentration in der Ausatemluft durchgeführt werden muss. Eine Untersuchung mittels H2-Atemtest bei Patienten mit IBD und anderen gastrointestinalen Erkrankungen an der Universität Augsburg fand bei 14% der eingeschlossenen 128 Patienten eine SIBO. Bei den Betroffenen handelte es sich signifikant häufiger um ältere Personen und Patienten mit MC als mit CU (41 vs. 17%). Frauen waren zudem häufiger betroffen als Männer. Der Anteil der Patienten in klinischer Remission mit einer SIBO war höher als der Anteil der Patienten mit einer aktiven Erkrankung (19,4 vs. 15,3%).16
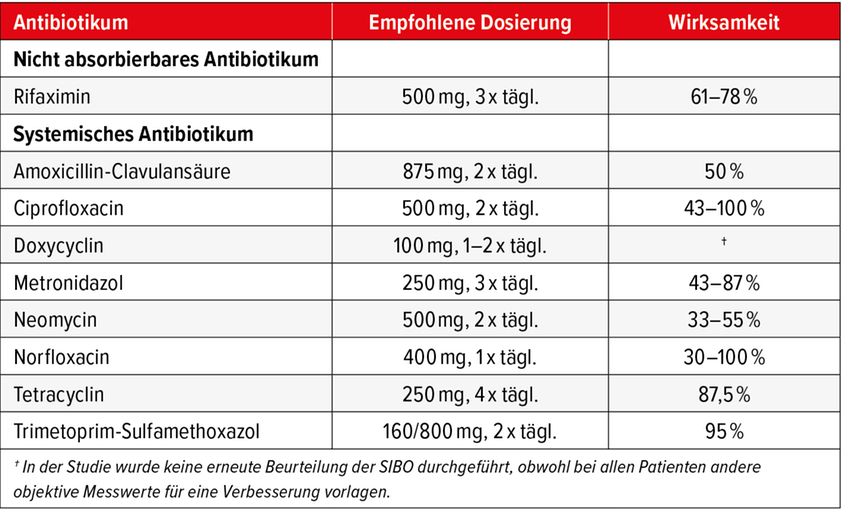
Zur Therapie bei SIBO werden Antibiotika eingesetzt. In Augsburg setzt man fast ausschliesslich auf die Verwendung des lokal wirksamen Antibiotikums Rifaximin. Daneben stehen diverse andere Antibiotika zur Verfügung (Tab. 1).17 Ein grosses Problem bei Patienten mit SIBO ist die häufige Rezidivrate. Diese erfordert erneut eine sorgfältige Abklärung (Abb. 1).18
Tab. 1: Empfohlene Antibiotika zur Behandlung bei «small intestinal bacterial overgrowth» (modifiziert nach Pimental M et al. 2020)17
Quelle:
IBDnet 9th Postgraduate Course, 5. bis 7. Dezember 2024, Ermatingen
Literatur:
1 Jostins L et al.: Host-microbe interactions have shaped the genetic architecture of inflammatory bowel disease. Nature 2012; 491: 119-24 2 Agrawal M et al.: Inflammatory bowel diseases among first-generation and second-generation immigrants in Denmark: a population-based cohort study. Gut 2021; 70: 1037-43 3 Khakoo NS et al.: Early life and childhood environmental exposures, more than genetic predisposition, influence age of diagnosis in a diverse cohort of 2952 patients with IBD. Clin Gastroenterol Hepatol 2024; 22: 1462-74 4 Sun Y et al.: The contribution of genetic risk and lifestyle factors in the development of adult-onset inflammatory bowel disease: a prospective cohort study. Am J Gastroenterol 2023; 118: 511-22 5 Lopes EW et al.: Lifestyle factors for the prevention of inflammatory bowel disease. Gut 2002 Dec 6. Online ahead of print. 6 Lo CH et al.: Healthy lifestyle is associated with reduced mortality in patients with inflammatory bowel diseases. Clin Gastroenterol Hepatol 2021; 19: 87-95 7 Schreiner P et al.: Vegetarian or gluten-free diets in patients with inflammatory bowel disease are associated with lower psychological well-being and a different gut microbiota, but no beneficial effects on the course of the disease. United European Gastroenterol J 2019; 7: 767-81 8 Greuter T et al.: Impact of obesity on disease activity and disease outcome in inflammatory bowel disease: Results from the Swiss inflammatory bowel disease cohort. United European Gastroenterol J 2020; 8: 1196-120 9 Rodriguez-Duque JC et al.: Increased risk of MAFLD and liver fibrosis in inflammatory bowel disease independent of classic metabolic risk factors. Clin Gastroenterol Hepatol 2023; 21: 406-14 10 Szalwińska P et al.: IBS-symptoms in IBD patients-manifestation of concomitant or different entities. J Clin Med 2020; 10: 31 11 Johansen I et al.: Symptoms and symptom clusters in patients newly diagnosed with inflammatory bowel disease: results from the IBSEN III Study. BMC Gastroenterology 2023; 23: 255 12 Lönnfors S et al.: IBD and health-related quality of life -- discovering the true impact. J Chrons Colitis 2014; 8: 1281-6 13 Fairbrass KM et al.: Prevalence of irritable bowel syndrome-type symptoms in patients with inflammatory bowel disease in remission: a systematic review and meta-analysis. Lancet Gastroenterol Hepatol 2020; 5: 1053-62 14 Perera LP et al.: Presence of irritable bowel syndrome symptoms in quiescent inflammatory bowel disease is associated with high rate of anxiety and depression. Dig Dis Sci 2019; 1923-28 15 Dukowicz A et al.: Small intestinal bacterial overgrowth: a comprehensive review. Gastroenterol Hepatol 2007; 3: 112-22 16 Wanzl J et al.: Impact of small intestinal bacterial overgrowth in patients with inflammatory bowel disease and other gastrointestinal disorders-a retrospective analysis in a tertiary single center and review of the literature. J Clin Med 2023; 12: 935 17 Pimentel M et al.: ACG Clinical Guideline: small intestinal bacterial overgrowth. Am J Gastroenterol 2020; 115: 165-78 18 Shah A, Holtmann G: Small intestinal bacterial overgrowth in inflammatory bowel disease. Indian J Gastroenterol 2022; 41: 23-9
Das könnte Sie auch interessieren:
Horror im Nachtdienst – Management von ösophagealen Notfällen
Um die Nachtdienste möglichst „horrorfrei“ zu halten, sind regelmäßige „Trockenübungen“, Leitlinienkenntnis und Wissen über endoskopische Hilfsmittel entscheidend. Drei Kasuistiken aus ...
Neuroimmunologische Aspekte bei chronisch-entzündlichen Darmerkrankungen
Psychische Belastungssituationen und chronisch-entzündliche Darmerkrankungen sind untrennbar miteinander verbunden, wobei Ursache und Wirkung oft schwer auseinanderzuhalten sind. Die ...
Fallbeispiel: retrograde cricopharyngeale Dysfunktion (R-CPD)
Ein 24-jähriger männlicher Patient stellte sich mit einer Unfähigkeit zu rülpsen sowie ausgeprägtem Meteorismus und anhaltendem abdominellem Spannungsgefühl vor. Die Symptomatik bestand ...