©
Getty Images/iStockphoto
Gicht: neue Medikamente und Ernährung
Jatros
Autor:
Univ.-Doz. Dr. Johann Gruber
Leiter Rheumatologie<br> Univ.-Klinik für Innere Medizin II, Innsbruck<br> E-Mail: johann.gruber@i-med.ac.at
30
Min. Lesezeit
28.03.2019
Weiterempfehlen
<p class="article-intro">Die Gicht ist zwar eine seit dem Altertum bekannte Erkrankung, die schon früh als eigene klinische Entität erfasst wurde. Der Einfluss der Natriumuratkristalle auf das Immunsystem und die genaue Rolle der Gichtkristalle für die Entstehung der Entzündung waren aber lange nicht bekannt. Sie ist in den letzten Jahren aufgrund neuer pathophysiologischer Erkenntnisse, besonders durch die Entdeckung der verschiedenen Formen des Zellunterganges, in den Blickpunkt gerückt. Dadurch ergeben sich neue Optionen in der Beeinflussung der Entzündung und damit in der Behandlung des akuten Gichtanfalles sowie der chronischen Gicht.</p>
<hr />
<p class="article-content"><h2>Zelltod</h2> <p>Natriumuratkristalle aktivieren mehrere „signalling pathways“, induzieren dadurch verschiedene Formen des Zelltodes (Apoptose, Ferroptose, Nekroptose) und führen zur Nekroinflammation (Abb. 1).</p> <p><img src="/custom/img/files/files_datafiles_data_Zeitungen_2019_Jatros_Infekt_1901_Weblinks_jatros_infekt_1901_s40_abb1.jpg" alt="" width="750" height="368" /></p> <h2>Kristall-induzierte zytotoxische Effekte</h2> <p>Monosodiumurat(MSU)-Kristalle induzieren eine epitheliale und mesenchymale Zellnekrose durch eine „receptor-interacting protein kinase 3“(RIPK3)-mediierte Phosphorylierung einer „mixed lineage kinase domain-like“ (MLKL). Diese Form einer regulierten Nekrose wird Nekroptose genannt und wird durch extrazelluläre Signale mithilfe von Tumornekrosefaktor( TNF)-Rezeptor 1, „Toll-like receptor“- (TLR)-4, TLR-3 oder CD-95 getriggert. MSU induziert über denselben Weg auch die Nekrose in neutrophilen Zellen. Diese als neutrophile Nekroptose bezeichnete Form des Zelltodes ist ein zentraler Prozess bei einer akuten Gichtarthritis. Dabei werden vom zerstörten Gewebe Alarmine wie z.B. Interleukin(IL)-1α und „neutrophil-extracellular traps“ (NETs) freigesetzt.<br /> Auch scheint die Apoptose, eine Form des programmierten Zelltodes, bei der Uratinduzierten Nephropathie eine Rolle zu spielen. Ein mitochondrialer Caspase-abhängiger Pathway führt in humanen Nierenzellen durch Induktion von oxidativem Stress zu dieser Art des Zelltodes. Wenn der Apoptoseweg blockiert ist, kann durch TNF auch die Nekroptose getriggert werden.<br /> MSU-Kristalle können auch eine weitere Form des Zelltodes, die Ferroptose, induzieren, direkt durch Supprimierung der Glutathionperoxidase-4 (GPX-4) oder durch Inhibierung von System Xc-, einem Cystin-Glutamat-Antiporter, der die zelluläre Verfügbarkeit von Cystein und Glutathion limitiert. Diese Form des Zelltodes ist morphologisch durch das Vorhandensein von kleineren Mitochondrien mit kondensierten mitochondrialen Membranverdichtungen, die Reduzierung der Cristae und die Ruptur der äußeren mitochondrialen Membran charakterisiert. Der Nukleus hat eine normale Größe und es fehlt die Kondensation des Chromatins. GPX 4, „heat shock protein beta-1“ (HSPB1) und „nuclear factor erythroid 2-related factor 2“ (NRF2) fungieren als negative Regulatoren einer Ferroptose durch Limitierung der Produktion von „reactive oxygen species“ (ROS) und Reduzierung der zellulären Eisenaufnahme.</p> <h2>Inflammation</h2> <p><strong>Kristall-induzierte Inflammation</strong><br /> Durch einen Kristall-induzierten Zelltod können in diesen Zellen proinflammatorische Moleküle, z.B. Alarmine, Proteasen oder sogenannte „damage-associated molecular patterns“ (DAMPs) freigesetzt werden. Diese Moleküle haben die Fähigkeit, TLR zu aktivieren. DAMPs inkludieren Nukleoproteine, Histone, ATP und auch die Harnsäure. Durch diese Aktivierung induzieren die Zellen die Expression und Sekretion von Zytokinen sowie Kininen und führen zu einer lokalen Vasodilatation, Schmerzen sowie zu einer endothelialen Dysfunktion mit erhöhter vaskulärer Permeabilität und Adhäsion von Leukozyten. Eine lokale Aktivierung von Komplement kann ebenfalls involviert sein. Dies führt zu den typischen klinischen Symptomen einer Entzündung.</p> <p><strong>NALP3-Inflammasom</strong><br /> Kristalle können jedoch eine Inflammation auch direkt triggern. Sowohl MSUals auch CPPD-Kristalle können das NALP3-Inflammasom aktivieren. Inflammasome sind Multiproteinkomplexe, bestehend aus zytosolischen Proteinen wie NLRP3 und ASC, welche die Aktivierung von inflammatorischen Caspasen mediieren. Diese intrazellulären Sensoren sind in der Lage, fremde und körpereigene „danger signals“ zu erkennen und eine Immunantwort zu induzieren. Ein wichtiger Vertreter ist das „NACHT-, LRR-, and pyrin domain-containing protein“(NALP)- Inflammasom. NALPs gehören gemeinsam mit den „nucleotide binding oligomerization domain containing proteins“ (NOD) und anderen Proteinen zur Gruppe der „NOD-like receptors“ (NLR). Zusammen mit den membranassoziierten TLR sind die zytosolisch gelegenen NLR ein Teil des angeborenen Immunsystems und spielen eine wesentliche Rolle bei der Erkennung und der Antwort auf körperfremde Signale. In einer ersten Phase internalisieren Phagozyten die Natriumuratkristalle. Sobald die Partikel phagozytiert sind, stimulieren sie wahrscheinlich über zwei verschiedene Mechanismen das Inflammasom, wobei ein Weg ROS und der zweite Phagozytenproteasen involviert.</p> <p>Nach der Bindung des Liganden und Freisetzung der NACHT-Domäne wird NALP3 aktiviert und rekrutiert dann zwei Adapterproteine (ASC und Cardinal) sowie Caspase 1. Dieser „Inflammasom“ genannte Komplex aktiviert IL-1β über die im Oligomer zusammengeführten Caspase-1-Dimere.</p> <h2>Interleukin-1</h2> <p>In der ersten Phase sezernieren die durch NALP3 aktivierten Monozyten IL-1β. In einer zweiten Phase werden vor allem Synoviozyten aktiviert und durch Vermittlung vom IL-1-Rezeptor und MyD88 die Chemokine Interleukin-8 oder MIP-2 induziert. IL-1 wird hauptsächlich von Monozyten als Antwort auf Infektion oder immunologische Reize produziert. Es verursacht Fieber, niedrigen Blutdruck und die Induktion von anderen proinflammatorischen Zytokinen wie Interleukin-6 (IL-6). Neben einem natürlichen IL-1-Rezeptor- Antagonisten (IL-1RA) bestehen zwei verschiedene Formen von IL-1, nämlich IL-1α und -β. IL-1α und -β werden in einer Proform gebildet, die 31 kd groß ist, wobei pro-IL-1α biologisch aktiv, pro-IL-1β aber biologisch nicht aktiv ist. Beide Formen werden in eine reife Form übergeführt, pro-IL-1β durch „interleukin-1 converting enzyme“ (ICE), pro-IL-1α kann z.B. durch Calpain gespalten werden oder durch andere noch nicht näher aufgeklärte Prozesse extrazellullär transportiert und dort durch Proteasen gespalten werden.</p> <h2>Neue Medikamente</h2> <p>Aus diesen pathophysiologischen Mechanismen ergeben sich therapeutische Optionen, die schon in der klinischen Praxis eingesetzt werden und viele neue Möglichkeiten für die zukünftige Behandlung eröffnen (Abb. 1).<br /> Zugelassen wurde inzwischen Lesinurad, ein Hemmer der Harnsäuretransporter URAT1 und OAT4, in Kombination mit einem Xanthin-Oxidase-Inhibitor bei Gichtpatienten, die den Harnsäurezielwert im Serum mit einer adäquaten Dosis eines Xanthin-Oxidase-Inhibitors allein nicht erreicht haben. Interessante neue Entwicklungen sind Arhalofenat, das neben der Blockade von Transportersystemen (URAT1, OAT4, OAT10) auch die IL-1β- Produktion hemmt, und Tranilast, das noch zusätzlich eine antiinflammatorische Aktivität hat (Abb. 2).</p> <p><img src="/custom/img/files/files_datafiles_data_Zeitungen_2019_Jatros_Infekt_1901_Weblinks_jatros_infekt_1901_s40_abb2.jpg" alt="" width="500" height="417" /></p> <h2>Gewichtsreduktion, Trinkmenge und Diät</h2> <p><strong>Langsame Gewichtsreduktion</strong><br /> Bei Übergewicht ist eine langsame Gewichtsreduktion anzustreben, weil mit einer Adipositas erhöhte Serumharnsäurespiegel assoziiert sind. Fastenkuren sind jedoch unbedingt zu vermeiden, da diese aufgrund der Ketoazidose Gichtanfälle provozieren können. Daneben soll auch auf regelmäßige körperliche Aktivität geachtet werden.</p> <p><strong>Genügende Trinkmenge</strong><br /> Die Trinkmenge sollte mindestens zwei Liter pro Tag betragen, wobei am besten zuckerlose, nicht alkoholische Getränke geeignet sind. Diese Flüssigkeitszufuhr ist insbesondere bei einer Urolithiasis mit Harnsäuresteinen mit gleichzeitiger Alkalinisierung des Urins zu empfehlen.</p> <p><strong>Auf die Ernährung achten</strong><br /> Regelmäßiger Verzehr von Fleisch und Innereien erhöht die Serumharnsäure und damit das Gichtrisiko nicht nur wegen der damit verbundenen Zufuhr von Purinen, sondern auch wegen der ungesättigten Fette, die die Insulinresistenz erhöhen und dadurch die Harnsäureausscheidung vermindern.<br /> Dagegen erhöhen protein- und purinreiche pflanzliche Produkte die Harnsäure nicht.</p> <p>Der Konsum von Milchprodukten vermindert die Serumharnsäure und damit das Gichtrisiko. Milchproteine wie Kasein und Laktalbumin, die urikosurisch wirken, dürften dafür verantwortlich sein. Zusätzlich haben Milchbestandteile wie Glykomakropeptid antiinflammatorische Eigenschaften.</p> <p><strong>Keine gesüßten Limonaden</strong><br /> Zugeführte Fruktose wird in der Leber phosphoryliert, wodurch ATP verbraucht und über Adenin zu Harnsäure abgebaut wird. Zusätzlich führt Fruktose zu einer erhöhten Insulinresistenz und zu einer Gewichtszunahme.</p> <p><strong>Kaffeekonsum</strong><br /> Regelmäßiger Kaffeekonsum senkt die Serumharnsäure und damit das Auftreten von Gichtanfällen. Wahrscheinlich wirken Inhaltsstoffe des Kaffees über eine Verminderung der Insulinresistenz und eine Hemmung der Xanthinoxidase.</p> <p><strong>Vitamin-C-Gabe</strong><br /> Die Einnahme von Vitamin C vermindert die Serumharnsäure, wobei eine Risikominderung bei einer Dosis von mindestens 500mg pro Tag auftritt.</p></p>
<p class="article-footer">
<a class="literatur" data-toggle="collapse" href="#collapseLiteratur" aria-expanded="false" aria-controls="collapseLiteratur" >Literatur</a>
<div class="collapse" id="collapseLiteratur">
<p>beim Verfasser</p>
</div>
</p>
Das könnte Sie auch interessieren:
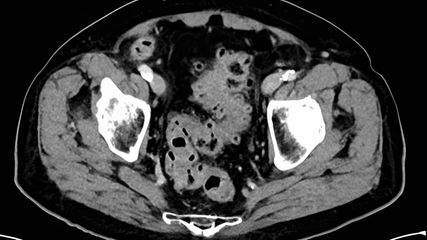
Behandlung der Sigmadivertikulitis
Die Divertikulitis gehört zu den häufigsten Krankheitsbildern bei akuten Bauchschmerzen. Die Inzidenz nimmt mit dem Alter stark zu und immer mehr jüngere Patienten erkranken an einer ...
Therapie des Morbus Crohn: bewährte Konzepte und neue Strategien
Welche Behandlungsziele haben Ärzt:innen, die Patient:innen mit Morbus Crohn (MC) behandeln, und haben die Betroffenen die gleichen Ziele? Lassen sich die Therapieziele erreichen, wenn ...
Therapie des Morbus Crohn: Biologikabehandlung optimieren
Prof. Dr. med. Iris Dotan, Rabin Medical Center, Petah Tikva, und Universität Tel Aviv (Israel), zeigte im Rahmen des 9. Postgraduate Course des IBDnet Möglichkeiten auf, wie die ...