
Metastasen-direktive Therapie beim Prostatakrebsrezidiv
Martini-Klinik, Universitätsklinikum <br>Hamburg-Eppendorf<br>Klinik für Urologie<br>E-Mail: t.maurer@uke.de
Martini-Klinik, Universitätsklinikum <br>Hamburg-Eppendorf
Martini-Klinik, Universitätsklinikum <br>Hamburg-Eppendorf
Martini-Klinik, Universitätsklinikum <br>Hamburg-Eppendorf<br>Klinik für Urologie
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Durch die verbesserte Detektionsrate hat sich die PSMA-PET in den letzten Jahren zunehmend als bildgebende Standarduntersuchung beim biochemischen Rezidiv eines Prostatakarzinoms etabliert. Gerade bei singulärer oder limitierter Metastasierung werden gezielte Metastasen-direktive Therapien (MDT) immer häufiger sowohl von Patienten als auch von behandelnden Ärzten nachgefragt.
Keypoints
-
Die PSMA-PET ermöglicht die Detektion von Prostatakrebsmetastasen bereits bei niedrigen PSA-Werten im Rezidivfall.
-
Bei Patienten mit niedrigem PSA, gutem Allgemeinzustand und singulärer bzw. limitierter Metastasierung in der PSMA-PET kann eine gezielte Metastasen-direktive Therapie (MDT) als individuelle Therapie erwogen werden.
-
Ziele der MDT sind Verhinderung von Komplikationen, Verlängerung des progressionsfreien Überlebens bzw. dasHinauszögern einer systemischen Therapie (Hormontherapie).
-
Die Entwicklung von intraoperativ nutzbaren PSMA-Liganden („PSMA-radioguided surgery“) erleichtert das Auffinden von kleinen bzw. atypisch gelegenen Prostatakarzinommetastasen bei Salvage-Operationen.
Aktuell beeinflusst die Positronenemissionstomografie (PET) in einem hohen Maße die Bildgebung des Prostatakarzinoms – vor allem seit dem Einsatz von Tracern, die gegen das meist auf Prostatakrebszellen deutlich überexprimierte Prostata-spezifische Membranantigen (PSMA) gerichtet sind.6 Im Rezidivfall kann die PSMA-PET bereits wesentlich früher und bei niedrigeren PSA-Werten Metastasen nachweisen, als wir dies durch die konventionelle Bildgebung mittels CT, MRT oder Knochenszintigrafie gewohnt waren.2 Durch diese genauere Diagnostik und Möglichkeit einer früheren Detektion, die in einigen Fällen nur eine singuläre oder limitierte Metastasierung zeigt, stellt sich die Frage, ob in solchen Fällen nicht eine gezielte Metastasen-gerichtete Therapie (MDT) zum Einsatz kommen sollte. Folgerichtig wird daher gegenwärtig die PSMA-PET sowohl von der deutschen S3-Leitlinie als auch von den Guidelines der European Association of Urology (EAU) für diese Indikation empfohlen.5, 9 Während eine unauffällige PSMA-PET zwar die weitere Therapie in der Regel nicht beeinflusst, kann sie bei Detektion einer Metastasierung Patienten eine offensichtlich ungenügende Lokaltherapie nicht nur ersparen (z.B. durch Vermeidung einer alleinigen lokalen Salvagebestrahlung der Prostataloge nach radikaler Prostatektomie bei Nachweis einer regionären oder Fernmetastasierung), sondern auch eine gezielte Behandlung der Metastasen ermöglichen.
Dabei verfolgt eine MDT unterschiedliche Ziele. Zum einen soll das Auftreten von Komplikationen durch beispielsweise pathologische Brüche metastatischer Knochen oder eine Kompression von Blutgefäßen durch Weichteilmetastasen verhindert oder zumindest verzögert werden (Abb. 1). Zum anderen zielt eine MDT vor allem darauf ab, Systemtherapien hinauszuzögern und den Patienten eine therapiefreie Zeit zu ermöglichen, wenngleich eine langfristige Heilung wohl nur bei einem geringen Prozentsatz der Patienten erreicht werden kann.
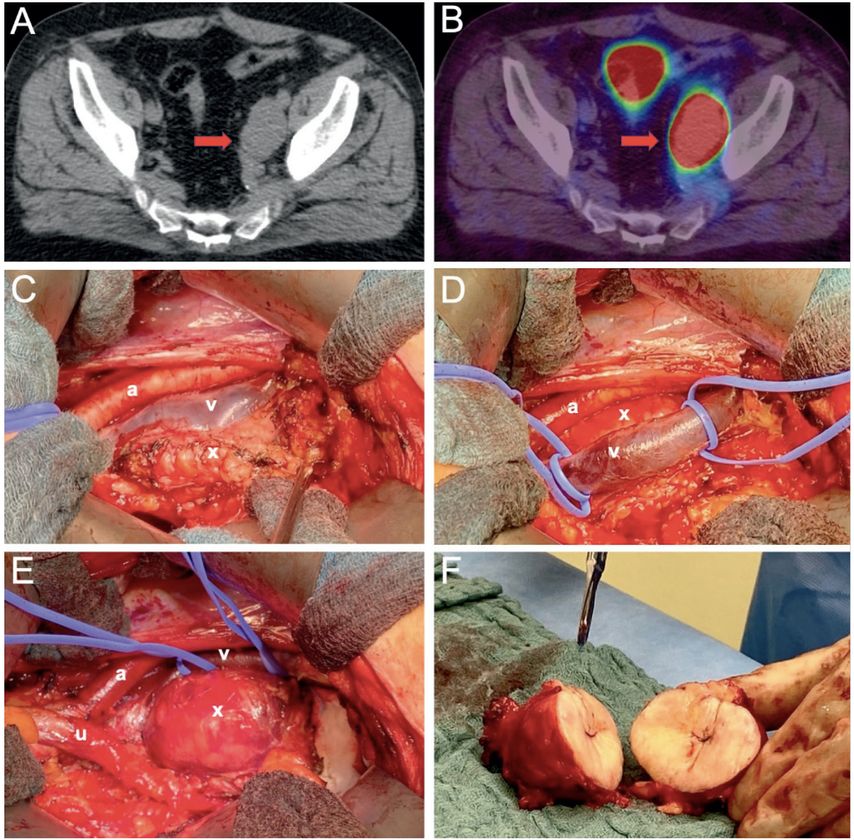
Abb. 1: 67-jähriger Patient nach radikaler Prostatektomie bei Prostatakarzinom pT3a pN1 (1/8) R0 Gleason-Score 4+3 mit initialem PSA-Wert von 5,6ng/ml. Native CT(A)- und PSMA-PET-Fusionsbildgebung (B) mit Nachweis einer großen linksseitigen singulären Lymphknotenmetastase (Pfeil) bei postoperativ persistierenden und rasch progredienten PSA-Werten auf 10,4 ng/ml. Intraoperativ zeigte sich eine subtotale Kompression der V. iliaca externa durch die Lymphknotenmetastase (C). Nach sorgfältiger Dissektion der Gefäße mit Anschlingen der V. iliaca externa (D) kann schließlich die Metastase in toto entfernt werden (E). Die postoperative Histologie nach Salvage-Lymphadenektomie zeigte eine solitäre Lymphknotenmetastase bei insgesamt 26 entfernten Lymphknoten (F). 4 Wochen postoperativ zeigte sich ein kompletter PSA-Abfall <0,2 ng/ml. (a: Arteria iliaca externa; v: Vena iliaca externa; u: Ureter; x: Lymphknotenmetastase)
Studien zum Einsatz stereotaktischer Strahlentherapie
In einer der ersten prospektiven Studien zur MDT mittels stereotaktischer Strahlentherapie (STOMP) konnte ein aufschiebender Effekt einer Hormonbehandlung im Vergleich zu einer Kontrollgruppe gezeigt werden.10 Insgesamt wurden 62 Patienten mit Oligometastasierung meist auf Grundlage einer konventionellen oder cholinbasierten PET in die zweiarmige Phase-II-Studie eingeschlossen. Bei insgesamt geringer Toxizität konnte eine Verzögerung der Notwendigkeit einer Hormontherapie im Median um 8 Monate erreicht werden (13 vs. 21 Monate).
In einer weiteren strahlentherapeutischen Studie, der SABR-COMET Studie, in die neben Patienten mit anderenTumorentitäten auch 16 Prostatakrebspatienten eingeschlossen wurden (wiederum auf Grundlage einer konventionellen Bildgebung), zeigte sich ein längeres Überleben nach MDT als unter alleiniger palliativen Behandlung.11
Im Rahmen der prospektiven ORIOLE-Studie (Phase-II-Studie) wurden 54 Patienten mit hormonsensitivem Prostatakarzinomrezidiv behandelt.12 Hier wiesen alle Patienten 1 bis 3 Metastasen in der konventionellen Bildgebung auf. Es zeigte sich eine Progression bei 7 von 36 (19%) der Bestrahlungsgruppe und bei 11 von 18 (61%) in der Kontrollgruppe nach 6 Monaten (p=0,005). Das mediane progressionsfreie Überleben wurde in der Bestrahlungsgruppe noch nicht erreicht und betrug in der Kontrollgruppe 5,8 Monate (p=0,002). Auch hier wurde keine höhergradige Toxizität durch die Bestrahlung beobachtet. Interessant bei dieser Studie ist, dass parallel zur Standardbildgebung jeweils PSMA-PET-Untersuchungen durchgeführt wurden, wobei für die Beurteilung die Strahlentherapeuten jedoch verblindet waren. Nach Korrelation der Ergebnisse der PSMA-PET-Bildgebung mit dem progressionsfreien Überleben nach 6 Monaten zeigte sich, dass nur bei 1 von den 19 Patienten, bei denen alle in der PSMA-PET verdächtigen Läsionen durch die Strahlentherapie erfasst wurden, eine Progression nach 6 Monaten festgestellt wurde. Im Gegensatz dazu wiesen 6 von den 16 Patienten, bei denen nicht sämtliche in der PSMA-PET verdächtigen Läsionen bestrahlt wurden, eine Progression auf. Dies wiederum unterstreicht die Bedeutung einer PSMA-PET-Bildgebung gerade für die MDT und zeigt, dass eine MDT möglichst nicht nur auf Grundlage einer konventionellen Bildgebung erfolgen sollte. Bemerkenswert ist zudem, dass in die Studie bereits Patienten mit etwas fortgeschrittener Erkrankung eingeschlossen wurden, was sich in den bereits höheren medianen PSA-Werten (6 bzw. 7ng/ml im Median) widerspiegelt. Trotz dieser Voraussetzungen zeigte sich eine niedrigere Progressionsrate in der strahlentherapeutisch behandelten Gruppe, obwohl die Autoren einschränkend angaben, dass durch die stereotaktische Strahlentherapie meist kein komplettes PSA-Ansprechen erreicht werden konnte.
Studien zum Einsatz von Salvage-Chirurgie
Die MDT mittels Salvage-Chirurgie unterscheidet sich in einigen Aspekten vom strahlentherapeutischen Ansatz. Während ein Großteil der Patienten, die mittels Strahlentherapie im Rezidivfall behandelt werden, bereits eine ossäre Metastasierung aufweist, ist dies in der Salvage-Chirurgie fast nie der Fall, da hier der Hauptfokus in der Regel auf der Entfernung einer limitierten lymphogenen Weichteilmetastasierung liegt. Darüber hinaus weisen die behandelten Patienten meist niedrigere PSA-Werte auf und befinden sich in einem früheren Rezidivstadium, wodurch die MDT mittels Salvage-Operation nicht nur eine Verlängerung des therapiefreien Verlaufs, sondern darüber hinaus auch ein komplettes und möglichst dauerhaftes PSA-Ansprechen zum Ziel hat. Während die Salvage-Lymphadenektomie auch schon vor der PSMA-PET-Ära eingesetzt wurde, zeigten sich nach initial vielversprechenden Ergebnissen längerfristigjedoch teilweise ernüchternde Verläufe.1Ursachen hierfür sind vor allem das Fehlen einer PSMA-PET als „Gatekeeper“ sowie der Einschluss von Patienten mit bereits höheren PSA-Werten. Eine sorgfältige Patientenauswahl anhand klinischer Parameter und auf Grundlage einer PSMA-PET führt daher zu besseren Ergebnissen. Ebenso können die eindeutige Detektion und sichere Resektion der oftmals kleinen und teilweise atypisch lokalisierten Lymphknotenmetastasen herausfordernd sein. Durch Weiterentwicklung der für die PSMA-PET verwendeten Tracer und durch Markierung mit Gammastrahlern (z.B. mit dem in der nuklearmedizinischen Diagnostik weit verbreiteten Radiopharmakon 99mTechnetium) besteht nun zusätzlich die Möglichkeit, Prostatakarzinomzellen molekular für die intraoperative Detektion zu markieren.3, 7, 8, 13 Insbesondere diese intraoperative Detektionsmöglichkeit nach PSMA-spezifischer radioaktiver Markierung erleichtert eine erfolgreiche Resektion der Metastasen. Nach Entwicklung des Verfahrens wurde die „PSMA-radioguided surgery“ erstmalsim April 2014 in der klinischen Therapie eingesetzt.
In einer ersten vergleichenden Arbeit zu Salvage-Lymphadenektomie mit bzw. ohne Einsatz der „PSMA-radioguided surgery“ wurde beschrieben, dass sich bei 9 von 29 konventionell operierten Patienten (31%) auf Grundlage einer auffälligen PSMA-PET kein histologischer Nachweis von metastatischem Prostatakrebsgewebe zeigte, während bei allen 13 Patienten, die mittels „PSMA-radioguided surgery“ operiert wurden, die Histologie Prostatakrebsgewebe erbrachte.4 Dies spiegelte sich auch im postoperativen PSA-Ansprechen wider: Ein PSA-Abfall >50% bzw. 90% zeigte sich bei 29% und 7% der konventionell operierten Patienten vs. 92% und 53% bei den Patienten mit „PSMA-radioguided surgery“ (p<0,01).
Die bisher größte von uns publizierte Serie beschreibt 121 Patienten, bei denen in nahezuallen Fällen (99%) die in der PSMA-PET auffälligen und histologisch verifiziert metastatischen Läsionen detektiert und reseziert werden konnten.3 Ein kompletter PSA-Abfall auf <0,2ng/ml ohne weitere prostatakrebsspezifische Therapie zeigte sich dabei bei 66% der Patienten postoperativ. Das mediane biochemischrezidivfreie bzw. therapiefreie Überleben in dieser Gruppe betrug ca. 6 und >18 Monate. Dabei ist zu beachten, dass sowohl mittels PSMA-PET als auch „PSMA-radioguided surgery“ kleine, nur wenige Millimeter messende Lymphknotenmetastasen übersehen werden können, sodass bei einer Salvage-Lymphadenektomie auch das umgebende Gewebe im unmittelbarem Lymphabfluss trotz negativer PSMA-PET bzw. negativer intraoperativer Messung bei „PSMA-radioguided surgery“ mitentfernt werden sollte.
Laufende Forschungsarbeiten
Weitere Untersuchungen, am besten im Rahmen prospektiver Studien, sind jedoch notwendig, um den Stellenwert der aktuell noch experimentell einzuordnenden MDT festlegen zu können. Um beispielsweise für eine Salvage-Lymphadenektomie geeignete Patienten zukünftig noch besser identifizieren zu können, könnten neben den oben bereits erwähnten klinischen Parametern (Ergebnis der PSMA-PET-Untersuchung, niedriger PSA-Wert) gegebenenfalls weitere Biomarker zum Einsatz kommen, die auf eine bereits systemische Erkrankung hinweisen.
Im Rahmen der von uns initiierten prospektiven BioPoP-Studie (NCT 04324983) werden zu diesem Zweck neue Biomarker wie beispielsweise zirkulierende Tumorzellen (CTC), extrazelluläre Vesikel oder zirkulierende DNA untersucht.
Auch ist bisher nicht geklärt, ob bei nur einseitig positiver PSMA-PET-Untersuchung im Rezidivfall eine beidseitige Salvage-Lymphadenektomie durchgeführt werden muss, was aktuell als Standard angesehen wird. Diese Frage soll in der prospektiven ProSTone-Studie (NCT 04271579) geklärt werden, in die Patienten mit bis zu 3 PSMA-PET-positiven unilateral gelegenen Lymphknoten und einem maximalen PSA-Wert von 4ng/ml eingeschlossen werden können. Im Rahmen der Studie erhalten die Patienten entweder eine beidseitige oder einseitige Salvage-Lymphadenektomie (1:1-Randomisierung). Primärer Endpunkt ist das biochemischrezidivfreie Überleben nach 2 Jahren.
Fazit
Obwohl aktuell die MDT beim Prostatakarzinomrezidiv noch nicht als leitlinienkonforme, sondern experimentelle Therapie anzusehen ist, wächst das Interesse an einer solchen gezielten Therapie – gerade weil mit der PSMA PET eine sensitive und spezifische Bildgebung zur Verfügung steht. Der genaue Stellenwert der MDT, sei es durch gezielte Strahlentherapie oder Operation, muss jedoch im Rahmen prospektiver Studien geklärt werden.
Literatur:
1 Bravi CA et al.: Long-term Outcomes of salvage lymph node dissection for nodal recurrence of prostate cancer after radical prostatectomy: not as good as previously thought. EurUrol2020; S0302-2838(20)30472-3. doi: 10.1016/j.eururo.2020.06.043 2 Fendler WP et al.: Assessment of 68Ga-PSMA-11 PET accuracy in localizing recurrent prostate cancer: aprospective single-arm clinical trial. JAMA Oncol2019; 5: 856-63 3 Horn T et al.: Single lesion on prostate-specific membrane antigen-ligand positron emission tomography and low prostate-specific antigen are prognostic factors for a favorable biochemical response to prostate-specific membrane antigen-targeted radioguided surgery in recurrent prostate cancer. EurUrol2019; 76: 517-23 4 Knipper S et al.:Metastases-yield and prostate-specific antigen kinetics following salvage lymph node dissection for prostate cancer: acomparison between conventional surgical approach and prostate-specific membrane antigen-radioguided surgery. Eur Urol Focus 2018; 5(1): 50-3 5 Leitlinienprogramm Onkologie (Deutsche Krebsgesellschaft, Deutsche Krebshilfe, AWMF): Interdisziplinäre Leitlinie der Qualität S3 zur Früherkennung, Diagnose und Therapie der verschiedenen Stadien des Prostatakarzinoms, Langversion 5.1, 2019, AWMF Registernummer: 043/022OL, http://www.leitlinienprogramm-onkologie.de/leitlinien/prostatakarzinom/ (abgerufen am: 15.05.2020). 6 Maurer T et al.: [PSA increase after definitive treatment]. Urologe A 2019; 58:569-82 7 Maurer T et al.: (99m)Technetium-based Prostate-specific membrane antigen-radioguided surgery in recurrent prostate cancer. Eur Urol2018; 75(4): 659-66 8 Maurer T et al.: Prostate-specific membrane antigen-radioguided surgery for metastatic lymph nodes in prostate cancer. Eur Urol2015; 68: 530-4 9 Mottet N et al.: EAU - ESTRO - ESUR - SIOG Guidelines on prostate cancer2020. https://uroweb.org/guideline/prostate-cancer/ (abgerufen am 10.07.2020) 10 Ost P et al.: Surveillance or metastasis-directed therapy for oligometastatic prostate cancer recurrence: aprospective, randomized, multicenter phase iitrial. JClinOncol 2018; 36: 446-53 11 Palma DA et al.: Stereotactic ablative radiotherapy for the comprehensive treatment of oligometastatic cancers: long-term results of the SABR-COMET phase iirandomized trial. J Clin Oncol2020; Jco2000818. doi: 10.1200/JCO.20.00818 12 Phillips R et al.: Outcomes of observation vs stereotactic ablative radiation for oligometastatic prostate cancer: The ORIOLE phase 2 randomized clinical trial. JAMA Oncol2020; 6: 650-9 13 Rauscher I et al.:Value of (111) In-prostate-specific membrane antigen (PSMA)-radioguided surgery for salvage lymphadenectomy in recurrent prostate cancer: correlation with histopathology and clinical follow-up. BJU Int 2017; 120: 40-7
Das könnte Sie auch interessieren:
Aktuelle Entwicklungen und Erkenntnisse beim Urothelkarzinom
Auf dem diesjährigen Genitourinary Cancers Symposium der American Society of Clinical Oncology (ASCO-GU-Kongress) wurden bedeutende Fortschritte in der Diagnose und Behandlung des ...
Aktuelles aus der 7. Version der S3-Leitlinie: wesentliche Leitlinienänderungen
Im Mai 2024 wurde die Prostatakarzinom-S3-Leitlinie unter der Federführung der Deutschen Gesellschaft für Urologie e.V. (DGU) im Rahmen des Leitlinienprogramms Onkologie in ihrer 7. ...
Neues vom ASCO GU zum Prostatakarzinom
Im Rahmen des ASCO GU 2025 in San Francisco wurden eine Vielfalt von neuen praxisrelevanten Studien zum Prostatakarzinom präsentiert. Mit Spannung wurde unter andem auch auf die finalen ...


