Infektprophylaxe bei der Prostatabiopsie
Autoren:
Dr. Mathias Tischler
OA Dr. Andreas Lunacek
Abteilung für Urologie
Hanusch-Krankenhaus, Wien
E-Mail: mathias.tischler@oegk.at
Steht eine Ablöse der transrektalen Biopsie bevor? Diese war lange Zeit unbestrittener Standard in der Diagnose des Prostatakarzinoms. Eine steigende Rate schwerer Infektkomplikationen und die Indikationseinschränkung für Fluorchinolone erfordern umfangreiche Anpassungen.
Keypoints
-
Aufgrund günstigerer Infektionsraten empfiehlt die EAU nun vorrangig die transperineale Prostatabiopsie.
-
Die Zulassungsbeschränkung der EU für Fluorchinolone umfasst die antibiotische Prophylaxe bei der Prostatabiopsie.
-
Eine alternative fluorchinolonfreie Prophylaxe mit Aminoglykosiden, Cephalosporinen oder Fosfomycin (z.B. 3g p.o. am Vorabend und 24h darauf) ist empfohlen.
-
Ebenso möglich sind eine augmentierte Prophylaxe (zwei oder mehr Substanzklassen) sowie eine zielgerichtete Prophylaxe nach Rektalabstrich/Stuhlkultur.
-
Eine rektale Vorbereitung mit Povidon-Iod ist bei transrektaler Biopsie empfohlen.
-
„Antibiotic stewardship“ ist notwendig, um der weiteren Ausbreitung multiresistenter Keime zu begegnen.
Die in der Literatur beschriebenen Infektionsraten in Zusammenhang mit der transrektalen Prostatabiopsie variieren aus unterschiedlichen Gründen (Zeitraum der Untersuchung, Endpunkte, Methodik, regionale Unterschiede etc.) dramatisch zwischen 0,1% und 36%.1,2 Mangels einer nationalen Auswertung muss für Österreich auf Daten anderer westlicher Länder zurückgegriffen werden. Infektiöse Komplikationen infolge einer transrektalen Biopsie treten demnach bei rund 5% auf. Bei 1–3% der Patienten erfolgt eine Hospitalisierung aufgrund einer Infektion und vereinzelt sind auch tödliche Verläufe beschrieben.3 Diese Infektionen verlaufen vereinzelt auch tödlich.4–6 Leider zeigen lokale, europäische und internationale Untersuchungen übereinstimmend einen besorgniserregenden Anstieg der Infektions- und Hospitalisierungsrate, was wiederum unzweifelhaft mit der Ausbreitung antibiotikaresistenter Darmkeime in Zusammenhang steht.6–8 In den 1990er- und frühen 2000er-Jahren war in den USA die Rate der Chinolon-Resistenzen von E. coli noch verschwindend gering. Inzwischen werden Raten von 10–22% beschrieben.1,9,10 In einer rezenten norwegischen Studie wurden gar Resistenzraten bis 40% festgestellt.5
Neue EAU-Leitlinie 2021
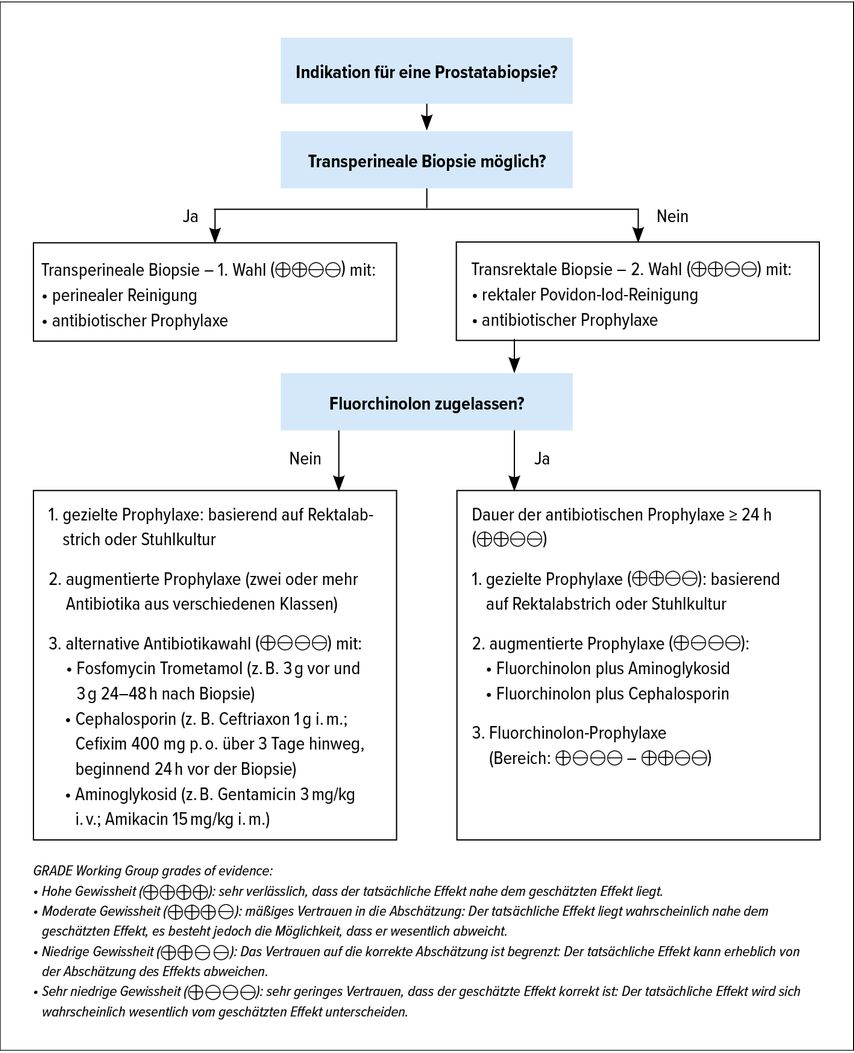
Die Leitliniengruppe Urologische Infektionen der EAU (ESIU) publizierte rezent zwei Metaanalysen von randomisiert-kontrollierten Studien (RCTs) zu antibiotischen und nicht antibiotischen Maßnahmen zur Reduktion von Infektionskomplikationen im Rahmen der transrektalen Prostatabiopsie.11,12 Diese Ergebnisse flossen entscheidend in die umfangreiche Überarbeitung der Empfehlungen zur Prostatabiopsie in den Prostatakarzinom-Leitlinien der Europäischen Gesellschaft für Urologie (EAU) ein.13 Anhand des darin enthaltenen Flowcharts (Abb.1) sollen die Maßnahmen inklusive Hintergrund im Folgenden Schritt für Schritt besprochen werden.
Abb. 1: Prostatabiopsie-Workflow zur Reduzierung infektiöser Komplikationen (übersetzt aus EAU Guidelines on Prostate Cancer 2021)
Transperineal first?
Ist die Entscheidung für die Durchführung einer Prostatabiopsie gefallen, so präferiert die EAU nunmehr als erste Wahl den transperinealen Zugangsweg gegenüber der transrektalen Biopsie. Diese Empfehlung fußt vorrangig auf der laut Metaanalyse von 7 RCTs halbierten Rate infektiöser Komplikationen (relatives Risiko [RR]: 0,55; 95%-Konfidenzintervall [CI]: 0,33–0,92).12 Allerdings zeigte eine Datenbankauswertung von über 70000 Biopsien aus England ein gemischtes Bild mit einer nur um 0,4% gesenkten Sepsisrate bei transperinealer Biopsie (1,0% vs. 1,4%), während eine Harnverhaltung mit Hospitalisierung häufiger auftrat (1,9% vs. 1,0%).14 Auch wenn mangels Randomisierung oder zumindest gematchter Kohorten diese retrospektiven Daten mit Vorsicht zu interpretieren sind, war in dieser Untersuchung die Rehospitalisierungsrate nach transperinealer Biopsie gesamt höher als nach transrektaler Biopsie. Die Amerikanische Urologische Gesellschaft (AUA) empfiehlt aufgrund des noch unklaren Bildes zur Gesamtkomplikationsrate ebenso wie die deutsche S3-Leitlinie bisher keinen Zugangsweg bevorzugt.1,15
Transrektal dominiert (noch?)
Zurzeit erfolgen österreichweit betrachtet in den urologischen Abteilungen der Krankenhäuser über 90% der Biopsien transrektal (Stand Oktober 2021, eigene Umfrage, Rücklaufquote 77%). Im niedergelassenen Bereich darf ein noch deutlicherer Überhang des transrektalen Zugangsweges angenommen werden. Vor einer etwaigen Anpassung des Verfahrens sind neben der abschließenden wissenschaftlichen Beurteilung auch noch Fragen der Versorgung und der Ausbildung zu lösen.
Weitere Vorzüge transperinealer Biopsie
Bei aller berechtigten Skepsis sollten die Fortschritte bei der transperinealen Biopsie und Argumente für sie keineswegs außer Acht gelassen werden. Neben dem durch Aussparung des Darmtrakts verminderten Risiko für infektiöse Komplikationen deuten Studien insbesondere bei weit apikal gelegenen Läsionen auf eine höhere Trefferquote klinisch signifikanter Tumoren hin.16 Frühere generelle Bedenken in Bezug auf die Durchführbarkeit in lokaler Anästhesie sind jedenfalls in erfahrenen Händen als überholt zu werten.17 In Fallserien wurden sehr niedrige Infektionsraten bei der transperinealen Biopsie auch ohne prophylaktische Antibiose beschrieben.18 Sollte sich dies unter der Bedingung einer negativen Harnkultur auch in randomisierten Studien (z.B. NCT04146142) als sicher erweisen, wäre dies ein weiteres stichhaltiges Argument für einen vorrangigen Einsatz der transperinealen Biopsie.
Indikationsbeschränkung für Fluorchinolone
Im März 2019 schränkte die Europäische Kommission nach umfangreicher Prüfung durch die Europäische Arzneimittelbehörde (EMA) das Anwendungsgebiet für Fluorchinolone deutlich ein.19 Diese Indikationsbeschränkung betrifft die prophylaktische Gabe im Rahmen von Prostatabiopsien in der gesamten EU.20
Basis der Entscheidung war die Erkenntnis, dass schwerwiegende Nebenwirkungen auf den Bewegungsapparat sowie das periphere und zentrale Nervensystem auftreten können, welche lang anhaltend und möglicherweise irreversibel sind. Die gemeldete Frequenz beträgt zwar lediglich 1:10 Millionen Tagesdosen, jedoch ist von einer nennenswerten Dunkelziffer auszugehen, da die beschriebenen Nebenwirkungen teils unspezifisch sind (chronische Muskelschmerzen, Tendinitis, Polyneuropathie, Schlafstörungen) und aufgrund des beschriebenen Mechanismus einer mitochondrialen Schädigung vereinzelt auch erst Monate nach der Anwendung auftreten. Es kann dennoch mit großer Sicherheit angenommen werden, dass die Frequenz sehr gering ist (<1:10000) und bei kürzerer Anwendung ein geringeres Risiko besteht.
Insbesondere bei mikrobiologisch bestätigter Sensibilität ist beispielsweise in den Niederlanden die Anwendung weiterhin durch die nationale Arzneimittelbehörde gedeckt. In Deutschland wurde den Fluorchinolonen die Zulassung zur Prophylaxe bei der Prostatabiopsie durch das BfArM explizit entzogen, während diese für die Anwendung im Falle einer Prostatitis unverändert aufrechtbleibt. In Österreich ist die Off-Label-Anwendung aufgrund der langjährigen Erfahrung noch vielfach angewandte Praxis, es verbleibt aber eine rechtliche Unsicherheit.
Alternative Antibiotika
Bisher hat sich kein neuer Goldstandard als Alternative zu den Fluorchinolonen herauskristallisiert. Im Rahmen einer transperinealen Biopsie empfiehlt die EAU mangels RCTs aus der gängigen Praxis die Single-Shot-Prophylaxe mit Cefuroxim, Cephalexin oder Cephazolin, im Falle einer Penicillinallergie eventuell mit Sulfametoxazol.13 Eine randomisiert-kontrollierte Studie (NCT04146142) sollte im Laufe dieses Jahres Ergebnisse dahingehend liefern, ob transperineal auf eine Antibiose auch ganz verzichtet werden kann.
Fosfomycin
Die Datenlage zu den antibiotischen Optionen bei der transrektalen Biopsie wurde durch Pilatz et al. einer Metaanalyse unterzogen.12 Fosfomycin-Trometamol erscheint als attraktive Alternative, da es über eine zufriedenstellende orale Bioverfügbarkeit verfügt und lange Wirkspiegel in der Prostata und im Harn aufweist.21 Die Metaanalyse ergab gegenüber Fluorchinolonen ein halbiertes Infektionsrisiko (relatives Risiko [RR]: 0,49; 95% CI: 0,27–0,87). Allerdings zeigte eine kanadische Kohortenstudie mit mehr als 9000 Patienten ein differenzierteres Bild: Obwohl dort nachweislich sehr niedrige Resistenzraten von E.coli gegenüber Fosfomycin vorliegen,22 war die Rate der Infektkomplikationen unter Fosfomycin höher als unter Ciprofloxacin.23 Dies dürfte maßgeblich mit der niedrigeren Fluorchinolon-Resistenzrate im Vergleich zu den in der Metaanalyse eingeschlossenen Studien liegen.
Unsere eigene Erfahrung aus mehreren hundert Rektalabstrichen ergab eine solche niedrige Chinolon-Resistenzrate von ca. 10%. Daher kann aktuell auch für Fosfomycin noch keine abschließende und uneingeschränkte Empfehlung gegeben werden. Hinsichtlich der Dosierung zeigt die Erfahrung, welche aus Studien mit Ciprofloxacin generiert wurde, dass eine Abschirmung für 24h einer Einmalgabe überlegen ist, während der Benefit einer längeren Anwendung fraglich erscheint und gegen die Nachteile aufgewogen werden muss. Vorbehaltlich neuer Evidenz, die von der EU-Kommission zur Rechtfertigung der 2. Gabe gegenüber einer Single-Shot-Prophylaxe eingefordert wurde, erscheint es aus den pharmakokinetischen/ -dynamischen Daten21,24 und der begrenzten Evidenz umsichtig, 2 prophylaktische Dosen zu je 3g Fosfomycin-Trometamol p.o. zu verschreiben, beispielsweise am Vorabend der Biopsie sowie 24h später.
Aminoglykoside und Cephalosporine
Weitere Alternativen, welche sich in jeweils zwei RCTs als gleichwertig zu Fluorchinolonen zeigten, sind prophylaktische Antibiotikaschemata von Aminoglykosiden und Cephalosporinen.12 Konkret wurden Gentamicin (3mg/kg i.v. vor der Biopsie), Amikacin (15mg/kg i.m. 1 bis 2h vor der Biopsie) sowie Ceftriaxon (1g i.m. 30min vor der Biopsie) und Cefixim (400mg p.o. täglich für 3 Tage ab dem Vortag der Biopsie) untersucht.
Zielgerichtete Prophylaxe
Die zielgerichtete Prophylaxe basiert auf einem Rektalabstrich beziehungsweise einer Stuhlkultur. Die antibiotische Abschirmung wird an das Antibiogramm angepasst. Unter Fluorchinolon-Monoprophylaxe traten in der Metaanalyse mehr als doppelt so häufig Infektionen auf wie unter gezielter Therapie (RR: 2,1; 95% CI: 1,53–2,88).12 Allerdings liegen keine Daten zur zielgerichteten Prophylaxe gegenüber anderen Substanzklassen als Fluorchinolonen vor. Gerade bei Verwendung von Fosfomycin ist die Interpretation erschwert und der Benefit der Nutzung von Rektalabstrichen noch ungewiss, da einerseits die Resistenzraten von E.coli äußerst niedrig sind und andererseits mangels validierter Breakpoints des Europäischen Komitees zur antimikrobiellen Empfindlichkeitstestung (EUCAST) eine Resistenzbestimmung für andere Darmkeime aktuell (EUCAST Breakpoint Tables, Version 11.0) nicht bzw. nicht mehr möglich ist. In der Praxis bedeutet dies, dass sich Fosfomycin trotz seiner unbestrittenen Wirksamkeit gegenüber einer Vielzahl von Darmkeimen nicht auf dem Antibiogrammbefund wiederfindet, was zu Schwierigkeiten in der korrekten Interpretation führen kann.
Augmentierte Prophylaxe
Die Option, mehrere Substanzklassen von Antibiotika zur Prophylaxe zu kombinieren, findet in den Guidelines explizite Erwähnung, da eine Metaanalyse von 10 RCTs einen Benefit gegenüber der Monoprophylaxe zeigte.25 Zwei valide Argumente sprechen aber dagegen, solch ein Schema generell zu verwenden: Einerseits hat diese Studienlage Fluorchinolon-basierte oder veraltete Antibiotikakombinationen als Grundlage und andererseits widerspricht die Kombination von Antibiotika in der prophylaktischen Anwendung den Prinzipien des „antibiotic stewardship“. Rational hingegen erscheint beim Risikopatienten eine gezielte Kombinationstherapie angepasst an das Resistenzmuster der im Abstrich nachgewiesenen Keime, sofern kein optimales Monopräparat das Spektrum abdeckt.
Nicht antibiotische Infektprophylaxe
Die umfangreiche Aufarbeitung bezüglich des Einflusses technischer Aspekte der transrektalen Biopsie (Nadeltyp, Zylinderanzahl, Infiltrationsanästhesie etc.) konnte für keinen Faktor eine signifikante Auswirkung auf das Auftreten von Infektkomplikationen ausmachen.11 Als einzige nicht antibiotische Maßnahme, die nach Metaanalyse der RCTs eine Infektreduktion bewirkt, stellt sich die antiseptische Darmvorbereitung mit Povidon-Iod (Betaisodona®) dar (RR: 0,50; 95% CI: 0,38–0,65). Jedoch ist festzustellen, dass die qualitativ hochwertigste Studie von Abughosh et al. in Kanada keinen signifikanten Unterschied fand, allerdings möglicherweise underpowert war.26 Die Datenbasis der Metaanalyse stammt zum Großteil aus außereuropäischen Studien mit außergewöhnlich hohen Komplikationsraten, weshalb eine gewisse Restunsicherheit in Bezug auf die Wertigkeit bestehen bleibt. Darüber hinaus ist die beste Applikationsform (Einlauf, Suppositorium, getränkter Tupfer) ungeklärt. Dies erklärt wohl, warum nach einer durch den Autor durchgeführten Umfrage an urologischen Abteilungen in Österreich bisher nur ein Drittel der Abteilungen (Stand Oktober 2021, Rücklaufquote 77%) dies in ihr Standardprozedere aufgenommen hat. Zwei Abteilungen berichteten ebenso wie die Autoren der erwähnten kanadischen Studie, aufgrund des Zusatzaufwandes bei fehlender Beobachtung eines gesicherten Benefits im eigenen Kollektiv die Praxis wieder verlassen zu haben. Die rektale Darmvorbereitung mit Povidon-Iod stellt, bei fehlender Iod-Allergie, eine sichere und kostengünstige Maßnahme dar. Die Wirksamkeit ist neben der erwähnten Metaanalyse auch durch mikrobiologisch nachgewiesene Keimreduktion im Enddarm untermauert27 und daher deren Anwendung durch die EAU-Guidelines klar empfohlen.
Ausblick
Multiresistente Keime verursachen in der gesamten Medizin in zunehmender Zahl lebensgefährliche Infektionen28 und werden auch für die Routinediagnostik wie die Prostatabiopsie zur zunehmenden Gefahr.5 Der Anstieg der Zahl infektiöser Komplikationen durch massiv gesteigerte Resistenzraten am Beispiel der Fluorchinolone sollte der Urologie und der Medizin im Allgemeinen auch als warnendes Beispiel dienen, um mittels verantwortungsvollen, zielgerichteten Antibiotikaeinsatzes („antibiotic stewardship“) ähnliche Entwicklungen in anderen Substanzgruppen wie beispielsweise bei Fosfomycin29 möglichst lange hintanzuhalten.
Literatur:
1 Liss MA et al.: An update of the American Urological Association White Paper on the prevention and treatment of the more common complications related to prostate biopsy. J Urol 2017; 198(2): 329-34 2 Ghafoori M et al.: Decrease in infection rate following use of povidone-iodine during transrectal ultrasound guided biopsy of the prostate: A double blind randomized clinical trial. Iran J Radiol 2012; 9(2): 63-6 3 Nam RK et al.: Increasing hospital admission rates for urological complications after transrectal ultrasound guided prostate biopsy. J Urol 2010; 183(3): 963-69 4 Loeb S et al.: Complications after prostate biopsy: Data From SEER-Medicare. J Urol 2011; 186(5): 1830-34 5 Johansen TEB et al.: Antibiotic resistance, hospitalizations, and mortality related to prostate biopsy: first report from the Norwegian Patient Registry. World J Urol 2020; 38(1): 17-26 6 Alidjanov JF et al.: The negative aftermath of prostate biopsy: prophylaxis, complications and antimicrobial stewardship: results of the global prevalence study of infections in urology 2010–2019. World J Urol 2021; 39(9): 3423-32 7 Steensels D et al.: Fluoroquinolone-resistant E. coli in intestinal flora of patients undergoing transrectal ultrasound-guided prostate biopsy-should we reassess our practices for antibiotic prophylaxis? Clin Microbiol Infect 2012; 18(6): 575-81 8 Loeb S et al.: Infectious complications and hospital admissions after prostate biopsy in a European randomized trial. Eur Urol 2012; 61(6): 1110-14 9 Feliciano J et al.: The incidence of fluoroquinolone resistant infections after prostate biopsy - are fluoroquinolones still effective prophylaxis? J Urol 2008; 179(3): 952-55 10 Al-Hasan M et al.: Antimicrobial resistance trends of Escherichia coli bloodstream isolates: a population-based study, 1998–2007. J Antimicrob Chemother 2009; 64(1): 169-74 11 Pradere B et al.: Nonantibiotic Strategies for the prevention of infectious complications following prostate biopsy: a systematic review and meta-analysis. J Urol 2021; 205(3): 653-63 12 Pilatz A et al.: Antibiotic prophylaxis for the prevention of infectious complications following prostate biopsy: A systematic review and meta-analysis. J Urol 2020; 204(2): 224-30 13 Mottet N et al.: EAU-EANM-ESTRO-ESUR-ISUP-SIOG. Guidelines on Prostate Cancer. Update. 2021; 53(February): 212. http://www.uroweb.org/fileadmin/tx_eauguidelines/2005/Pocket/Prostate_Cancer.pdf 14 Berry B et al.: Comparison of complications after transrectal and transperineal prostate biopsy: a national population-based study. BJU Int 2020; 126(1): 97-103 15 AWMF: S3-Leitlinie Prostatakarzinom Version 6.0 – Mai 2021 16 Pepe P et al.: Transperineal versus transrectal mri/trus fusion targeted biopsy: detection rate of clinically significant prostate cancer. Clin Genitourin Cancer. 2017; 15(1): e33-e36 17 Wetterauer C et al.: Feasibility of freehand MRI/US cognitive fusion transperineal biopsy of the prostate in local anaesthesia as in-office procedure-experience with 400 patients. nature.com 18 Grummet JP et al.: TREXIT is now: Should we abandon the transrectal route for prostate biopsy? Yes. Eur Urol Open Sci 2021; 31: 14-6 19 Medicines Agency E. Disabling and potentially permanent side effects lead to suspension or restrictions of quinolone and fluoroquinolone antibiotics. EMA/175398/2019 20 European Medicines Agency: Quinolones and fuoroquinolones - Annex III A - Amendments to relevant sections of the product information. 2019: 164-86 21 Kwan ACF, Beahm NP: Fosfomycin for bacterial prostatitis: a review. Int J Antimicrob Agents 2020; 56(4): 1-7 22 Karlowsky JA et al.: In vitro activity of fosfomycin against Escherichia coli isolated from patients with urinary tract infections in Canada as part of the CANWARD surveillance study. Antimicrob Agents Chemother 2014; 58(2): 1252-56 23 Carignan A et al.: Effectiveness of fosfomycin tromethamine prophylaxis in preventing infection following transrectal ultrasound-guided prostate needle biopsy: Results from a large Canadian cohort. J Glob Antimicrob Resist 2019; 17: 112-6 24 Falagas ME et al.: Fosfomycin. Clin Microbiol Rev. 2016; 29(2): 321-47 25 Pilatz A et al.: European Association of Urology Position Paper on the prevention of infectious complications following prostate biopsy. Eur Urol 2021; 79(1): 11-5 26 Abughosh Z et al.: A prospective randomized trial of povidone-iodine prophylactic cleansing of the rectum before transrectal ultrasound guided prostate biopsy. J Urol 2013; 189(4): 1326-31 27 Park DS et al.: Control of infective complications of transrectal prostate biopsy. Surg Infect (Larchmt) 2014; 15(4): 431-36 28 Cuevas O et al.: Significant ecological impact on the progression of fluoroquinolone resistance in Escherichia coli with increased community use of moxifloxacin, levofloxacin and amoxicillin/clavulanic acid. J Antimicrob Chemother 2011; 66(3): 664-9 29 Oteo J et al.: Parallel increase in community use of fosfomycin and resistance to fosfomycin in extended-spectrum β-lactamase (ESBL)-producing Escherichia coli. J Antimicrob Chemother 2010; 65(11): 2459-63
Das könnte Sie auch interessieren:
Aktuelle Entwicklungen und Erkenntnisse beim Urothelkarzinom
Auf dem diesjährigen Genitourinary Cancers Symposium der American Society of Clinical Oncology (ASCO-GU-Kongress) wurden bedeutende Fortschritte in der Diagnose und Behandlung des ...
Aktuelles aus der 7. Version der S3-Leitlinie: wesentliche Leitlinienänderungen
Im Mai 2024 wurde die Prostatakarzinom-S3-Leitlinie unter der Federführung der Deutschen Gesellschaft für Urologie e.V. (DGU) im Rahmen des Leitlinienprogramms Onkologie in ihrer 7. ...
Neues vom ASCO GU zum Prostatakarzinom
Im Rahmen des ASCO GU 2025 in San Francisco wurden eine Vielfalt von neuen praxisrelevanten Studien zum Prostatakarzinom präsentiert. Mit Spannung wurde unter andem auch auf die finalen ...