©
Getty Images/iStockphoto
Ein großer Schritt voran: aktuelle Empfehlungen zur Therapie der Psoriasisarthritis
Jatros
Autor:
Dr. Felicitas Witte
30
Min. Lesezeit
15.02.2018
Weiterempfehlen
<p class="article-intro">Eine Psoriasisarthritis gilt als unheilbar, sie schränkt die Lebensqualität der Patienten enorm ein und wirkt sich negativ auf das Arbeitsleben aus. Mit neuen Medikamenten gelingt es aber, die Gelenkentzündungen weitgehend zu unterdrücken und die Zerstörung der Gelenke zu verhindern. Wir haben für Sie die aktuellen Empfehlungen der EULAR zusammengefasst.<sup>1</sup> </p>
<hr />
<p class="article-content"><p>Bei bis zu 30 % der Patienten mit Psoriasis tritt eine Psoriasisarthritis auf.<sup>2, 3</sup> Gelenk- und Hautbefall müssen nicht parallel verlaufen, meist geht die Hautpsoriasis der Gelenkpsoriasis um etwa 8 bis 10 Jahre voraus.<sup>4, 5</sup> Die Arthritis äußert sich typischerweise durch Schmerzen und Schwellungen peripherer Gelenke oder an der Wirbelsäule sowie durch Entzündungen der Sehnenansätze, Schleimbeutel und Sehnenscheiden. Die chronische Haut- und Gelenkentzündung belastet die Patienten enorm. Sie berichten über eine reduzierte Lebensqualität, haben mehr Probleme am Arbeitsplatz, gehen öfter zum Arzt und müssen öfter ins Spital als Patienten, die „nur“ an Psoriasis der Haut leiden.</p> <h2>Große Probleme im Job</h2> <p>In einer Umfrage unter 3426 Psoriasispatienten aus Europa und Nordamerika – der größten dieser Art – litten 712, also 21 % , unter einer Psoriasisarthritis.<sup>6</sup> 60 % der Patienten gaben an, mehr als vier Gelenke seien involviert. 53 % stuften ihre Psoriasisarthritis als schwer ein (Abb. 1) und vergaben einen Score von 8–10 auf einer Skala von 1 (sehr mild) bis 10 (sehr schwer). Die Psoriasisarthritis beeinträchtigte die Produktivität der Betroffenen bei der Arbeit enorm: 31 % berichteten, sie seien in den 12 Monaten vor der Umfrage wegen der Arthritis krankgeschrieben gewesen. Ähnlich viele gaben an, dass sie nicht Vollzeit arbeiten konnten. Jeder vierte Patient sagte, die Krankheit würde es „sehr“ oder „etwas“ schwierig machen, einen Job zu bekommen, den Job zu behalten oder sich für eine bestimmte Karriere zu entscheiden (Abb. 2).</p> <p><img src="/custom/img/files/files_datafiles_data_Zeitungen_2018_Jatros_Ortho_1801_Weblinks_s64_2.jpg" alt="" width="1419" height="529" /></p> <p><br />Die Ergebnisse der internationalen Umfrage sollten jeden Rheumatologen hellhörig werden lassen: 59 % der Patienten berichteten, sie würden keine systemische Therapie gegen ihre Psoriasisarthritis bekommen. 31 % wurden nur mit topischer Therapie behandelt, 19 % mit einer konventionellen oralen Therapie (DMARDs, siehe Tab. 1), 14 % mit Biologika und 8 % mit einer Kombination aus konventionellen DMARDs und Biologika. Mehr als die Hälfte der Patienten empfanden die Behandlung mit konventionellen DMARDs und Biologika als Belastung, vor allem wegen der Nebenwirkungen, der notwendigen Laborkontrollen oder aus Angst vor den Injektionen. Die Unterbehandlung der Patienten, so ein Fazit der Autoren, zeige, dass es mehr Aufklärung bräuchte über die Therapieoptionen und Therapieadhärenz.</p> <p><img src="/custom/img/files/files_datafiles_data_Zeitungen_2018_Jatros_Ortho_1801_Weblinks_s64_1.jpg" alt="" width="1419" height="529" /></p> <h2>Neu: Therapieziel Remission</h2> <p>Wie man Patienten mit Psoriasisarthritis effektiv und sicher therapiert, steht in der 2015 aktualisierten EULAR-Leitlinie.<sup>1</sup> „Bei der pharmakologischen Behandlung der Psoriasisarthritis sind wir in den letzten Jahren einen großen Schritt weitergekommen“, sagt Dr. Sofia Ramiro, Rheumatologin an der Universität Leiden und eine der Autorinnen der neuen Leitlinie. Zuerst basierte die Therapie auf Erfahrungen mit der rheumatoiden Arthritis (RA). Als sich herausstellte, dass die RA-Medikamente auch bei Psoriasisarthritis wirkten, wurden erste Studien speziell bei dieser Gelenkentzündung durchgeführt. Vor Kurzem haben aber randomisierte klinische Studien gezeigt, dass auch Medikamente, die nicht gegen RA eingesetzt werden, bei Psoriasisarthritis wirken. „Das bietet Rheumatologen neue Therapieoptionen“, sagt Ramiro. „Deshalb musste die Leitlinie aktualisiert werden.“ Als Basis für die EULAR-Leitlinie analysierten die Autoren 25 randomisierte klinische Studien und 12 Abstracts von Konferenzen. <br />Die Leitlinie besteht aus 5 übergreifenden Prinzipien (A–E) und 10 Empfehlungen. Letztere gelten als Basis für den Therapiealgorithmus. Das Prinzip B wurde ergänzt um den Zusatz, dass man Wirksamkeit, Sicherheit und Kosten bei der gemeinsamen Entscheidungsfindung mit dem Patienten bedenken müsse. „Natürlich kann man Rheumatologen und Patienten nicht verantwortlich machen für die Kosten der Medikamente“, sagt Prof. Dr. Josef Smolen, Leiter der Klinischen Abteilung für Rheumatologie an der Universitätsklinik für Innere Medizin III, Wien, und ebenfalls einer der Autoren. „Aber Arzt und Patient müssen sich bewusst sein, dass Kostenüberlegungen Teil der evidenzbasierten Medizin sind, vor allem in Anbetracht der neuen Biologika und der Verfügbarkeit von Biosimilars.“ <br />Auch das Prinzip E ist modifiziert worden, darin wird jetzt erwähnt, wie wichtig es ist, bei der Therapieauswahl auf Komorbiditäten zu achten. „Patienten mit Psoriasisarthritis haben häufig noch andere Krankheiten, nach denen man suchen und die man behandeln muss“, sagt Dr. Ramiro. Vor allem kardiovaskuläre Erkrankungen kommen häufiger vor, das metabolische Syndrom, Diabetes, Übergewicht, Fettleber, Morbus Crohn, Depressionen und Angststörungen.<sup>7, 8</sup> <br />Neu bei der 1. Empfehlung ist, dass das Therapieziel eine Remission sein soll oder zumindest eine nur minimale oder niedrige Krankheitsaktivität. Hierfür muss man den Therapieerfolg regelmäßig kontrollieren und, falls notwendig, die Therapie anpassen. „Auf ein optimales Outcome zu zielen, indem man immer wieder die Therapie anpasst, fanden wir so wichtig, dass wir es zur 1. Empfehlung machten“, sagt Dr. Ramiro, „vor allem, weil es eine generelle Behandlungsstrategie darstellt.“ So gilt auch bei der RA das Therapieziel einer Remission, denn das führt zu einem besseren strukturellen und funktionellen Outcome.<sup>9, 10</sup><br />Die zweite Empfehlung – „In patients with PsA, non-steroidal anti-inflammatory drugs (NSAID) may be used to relieve mus­culoskeletal signs and symptoms“ – hat sich nicht geändert. „NSAID wirken gut bei Gelenksymptomen“, sagt Prof. Smolen. „Vor allem Patienten mit mildem Gelenkbefall können davon profitieren.“ Allerdings wirken die NSAID nicht bei Hauterscheinungen und man muss die Kontraindikationen berücksichtigen. Einen Benefit von NSAID sollte man innerhalb einiger Wochen sehen. <br />Die 3. Empfehlung sieht den Einsatz von konventionellen synthetischen DMARDs (csDMARDs) bei peripherer Arthritis vor. Sie kombiniert die Empfehlungen 2 und 3 der alten Leitlinie von 2012. „Bei Patienten mit peripherer Arthritis und schlechter Prognose sollte man rasch eine Therapie mit einem csDMARD starten“, empfiehlt Prof. Smolen. „Und auch bei jenen mit milder Krankheit, wenn die Arthritis sich trotz NSAID und Glukokortikoidinjektionen nicht bessert.“ Als periphere Arthritis gelten ein oder mehrere schmerzhafte und geschwollene Gelenke.</p> <h2>Erste Wahl: Methotrexat</h2> <p>Das csDMARD der ersten Wahl ist Methotrexat, weil es auch gut gegen die Hauterscheinungen wirkt. Die 4. Empfehlung („Local injections of glucocorticoids should be considered as adjunctive therapy in PsA; systemic glucocorticoids may be used with caution at the lowest effective dose.“) blieb unverändert, weil es keine neue Evidenz gibt. Profitieren können vor allem Patienten mit Oligo- oder Monarthritis oder Daktylitis und Enthesitis. Bei Patienten, die nach 3–6 Monaten nicht oder nicht genügend auf ein csDMARD ansprechen, sollte man gemäß der 5. Empfehlung ein biologisches DMARD einsetzen, in erster Linie einen TNF-Hemmer. Die Empfehlung blieb im Prinzip gleich, aber weil es jetzt neue Medikamente gibt, wurde statt „TNF-Hemmer“ „bDMARD“ empfohlen. „Es sind nun schon seit einiger Zeit Antikörper gegen IL-12/23 (Ustekinumab) und gegen IL-17 (Secukinumab, Ixekizumab) bei Psoriasis­arthritis zugelassen, die ähnlich wirksam sind wie TNF-Blocker", sagt Prof. Smolen. „Getestet werden zurzeit auch Anti-IL-23-Antikörper in klinischen Spätphasen. Die Resultate werden wohl noch in diesem Jahr bekannt werden." Das csDMARD kann weiter gegeben werden, denn es scheint die Therapieadhärenz und die Ansprechrate zu erhöhen. <br />Für Patienten, bei denen sich TNF-Hemmer nicht eignen, werden gemäß Empfehlung 6 Ustekinumab oder Secukinumab oder ein anderer TNF-Hemmer empfohlen. Ob es besser ist, das csDMARD abzusetzen oder nicht, lässt sich wegen mangelnder Daten noch nicht sagen. Eignen sich Ustekinumab oder Secukinumab nicht, sollte man gemäß Empfehlung 7 zielgerichtete synthetische DMARDs (tsDMARDs) verabreichen, wie den PDE-4-Hemmer Apremilast. Dieser käme beispielsweise infrage für Patienten mit Komorbiditäten oder einer Vorgeschichte mit schweren oder chronischen Infektionen, die eine Kontraindikation für bDMARDs darstellen, eventuell auch für Patienten ohne Zeichen für einen schweren Verlauf, die keine parenterale Therapie wünschen. Auch Patienten mit aktiver Enthesitis und/oder Daktylitis, die auf NSAID nicht genügend ansprechen, werden gemäß Empfehlung 8 mit einem bDMARD behandelt, in erster Linie mit einem TNF-Hemmer. „Bei Enthesitis sind csDMARDs unwirksam“, erklärt Prof. Smolen. Ebenso ist bei Patienten mit aktiver axial betonter Psoriasis­arthritis – definiert durch einen BASDAI über 4 Punkte – nach Empfehlung 9 ein bDMARD einzusetzen, auch hier vornehmlich ein TNF-Hemmer. <br />Allen Patienten, die nicht genügend auf ein bDMARD ansprechen, wird gemäß Empfehlung 10 zu einem anderen bDMARD geraten. Auch ein Wechsel auf einen anderen TNF-Hemmer ist möglich. „Wechsel sind nicht nur einmal möglich und man kann innerhalb einer Klasse oder auch zwischen Klassen wechseln“, so Prof. Smolen. Das schliesst zum Beispiel auch einen Wechsel von einem bDMARD zu einem tsDMARD ein. Ob man die Therapie reduzieren kann, wenn das Therapieziel erreicht wird, ist wegen ungenügender Daten noch nicht klar – deshalb gibt es hierzu auch noch keine Empfehlung. <br />Zwei der Empfehlungen (1. und 2.) beruhen auf einer Grad-A-Evidenz, eine (4.) auf einer Grad-C-Evidenz, die übrigen auf dem Grad B. Fast immer waren sich die Experten ziemlich einig bei den Entscheidungen, was man an einem Übereinstimmungsgrad zwischen 9 und 10 erkennen konnte. „Allein bei der Empfehlung 7 waren sich die Experten weniger einig und die Gruppe diskutierte am längsten“, erzählt Dr. Ramiro. Denn Apremilast war zwar in den Studien nur mäßig wirksam und es gibt keine Vergleichsstudien mit Methotrexat, anderen csDMARDs oder bDMARDs, aber dafür ist es recht gut verträglich.<br />Die Leitlinie fasse Empfehlungen zusammen, betont Dr. Ramiro, die zwar auf dem Expertenkonsens beruhten, aber nicht zwingend bindend seien: „Es gibt genügend Spielraum für den einzelnen Arzt, im individuellen Fall anders vorzugehen. Das muss dann keinesfalls falsch sein.“ Trotzdem zeige die hohe Übereinkunft der Experten bei fast allen Empfehlungen, dass diese geeignet und valide seien.</p></p>
<p class="article-footer">
<a class="literatur" data-toggle="collapse" href="#collapseLiteratur" aria-expanded="false" aria-controls="collapseLiteratur" >Literatur</a>
<div class="collapse" id="collapseLiteratur">
<p><strong>1</strong> Gossec L et al.: Ann Rheum Dis 2016; 75(3): 499-510 <strong>2</strong> Villani AP et al.: J Am Acad Dermatol 2015; 73: 242-8 <strong>3</strong> Dominguez-Rosado I et al.: J Am Coll Surg 2016; 222: 961-6 <strong>4</strong> Gladman DD et al.: Ann Rheum Dis 2005; 64(Suppl 2): ii14–ii17 <strong>5</strong> Lebwohl MG et al.: J Am Acad Dermatol 2014; 70: 871-81 <strong>6</strong> Kavanaugh A et al.: Rheumatol Ther 2016; 3: 91-102 <strong>7</strong> Ogdie A et al.: Curr Opin Rheumatol 2015; 27: 118-26 <strong>8</strong> Di Minno MND et al.: Ann Med 2015; 47: 346-53 <strong>9</strong> Stoffer MA et al.: Ann Rheum Dis 2015. Pub­lished online first 19 May 2015. 10.1136/annrheumdis-2015-207526 <strong>10</strong> Smolen JS et al.: Ann Rheum Dis 2015. Published online first 12 May 2015. 10.1136/ annrheumdis-2015-207524</p>
</div>
</p>
Das könnte Sie auch interessieren:
Neue Therapieansätze für Arthrose
Dass Zellen altern, könnte eine entscheidende Rolle bei der Entstehung von Arthrose spielen. Welche Mechanismen dahinterstecken und welche Ansätze sich für neue Therapien ergeben, ...
Fertilität und Schwangerschaft bei entzündlicher Arthritis
Auf der 13. International Conference on Reproduction, Pregnancy and Rheumatic Diseases (RheumaPreg 2025) in Wien präsentierte Prof. Dr. Radboud Dolhain (Rotterdam, NL) aktuelle ...
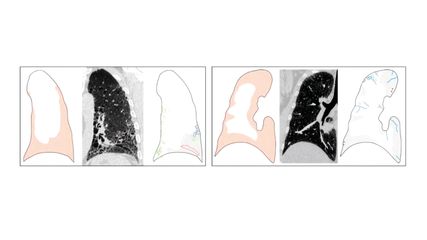
Therapieauswahl nach pulmonalem Inflammations- und Fibrosemuster
Da Fibrose und Entzündung in unterschiedlichem Ausmaß zu Lungenbeteiligungen bei rheumatologischen Erkrankungen beitragen, werden im klinischen Alltag Methoden gebraucht, um beide ...