Biomarker-gesteuerte Antidepressiva-Therapie
Bericht:
Dr. Jürgen Sartorius
Etwa 30–50% der Patienten mit Depressionen sprechen nicht auf das verordnete Erstlinien-Antidepressivum an, was für die Patienten eine immense Belastung darstellt. Daher ist die Suche nach Biomarkern, die zuverlässige Hinweise auf eine effizientere antidepressive Behandlung geben, dringend erforderlich.
Prof. Dr. med. Martin Hatzinger, Direktor der Psychiatrischen Dienste und Chefarzt der Kliniken für Psychiatrie, Psychotherapie und Psychosomatik, Solothurn, sowie Professor für Psychiatrie, Universität Basel, trug zum Thema «Biomarker-gesteuerte Antidepressiva-Therapie» vor. Der engere Rahmen war ein Symposium zum Thema «Update affektive Störungen» der Schweizerischen Gesellschaft für Angst und Depression (SGAD), die sich als Informationsplattform und Anlaufstelle für Betroffene, Angehörige, Ärzte, Fachpersonen, Medien, Unternehmen und Politik versteht.
In der Praxis sprechen nur ca. 50–70% der Patienten auf eine Antidepressiva-Therapie an und die Wirklatenz liegt bei etwa 4 Wochen. «Das bedeutet, dass bei vielen unserer Patienten im ersten Monat nichts passiert und man erst danach sagen kann, ob ein Antidepressivum wirkt, was aber nur bei ca. der Hälfte der Fälle gegeben ist», sagte Hatzinger. «Es gilt, Prädiktoren auszumachen, mit denen wir dieses ‹Try and error›-System verbessern können. Für eine Präzisierung der Therapie eignen sich verschiedene Biomarker.»
Die hauptsächlichen klinischen Faktoren für eine therapieresistente Depression sind begleitende Angststörung, Suizidrisiko, schwere Symptomatik und hohe Anzahl depressiver Episoden. Aber dieser klinische Phänotyp reflektiert die zugrunde liegende Pathophysiologie nicht. Objektiv messbare Biomarker können hingegen pathogenetische Prozesse und das Ansprechen auf eine therapeutische Intervention widerspiegeln.
Die «Stressachse»
Der seit den 1980er-Jahren bekannte Dexamethason/Corticotropin-Releasing-Hormon(DEX/CRH)-Test kann über Feststellung der Veränderungen im Hypothalamus-Hypophysen-Nebennierenrinden(HPA)-System bereits 14 Tage nach der ersten Anwendung eine Aussage zum Ansprechen eines Antidepressivums erlauben. Allerdings ist dieser Test für eine mögliche klinische Routine sehr aufwendig und deshalb in einem klinischen Setting schwierig durchzuführen.
Marker aus dem Schlaf
Eine erhöhte Rapid-Eye-Movement- (REM)-Dichte ist nicht nur ein Zeichen für den Beginn einer depressiven Episode oder eines Rezidivs, sondern kann auch auf das Ansprechen einer antidepressiven Therapie (unabhängig von der Medikation/Methode) hinweisen. Deshalb wird auch intensiv nach weiteren Biomarkern aus der Schlafregulation gesucht.
Präfrontale Theta-Cordance
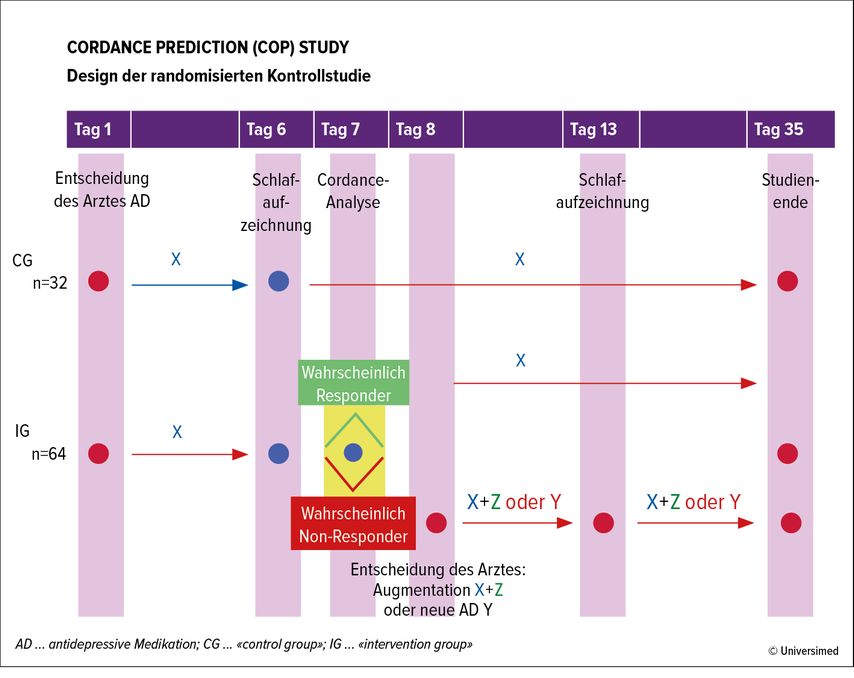
Einer davon ist ein Biomarker, der während der REM-Phase mittels Polysomnografie (PSG) gemessen werden kann: die präfrontale Theta-Cordance. Dabei werden über 19 Elektroden die relative und absolute Theta-Power von Fp1 und Fp2 gemessen und einander gegenübergestellt. Diese korrelieren mit der medialen präfrontalen Hirnaktivität. Wird nach 7 Tagen ein niedriger Wert dieser Cordance gefunden, wird die Therapie mit einer Wahrscheinlichkeit von über 90% nicht anschlagen. Damit kann man sehr früh im Therapieverlauf das Antidepressivum wechseln und dadurch die Wahrscheinlichkeit eines Ansprechens erhöhen (Abb 1).1,2
Abb. 1: Vorhersage des Ansprechens eines Antidepressivums durch Analyse der präfrontalen Cordance (mod. nach Mikoteit et al. 2020)2
Inzwischen läuft eine Studie, in der bisher bei den ersten 30 Patienten die Rate des Gesamtansprechens auf eine antidepressive Therapie durch die «cordance prediction» (COP) signifikant gesteigert wurde. Die Methode ist zwar wegen des hohen Aufwands eines EEG im Schlaflabor aufwendig, aber sehr spezifisch und unabhängig von Alter, Geschlecht und vor allem der Anzahl vorangegangener Episoden.
Pharmako-Genotypisierung zum Abbau in der Leber
Für eine individuelle Antidepressiva-Therapie zur Erhöhung der Responserate gibt es inzwischen – auch durch die Initiative der SGAD – Datenbanken mit Genen, die die Pharmakokinetik und Pharmakodynamik von Antidepressiva beeinflussen können, etwa bei PharmGKB. Dazu gibt es Labore, die eine individualisierte Analyse von z.B. etwa 25 für die Bioverfügbarkeit von Antidepressiva relevanten Genen durchführen und daraufhin Empfehlungen für erfahrungsgemäss bei den betreffenden Genvarianten geeignete Wirkstoffe geben.
Auf die Pharmakokinetik von Antidepressiva nehmen hauptsächlich der Transport durch die Blut-Hirn-Schranke und der Abbau in der Leber durch die Cytochrom-P-Enzyme Einfluss. So ist beispielsweise seit Langem bekannt, dass etwa 10% der westeuropäischen Bevölkerung genetisch bedingte Veränderungen im Cytochrom-P450(CYP)-System haben, welche den Metabolismus von Antidepressiva beinflussen können. Aktuelle Erkenntnisse zu Einschränkungen in Bezug auf Cytochrom- P-Enzyme und Empfehlungen, die sich daraus für die Verwendung verschiedener Antidepressiva ergeben, sind bei BousmanCA et al.3 beschrieben. Die Untersuchungen auf individuelle Variationen in diesen Cytochrom-Systemen werden inzwischen von verschiedenen Leitlinien empfohlen.
Pharmako-Genotypisierung zur Passage der Blut-Hirn-Schranke
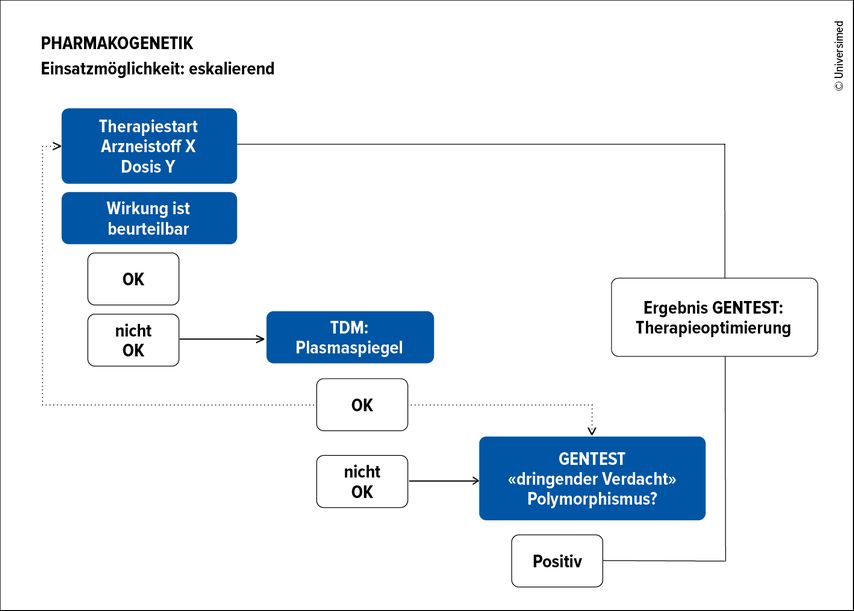
Das Transportmolekül P-Glykoprotein, das viele Antidepressiva transportiert, ist in die Zellmembran der Blut-Hirn-Schranke eingebunden und wird von dem Gen ACBC1 codiert. Viele der bekannten Antidepressiva werden von diesem Protein nicht oder nur in geringer Menge in das zentrale Nervensystem aufgenommen, wofür zahlreiche Varianten des ABCB1-Gens verantwortlich sind. Durch eine individuelle Analyse des ACBC1-Genotyps lässt sich häufig voraussagen, welches Antidepressivum die Blut-Hirn-Schranke passieren und so einfacher an den Wirkungsort gelangen kann. Inwiefern auch Genanalysen der Transportmoleküle an der Blut-Hirn-Schranke in allgemeine Empfehlungen übernommen werden können, ist zurzeit Gegenstand der Forschung (Abb. 2).
Abb. 2: Einsatz von Pharmakogenetik im Rahmen eines eskalierenden Therapiealgorithmus (mod. nach Stäuble CK et al. 2022)4
Genotypisierung als Bestandteil einer eskalierenden Therapie
Grundsätzlich kann man Genotypisierung als Biomarker in einem Algorithmus in 2 möglichen Varianten anwenden: (1) im Rahmen eines eskalierenden Vorgehens oder (2) im Rahmen einer A-priori-Genanalyse, um die Therapie von Beginn weg zu steuern. «Der Vorteil eines eskalierenden Therapiealgorithmus ist, dass man zunächst die 50%ige Chance auf ein Ansprechen nutzt, die ja ohnehin besteht, und die DNA-Diagnostik auf die Problemfälle beschränkt», erläuterte Hatzinger. «Demgegenüber stehen aber die Nachteile des Zeitverlustes, den man bei ausbleibender Wirkung des ersten Antidepressivums riskiert, und damit des Risikos, dass Patienten länger unter ihren Depressionen leiden und/oder die Therapie komplett abbrechen» (siehe auch Abb.2).
Dazu nannte Hatzinger zwei Beispiele: Eine Patientin mit Depression befand sich in einer erfolglosen Therapie mit Escitalopram und Agomelatin. Die pharmakogenetische Analyse ergab bei ihr eine CYP2C19-Variante, die für einen raschen Abbau von Escitalopram sorgte, sowie eine CYP1A2-Variante, induziert durch Rauchen, wodurch auch Agomelatin in ihrer Leber schneller abgebaut wurde. Zusätzlich verursachte auch eine Variante des ABCB1-Gens eine verminderte Verfügbarkeit dieser Antidepressiva. Die Empfehlung des Genlabors lautete Vortioxetin, Bupropion oder Venlafaxin. Nach Umstellung auf Vortioxetin erlebte die Patientin nach 5 Wochen eine Remission von 33 auf 4 Punkte auf der HAMD-Skala.5
Ein anderes Beispiel: Ein Patient hatte auf keinen der beiden SSRI-Wirkstoffe Venlafaxin und Fluoxetin angesprochen. Bei ihm ergab die pharmokogenetische Analyse ein pharmakodynamisches Problem: Eine homozygote Varianz im Gen SLC6A4 sorgte für eine reduzierte Expression des Serotonintransporters SERT1. Nach Wechsel auf den nicht serotonergen Wirkstoff Bupropion erlebte der Patient nach 4 Wochen eine komplette Remission.6
«Bei der 2. Variante, das heisst einer A-priori-Genanalyse, kann man natürlich von Anfang an einen wahrscheinlich besser funktionierenden Wirkstoff einsetzen und damit die individuelle Wahrscheinlichkeit eines Ansprechens stark erhöhen», resümierte Hatzinger zum Abschluss. «Man spart Zeit und Leidensdruck für die Patienten und erreicht auch eine hohe Akzeptanz der Therapie.» Hatzinger ist Mitinitiator einer grösseren laufenden Studie, die diese Zukunftsaussicht auch statistisch belegen soll.
Quelle:
Jahreskongress der Schweizerischen Gesellschaft für Psychiatrie und Psychotherapie, SGPP, Vortrag von Prof. Dr. med. Martin Hatzinger, 7. September 2023, Bern
Literatur:
1 Pawlowski MA et al.: Heart rate variability and cordance in rapid eye movement sleep as biomarkers of depression and treatment response. J Psychiatric Res 2017; 92: 64-73 2 Mikoteit T et al.: Antidepressant response prediction by early response, prefrontal theta cordance in rapid eye movement sleep and ABCB1 genotype. Europ Neuropsychopharmacol 2021; 53 (Suppl. 1): S517 3 Bousman CA et al.: Review and consensus on pharmacogenomic testing in psychiatry. Pharmacopsychiatry 2021; 54(1): 5-17 4 Stäuble CK et al.: A guide to a pharmacist-led pharmacogenetic testing and counselling service in an interprofessional healthcare setting. Pharmacy 2022; 10(4): 86 5 Stäuble CK et al.: Pharmacogenetic-guided antidepressant selection as an opportunity for interprofessional collaboration: A case report. Life 2021; 11: 673 6 Stäuble CK et al.: Case report: Non-response to fluoxetine in a homozygous 5-HTTLPR-S-allele carrier of the serotonin transporter gene. Frontiers in Psychiatry 2022; 13: 942268
Das könnte Sie auch interessieren:
Regionale interdisziplinäre Umsetzung des Anordnungsmodells
Vor drei Jahren wurde das Anordnungsmodell für die psychologische Psychotherapie eingeführt. Das Modell sollte die psychische Gesundheitsversorgung in der Schweiz verbessern, wurde ...
Jahresbericht 2025 – Schweizerische Gesellschaft für Sportpsychiatrie und -psychotherapie (SGSPP)
Die SGSPP stärkte 2025 ihre interprofessionelle Ausrichtung, erweiterte die Mitgliedschaft, förderte Weiterbildung, Forschung und Vernetzung und engagierte sich im Leistungs- wie im ...
Insomnische Störung – vom Symptom zur eigenständigen Diagnose und evidenzbasierten Therapie
Insomnie zählt zu den häufigsten Gesundheitsproblemen im klinischen Alltag. Aktuelle Arbeiten zeigen, dass die chronische insomnische Störung nicht primär durch «Schlaflosigkeit», ...