Thérapie d’une entité aux multiples facettes
Auteure:
Dre méd. Ilaria Colombo
Istituto Oncologico della Svizzera Italiana
Bellinzona
E-mail: ilaria.colombo@eoc.ch
La prise en charge des patient·es atteint·es d’un cancer de l’endomètre a été fondamentalement transformée par la définition de sous-types moléculaires et l’introduction des inhibiteurs de points de contrôle immunitaire. De nombreuses études évaluent de nouvelles options thérapeutiques ainsi que des biomarqueurs potentiels.
Le cancer de l’endomètre (CE) comprend quatre sous-types moléculaires ayant une valeur pronostique et prédictive, pertinents pour le choix du traitement adjuvant: POLE muté, déficit de réparation des mésappariements (dMMR), p53 muté et NSMP («non-specific molecular profile»).1Dans l’étude PORTEC-3, les patient·es présentant une mutation POLE n’ont développé aucune récidive, indépendamment du traitement adjuvant, tandis que celles et ceux avec un CE muté p53 présentaient le plus mauvais pronostic, mais tiraient un bénéfice d’une chimiothérapie adjuvante.2Les sous-types dMMR et NSMP étaient associés à un pronostic intermédiaire et à un bénéfice minimal d’un traitement systémique adjuvant.
Récemment, le statut du récepteur des œstrogènes (ER) a été intégré dans la classification moléculaire selon les directives ESGO-ESTRO-ESP, permettant d’affiner davantage la stratification du risque.3 Au sein du sous-groupe NSMP, le pronostic des patient·es ER négatif·ves est défavorable, tandis qu’une positivité ER est associée à une probabilité de survie nettement plus élevée.4
Immunothérapie en cas de CE précoce et avancé
Les inhibiteurs de points de contrôle immunitaire (ICI) sont actuellement évalués dans le cadre adjuvant. L’étude KEYNOTE-B21 a évalué le pembrolizumab en complément d’une chimiothérapie adjuvante chez des patient·es à haut risque après une chirurgie curative. Comparée au placebo plus chimiothérapie, l’association n’a pas prolongé la survie sans maladie dans la population globale, bien que l’analyse de sous-groupe ait montré une amélioration significative chez les patient·es présentant une dMMR (HR: 0,31).5 L’étude RAINBO évalue actuellement, dans une optique de personnalisation, des traitements adjuvants adaptés au profil moléculaire, y compris en cas de maladie précoce.
Dans le CE avancé, l’association carboplatine/paclitaxel plus ICI avec ou sans inhibition de PARP constitue désormais le traitement standard de première ligne – sur la base des quatre études randomisées de phaseIII RUBY (dostarlimab), NRG-GY018 (pembrolizumab), AtTEnd (atezolizumab) et DUO-E (durvalumab+olaparib). Dans ces études, les sous-groupes présentant dMMR/instabilité élevée des microsatellites ont montré des prolongations comparables, cliniquement pertinentes et durables de la survie sans progression (PFS).6–9 En revanche, le bénéfice en termes de PFS était nettement plus faible dans toutes les populations présentant une réparation des mésappariements compétente (pMMR)/stabilité des microsatellites. Des résultats similaires ont été observés dans l’étude RUBY concernant la survie globale; là encore, les sous-groupes dMMR ont tiré un bénéfice plus important que les sous-groupes pMMR.10,11
Thématique de la sélection des patient·es approprié·es
Au vu de ces données, la question centrale est de savoir si les patient·es dMMR nécessitent réellement une chimiothérapie. Les études KEYNOTE-C93 et DOMENICA comparent actuellement les ICI à la chimiothérapie afin d’apporter des données dans ce domaine. En revanche, dans le cas des tumeurs pMMR, l’identification de biomarqueurs permettant de sélectionner les patient·es susceptibles de bénéficier d’un traitement par ICI sera déterminante.
L’ajout d’inhibiteurs de PARP au traitement d’entretien par ICI en première ligne peut améliorer les résultats en cas de pMMR, comme l’a montré l’étude DUO-E à trois bras, qui évaluait un traitement d’entretien par durvalumab avec ou sans olaparib.9 Dans cette étude, les mutations TP53 et HRR (réparation de recombinaison homologue) étaient prédictives du bénéfice clinique de la combinaison.12
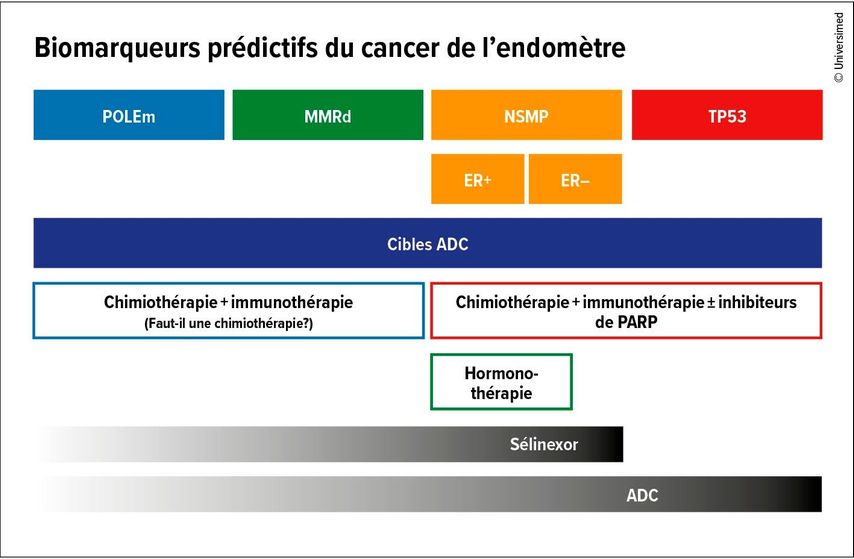
Ainsi, le traitement standard des tumeurs dMMR repose sur la chimiothérapie associée aux ICI (Fig.1). La chimiothérapie plus ICI est également utilisée en cas de NSMP et de mutations TP53, les inhibiteurs de PARP pouvant jouer un rôle additionnel. Par ailleurs, le traitement endocrinien ne doit pas être négligé chez les patient·es ER positif·ves. D’autres options actuellement à l’étude incluent le sélinexor, inhibiteur de XPO1, ainsi que des conjugués anticorps-médicament (ADC), dont les cibles sont exprimées dans l’ensemble des sous-types.
Nouvelles substances
Différents ADC ciblant notamment HER2, FRα, TROP2 et B7-H4 sont actuellement évalués chez des patient·es atteint·es de CE. Dans l’étude DESTINY-PanTumor02, le trastuzumab deruxtecan a montré des résultats prometteurs chez des patient·es prétraité·es atteint·es de CE; dans le groupe présentant une forte expression de HER2, le taux de réponse objective (ORR) était de 84,6%.13 Les ADC dirigés contre TROP2 – sacituzumab govitecan, sacituzumab tiroumotécan et datopotamab deruxtecan – ont montré une activité comparable, avec des ORR de 22 à32%.14–16 Les résultats des études de phaseIII sont actuellement attendus.
Le sélinexor, inhibiteur de XPO1, administré en traitement d’entretien après une chimiothérapie de première ligne à base de platine, a prolongé la PFS par rapport au placebo, en particulier dans la population TP53 de type sauvage (HR: 0,407), alors qu’aucun bénéfice n’a été observé chez les patient·es présentant une mutation TP53.17 Les patient·es présentant des tumeurs pMMR/TP53 de type sauvage ont bénéficié d’un avantage durable en termes de PFS.18 L’étude de phaseIII XPORT-EC-042 évalue actuellement le sélinexor dans le CE avancé avec TP53 de type sauvage après chimiothérapie à base de platine. D’autres approches, telles que les inhibiteurs des points de contrôle du cycle cellulaire et les combinaisons d’inhibiteurs CDK4/6 avec une thérapie endocrinienne, font également l’objet de recherches. Les résultats de nombreuses études de phaseIII continueront à transformer le paysage thérapeutique à l’avenir.
Littérature:
1 Oaknin A et al.: Endometrial cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol 2022; 33(9): 860-77 2 León-Castillo A et al.: Molecular classification of the PORTEC-3 trial for high-risk endometrial cancer: impact on prognosis and benefit from adjuvant therapy. J Clin Oncol 2022; 38(29): 3388-97 3 Concin N et al.: ESGO-ESTRO-ESP guidelines for the management of patients with endometrial carcinoma: update 2025. Lancet Oncol 2025; 26(8): e423-35 4 Vermij L et al.: Prognostic refinement of NSMP high-risk endometrial cancers using oestrogen receptor immunohistochemistry. Br J Cancer 2023; 128(7): 1360-8 5 Van Gorp T et al.: ENGOT-en11/GOG-3053/KEYNOTE-B21: a randomised, double-blind, phase III study of pembrolizumab or placebo plus adjuvant chemotherapy with or without radiotherapy in patients with newly diagnosed, high-risk endometrial cancer. Ann Oncol 2024; 35(11): 968-80 6 Mirza NR et al.: Dostarlimab for primary advanced or recurrent endometrial cancer. Engl J Med 2023; 388(23): 2145-58 7 Eskander RN et al.: Pembrolizumab plus chemotherapy in advanced endometrial cancer. N Engl J Med 2023; 388 (23): 2159-70 8 Colombo N et al.: Phase III double-blind randomized placebo controlled trial of atezolizumab in combination with carboplatin and paclitaxel in women with advanced/recurrent endometrial carcinoma. Ann Oncol 2023; 34(Suppl_2): 1281-2 9 Westin SN et al.: Durvalumab plus carboplatin/paclitaxel followed by maintenance durvalumab with or without olaparib as first-line treatment for advanced endometrial cancer: the phase III DUO-E trial. J Clin Oncol 2024; 42(3): 283-99 10 Powell MA et al.: Overall survival in patients with endometrial cancer treated with dostarlimab plus carboplatin–paclitaxel in the randomized ENGOT-EN6/GOG-3031/RUBY trial. Ann Oncol 2024; 35(8): 728-38 11 Barretina Ginesta MP et al.: Final overall survival results from the randomized double-blind phase III AtTEnd/ENGOT-EN7 trial evaluating atezolizumab in combination with paclitaxel and carboplatin in women with advanced/recurrent endometrial cancer. Ann Oncol 2023; 36(Suppl_2): S1698 12 Moore K et al.: Durvalumab plus carboplatin/paclitaxel followed by durvalumab with/without olaparib in endometrial cancer: biomarkers, histological heterogeneity, baseline circulating tumor DNA, and efficacy in the DUO-E mismatch repair proficient subpopulation. Gynecol Oncol 2025; 200(Suppl. 1): 345-6 13 Meric-Bernstam F et al.: Efficacy and safety of tastuzumab deruxtecan in patients with HER2-expressing solid tumors: primary results from the DESTINY-PanTumor02 phase II Trial. J Clin Oncol 2024; 42(1): 47-58 14 Santin AD et al.: Efficacy and safety of sacituzumab govitecan in patients with advanced solid tumors (TROPiCS-03): analysis in patients with advanced endometrial cancer. J Clin Oncol 2024; 42(29): 3421-9 15 Wang K et al.: Sacituzumab tirumotecan monotherapy in advanced/metastatic endometrial carcinoma (EC): results from a phase I/II study (MK-2870-001/KL264-01). Ann Oncol 2025; 36(Suppl_2): 739-40 16 Oaknin A et al.: Datopotamab deruxtecan in patients with endometrial or ovarian cancer: Results from the phase II TROPION-PanTumor03 study. Ann Oncol 2024; 35(Suppl_2): 547-8 17 Vergote I et al.: Oral selinexor as maintenance therapy after first-line chemotherapy for advanced or recurrent endometrial cancer. J Clin Oncol 2023; 41(35): 5400-10 18 Valabrega G et al.: Longer-term safety and efficacy of selinexor maintenance therapy for patients with TP53wt advanced or recurrent endometrial cancer: follow-up subgroup analysis of the ENGOT-EN5/GOG-3055/SIENDO study. Int J Gynecol Cancer 2025; 35(Suppl_1): 100081
Das könnte Sie auch interessieren:
Cancer de l’endomètre métastatique, avancé et récidivant
L’association d’inhibiteurs de point de contrôle et de chimiothérapie peut être considérée comme une nouvelle norme thérapeutique dans les cancers de l’endomètre avec déficit de ...
Parfois, il suffit d’attendre
Compte tenu de la multitude d’options thérapeutiques ciblées et immunothérapeutiques désormais disponibles, la prise en charge du carcinome à cellules rénales en situation adjuvante et ...
Les néoplasies myélodysplasiques: stratégies thérapeutiques personnalisées
Les progrès réalisés dans la compréhension moléculaire des néoplasies myélodysplasiques (MDS, myelodysplastic syndrome) ont permis de mettre au point des approches thérapeutiques ...