Geeignete Therapien für MS-Patientinnen bei einer Schwangerschaft
Bericht:
Torsten U. Banisch, PhD
Anhand von mehreren Fallbeispielen verdeutlichte Prof. Caroline Pot vom Universitätsklinikum Lausanne die neuesten Empfehlungen für die Behandlung von MS-Patientinnen vor, während und nach einer Schwangerschaft. In einer anschliessenden Podiumsdiskussion mit mehreren Experten wurde das Thema weiter vertieft, ein Ausblick in die Zukunft der Therapierung gegeben und eine neue Schweizer Leitlinie angekündigt.
In der Vergangenheit wurde von einer Schwangerschaft bei einer MS-Erkrankung eher abgeraten und werdende Mütter wurden bisweilen unterbehandelt, um die Entwicklung des Fötus nicht zu gefährden. Aus heutiger Sicht und mit dem derzeitigen Forschungsstand gibt es jedoch keine generellen Gründe, von einer Schwangerschaft bei MS abzuraten.
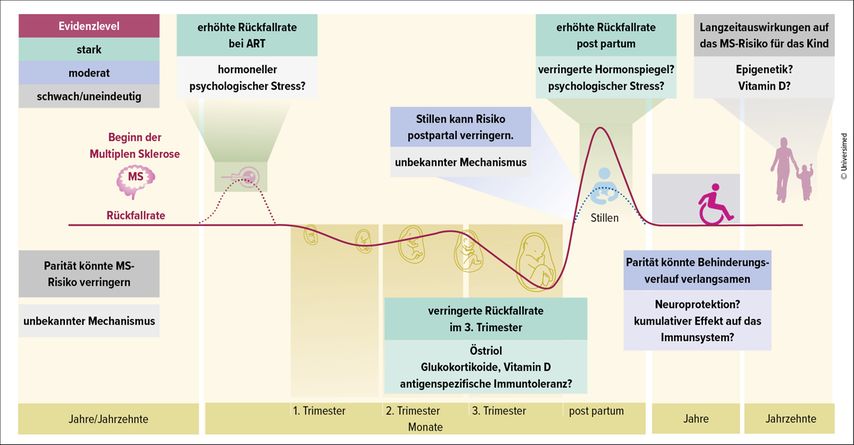
Für Patientinnen mit MS-Aktivität und angepasster Therapie besteht lediglich ein niedriges Restrisiko. Es gibt starke Evidenzen, dass während einer Schwangerschaft gerade im dritten Trimester die Rückfallraten reduziert sind, jedoch kann postpartal ein Rebound-Effekt auftreten (Abb. 1).1 Des Weiteren hat sich gezeigt, dass ein Vorhandensein von Kindern möglicherweise das Fortschreiten von MS verlangsamt. Verfügbare Daten belegen auch, dass Patientinnen mit MS ohne Aktivität und ohne Behandlung ein höheres Risiko für Frühgeburten haben. Bei der Nutzung von Techniken der assistierten Reproduktion liegt ebenfalls ein erhöhtes Rückfallrisiko vor.
Familienplanung mit MS
Wenn es um die Familienplanung bei einer MS-Patientin geht, müssen die Präkonzeption, die Schwangerschaft und die Zeit post partum ausführlich geplant werden. Hierzu sind bereits einige länderspezifische Leitlinien verfügbar.2–4 Zudem muss das Risiko einer ungeplanten Schwangerschaft immer berücksichtigt werden: Allein in Europa waren zwischen 2015 und 2019 35% der Schwangerschaften ungeplant, bei MS-Patientinnen liegt die Zahl bei circa 10%.5
Bei diesen Patientinnen sollten nach Bekanntwerden das individuelle Risiko und der Nutzen einer Weiterbehandlung oder eines Therapiestopps evaluiert werden. Gegebenenfalls muss der genaue Zeitpunkt eines Abbruchs bestimmt und ein Plan für den Fall eines Rückfalls erarbeitet werden.3–6
Behandlungsoptionen in der Präkonzeptionsphase
Bei einer geplanten Schwangerschaft sollte schon Jahre zuvor die passende krankheitsmodifizierende Therapie (DMT) ausgesucht werden, keinesfalls sollte die Therapie aufgeschoben werden.
Inkompatible DMTs mit Sphingosin-1-Phosphat oder Teriflunomid sollten bei einem Schwangerschaftsbeginn innerhalb der nächsten 5 Jahre oder bei jungen Frauen aufgrund des Risikos einer ungeplanten Schwangerschaft vermieden werden. Eine Induktionstherapie mit Cladribin und Anti-CD20-Antikörper-Therapien sind hingegen kompatible Behandlungsmethoden.6
Sollte ein teratogener Wirkstoff eingesetzt werden, muss die Wichtigkeit einer Verhütung regelmässig angesprochen werden. Eine entsprechende Schweizer Leitlinie zu diesem Themenkomplex wird gerade erstellt.
Kontrolle der Krankheitsaktivität während der Schwangerschaft
In einer rezent analysierten Kohorte wurde das Zusammenspiel von DMTs und der MS-Krankheitsaktivität während der Schwangerschaft und postpartal analysiert.7 Patientinnen, die vor einer Schwangerschaft nicht behandelt wurden, und solche, die eine Erstlinientherapie mit Interferon, Glatirameracetat oder DMF erhielten, zeigten vergleichbare Rückfallraten, mit einem Rückgang während der Schwangerschaft und einem kurzen Wiederanstieg post partum.
Bei Patientinnen unter einer Zweit- oder Drittlinienbehandlung wie Fingolimod oder Natalizumab, welche zum Beginn der Schwangerschaft abgebrochen wurde, wurde ein hoher Anstieg der Rückfallraten während der Schwangerschaft verzeichnet, was generell gegen Therapieabbrüche und für eine Weiterbehandlung spricht.7
Patientinnen mit negativer JC-Virus-Testung können während einer Schwangerschaft mit dem monoklonalen Antikörper Natalizumab bei erhöhtem Intervall bis hin zur 30.–34. Schwangerschaftswoche weiterbehandelt werden. Generell ist der Einsatz von monoklonalen Antikörpern gerade im 1. Trimester zu vertreten, da die Wirkstoffe zu dieser Zeit mit höchster Wahrscheinlichkeit nicht durch die Plazenta weitergegeben werden. Eine rezente Studie berichtet zwar, dass bei einer Natalizumab-Therapie während der Schwangerschaft 21,8% der Neugeborenen bezogen auf das Reifealter klein waren, dies ist jedoch laut Expertenmeinung klinisch handhabbar im Gegensatz zu den Folgen einer Nichtbehandlung der werdenden Mutter.8
Bei positivem JCV-Test sollte eine mögliche Behandlung mit DMF zu Schwangerschaftsbeginn, oder eine Ocrelizumab-Therapie schon 2 Monate vorher abgebrochen werden.6 Anti-CD20-Wirkstoffe sollten nicht routinemässig während der Schwangerschaft eingesetzt werden.6 S1P-Inhibitoren müssen in jedem Fall abgesetzt werden, da sie inkompatibel mit einer Schwangerschaft sind. Dies sollte je nach verwendetem Wirkstoff 3 Monate bis 1 Woche vor Beginn der Schwangerschaft erfolgen. Hier sollte gegebenenfalls auf eine Therapie mit monoklonalen Antikörpern umgestiegen werden, um das Risiko eines Rückfalls zu minimieren.6
Neue Schweizer Leitlinie
Gerade bei der Behandlung von Schwangeren werden viele Medikamente «off-label» verwendet, was vor allem dadurch bedingt ist, dass Schwangere von klinischen Studien zumeist ausgeschlossen werden und vorhandene Daten nicht immer frei zugänglich sind. Momentan wird eine neue Schweizer Richtlinie zur Behandlung schwangerer MS-Patient:innen erstellt. Diese basiert auf bereits publizierten Daten, öffentlichen Geburtenregistern und zugänglichen Datenbanken von Krankenversicherern. Zudem gibt es Anstrengungen, in der Schweiz ein zentrales, öffentliches Register zu erstellen, welches signifikant zur Weiterentwicklung der Leitlinien beitragen wird.
Quelle:
Vortrag von Prof. Caroline Pot: «DMT use in pregnancy» und anschliessende Podiumsdiskussion auf dem MS State of the Art Symposium 2024 am 27. Januar 2024, Luzern
Literatur:
1 Gold SM et al.: Semin Immunopathol 2016; 38: 709-18 2 Dobson R et al.: Pract Neurol 2019; 19(2): 106-14 3 Vukusic S et al.: Pratique Neurologique FMC 2022; 13(3): 162-71 4 Hemmer B et al.: S2k-Leitlinie 2023, Stand November 2023 5 Bearak J et al.: Lancet Glob Health 2020; 8(9): e1152-61 6 Krysko KM et al.: Lancet Neurol 2023; 22(4): 350-66 7 Lescot L et al.: Mult Scler Relat Disord 2022; 68: 104122 8 Thiel S et al.: J Neurol Neurosurg Psychiatry 2023; jnnp-2023-332804
Das könnte Sie auch interessieren:
«Kommunikation ist sehr oft Therapie»
Sara Rubinelli, Professorin für Gesundheitswissenschaften mit Schwerpunkt Gesundheitskommunikation an der Fakultät für Gesundheitswissenschaften und Medizin der Universität Luzern, im ...
Schweiz setzt neue Akzente für Frauengesundheit
Der Bundesrat hat diese Woche einen Postulatsbericht verabschiedet, der breiten Handlungsbedarf bei der Gesundheitsversorgung von Frauen aufzeigt. Von BAG bis Swissmedic werden mehrere ...
Studie: Höheres Einkommen senkt Schlaganfallrisiko
Aktuelle Forschungsergebnisse zeigen den Zusammenhang zwischen der Höhe des Einkommens und dem Risiko, an einem Schlaganfall zu sterben.