Schweres Asthma
Bericht:
Dr. med. Sabina Ludin
Chefredaktorin
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Wie kann man verhindern, dass ein Patient mit schwerem Asthma mit oralen Kortikosteroiden behandelt werden muss? Welches Biologikum passt zu welchem Patienten? Diese und andere Fragen zur Behandlung des schweren Asthmas wurden am SGP-Kongress von internationalen Experten beantwortet. Zudem gab Prof. Jörg Leuppi einen ersten Einblick in das Swiss Severe Asthma Register.
Langzeitnebenwirkungen der oralen Kortikosteroide
Weltweit nehmen je nach Studie 15–57% der Patienten mit schwerem Asthma regelmässig orale Kortikosteroide (OCS) ein.1–5 Die dadurch verursachten langfristigen Probleme sind vielfältig. Erhöhtes Risiko für Diabetes, Adipositas und die damit verbundenen Komorbiditäten, ossäre und muskuläre Komplikationen, Hypertonie, Hypercholesterinämie und kardiovaskuläre Erkrankungen, psychiatrische Komplikationen sowie die Katarakt gehören zu den Nebenwirkungen einer Behandlung mit OCS.6 In einer britischen Studie hatten 93% der Patienten mit schwerem Asthma mindestens eine mit der Einnahme von OCS assoziierte Komorbidität und die Prävalenz dieser Erkrankungen war bei Asthmapatienten mit OCS-Therapie signifikant häufiger als bei jenen ohne OCS.7
Das Risiko für akute und chronische Komplikationen ist abhängig von der täglichen OCS-Dosis und der kumulativen Dosis.8, 9 «Interessanterweise steigt das Risiko für langfristige Komplikationen aber bereits nach zwei bis drei kurzfristigen OCS-Behandlungen. Dies zeigt, wie wichtig es ist, OCS so selten wie möglich einzusetzen und, wenn es unumgänglich ist, in möglichst niedriger Dosis»,9 sagte Prof. Dr. med. Louis-Philippe Boulet, Quebec.
Strategien zur Vermeidung von OCS
Zu den nichtmedikamentösen Massnahmen zur Vermeidung von OCS gehören u.a. die Bestätigung der Asthmadiagnose, das Vermeiden von auslösenden Faktoren, soweit möglich, sowie die Patientenschulung und die Förderung der Therapietreue. Um das Risiko von Exazerbationen zu vermindern, bedarf es nicht nur einer guten Inhalationstherapie, sondern auch der korrekten Inhalationstechnik.
«Inhalative Steroide (ICS) gehören heute von Beginn weg zur Asthmatherapie»,10 betonte Boulet. Durch die regelmässige Behandlung mit ICS kann die Notwendigkeit von OCS signifikant vermindert werden.11 Bei Patienten mit schwerem Asthma kann der Einsatz von OCS auch durch die Behandlung mit Biologika effektiv vermindert werden.
Ausschleichen der OCS
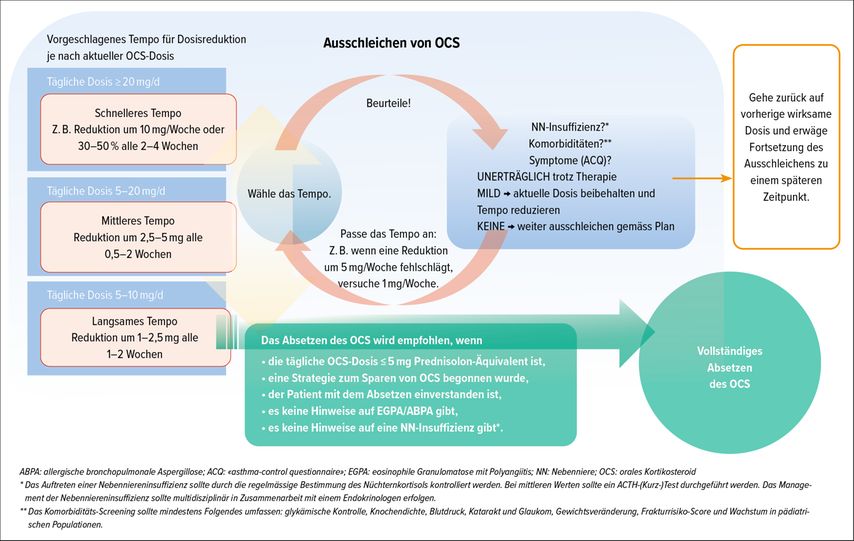
Eine Schwierigkeit beim Absetzen der OCS besteht darin, die Dosis im richtigen Tempo zu reduzieren, um einerseits das erneute Auftreten von Asthmasymptomen und andererseits die Entwicklung einer Nebennierenrinden(NNR)-Insuffizienz zu vermeiden. Kürzlich wurde dazu ein Konsensusstatement publiziert, in dem ein Vorgehen nach einem personalisierten Algorithmus vorgeschlagen wird.12 Das Tempo und der Umfang der Dosisreduktion werden dabei u.a. von der initialen OCS-Dosis, Zeichen einer NNR-Insuffizienz und dem Auftreten von Asthmasymptomen abhängig gemacht (Abb. 1).
Abb. 1: Ausschleichen der oralen Kortikosteroide (OCS) bei Patienten mit schwerem Asthma (adaptiert nach Suehs et al., 2021)12
Biologika zur Behandlung des schweren Asthmas
Für die Behandlung des schweren Asthmas wird in den GINA-Guidelines (Stufe 5) der Einsatz eines Biologikums empfohlen, wenn die Asthmakontrolle trotz inhalativer Dreierkombination (ICS + LABA + LAMA) ungenügend ist.10 Niedrig dosierte OCS werden nur noch empfohlen, wenn alle anderen Optionen ausgeschöpft sind.10 Derzeit stehen fünf verschiedene Biologika mit unterschiedlichen Angriffspunkten zur Verfügung:
-
Anti-IgE-Antikörper (Ak): Omalizumab (Xolair®)
-
Anti-Interleukin(IL)-5-Ak: Mepolizumab (Nucala®), Reslizumab (Cinqaero®)
-
Anti-IL-5-Rezeptor-Ak: Benralizumab (Fasenra®)
-
Anti-IL-4-Rezeptor-Ak: Dupilumab (Dupixent®)
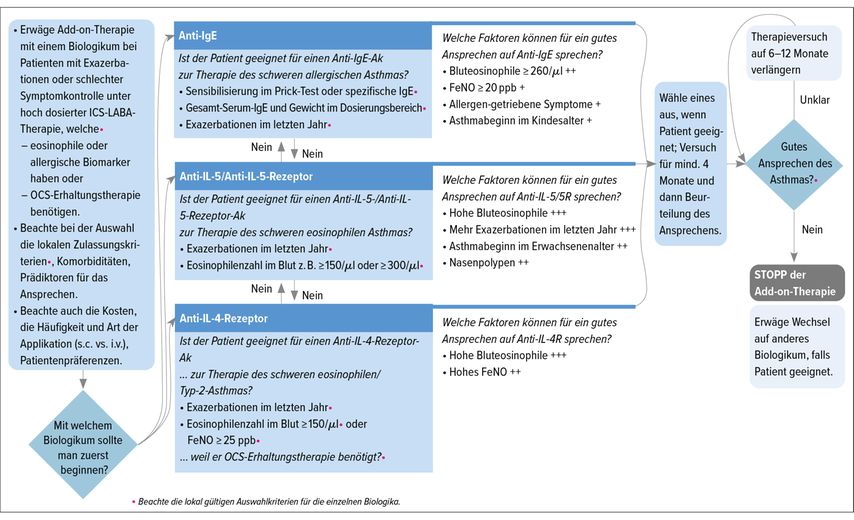
«Eine der häufigsten Fragen, die mir in diesem Zusammenhang gestellt wird, ist: Welches dieser Biologika soll ich meinem Patienten verschreiben?», sagte Prof. Dr. med. Roland Buhl, Mainz. Zuerst muss festgestellt werden, ob der Patient überhaupt für die Behandlung mit einem Biologikum qualifiziert, d.h., ob er entweder ein allergisches oder ein eosinophiles Asthma, erhöhte FeNO-Werte (fraktioniertes exhaliertes Stickstoffmonoxid) und/oder eine Erhaltungstherapie mit OCS hat. Für die Wahl des Biologikums können dann die GINA-Guidelines zurate gezogen werden, die einen einfachen Algorithmus mit klaren Entscheidungskriterien vorschlagen (Abb.2).10 Bei Patienten mit einem eindeutig allergischen Asthma ist ein Anti-IgE-Ak die erste Wahl. Bei schwerem eosinophilem Asthma mit häufigen Exazerbationen ist ein Anti-IL-5(Rezeptor)-Ak oder, wenn die FeNO-Werte sehr hoch sind, ein Anti-IL-4-Rezeptor-Ak angezeigt. Der Behandlungserfolg kann frühestens nach vier bis sechs Monaten beurteilt werden.
Aktuelle Daten zu den Biologika
In den letzten Monaten wurden einige Real-World-Studien zum Einsatz von Biologika bei schwerem Asthma publiziert, welche die Ergebnisse aus den klinischen Studien untermauern. Ein Beispiel dafür ist die REALITI-A-Studie, die belegt, dass Mepolizumab die Exazerbationshäufigkeit und die Dosis der OCS-Erhaltungstherapie auch unter realen Bedingungen signifikant reduziert.13
Eine andere Real-World-Studie ging der Frage nach, wie gross der Anteil der Asthmapatienten ist, die langfristig auf Anti-IL-5-Biologika ansprechen.14 Nach einem Follow-up von 2 Jahren zeigten insgesamt 83% der Patienten ein gutes Ansprechen auf das Biologikum. Bei 69% waren noch gewisse Residuen – am häufigsten eine eingeschränkte Lungenfunktion, unkontrollierte sinunasale Beschwerden und Asthmasymptome – zu verzeichnen. 14% waren sog. Super-Responder, die völlig beschwerdefrei waren. «Diese Patienten kommen in die Sprechstunde und sagen uns, sie seien geheilt und hätten kein Asthma mehr. Unsere Aufgabe besteht darin, sie davon zu überzeugen, dass sie trotzdem zumindest mit der Inhalationstherapie fortfahren müssen», sagte Buhl. 17% der Patienten haben in dieser Studie nicht auf das Biologikum angesprochen und das Medikament wegen einer Verschlechterung der Asthmakontrolle oder aus anderen Gründen abgesetzt.14
Die Biologika wirken nicht nur auf das Asthma, sondern auch auf eine Reihe von Komorbiditäten. So wirkt der Anti-IgE-Ak Omalizumab beispielsweise auch gut gegen Urtikaria und die chronische Rhinosinusitis mit nasaler Polyposis.15,16 Für den Anti-IL-5-Ak Mepolizumab wurde gezeigt, dass er auch bei Patienten mit einem hypereosinophilen Syndrom und bei solchen mit einer chronischen Rhinosinusitis mit nasaler Polyposis gut wirksam ist.17,18 Der Anti-IL-4-Rezeptor-Ak Dupilumab zeigt auch bei atopischer Dermatitis und chronischer Rhinosinusitis mit nasaler Polyposis eine gute Wirksamkeit und ist auch für diese beiden Indikationen zugelassen.19, 20 «Die Wirksamkeit bei diesen typischen Komorbiditäten von Asthma kann die Wahl des Biologikums unter Umständen beeinflussen», so der Experte.
Neues Biologikum in der Pipeline
Tezepelumab, ein neuer humaner monoklonaler Antikörper, der zurzeit in klinischen Studien untersucht wird, ist gegen ein völlig neues Target gerichtet, nämlich das Zytokin TSLP («thymic stromal lymphopoietin»). TSLP ist ein sog. Alarmin und wird bei Asthma von Epithelzellen in den Atemwegen ausgeschüttet, wenn sie einem Reiz ausgesetzt sind. «TSLP spielt in der Pathogenese sowohl des allergischen als auch des eosinophilen Asthmas eine Rolle, weshalb ein Anti-TSLP-Antikörper eine sehr attraktive neue Behandlungoption darstellt», erklärte Buhl. Die im Mai 2021 publizierte NAVIGATOR-Studie ist die erste Phase-III-Studie mit Tezepelumab.21 Bei Erwachsenen und Jugendlichen mit schwerem unkontrolliertem Asthma reduzierte Tezepelumab die jährliche Exazerbationsrate im Vergleich zu Placebo (primärer Endpunkt) sowohl in der gesamten Population signifikant (0,93 vs. 2,1; RR: 0,44; 95% CI: 0,37–0,53; p<0,001) als auch in allen Subgruppen mit unterschiedlich hoher Eosinophilenzahl im Blut (<300, ≥300, <150 und ≥150 Zellen/μl). In der Verumgruppe verbesserten sich zudem die Lungenfunktion, die Asthmakontrolle und die Lebensqualität. Häufigkeit und Art der Nebenwirkungen waren in beiden Gruppen (Verum und Placebo) vergleichbar. «Diese Resultate lassen hoffen, dass wir schon bald ein weiteres Biologikum zur Behandlung des schweren Asthmas zur Verfügung haben werden», schloss Buhl.
Schweizer Register für Patienten mit schwerem Asthma
In der Schweiz leiden rund 5–10% der Asthmapatienten unter schwerem Asthma, es gibt aber noch relativ wenig Real-Life-Daten zu dieser Population. Um dies zu ändern, wurde im Jahr 2018 ein klinisches Register für Patienten mit schwerem Asthma (Swiss Severe Asthma Register, SSAR) eingeführt.22 «Unser Ziel ist, mehr über die Krankheit und ihren Verlauf zu erfahren, Zusammenhänge zwischen verschiedenen Variablen, die einen Einfluss auf das schwere Asthma haben, zu entdecken und eine Bestandesaufnahme unter Berücksichtigung verschiedener Aspekte der Krankheit zu machen», erläuterte Prof. Dr. med. Jörg D. Leuppi, Liestal.
Bisher wurden etwas mehr als 200 Patienten aus allen Regionen der Schweiz in das Register aufgenommen. Um ein möglichst ganzheitliches Bild der Patienten zu bekommen, werden neben der Asthmaanamnese, der Familienanamnese, dem Asthmatyp, dem Raucherstatus usw. die Symptome, die Ergebnisse von asthmaspezifischen Fragebögen und verschiedensten Untersuchungen (Lungenfunktion, Labor, Bildgebung usw.), die aktuelle und die frühere Medikation sowie die Allergien und Komorbiditäten erhoben. «Wir arbeiten zudem mit anderen europäischen Asthmanetzwerken zusammen, erhalten Einblick in ihre Daten und teilen unsere Daten mit ihnen», so Leuppi.
Analyse der ersten 200 Patienten
Prof. Leuppi präsentierte am Kongress einige bisher noch unveröffentlichte Daten der ersten 200 in das Register eingeschlossenen Patienten. 114 davon sind Männer und 86 Frauen, das mittlere Alter liegt bei 55,6 Jahren, der jüngste Patient ist 13 Jahre alt, der älteste 87. Etwa 50% haben ein allergisches Asthma, 35% ein nicht allergisches Asthma und der Rest eine Mischform. Im Jahr vor der Aufnahme ins Register hatten 40% der Patienten keine und etwa die Hälfte eine oder mehr Exazerbationen. Einige wenige hatten mehr als eine Exazerbation pro Monat. «Fast 80% der Patienten werden mit einer ICS/LABA-Kombination behandelt und 40% verwenden zusätzlich ein Anticholinergikum. Fast alle Patienten werden ausserdem mit einem Biologikum behandelt», so Leuppi. Unerfreulich ist der mit 17,5% hohe Anteil an Patienten, die eine Erhaltungstherapie mit OCS haben.
«Die Rekrutierung von Patienten und Zentren geht weiter und wir hoffen, dass das Register eine Selbstverständlichkeit wird. Bleiben bitte auch Sie aktiv und melden Sie Ihre Patienten, die an einem schweren Asthma leiden, beim Register an», forderte Leuppi das Publikum auf.
Quelle:
Jahrestagung der Schweizerischen Gesellschaft für Pneumologie (SGP), 17. und 18. Juni 2021
Literatur:
1 Broder MS et al.: Cost and health care utilization in patients with asthma and high oral corticosteroid use. Ann Allergy Asthma Immunol 2017; 118: 638-9 2 Phipatanakul W et al.: Effects of age and disease severity on systemic corticosteroid responses in asthma. Am J Respir Crit Care Med 2017; 195: 1439-48 3 Shaw DE et al.: Clinical and inflammatory characteristics of the European U-BIOPRED adult severe asthma cohort. Eur Respir J 2015; 46: 1308-21 4 Sweeney J et al.: Clinical management and outcome of refractory asthma in the UK from the British Thoracic Society Difficult Asthma Registry. Thorax 2012; 67: 754-6 5 Heffler E et al.: The Severe Asthma Network in Italy: findings and perspectives. J Allergy Clin Immunol Pract 2019; 7: 1462-8 6 Bleecker ER et al.: Systematic literature review of systemic corticosteroid use for asthma management. Am J Respir Crit Care Med 2020; 201: 279-93 7 Sweeney J et al.: Comorbidity in severe asthma requiring systemic corticosteroid therapy: cross-sectional data from the Optimum Patient Care Research Database and the British Thoracic Difficult Asthma Registry. Thorax 2016; 71: 339-46 8 Volmer T et al.: Consequences of long-term oral corticosteroid therapy and its side-effects in severe asthma in adults: a focused review of the impact data in the literature. Eur Respir J 2018; 52: 1800703 9 Price DS et al.: Adverse outcomes from initiation of systemic corticosteroids for asthma: long-term observational study. J Asthma Allergy 2018; 11: 193-204 10 Global Initiative for Asthma, GINA: Global strategy for asthma management and prevention. 2021; www.ginasthma.org 11 Ververeli K, Chipps B: Oral corticosteroid-sparing effects of inhaled corticosteroids in the treatment of persistent and acute asthma. Ann Allergy Asthma Immunol 2004; 92: 512-22 12 Suehs CM et al.; Oral Corticosteroids Tapering Delphi Expert Panel: Expert consensus on the tapering of oral corticosteroids for the treatment of asthma. A Delphi study. Am J Respir Crit Care Med 2021; 203: 871-81 13 Harrison T et al.: Real-world mepolizumab in the prospective severe asthma REALITI-A study: initial analysis. Eur Respir J 2020; 56: 2000151 14 Eger K et al.: Long-term therapy response to anti-IL-5 biologics in severe asthma-a real-life evaluation. J Allergy Clin Immunol Pract 2021; 9: 1194-200 15 Maurer M et al.: Omalizumab for the treatment of chronic idiopathic or spontaneous urticaria. N Engl J Med 2013; 368: 924-35 16 Gevaert P et al.: Efficacy and safety of omalizumab in nasal polyposis: 2 randomized phase 3 trials. J Allergy Clin Immunol 2020; 146: 595-605 17 Roufosse F et al.: Efficacy and safety of mepolizumab in hypereosinophilic syndrome: a phase III, randomized, placebo-controlled trial. J Allergy Clin Immunol 2020; 146: 1397-405 18 Han JK et al.; SYNAPSE study investigators: Mepolizumab for chronic rhinosinusitis with nasal polyps (SYNAPSE): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Respir Med 2021: S2213-2600(21)00097-7 19 Simpson EL et al.; SOLO 1 and SOLO 2 Investigators: Two phase 3 trials of dupilumab versus placebo in atopic dermatitis. N Engl J Med 2016; 375: 2335-48 20 Boyle JV et al.: Dupilumab in the treatment of chronic rhinosinusitis with nasal polyposis. Immunotherapy 2020; 12: 111-21 21 Menzies-Gow A et al.: Tezepelumab in adults and adolescents with severe, uncontrolled asthma. N Engl J Med 2021; 384: 1800-9 22 Swiss Severe Asthma Register. ClinicalTrials.gov Identifier: NCT03984253
Das könnte Sie auch interessieren:
COPD: die Suche nach undiagnostizierten Patienten
Zahlreiche von COPD und/oder Asthma betroffene Menschen haben niemals eine Diagnose erhalten und stehen folglich nicht unter Behandlung. Mehrere in den vergangenen Monaten publizierte ...
Innovative Pharmakotherapien bei ILD
Derzeit befinden sich mehrere Wirkstoffe für die Behandlung von idiopathischer pulmonaler Fibrose (IPF) und progredienter pulmonaler Fibrose (PPF) in der Entwicklung, wobei verschiedene ...