Die Verwendung von 3D, 4D, VR/AR und Mobile Apps in der Fazialischirurgie
Autoren:
Dr. med. Aaron Metz1
Dr. med. Johannes Steinbacher1
Assoc. Prof. Priv.-Doz. Dr. med. Chieh-Han John Tzou, MBA1,2
1Abteilung für Plastische und Rekonstruktive Chirurgie, Krankenhaus Göttlicher Heiland
2Sigmund Freud Universität Wien, Medizinische Fakultät
E-Mail: aaron.metz@khgh.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Fazialischirurgie befasst sich mit der Reanimation des gelähmten Gesichtes. Um Gesichtsbewegungen und Emotionen zu quantifizieren, existieren bereits verschiedene Bewertungssysteme. Mit zunehmendem technischem Fortschritt steht dem Behandler auch eine wachsende Anzahl an interessanten und vielversprechenden digitalen Software- und Analysetools zur Verfügung.
Keypoints
-
3D-Bildgebungssysteme sind ein schnelles, nicht invasives und objektives Instrument, das zur Analyse verschiedener Gesichtsreanimationsverfahren sowie zur präoperativen Beratung eingesetzt werden kann.
-
4D-Bildgebungssysteme ermöglichen darüber hinaus die Erfassung der Bewegung einer dreidimensionalen Oberfläche im Zeitverlauf und eignen sich daher besonders für dynamische Messungen, wie z.B. der Mimik.
-
Mobile Apps sind ein neuer Trend, der sich weiterentwickeln und den plastischen Chirurgen weiter unterstützen wird (Rehabilitation, Simulation, Patientenbetreuung etc.).
-
Der Einsatz von VR/AR ermöglicht ein schnelles und patientensicheres Training beim Erlernen chirurgischer Fertigkeiten und kann den plastischen Chirurgen in seiner Aus- und Weiterbildung unterstützen.
Die Fazialisparese
Die Gesichtslähmung, auch Fazialisparese genannt, ist eine Schwäche oder Lähmung der Gesichtsmuskeln, die durch Erkrankungen oder Verletzungen des Gesichtsnervs (N. facialis bzw. N. VII) verursacht wird.1 Sie kann eine, manchmal auch beide Gesichtshälften betreffen. Sie kann erworben oder angeboren sein, junge und alte Menschen betreffen und unterschiedlich stark ausgeprägt sein. Die Symptome können von leicht bis schwer variieren, im Laufe der Zeit verschwinden oder sogar dauerhaft bestehen bleiben. Aufgrund der komplexen Anatomie des Gesichtsnervs und des breiten Spektrums an Funktionen des Gesichts kommt es bei den Betroffenen nicht nur zu körperlichen Einschränkungen, wie zu Problemen bei der Nahrungsaufnahme und Speichelverlust, sondern auch zu mangelndem Ausdruck von Emotionen durch eine angemessene Mimik.2
Ursachen für eine Fazialisparese
Eine solche Lähmung des Gesichtes kann durch eine Vielzahl von Pathologien verursacht werden, die alle anatomischen Segmente im Verlauf des Nervus facialis betreffen können. Läsionen können kortikale und subkortikale Regionen, den Nucleus facialis, den Kleinhirnbrückenwinkel, den inneren Gehörgang, das Foramen stylomastoideum, die Ohrspeicheldrüse und die peripheren Äste des Nervus facialis betreffen.3 Zu den Ursachen für Gesichtslähmungen gehören beispielsweise iatrogene Läsionen, neoplastische Erkrankungen, neurologische und angeborene Erkrankungen sowie metabolische Ursachen4 und Infektionskrankheiten,5,6 sie können aber auch im Rahmen von systemischen oder Autoimmunerkrankungen auftreten.7,8 Periphere Gesichtslähmungen können beispielsweise durch iatrogene oder traumatische Ursachen entstehen.9,10 Es existiert jedoch noch eine Vielzahl weiterer Ursachen.
Behandlungsmöglichkeiten
Konservativ
Gemäss internationalen Leitlinien11 wie auch denen der Deutschen Gesellschaft für Neurologie steht derzeit für die idiopathische Fazialisparese vor allem die konservative Behandlung mit Glukokortikoiden und antiviralen Medikamenten im Vordergrund.12
Operativ
Bei irreversiblen Gesichtslähmungen und nach unvollständiger oder mangelhafter Regeneration des Gesichtsnervs wird eine sogenannte chirurgische «Gesichtsreanimation» durchgeführt.13,14 Die Behandlung hängt von der Ätiologie und dem Schweregrad der Nervenverletzung ab. Das ultimative Ziel der chirurgischen Behandlung ist die Wiederherstellung der statischen und dynamischen Symmetrie des Gesichts mit einer emotional verbundenen Gesichtsbewegung.15,16 Die Behandlung muss individuell an jeden Patienten angepasst werden, je nach Ätiologie, klinischer Präsentation, Begleiterkrankungen und auch psychologischer Situation.17 Es gibt eine Vielzahl von chirurgischen Optionen für die Behandlung von Gesichtslähmungen, die grob in Reinnervation (z.B. direkte Nervennaht, Cross-Face-Nerve-Graft) statische Rekonstruktion (z.B. Fascia-lata-Suspension) und dynamische Rekonstruktion (z.B. freier funktionaler Muskeltransfer mittels M. gracilis) unterteilt werden können.18
Klassische analoge Bewertungssysteme
Für die Beurteilungen der Gesichtsbewegung und den Grad der sogenannten «fazialen Dysfunktion» existieren verschiedene Bewertungssysteme, wie z.B. die Gradeinteilung nach House-Brackmann oder das «Sunnybrook»-System.19,20 Weitere Möglichkeiten sind z.B. auch ein patientenbasierter Fragebogen wie das «FaCE»-Skaleninstrument oder das «Chuang Smile Excursion Score System».21,22
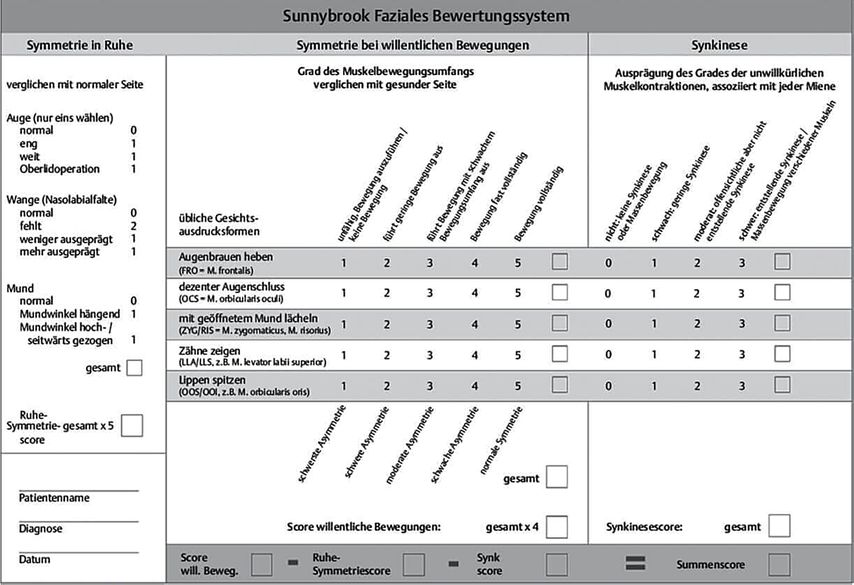
Bei dem weithin etablierten klassischen «Sunnybrook Facial Grading System» nach Brenda Ross et al. werden beispielsweise lokale Parameter untersucht. Mittlerweile existiert davon auch eine deutsche Validierung von Neumann et al. (Abb. 1).23 Mit hoher Sensitivität und Reliabilität stellt dieses ein anerkanntes und verbreitetes diagnostisches Hilfsmittel dar.24 Es werden Ruhesymmetrie, Symmetrie in der Bewegung und Synkinesien anhand eines festgelegten Schemas bewertet (Abb. 1).
Abb. 1: Deutsche Version der Sunnybrook-Skala von Neumann et al.
3D- und 4D-Oberflächenabbildungssoftware
Die Qualitätssicherung in der Behandlung von Patienten mit einer Fazialisparese ist essenziell und erfordert adäquate Instrumente zur Dokumentation des prä- und postoperativen Zustandes. Aufgrund der vielfältigen und dreidimensionalen Veränderungen der Oberfläche, hervorgerufen durch Gesichtsbewegungen und -ausdrücke, stellt deren Darstellung hohe Anforderungen an 3D- und 4D-Systeme.25,26 Im Folgenden soll ein exemplarischer Überblick über Analyseprogramme bzw. Hersteller und ihre 3D- und 4D-Systeme, mobilen Apps und virtuelle Technologien gegeben werden, die für die Behandlung von Gesichtslähmungen relevant sind. Angesichts der rasanten Fortschritte bei den optischen Systemen und der Datenverarbeitungssoftware kann dies nur ein grober Überblick sein.27
Das «Wiener» 3D-Videoanalyse-System
Mit dem von Frey et al. entwickelten System werden Videoaufnahmen von Probanden nach Auswahl der am besten geeigneten Videosequenzen bearbeitet und die 3D-Koordinaten von Landmarken im Gesicht mit der speziell programmierten Software Facialis® generiert. Die Visualisierung der generierten Daten erfolgt mit dem Programm FaciShow®. Damit können zwei- und dreidimensionale Trajektorien jedes gesetzten Markers in Bewegung ausgewertet werden.28
Canfield
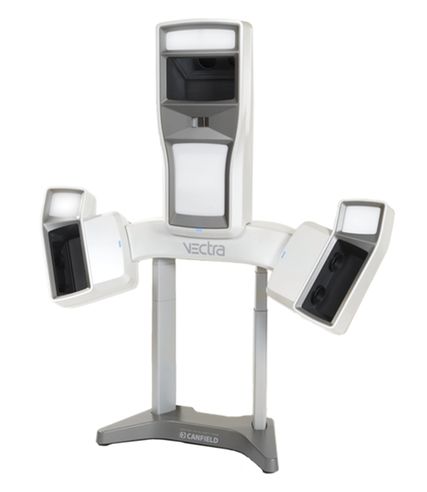
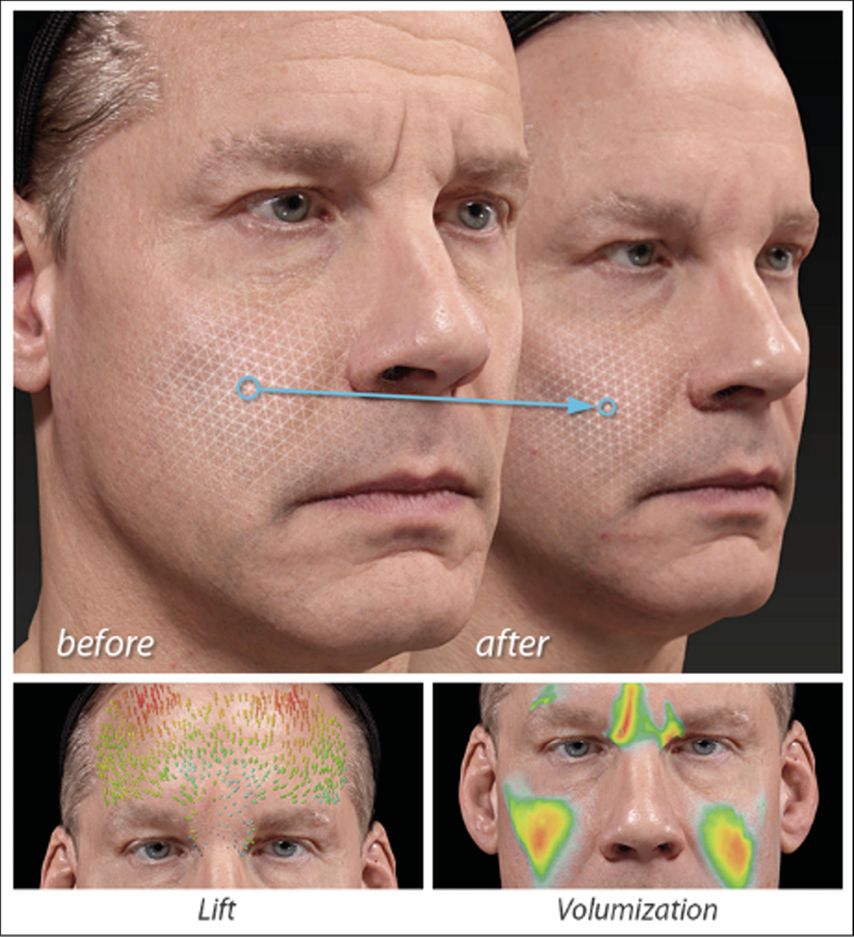
Die 3D-Oberflächenabbildungssysteme von Canfield basieren auf passiver Stereophotogrammetrie. VECTRA® XT (Abb. 2) z.B. erstellt 3D-Bilder von Gesicht, Brust und Körper als 360°-Bilder und Umfangsmessungen. Mithilfe der Software von Canfield sind vielfältige Messungen möglich (Abb. 3). Das Oberflächenregistrierungsverfahren von Canfield wurde bereits bei Patienten mit Gesichtslähmung angewandt und hat sich als äusserst gut reproduzierbar erwiesen.29 Sawyer et al. stellten in ihrer Untersuchung fest, dass die Zuverlässigkeit der Messungen der Bewegung und des Winkels der fazialen Orientierungspunkte zwischen den Beurteilern sehr genau war.30
Abb. 3: Die Software von Canfield bewertet verschiedene Aspekte der 3D-Oberflächenveränderung
Artec 3D
Mit dem Artec Eva wird ein portabler Scanner, der mithilfe von strukturiertem (Weiss-)Licht arbeitet, angeboten. Durch das frei verfügbare Software-Development-Kit (SDK) wird es dem einzelnen Anwender oder Unternehmen ermöglicht, bestehende Software zu modifizieren oder neue Software zu entwickeln. Koban et al. verglichen den Artec-3D-Scanner mit einem Referenzbildgebungssystem (Vectra XT von Canfield Scientific, Inc.) und wiesen nach, dass dreidimensionale Oberflächen, die von Artec Eva für die Gesichtsbildgebung erfasst wurden, eine ähnliche Genauigkeit aufweisen wie die Referenzbilder des Vectra XT.31
Kinect
Kinect (Version I und II, Microsoft) basiert auf der Technologie des strukturierten Lichts und der Laufzeitmessung. Kinect II wurde bereits zur Bewertung von Gesichtslähmungen eingesetzt und bietet Bewertungspunkte nach drei weitverbreiteten traditionellen Klassifizierungssystemen.32 In verschiedenen Studien wurde das Kinect-System für die automatische Klassifizierung von Gesichtslähmungen,33 für ein interaktives orales Rehabilitationsprogramm und für ein System zur Bewertung von Gesichtslähmungen zur Erstellung eines geeigneten Rehabilitationsprogramms eingesetzt.34
Facegram
Dieses System ist in der Lage, komplexe 3D-Gesichtsbewegungen quantitativ und objektiv zu bewerten, indem es eine Reihe von morphologischen, statischen und dynamischen Messungen vornimmt. RGB-D-Kameras nehmen Farb- und Tiefenbilder auf und ein Algorithmus verfolgt die Position der anatomischen Orientierungspunkte von Interesse. Das System liefert nützliche und detaillierte quantitative Informationen, sowohl statisch als auch dynamisch, was es zu einer geeigneten Lösung für die objektive und quantitative Charakterisierung von Gesichtsbewegungen in einer klinischen Umgebung macht.35
Face2Face® App
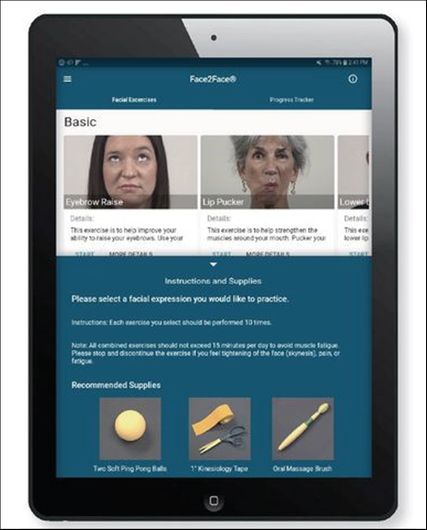
Die Face2Face Facial Palsy App (Kapios Health, Toledo, USA) unterstützt die Behandlung und Rehabilitation von Patienten mit Gesichtslähmung (Abb. 4). Die Anwendung nutzt das Prinzip der Spiegel-Biofeedback-Therapie, das mit positiven Ergebnissen bei der Behandlung idiopathischer Gesichtslähmungen in Verbindung gebracht wurde.36 Das Programm funktioniert wie ein doppelt spiegelnder Spaltspiegel und projiziert die nicht betroffene Seite auf die betroffene Seite, wodurch die Illusion eines vollständigen, symmetrischen Gesichts entsteht. Dies soll den Patienten in eine positive und motivierende Umgebung versetzen, während er die Übungen mit ausreichender Wiederholung durchführt, um langfristige synaptische Veränderungen zu bewirken.37
Virtuelle, erweiterte und gemischte Realität in der plastischen Chirurgie
Virtuelle Realität (VR) ist die Darstellung und gleichzeitige Wahrnehmung der Realität in einer in Echtzeit computergenerierten interaktiven virtuellen Umgebung. Mit anderen Worten: Es handelt sich um eine vollständig immersive Erfahrung, bei der der Nutzer die reale Umgebung hinter sich lässt und über ein VR-Headset eine vollständig digitale Umgebung betritt. Im Gegensatz dazu erlebt ein Nutzer in der erweiterten Realität («Augmented Reality», AR) virtuelle Objekte, die der realen Umgebung über Smartphones, Tablets und Head-up-Displays über AR-Brillen oder -Displays überlagert werden. «Mixed Reality» arbeitet mit digitalen Overlay-Displays, die interaktive Hologramme in das Sichtfeld des Nutzers projizieren. Diese Technologien bieten Ärzten einen freihändigen Echtzeitzugang zu Internetressourcen, vorgefertigten Inhaltsumgebungen oder sogar elektronischen Krankenakten. VR ist ein leistungsfähiges Werkzeug, das zunehmend in der chirurgischen Ausbildung für laparoskopische Eingriffe eingesetzt wird.38,39 Mit AR-Brillen können Chirurgen Details von Ultraschall-, Röntgen- oder MRT-Bildern direkt in den Operationsbereich projizieren.40 Diese Funktion kommt den Auszubildenden bei technisch sensiblen Eingriffen zugute, indem das Operationsfeld mit patientenspezifischen klinischen Informationen (z.B. Lappenperfusion oder Tiefe und Lage von Gefässen) überlagert wird,41 was sich nachweislich positiv auf die Lernkurve und die Verbesserung der grundlegenden psychomotorischen Fähigkeiten im Operationssaal auswirkt.42–44 Radiologische 3D-VR-Trainings in der Anatomie können durch die Umwandlung von 2D-Bildern in ein 3D-Modell unter Verwendung spezieller Algorithmen durchgeführt werden.45 Bei hochspezialisierten und komplexen Operationen wäre es für Ärzte und Patienten von Vorteil, für jede einzelne Gesichtslähmungsoperation individuell zu trainieren. Für jede spezifische Gesichtslähmungsoperation können Regionalmodule mit Eingaben zur Steuerung der Rotations- und Translationsbewegung von 3D-Modellen im virtuellen Raum erstellt werden. Die 3D-Modelle können so gerendert werden, dass die Benutzer die 3D-Modelle durch Neigung des Kopfes und Eingabe des Controllers erkunden können, um die wesentlichen Schritte und Strukturen während jedes chirurgischen Eingriffs zu visualisieren. Diese modularen VR-Schulungen werden die pädagogische Interaktivität erhöhen ( www.facialpalsy.eu ). VR bietet einen reichhaltigen, interaktiven und fesselnden Ausbildungskontext, der «learning by doing» und das intuitive Verständnis anatomischer Strukturen im 3D-Raum unterstützt. Die verbesserte Lernkurve steigert das Interesse und die Motivation und unterstützt wirksam die Wissensspeicherung und den Erwerb von Fähigkeiten.46 Die Vorteile mikrochirurgischer VR-Simulatoren sind endlose Wiederholungen von Operationen, eine sichere Umgebung für Auszubildende und Patienten, eine Rückkehr zum Trainingsprogramm, wo immer der Benutzer es verlassen hat, mögliche stressfreie Bedingungen für bestes Lernen und reduzierte Kosten im Vergleich zu denjenigen, die mit der Aufrechterhaltung von tierbasiertem und leichenbasiertem chirurgischem Training verbunden sind.47 In der heutigen Gesellschaft wächst das Interesse an sichereren Arbeitsplätzen für Patienten und medizinisches Personal. Der Bedarf an einer kosteneffizienten Ausbildung von Personal und die Nutzung von Live-Daten als Trainingsmodule zur Modellierung bestimmter chirurgischer Szenarien steigen. Die virtuelle chirurgische Planung (VSP) ist eine sich entwickelnde Technologie, die die rekonstruktive Chirurgie mit erhöhter rekonstruktiver Genauigkeit, schnelleren chirurgischen Verfahren und verbesserten Ergebnissen erweitern wird.48 AR wurde bereits erfolgreich für die präoperative Planung und Durchführung verschiedener plastisch-chirurgischer Eingriffe eingesetzt.49,50
Abb. 5: Bei «Mixed Reality» werden interaktive Hologramme als digitale Overlay-Displays in das Sichtfeld des Nutzers projiziert
Diskussion und Fazit
Obwohl im Laufe der Zeit bereits zahlreiche Forschungsarbeiten zur Analyse von Gesichtsbewegungen durchgeführt worden sind, hat sich bisher noch keine objektive Methode zur Bewertung des Gesichts durchgesetzt. Die Ergebnisse der chirurgischen Therapie sind daher schwer oder gar nicht vergleichbar.51 Subjektive Methoden zur Klassifizierung von Gesichtslähmungen, wie die House-Brackmann-Skala und das Sunnybrook Facial Grading System, sind zuverlässig und einfach anzuwenden. Da es sich bei diesen Systemen jedoch um beobachterabhängige und somit subjektive Einschätzungen handelt,52 weisen sie eine ausgeprägte Variabilität zwischen den Probanden und zwischen den Beobachtern auf.53 Das schränkt den klinischen Einsatz solcher subjektiven Analyseinstrumente ein, insbesondere bei der Planung von Behandlungen oder der Bewertung von Interventionen.54
Die Technologien haben sich in den letzten Jahrzehnten rasant entwickelt und führen Chirurgen in eine neue Ära der Möglichkeiten, die die Arbeit als Chirurg, die Ausbildung, die präoperative Planung, den Vergleich von Ergebnissen und die Kommunikation mit den Patienten verändern wird. Technologien, die in 3D- und 4D-Bildgebungssystemen sowie in virtueller, erweiterter und gemischter Realität zum Einsatz kommen, sind auf dem Vormarsch und werden allmählich klinisch angewandt. Es sind jedoch weitere Studien und Nachweise erforderlich, um die Praxistauglichkeit dieser Systeme für die Routinearbeit zu definieren.
Quelle:
Inhalt, Abbildungen und Tabellen entstammen dem Buchkapitel «3D, 4D, Mobile APP, VR, AR, and MR Systems in Facial Palsy». Steinbacher J, Metz A, Tzou CHJ. In: Tzou CHJ, Rodríguez-Lorenzo A (eds.): Facial Palsy. Springer International Publishing; 2021. p.405-25.
Mit freundlicher Genehmigung des Springer Nature Verlages und Copyright Clearance Center Lizenz-Nummer 5360051225359.
Literatur:
1 Finsterer J: Eur Arch Otorhinolaryngol 2008; 265(7); 743-52 2 Rosson GD, Redett RJ: J Reconstr Microsurg 2008; 24(6): 379-89 3 Gilden DH: N Engl J Med 2004; 351(13): 1323-31 4 Kariya S et al.: Otol Neurotol 2009; 30(3): 402-7 5 Kangsanarak J et al.:J Laryngol Otol 1993; 107(11): 999-1004 6 Kanerva M et al.: Acta Otolaryngol 2008; 128(4): 460-4 7 van Doorn PA et al.: The Lancet Neurol 2008; 7(10): 939-50 8 Zadro I et al.: Clin Neurol Neurosurg 2008; 110(9): 886-8 9 Mohammed F et al.: J Otolaryngol Head Neck Surg; 37(3): 340-6 10 Tripathi PB et al.: Facial Plastic Surg 2017; 33(1): 116-8 11 Gronseth GS et al.: Neurology 2012; 79(22): 2209-13 12 Heckmann JG: Therapie der idiopathischen Fazialisparese (Bell’s palsy), S2k-Leitlinie, 2022. In: Deutsche Gesellschaft für Neurologie (Hrsg.), Leitlinien für Diagnostik und Therapie in der Neurologie, 2022 13 Frey M et al.: Plast Reconstr Surg 2006; 117(2): 597-608 14 Jowett N, Hadlock TA: JAMA facial plastic surg 2015; 17(4): 293-300 15 Ho AL et al.: Plast Reconstr Surg 2012; 130(1): 91-9 16 Fattah A et al.: Plast Reconstr Surg 2012; 129(2): 340e-352e 17 Michaelidou M et al.: Plast Reconstr Surg 2009; 123, 121-9 18 Tzou CHJ, Rodríguez-Lorenzo A: Principles of smile reanimation. In: Facial palsy: techniques for reanimation of the paralyzed face. Eds. Tzou CH J, Rodríguez-Lorenzo A. Cham: Springer International Publishing, 2021; 129-43 19 House JW: Laryngoscope 1983; 93(8): 1056-69 20 Ross BG et al.: Otolaryngol Head Neck Surg 1996; 114(3): 380-6 21 Kahn JB et al.: Laryngoscope 2001; 111(3): 387-98 22 Tzou CHJ et al.: Annals of Plastic Surg 2015; 74(2) 210-3 23 Neumann T et al.: Laryngorhinootologie 2017; 96: 168-74 24 Coulson SE et al.: Otolaryngol Head Neck Surg 2005; 132(4): 543-9 25 Tzou CHJ, Frey M: Facial Plast Surg Clin North Am 2011; 19(4): 591-602 26 Zhao Y et al.: Head & Face Med 2020; 16(1): 1-10 27 Steinbacher J et al.: 3D, 4D, Mobile App, VR, AR, and MR systems in facial palsy. I In: Facial palsy: techniques for reanimation of the paralyzed face. Eds. Tzou CH J, Rodríguez-Lorenzo A. Cham: Springer International Publishing, 2021; 405-25 28 Tzou CHJ et al.: Annals of plastic surg 2012; 69(2) 173-85 29 Gibelli D et al.: Int J Oral Maxillofac Surg 2020; 49(4): 536-42 30 Sawyer A, See M et al.: J Plast Reconstr Aesthet Surg 2010; 63(1): 65-72 31 Koban KC et al.: J Plast Reconstr Aesthet Surg 2020; 73(1): 141-8 32 Gaber A et al.: Quantifying facial paralysis using the kinect v2. 2015 37th Annual International Conference of the IEEE Engineering In Medicine And Biology Society (EMBC). IEEE 2015: 2497-501 33 Pöhlmann ST et al.: J Med Biol Eng 2016; 36(6): 857-70 34 Pan TY et al.: A Kinect-based oral rehabilitation system. 2015 International Conference on Orange Technologies (ICOT). IEEE 2015: 71-4 35 Gerós A et al.: J Biomedical Inform 2016; 61: 1-9 36 Lindsay R W et al.: Physical Ther 2010; 90(3): 391-7 37 Dorion J: Perspectives on Swallowing And Swallowing Disorders (Dysphagia) 2005; 14: 18-23 38 Schijven M, Jakimowicz J: Surg Endosc 2003; 17(12): 1943-50 39 Pitzul KB et al.: Stud Health Technol Inform 2012; 173: 349-55 40 Tepper OM et al.: Plast Reconstr Surg 2017; 140(5): 1066-70 41 Sayadi LR et al.: Aesthetic surgery J 2019; 39(9): 1007-16 42 Larsen CR et al.: BMJ 2009; 338:b1802 43 Palter VN, Grantcharov TP: J Am Coll Surg 2011; 213: S126 44 Seymour NE: VR to OR.World J Surg 2008; 32: 182-8 45 Ammanuel S et al.: J Med Syst 2019; 43(6): 1-3 46 Sultan L et al.: Adv Med Educ Pract 2019; 10: 907 47 Erel E et al.: Microsurgery 2003; 23(2): 147-52 48 Vles M et al.: J Plast Reconstr Aesthet Surg 2020; 73(11): 1951-9 49 Avraham T et al.: Plast Reconstr Surg 2014; 134(4): 628e-34e 50 Chang EI et al.: Plast Reconstr Surg 2016; 137(2): 619-23 51 Frey M et al.: Plast Reconstr Surg 1994; 93(7): 1334-49 52 Hontanilla B, Aubá C: J Plast Reconstr Aesthet Surg 2008; 61(1): 18-30 53 Linstrom CJ: Laryngoscope 2002; 112: 1129-47 54 Giovanoli P et al.: Br J Plast Surg 2003; 56(7): 644-52
Das könnte Sie auch interessieren:
Medizintourismus für ästhetische Eingriffe und seine Folgen
Günstige Preise und schnelle Termine locken viele Menschen für Schönheitsoperationen ins Ausland. Doch Komplikationen zeigen sich oft erst nach der Rückkehr in die Schweiz – mit teils ...
Pre-pectoral breast reconstruction: PU versus ADM
In immediate pre-pectoral direct-to-implant breast reconstruction, the “interface” choice matters. In this cohort, polyurethane(PU)-coated implants used without acellular dermal matrices ...
Lebensqualität durch minimalinvasive funktionelle Gaumenrekonstruktion
Die funktionelle Rekonstruktion im Kopf-Hals-Bereich zählt zu den anspruchsvollsten Aufgaben moderner Chirurgie, da sie zentrale Lebensfunktionen unmittelbar betrifft. Wenn der weiche ...