Auf die Oberfläche kommt es an
Bericht:
Mag. Sonja Streit
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Brustimplantate können in seltenen Fällen mit der Entstehung des anaplastischen großzelligen Lymphoms assoziiert sein. Die Ätiologie ist bislang noch nicht gänzlich geklärt, wenngleich das Brustimplantat-assoziierte anaplastische großzellige Lymphom (BIA-ALCL) bereits 1997 erstmals beschrieben wurde.
Beim anaplastischen großzelligen Lymphom, das der Obergruppe der Non-Hodgkin-Lymphome angehört, handelt es sich um eine spezielle Form des T-Zell-Lymphoms, das sich im Unterschied zu systemischen T-Zell-Lymphomen wie ein indolentes Lymphom verhält (siehe Factbox). Es kann sich als Spätserom im Implantatlager sowie als solider Tumor mit oder ohne Serom manifestieren und sowohl nach einer Brustrekonstruktion mit Implantaten nach Mammakarzinom als auch nach Augmentation auftreten.
Factbox
Obwohl das ALCL generell als klinisch aggressives Lymphom eingestuft wird, variiert der klinische Verlauf je nach Subtyp stark. So weist zum Beispiel das primär systemische ALCL eine schnelle Progression und Ausbreitung auf. Das PC-ALCL ist im Vergleich zu den systemischen Formen klinisch benigner mit über 95% 5-Jahres-Überleben bei den Betroffenen. Basierend auf den bislang längerfristig nachuntersuchten Fällen scheint das BIA-ALCL dem PC-ALCL mit einem eher wenig aggressiven Verlauf im Vergleich zu den systemischen Formen zu folgen, nichtsdestotrotz wird es von der WHO weiter als lymphoproliferative Krebserkrankung klassifiziert.1
Ätiologie nicht eindeutig
Wenngleich die FDA vor über zehn Jahren bestätigte, dass Brustimplantate als Auslöser für diese neue Tumorentität verantwortlich sind, konnte die Pathogenese noch immer nicht eindeutig analysiert werden. Dies bestätigt auch der Facharzt für Hämatologie und Onkologie Dr. Andreas Pircher: „Es gibt verschiedene Hypothesen, wie jene zum subklinischen Biofilm. Des Weiteren wird eine chronische T-Zell-induzierte Immunantwort auf Bakterien oder Silikon ebenso diskutiert wie eine direkte immunologische Antwort des Körpers in Form einer implantatinduzierten chronischen Inflammation.“ Auch Partikelabrieb kommt als möglicher Trigger infrage. Eine große Rolle spielt vermutlich die Texturierung der Implantate, wie der Facharzt für Plastische, Ästhetische und Rekonstruktive Chirurgie Dr. David Lumenta erläutert: „Nach derzeitigem Wissensstand geht man davon aus, dass eher texturierte Implantate mit der Entstehung eines BIA-ALCL vergesellschaftet sind.
Es liegen zwar relativ wenig Fälle vor, aber der Großteil der Erkrankten trug texturierte Implantate. Ein Hersteller war besonders betroffen und nahm seine Brustimplantate freiwillig vom Markt. Diese waren extrem mit der Umgebung verwachsen. Wir gehen davon aus, dass Texturierung und möglicherweise die Herstellungsart hier eine Rolle gespielt haben.“ Das BIA-ALCL tritt frühestens ein Jahr nach der Implantation auf, die mittlere Implantatverweildauer liegt bei acht bis zehn Jahren. Es empfiehlt sich, BIA-ALCL als Differenzialdiagnose in Erwägung zu ziehen, wenn mindestens ein Jahr nach Einsetzen der Implantate ein Serom auftritt und Trauma oder Infektion als Ursache ausgeschlossen werden kann. David Lumenta empfiehlt: „Eine unspezifische Schwellung, die plötzlich auftritt, kann auf die Erkrankung hindeuten. Beim BIA-ALCL spielt die Verweildauer der Implantate eine Rolle, während das Alter der Patientin diesbezüglich keinen besonderen Stellenwert hat.“
Mehrstufige Diagnostik
Das BIA-ALCL äußert sich in Form einer optisch erkennbaren Schwellung oder einer Asymmetrie. Des Weiteren können Schmerzen bestehen, Knoten oder Veränderungen der Haut, wie z.B. Rötungen aufgrund einer Inflammation, erkennbar sein. Da die Mammografie in Bezug auf die Erkrankung keine Rolle spielt, hat sich die Sonografie als unverzichtbares Diagnosetool etabliert. Diese ermöglicht im Rahmen der Untersuchung die Detektion periimplantärer Flüssigkeit sowie eine ultraschallüberwachte Punktion zum Zwecke einer Zytodiagnostik und einer mikrobiologischen Diagnostik. „Mithilfe der Sonografie lassen sich außerdem Lymphknoten und ableitende Lymphwege axillär, supraklavikulär und parasternal untersuchen“, so Andreas Pircher. „Aus dem Serom sollten eine Aspirationszytologie und eine Flow-Zytometrie zur weiteren Diagnostik veranlasst werden. Eine zusätzliche MRT ist bei unklaren Fällen ebenfalls empfehlenswert. Bezüglich der Abklärung gibt es seit März 2017 die ersten Konsensus-Leitlinien zur Diagnostik und Therapie des BIA-ALCL, welche von Clemens et al.2 veröffentlicht wurden.“ Bestätige sich der Verdacht durch die zytologische Untersuchung und sei eine immunhistochemische Testung auf CD30 positiv, so könne die Diagnose eines BIA-ALCL gestellt werden. Der ALCL-Nachweis gelinge über die immunhistochemische Testung von CD30.
Dieses Oberflächenprotein aus der Gruppe der TNF-Rezeptoren sei in einem benignen periprothetischen Serom nicht nachweisbar. „Die pathologische Aufarbeitung ist ein Kernbestandteil und sehr wichtig, um die weitere Therapie zu planen. Ist die Diagnose eindeutig, sollte im weiteren Verlauf zum Zwecke des Stagings ein PET-CT erfolgen, um festzustellen, ob es sich um eine lokale Manifestation, also um eine auf die Kapsel begrenzte Form des Lymphoms, handelt. Die Therapie richtet sich nach dem Erstdiagnosestadium.“
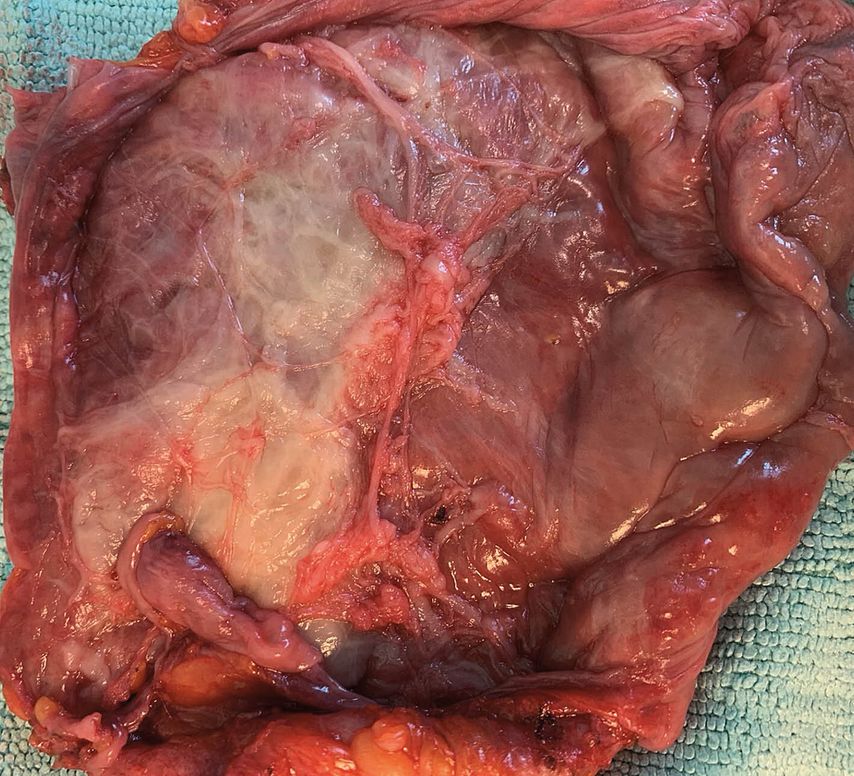
Multimodales Therapiekonzept
Wurde das BIA-ALCL eindeutig diagnostiziert, ist eine Operation unumgänglich, wie Dr. Lumenta erklärt: „Aus chirurgischer Sicht ist im Falle dieser Erkrankung eine En-bloc-Resektion indiziert. Diese umfasst eine vollständige Entfernung der Kapsel inklusive Implantat sowie angrenzender Tumormasse und verdächtiger Lymphknoten.“ Dr. Pircher ergänzt: „Gegebenenfalls ist je nach Ausbreitung eine Nachbestrahlung der Brust oder eine Systemtherapie angezeigt, sobald die Operation erfolgt ist. Die radikale Entfernung im frühen Stadium ist nach bisheriger Datenlage kurativ. Nur bei disseminierter Erkrankung oder Inoperabilität sollte eine Chemotherapie beziehungsweise eine Bestrahlung zusätzlich durchgeführt werden, die Daten hierfür sind limitiert. Die Besprechung in einem hämatologischen Tumorboard und Referenzzentrum sollte vor Beginn einer Therapie immer erfolgen.“ Dr. Lumenta plädiert dafür, Patientinnen im Aufklärungsgespräch auch über diese Erkrankung zu informieren, erklärt aber: „Ich habe dazu einen recht pragmatischen Zugang. Nachdem noch immer nicht alles eindeutig hinsichtlich der Entstehung geklärt ist, würde ich Patientinnen keineswegs prophylaktisch von texturierten Implantaten abraten. Aber ich halte es für wichtig, sie über BIA-ALCL aufzuklären. Auch wenn jährlich nur 0,35–3/1 Million Frauen betroffen sind.“ Dr. Pircher empfiehlt eine regelmäßige Nachbeobachtung in einer hämatologisch-onkologischen Ambulanz.
Beide Experten plädieren dafür, das BIA-ALCL interdisziplinär zu diagnostizieren und zu behandeln. Es gebe keine Garantie, nicht daran zu erkranken, wenn man glatte Implantate trage, wenngleich es häufiger bei texturierten Brustimplantaten vorkomme. Wichtig sei, umfassend darüber aufzuklären und eine plötzlich auftretende Flüssigkeitsansammlung, die frühestens nach einem Jahr unvermittelt auftrete, mit dieser Erkrankung in Verbindung zu bringen und dies entsprechend abzuklären.
Literatur:
1 Kricheldorff J et al.: Brustimplantat-assoziiertes Lymphom – Diagnostik und Therapie einer neuen Tumorentität. Übersichtsarbeit. Dtsch Arztebl Int 2018; 115: 628-35 2 Clemens MW, Horwitz SM: NCCN Consensus Guidelines for the diagnosis and management of breast implant-associated anaplastic large cell lymphoma. Aesthet Surg J 2017; 37(3): 285-9
Das könnte Sie auch interessieren:
Diabetes und ästhetische Behandlungen
Diabetes ist mit einer Prävalenz von über 10% eine der häufigsten Erkrankungen und sollte daher auch bei ästhetischen Leistungen beachtet werden. Die Mehrheit unserer ästhetischen ...
Aktuelle Versorgungssituation von trans Männern
Die Versorgung von trans Personen ist in Österreich auf wenige Kliniken und Fachabteilungen beschränkt. Noch immer bestehen Ressentiments und die Patientengruppe wird in ...
Funktionell-ästhetische Nagelchirurgie
Die Entwicklung der Nagelchirurgie ist im Vergleich zu anderen chirurgischen Disziplinen noch wenig weit fortgeschritten. Dennoch stehen verschiedene Methoden sowohl zur Diagnosestellung ...