Chirurgische Knorpeltherapie der Schulter
Autoren: PD Dr. med. Patrick Vavken1, 2
Dr. med. Jana Jensen1
1 alphaclinic Zurich, Zürich
2 ADUS Klinik, Dielsdorf
E-Mail: vavken@alphaclinic.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Arthrose der Schulter gehört zu den am stärksten wachsenden Indikationen für operative Eingriffe in der Orthopädie und Unfallchirurgie. Obwohl dies vor allem den Gelenkersatz bei Arthrose betrifft, gibt es auch Bestrebungen, frühe, fokale Knorpeldefekte zu behandeln, um Ersteres zu vermeiden bzw. zu verzögern. Aber nicht nur die Entschleunigung der arthritischen Degeneration der Schulter ist ein Ziel; es zeigt sich auch zunehmend, dass Knorpeldefekte die postoperativen Ergebnisse von Schulterstabilisierung und Rotatorenmanschettennaht negativ beeinflussen können, sodass deren Behandlung wiederum auch hier an Bedeutung gewinnt. Dieser Artikel gibt einen Überblick über die limitierte, aber stetig wachsende Evidenz zur chirurgischen Knorpelbehandlung der Schulter.
Keypoints
-
Knorpeldefekte des Schultergelenks treten in bis zu einem Drittel der Patienten auf. Zumeist sind sie asymptomatisch. Behandlungswürdige Probleme sind aber möglich, sowohl bei isolierten Defekten, besonders aber auch in Verbindung mit anderen Pathologien.
-
Knorpeldefekte haben einen negativen Effekt auf das Ergebnis von Stabilisierungseingriffen. Eine Behandlung des Knorpels im Rahmen des Stabilisierungseingriffs muss abgewogen werden, Hilfestellungen dafür sind publiziert.
-
Knorpeldefekte haben keine gesicherten Auswirkungen auf die Ergebnisse der Rotatorenmanschettennaht und können oft abwartend behandelt werden.
-
Für die Behandlung von Knorpeldefekten der Schulter haben sich, analog zum Knie, verschiedene Therapieoptionen entwickelt.
-
Unter den regenerativen Therapien hat sich zurzeit noch kein definitiver Favorit entwickelt. Verfügbarkeit von und Erfahrung mit einzelnen Methoden dürfen in die Behandlungsplanung einfliessen.
-
Komplikationen und Revisionen sind nicht kohärent analysiert und publiziert, sie sind aber nicht selten. Bis zu 30% der Patienten werden zu Prothesen konvertiert, zum Teil aber erst nach Jahren. Somit sind diese Therapien erfolgreich im Verzögern, aber nicht Verhindern eines Gelenkersatzes.
Fokale Knorpelschäden der Schulter
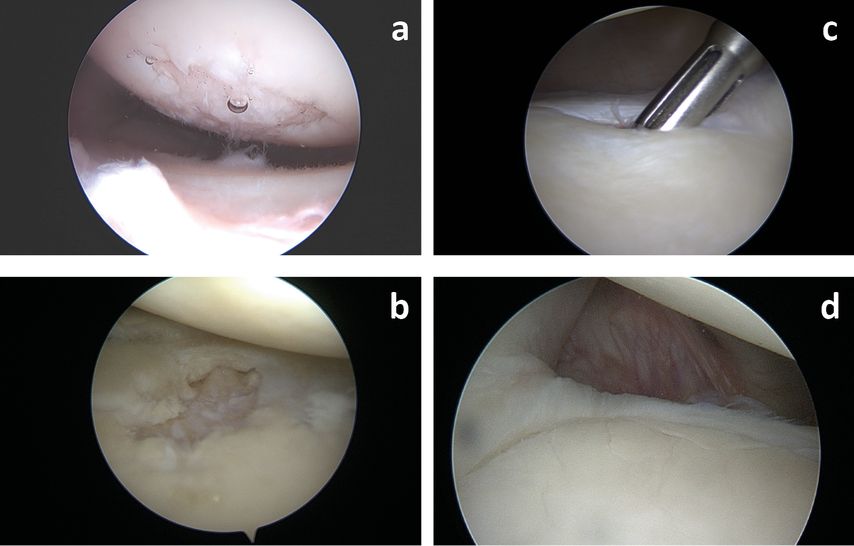
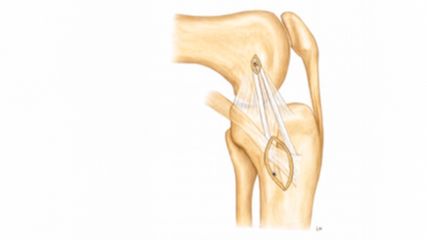
Generell sind fokale Knorpeldefekte in der Schulter verhältnismässig selten, in der klinischen Wahrnehmung aber noch viel seltener (Abb.1). Typischerweise treten sie in Verbindung mit einer anderen Pathologie auf. So untersuchten Gartsman et al. 200 Patienten mit Rotatorenmanschettenläsionen und fanden 9 (4,5%) Knorpeldefekte. In Verbindung mit Instabilität treten Knorpeldefekte häufiger auf, wobei der Grossteil (ca. 40%) durch Hill-Sachs-Läsionen verursacht wird. Wirkliche fokale Knorpelabscherungen sind eher mit hinteren Instabilitäten assoziiert und starten oft mit einer feinen Rissbildung, die sich später auswächst. Nachgewiesen, aber nicht quantifiziert, sind zum Beispiel weitere Assoziationen mit chemischer und mechanischer Chondrolyse, avaskulärer Nekrose und septischer Arthritis. Zuletzt gibt es noch eine hohe Dunkelziffer iatrogener Schäden durch intraartikuläre Infiltrationen, Fadenanker, Instrumentenhandling und dergleichen. Es scheint, dass humerale Defekte zwei- bis dreimal häufiger sind als glenoidale Defekte, aber daraus sollte keine Schlussfolgerung auf klinische Relevanz gezogen werden.
Abb. 1: Knorpeldefekte in der Schulter treten, laut aktueller Literatur, in bis zu einem Drittel der Patienten auf, aber als sehr heterogene Gruppe. Humerale Knorpeldefekte (a) sind in rezenten Studien eher mit höherem Patientenalter assoziiert, während fokale Knorpeldefekte des Glenoids (b) auch oft bei jüngeren Patienten iatrogen auftreten. Bei Instabilitäten kommt es oft zu einer Chondromalazie im Sinne von Erweichen des Knorpels (c) oder Rissbildung (d)
Zunehmend erschwert wird die Diagnostik der fokalen Knorpelschäden durch die oft geringen Symptome und die Probleme der apparativen Diagnostik. In vielen Fällen sind die Patienten weitgehend asymptomatisch. Fokale Defekte führen aber auch zu den für Knorpeldefekte klassischen, aber für den «Hausgebrauch» der Schulter oft untypischen Beschwerden, wie tiefen Schmerzen im Gelenk, Krepitus, unspezifischer Bewegungseinschränkung (im Vergleich zur sehr spezifischen Einschränkung der Frozen Shoulder) und belastungsabhängigem Schmerz auch ausserhalb der Provokationsvektoren der Manschette.
Mehrere Studien haben sich mit der apparativen Diagnostik der glenohumeralen Knorpelschäden auseinandergesetzt. Jene schneidet dabei eher bescheiden ab. Spencer et al. verglichen 2013 das native MRT mit Ergebnissen der Arthroskopie als Goldstandard und fanden eine Sensitivität von knapp 30% und eine Spezifität von 80%. Van Beek et al. konnten bereits 2007 ähnliche Ergebnisse sehen, aber bemerkten vor allem bei den Low-Grade-Defekten Probleme mit der Reliabilität. Das heisst aber nicht, dass glenohumerale Knorpeldefekte selten am MRT gesehen werden. Guntern et al. fanden 2003 solche Defekte bei einem Drittel aller Patienten, die eine MR-Arthrografie für subakromiales Impingement (sic!) vornehmen liessen. Die relevanteren Probleme sind eher die Interpretation der Schwere und das Interobserver-Agreement.
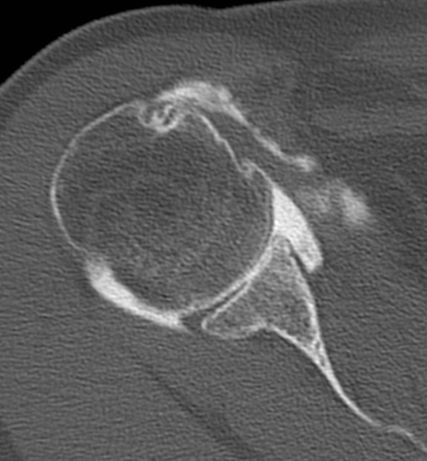
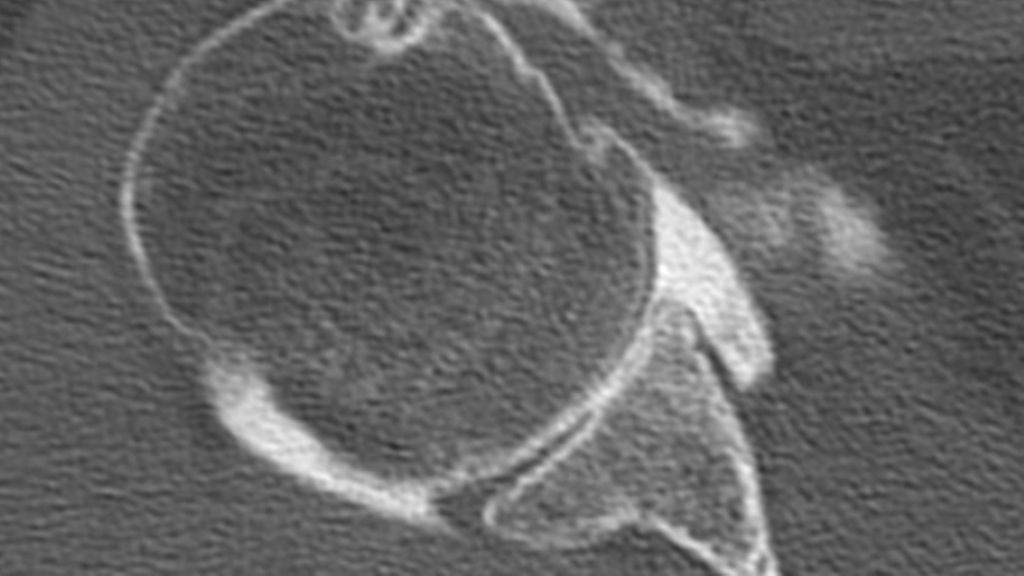
Abb. 2: Anhaltende Instabilität kann zur Abrasion von Gelenkknorpel und Labrum führen und damit die Geometrie der Schulter verändern. Man spricht von einer chondrolabralen Ante(Retro)version. Achtung: Diese ist im nativen CT nicht zu sehen, kommt aber im Arthro-CT zur Darstellung. Dies ist auch als negativer Risikofaktor im postoperativen Ergebnis nach Schulterstabilisierung publiziert.
Erst jüngst wurde die Bedeutung von fokalen Knorpeldefekten für operative Ergebnisse besser untersucht. Nourissat et al. untersuchten 2020 150Patienten nach einer hinteren Stabilisierung. Ihr Interesse galt dem Einfluss mehrerer Variablen (Alter, Geschlecht, Art der Läsion, Art der Operation, Trauma etc.) auf die Ergebnisse der Operation in klinischen Scores nach 51Monaten. Sie fanden dabei heraus, dass lediglich der glenoidale Knorpeldefekt ein relevanter Risikofaktor für ein schlechteres Ergebnis war. Der vorgeschlagene Pathomechanismus dahinter ist eine Übergangssituation von einem normalen Glenoid mit instabiler, aber reduzierbarer glenohumeraler Zentrierung hin zu einer statischen posterioren Subluxation (Abb. 2). Das führt sogar dahin, dass Fernando et al. erst dieses Jahr im «Journal of Shoulder and Elbow Surgery» (JSES) den «cartilage wear index» vorschlugen. Anhand von 26 Patienten konnte diese Gruppe zeigen, dass die präoperative Klassifikation von glenoidalen Knorpeldefekten die Entscheidung zu und die klinischen Ergebnisse nach einer Refixation des hinteren Labrums leiten kann.
Für die Rotatorenmanschettennaht zeigt sich eine ähnliches, aber weniger gravierendes Bild. So untersuchten Baumgarten et al. 2020 knapp 300 Rotatorenmanschettenrefixationen nach und fanden chondrale Schäden bei einem Drittel der Patienten. Nach fast 4 Jahren zeigte sich bei allen Patienten eine klinisch relevante Verbesserung (gemäss «minimal clinically important difference», MCID) nach der Sehnennaht. Knorpelschäden, vor allem bipolare Läsionen, zeigten einen negativen Effekt auf das postoperative Ergebnis, aber nicht in einem Ausmass, das die klinisch relevante Verbesserung aufheben würde. Interessanterweise zeigten sich Knorpeldefekte statistisch signifikant gehäuft bei Patienten mit reparaturwürdigen Subscapularisläsionen, was wiederum das klinische Bild der Instabilität unterstellt. Kukkonen et al. untersuchten 2013 85 Patienten mit arthroskopischer Manschettennaht, von denen wiederum ein Drittel mittel- bis höhergradige Knorpeldefekte hatte. Hier wurde ein relevanter Einfluss auf prä- und postoperative Constant-Scores gesehen. Weitere Studien unterstützen diese Daten und zeigen einen konstanten, schweregradabhängigen Einfluss von Knorpelschäden auf die gesamthafte Verbesserung nach einer Rotatorenmanschettennaht.
Konservative Behandlung
Obschon der Schwerpunkt des Artikels die chirurgische Behandlung ist, soll die konservative Behandlung von Knorpelschäden der Schultern nicht unterschlagen werden. Wie bei jedem anderen Gelenk empfiehlt sich auch hier initial zumindest der Versuch einer konservativen Therapie. Die Aktivitätsmodifikation in Beruf und Freizeit steht an erster Stelle. Gerade bei manuell tätigen Patient*innen oder Personen mit hohem sportlichem Anspruch ist dies aber meist sehr schwer, wenn nicht sogar unmöglich. Analgetika können schmerzlindernd wirken. Begleitprobleme wie Kapsulitiden können effektiv behandelt werden, um Schmerzspitzen zu kupieren. Infiltrationen mit Hyaluronsäure oder Thrombozytenkonzentraten wurden auf ihren symptomlindernden oder krankheitsverzögernden Effekt hin untersucht, und wenn es auch teils vielversprechende Ergebnisse hat, ist die Gesamtlage der Evidenz noch immer karg. Wiederholte Kortisoninfiltrationen haben Gewebeschäden und erhöhtes Infektrisiko gezeigt. Wenn die konservative Therapie ausgeschöpft ist, sollte eine stufenweise eskalierende chirurgische Strategie verfolgt werden. Ziel dabei ist es, bei wenig Schmerz eine gute Funktion zu erreichen und die prothetische Versorgung so lange wie möglich/nötig hinauszuzögern.
Synovektomie und Debridement
Die wahrscheinlich bekannteste chirurgische Behandlung von Knorpelschäden der Schulter ist die Synovektomie, die Entfernung freier Gelenkkörper und loser «Flaps» mit oder ohne Chondroplastik bzw. Knorpelglättung. Dieses Debridement hat im Vergleich zu den anderen hier aufgeführten Eingriffen zwei Alleinstellungsmerkmale: 1) Es zielt auf eine symptomatische Therapie, aber nicht auf Regeneration ab. 2) Es braucht für die adäquate Indikation keine «Full thickness»-Defekte.
Obwohl diese Therapie sicherlich global am häufigsten zum Einsatz kommt, gibt es wenig strukturierte Untersuchungen. Eine besondere Dunkelziffer hat es zusätzlich bei Debridements als Knorpeltherapie in Verbindung mit anderen Eingriffen. Aus einer Reihe von Fallstudien und retrospektiven Kohorten wird ein positiver, aber nicht immer statistisch signifikanter Effekt berichtet. Wie bereits oben beschrieben, haben bipolare Läsionen schlechtere Ergebnisse als unipolare Läsionen.
Die untersuchten Patientenpopulationen verdienen aber genauere Aufmerksamkeit. In den meisten Fällen handelte es sich in den Studien zum Debridement eher um frühe oder mittelschwere Fälle von (generalisierten) Omarthrosen und nicht um fokale Defekte. Hier stellt sich aber die Frage, ob die deutlich umfänglichere CAM («comprehensive arthroscopic management») Procedure, welche auch eine Osteophytenresektion und Kapselresektion beinhaltet, eine bessere Option wäre, besonders in Hinblick auf Verbesserung von Beweglichkeit und Kapselschmerz. Die CAM Procedure – wie von Millet et al. beschrieben – ist aber technisch nicht unaufwendig und als arthrosetherapeutische Alternative zum Gelenkersatz entwickelt, nicht als typische Knorpeltherapie.
Regenerative Therapie für Knorpeldefekte der Schulter
Eine Reihe von regenerativen Knorpeltherapien, die auf eine Heilung mit knorpeligem Narbengewebe abzielen, ist zurzeit verfügbar. Sie sind aus den Knorpeltherapien des Knies abgeleitet bzw. weiterentwickelt. Der Bedarf an Anpassung entsteht, da die Schulter – anders als das Knie – kein lasttragendes Gelenk ist und sich auch die Biologie und die Mechanik des glenohumeralen Gelenks von denen des Knies unterscheiden. Wie bei vielen anderen orthopädischen Themen ist auch hier die Studienlage von Nachuntersuchungen und heterogenen Patientenkollektiven geprägt. Die Evidenz ist daher in ihrer Qualität limitiert und kann nicht immer automatisch extrapoliert werden.
Mikrofrakturierung
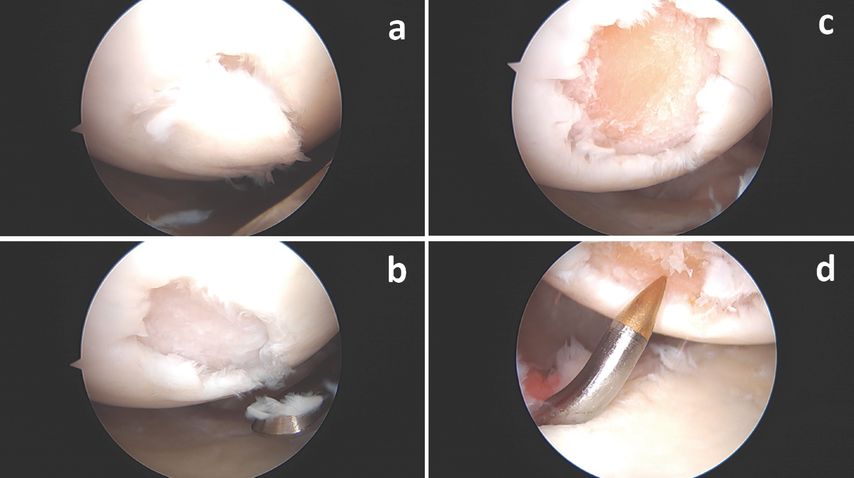
Die geringe technische Schwierigkeit (prima vista) und der begrenzte Materialbedarf machen die Mikrofrakturierung zu einer sehr häufigen Behandlungsoption für Knorpeldefekte der Schulter (Abb. 3). Millet et al. publizierten eine Serie mit 30 Patienten (31 Schultern) und zeigten, dass der Schmerz gemäss VAS (0–10) sich effektiv von 4 auf 2 Punkte halbierte. Frank et al. zeigten in ihrer Serie von 17 Schultern und 2 Jahren Nachuntersuchung eine Reduktion von 5,8 auf 1,9 Punkte. Snow und Funk konnten in ihrer Studie 2008 auch entsprechende Ergebnisse sehen.
Wang et al. publizierten 2018 eine Langzeitstudie mit 10 Jahren Nachuntersuchungszeitraum. Hier mussten 20% binnen 10 Jahren zu einer Prothese konvertieren, ein Drittel der Fälle wurde als Therapieversager angesehen. Dies ist aber konsistent mit Daten aus Langzeitstudien zur Mikrofrakturierung des Knies. Auch hier wird eine ähnlich hohe Versagensrate gesehen, respektive eine höhere als mit anderen Knorpeltherapietechniken. Zur Art des Versagens im Bereich der Schulter ist wenig publiziert, und die Frage nach intraläsionalen Osteophyten ist noch offen. Eine Bewegung von der Mikro- zur Nanofrakturierung steht in der Schulterchirurgie offiziell noch aus. Aber da bei einer guten Zahl der Patienten die verhältnismässig dünnen Ankersetzinstrumente und nicht die spezifischen Mikrofrakturierungsahlen benutzt werden, muss von einer Dunkelziffer oder Mischform ausgegangen werden.
Osteochondrale Transfers
Transfers osteochondraler Zylinder sind eine attraktive Option in der Knorpeltherapie. Das Knorpelgewebe ist hoch differenziert und gut mit dem Knochenzylinder verbunden. Das Einheilen erfolgt Knochen auf Knochen und damit schnell und fest. Aber es gibt auch Nachteile. Die Verfügbarkeit autologer Gewebe ist durch Durchmesser und Kongruenz begrenzt, bei allogenem Gewebe sind der Gesetzgeber und die verbundenen Kosten limitierende Faktoren. Da der Zylinder orthogonal eingebracht werden muss, ist die Anwendbarkeit in der Schulter durch die Erreichbarkeit begrenzt, speziell bei Nutzung der handelsüblichen und auf die Kniechirurgie ausgerichteten Instrumente. Meist wird hier ein offener Zugang, unter Umständen mit einer chirurgischen (Sub)luxation, gewählt.
Scheibel et al. berichten von 8 Patienten mit Transfers autologer osteochondraler Zylinder vom Knie zur Schulter. Nach 32 Monaten zeigten sich exzellente klinische Ergebnisse im Constant-Score und gutes Einheilen im MRT. Kircher et al. untersuchten die gleiche Population ein weiteres Mal und zeigten den Erhalt der Verbesserung und eine erfolgreiche Verzögerung der weiteren arthrotischen Degeneration nach 8,8 Jahren.
Als besondere Form der osteochondralen Knorpeltherapie sei hier auch der Transfer der lateralen Klavikula zur Rekonstruktion des Glenoids zu erwähnen. Diese Therapie kann als Alternative zum Latarjet angesehen werden, die nicht nur Knochenverlust adressiert, sondern auch neues Knorpelgewebe beibringt. Natürlich geht dafür aber der Weichteileffekt durch die Verschlingung des «conjoint tendon» mit der Sehne des Subscapularis verloren.
Global gesehen sind «Fresh frozen»-Allografts von Bedeutung, im deutschsprachigen Raum ist deren Anwendung aber durch die gesetzlich geforderten Inaktivierungsverfahren deutlich limitiert. Die Nutzung aufbereiteter Allografts ist in unseren Breitengraden einfacher durchführbar, zeigt aber ähnliche Vorteile. Die Operationszeit verkürzt sich und die «donor site morbidity» entfällt. Das suggeriert eine schnellere Rekonvaleszenz. Was die Kongruenz, sprich Passform, angeht, haben einzelne Studien gezeigt, dass das mediale Tibiaplateau eine ähnliche Geometrie wie das zentrale Glenoid hat, sodass Allografts auch von hier gewonnen werden können. Die Literatur unterstützt die Nutzung von Allografts. Riff et al. haben 2017 eine Studie zu 20 Patienten mit Allografttransfers für den Humeruskopf publiziert. Dort fand man nach 2 Jahren signifikante Verbesserungen von Schmerz per VAS und Funktion per SST, ASES und SF-12. Notabene wurden aber mehr als die Hälfte der Patienten (11/20) ebenso mit einer Mikrofrakturierung und einem Meniskus-Allograft-Resurfacing des Glenoids behandelt. 4Patienten wurden nach Ende der offiziellen Nachuntersuchung zu einer vollen Schulterprothese konvertiert. Man muss also hier eher von einer versuchten Salvage Procedure ausgehen und nicht von einer regenerativen Therapie. Diklic et al. hatten 2010 13 Patienten mit Knorpeldefekten und chronischer hinterer Instabilität mit Allografts aus Femurköpfen behandelt. Diese Gruppe sah über einen Nachuntersuchungszeitraum von 54 Monaten keine Einschränkung in Schmerz oder Beweglichkeit bei 9 (69%) der behandelten Patienten. 3 Patienten berichteten von anhaltenden Schmerzen postoperativ, 1 Patient entwickelte eine Osteonekrose im Humeruskopf.
In Summe zeigt sich, dass in der Gesamtheit der Literatur osteochondrale Transfers oft bei fortgeschrittenen Defekten und in Verbindung mit anderen Techniken eingesetzt werden. Das erschwert die Vergleichbarkeit, kann aber erklären, warum die Ergebnisse in der Schulter in der Literatur tendenziell schlechter sind als die für Knorpeldefekte am Knie, die meist früh und isoliert behandelt werden (können).
Knorpelzelltransfers
Wie im Knie ist auch in der Schulter der Knorpelzelltransfer eine interessante Option für die Behandlung fokaler Defekte. Im klassischen Verfahren wird dabei Knorpel chirurgisch gewonnen (1. Eingriff), im Labor bearbeitet und gezüchtet und dann wieder in die Schulter implantiert (2. Eingriff).
Ein solches Vorgehen wurde von Romeo et al. 2002 im Rahmen eines Fallberichts eines 16-jährigen Patienten beschrieben. Dies war ein Eingriff der sog. 1. Generation, bei der ein Periostlappen benutzt wird, um den Defekt zu decken. Nach 12 Monaten zeigten sich zwar gute Ergebnisse, aber als einzelner Fall ist der Zuwachs an Evidenz beschränkt. Buchmann et al. benutzten 2012 bereits ein Biomaterial, um 4 Patienten zu behandeln. Nach 41Monaten zeigten sich gute klinische und MR-tomografische Ergebnisse. Boehm et al. publizierten 2020 gute klinische Ergebnisse für SSV, VAS und Constant-Score für 7 Patienten, die mit 3D-Sphäroiden mit autologen Chondrozyten behandelt wurden.
Technisch und ökonomisch besonders interessant ist die Möglichkeit des «minced tissue». Hier wird Knorpel in einer einzigen Operation gewonnen, fragmentiert, mit autologem Plasma vermengt und in einen Defekt appliziert. Lorenz et al. beschrieben 2021 die Technik en détail. Spezifisch für die Schulter gibt es wenig Daten zu «Minced tissue»-Prozeduren, aber Studien mit anderen Gelenken wie Knie, Sprunggelenk oder Hüfte zeigten für die Technik, teils auch unter «particulated juvenile cartilage», positive Ergebnisse.
Azelluläre Techniken
Zuletzt gibt es auch azelluläre Techniken, die sich durch eine sofortige «Off the shelf»-Verfügbarkeit auszeichnen, d.h. Bedarfserfüllung durch Lagerhaltung. In der eigenen Praxis benutzen wir eine bioabsorbierbare Trägermatrix, um Knorpeldefekte in der Schulter zu füllen, entsprechend einer autologen Matrix-induzierten Chondrogenese (AMIC). In unserer Serie wurden 12 Patienten über 1 Jahr nachuntersucht. Indikationen waren dabei sowohl humerale (Abb. 4) als auch glenoidale (Abb. 5) Defekte, letztere auch als iatrogene Schäden nach Ankerplatzierung (Abb. 6). Wir fanden dabei statistisch signifikante Verbesserungen in der klinischen Untersuchung (VAS, SSV, Rowe, qDASH) und der MR-Kontrolle. Letztere zeigte eine verlässliche Defektfüllung nach 12 Monaten sowohl für den Humerus (Abb. 7) als auch das Glenoid (Abb. 8). Cuellar et al. publizierten eine Beschreibung ihrer eigenen Technik 2016. Bemerkenswert ist die Nutzung eines Urinkatheters, um die Matrix im Gelenk anzupressen. Während es für AMIC-Verfahren an der Schulter noch nicht viel Evidenz gibt, ist die Technik für andere Gelenke gut untersucht und durch die Datenlage gut untermauert.
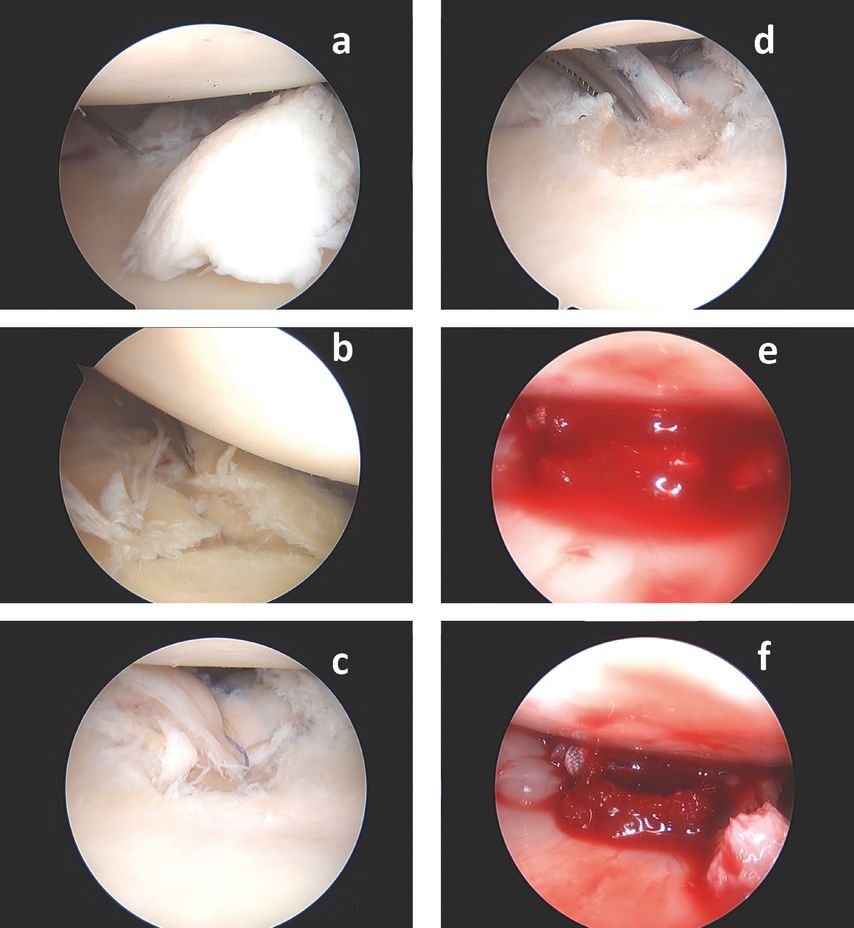
Abb. 3: Die Mikrofrakturierung kommt auch in der Schulter zum Einsatz. In diesem Fall war ein grosser Knorpellappen am Humerus (a) präsent. (b) Die losen Teile werden entfernt. (c) Der Defekt wird bis zu einer stabilen Schulter debridiert. (d) Die Mikrofrakturierung kann mit kommerziellen Instrumenten durchgeführt werden oder auch durch die Bohrahlen aus dem Ankersetzinstrument.
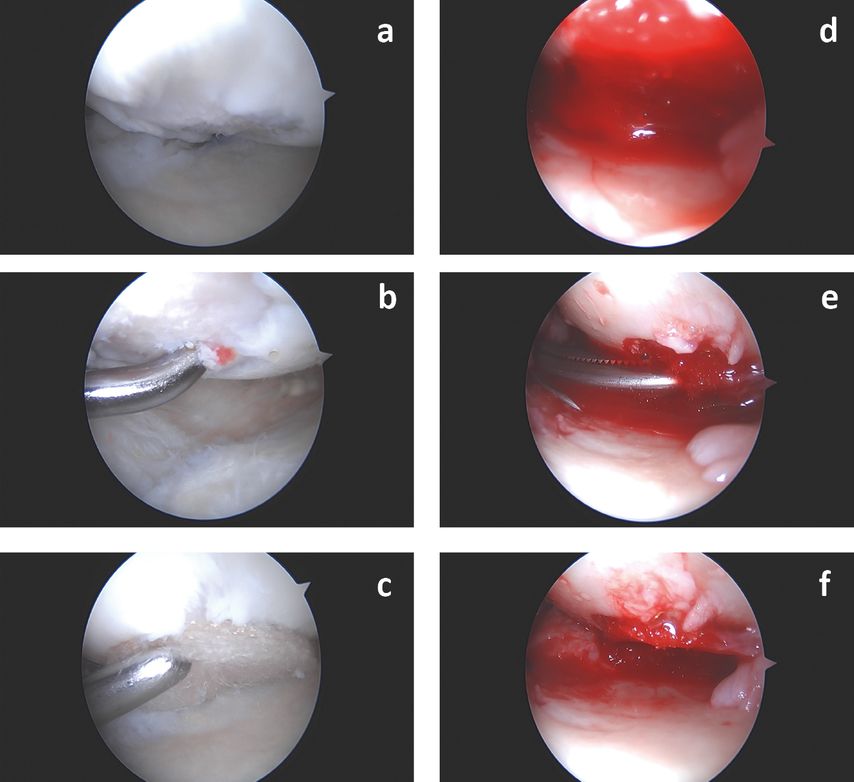
Abb. 4: Revision einer Patientin mit einem fokalen humeralen Knorpeldefekt (a) und Rotatorenmanschettenreruptur nach Erstoperation vor 12 Jahren. Die Sehnennaht erfolgt in normaler Technik (nicht dargestellt). Unter nun stabilen Verhältnissen wird der Defekt angefrischt (b) und ein Biomaterial passender Grösse eingebracht (c). Die Spülflüssigkeit wird abgesaugt und das Biomaterial mit autologem Blut gefüllt (d). Einpressen des Materials mit einer Klemme (e) oder alternativ mit dem Ballon eines Blasenkatheters. Das Biomaterial wird durch das koagulierte Blut im Defekt fixiert (f)
Abb. 5: Ein Patient mit einem fokalen Knorpeldefekt und eingeschlagener Labrumläsion (a). Der Defekt wird arthroskopisch vorbereitet (b) und es erfolgt eine Labrumnaht mit Anker (c). Grössere Defekte können noch angebohrt werden, aber oft ist der Blutaustritt aus dem Ankerkanal ausreichend. Einbringen des Biomaterials (d). Absaugen der Spülflüssigkeit und Verkleben des Biomaterials mit autologem Blut (e). Das Biomaterial wird durch das koagulierte Blut im Defekt fixiert (f)
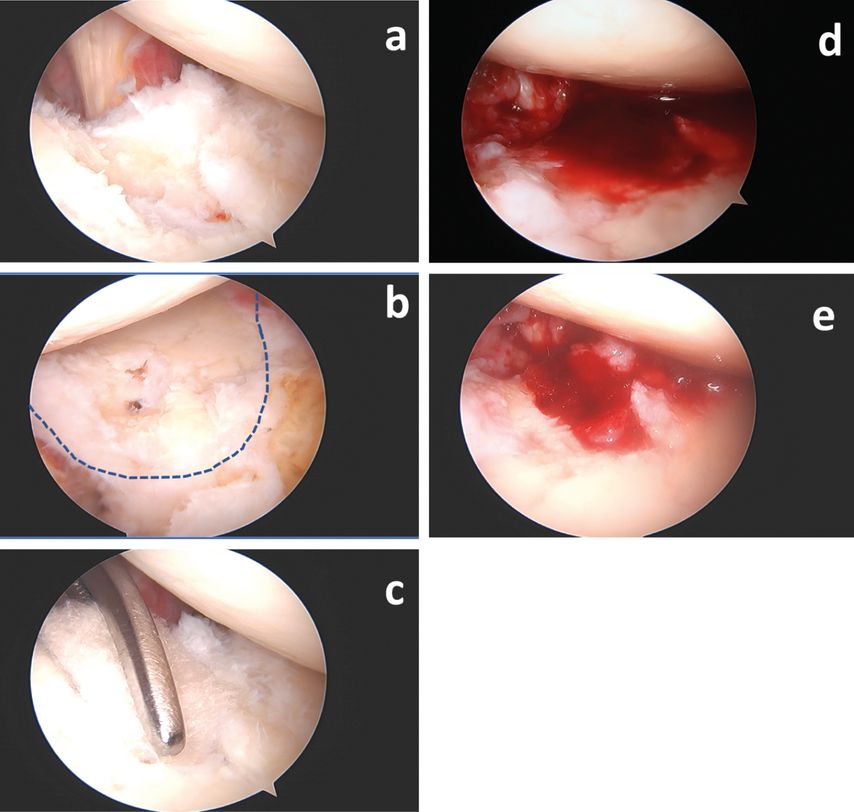
Abb. 6: Iatrogener Knorpeldefekt durch Ankersetzen bei einem SLAP-Repair. Der Anker wurde entfernt und der Defekt debridiert und angebohrt (a und b). Die blaue Linie visualisiert den Rand des Glenoids (b). Das formgerechte Biomaterial wird eingesetzt (c). Durch Absaugen der Spülflüssigkeit wird das Material mit Blut getränkt (d) und so im Defekt fixiert (e)
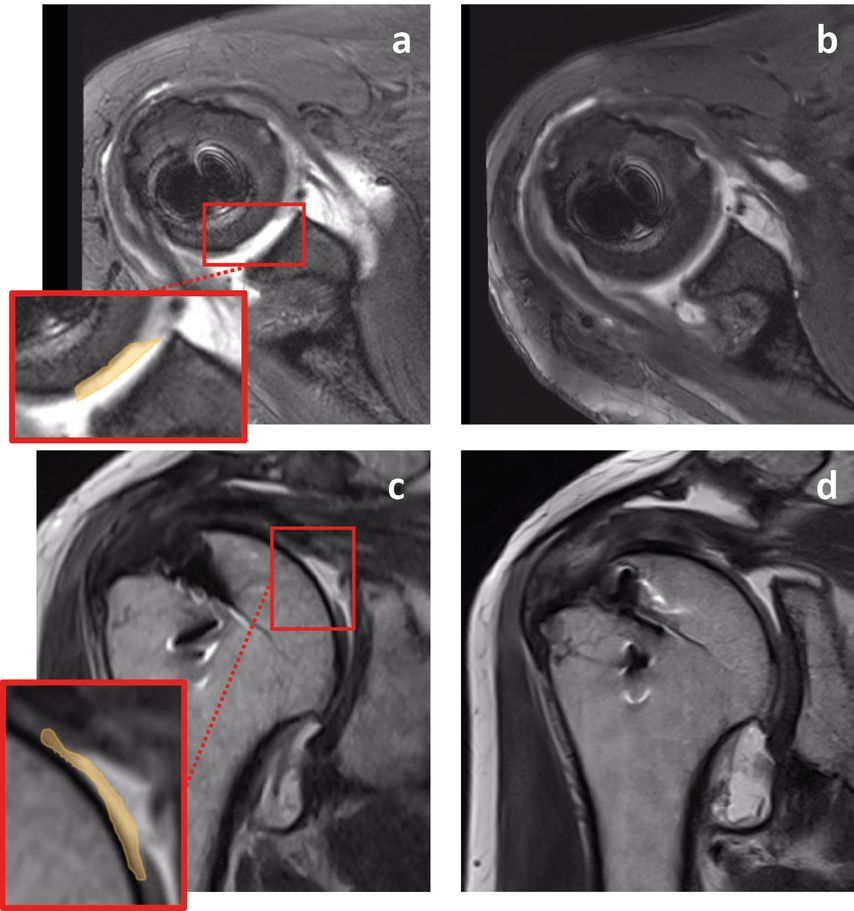
Abb. 7: MRT-Kontrolle der Patientin aus Abb. 4, 12 Monate nach der Operation. Der Knorpeldefekt ist präoperativ (a und c) gut sichtbar, ebenso altes Implantatmaterial aus der ersten Operation. Nach 12 Monaten (b und d) hat das Biomaterial den Defekt komplett gefüllt. Das Signal ist homogen mit dem Signal des nativen Knorpelgewebes (vgl. Abb. 8). Die Oberfläche ist leicht unregelmässig.
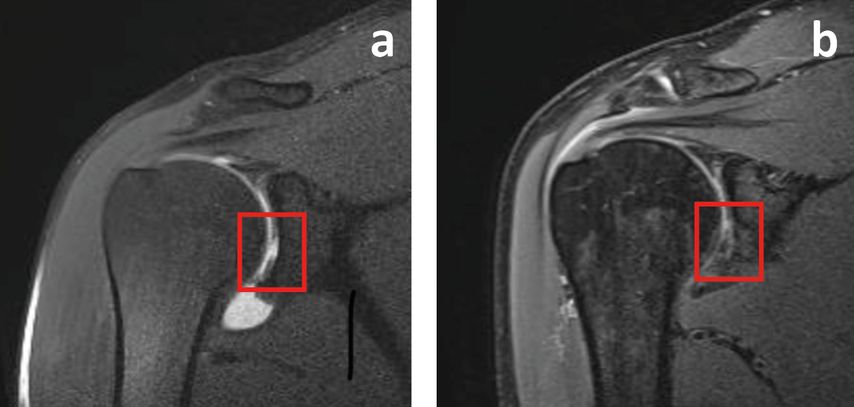
Abb. 8: MRT-Kontrolle eines Patienten mit Knorpelbehandlung am Glenoid. Ebenso wie in Abb. 7 zeigt sich hier eine komplette Defektfüllung, aber mit einem inhomogenen Signal.
Im Sinne der Vollständigkeit sollen auch noch weitere Biomaterialien erwähnt werden, die prinzipiell in der Knorpelbehandlung zur Anwendung kommen. So gibt es kommerzielle Produkte aus Kohlenstoff, «carbon fibre pins», die als Biomaterial die fibrokartilaginäre Heilung stimulieren. Obwohl es für die Anwendung in der Schulter keine Daten gibt, ist Evidenz aus der Vergleichsstudie (Pins gegen Mikrofrakturierung) von Dasar et al. verfügbar. Hier zeigte die Mikrofrakturierung deutlich bessere Ergebnisse im Tegner-Lysholm-Score und in der MRT-Nachuntersuchung. Ebenso ist auch der partielle Oberflächenersatz für die Schulter verfügbar und zeigte in klinischen Studien gute Ergebnisse.
Komplikationen
Komplikationen der chirurgischen Knorpeltherapie der Schulter sind in der Literatur sehr heterogen untersucht. Eine aktuelle Metaanalyse von Fiegen et al. zu dieser Fragestellung zeigte aber, dass die durchschnittliche Versagensrate in 14 Studien mit in Summe 100 Schultern und 98 Patienten (62 Mikrofrakturierungen, 5 Mikrofrakturierungen mit Periostlappen, 23 Allografts, 5 autologe Knorpel-Knochen-Transfers, 4 ACT und 1 Fixation mit Pins) bis zu 35% betrug. 30% wurden reoperiert, am häufigsten im Sinne einer Konversion zu einer Totalprothese. Hier stellt sich einmal mehr eine philosophische Grundsatzfrage der Knorpeltherapie: Ist das effektive Ziel eine komplette Heilung oder das Verzögern einer Prothese? Falls Letzteres der Fall ist, so muss die Begriffsdefinition von «Therapieversagen» angepasst benutzt werden.
Der schmerzlose/symptomarme Knorpeldefekt in der Schulter
Eine wichtige, aber in der Literatur nicht geklärte Frage betrifft den Umgang mit asymptomatischen Knorpelläsionen, wie sie oft als Zufallsbefund auftreten. Per se gilt hier natürlich die oberste Maxime des Patientenwohls und der ausgewogenen Risiko-Nutzen-Analyse und daraus resultierend die Empfehlung einer abwartenden Haltung. Allerdings verdient die Problematik genauere Untersuchungen.
Zuerst stellt sich die Frage, ob es in der Tat eine asymptomatische Läsion ist. Zuallererst muss hier die Symptomatik des Patienten bedacht werden. Gibt es Symptome, die sich nicht durch die Primärpathologie erklären lassen? Gibt es Symptome, die sich durch die Primärpathologie erklären lassen, aber nicht im Ausmass wie festgestellt? Weiter stellt sich die Frage, ob der Knorpeldefekt Teil der Pathomechanik ist? So kann ein randständiger Knorpeldefekt am Glenoid eine chondrolabrale Versionsänderung bedeuten, die wiederum eine Instabilität verschlechtern kann. Wird das Ergebnis des Primäreingriffs durch Belassen des Knorpeldefekts nicht verschlechtert bzw. durch Beheben nicht verbessert? Hintere Instabilitäten mit Knorpeldefekt am Glenoid zeigen in Studien bessere postoperative Resultate, wenn die Stabilisierung durch eine Knorpelbehandlung ergänzt wird. Für Defekte der Rotatorenmanschette konnte das nicht bestätigt werden.
Zuletzt stellt sich die Frage der möglichen Progression. Per se ist die Verschlechterung von glenohumeralen Knorpelschäden im Allgemeinen eher langsam und zumeist sind auch höhergradige Defekte oft wenig symptomatisch, wenn nicht gar asymptomatisch. Dies ist aber natürlich durch weitere Faktoren wie Leistungsanspruch, Alter etc. oft perspektivisch veränderlich und muss fallbezogen bedacht werden.
Fazit
In Summe sind Knorpeldefekte am Schultergelenk selten. Das heisst aber nicht, dass sie keine klinische Bedeutung haben. Man kann davon ausgehen, dass sie bei einem Viertel bis zu einem Drittel aller Patienten, oftmals als Zufallsbefund, auftreten. Obwohl die aktuelle Literatur eher spärlich ist, gibt es gute Evidenz, dass Knorpeldefekte in der Entscheidungsplanung berücksichtigt werden sollten. Speziell für Patienten mit Instabilität zeigen aktuelle Studien deutlich bessere klinische Ergebnisse bei gleichzeitiger Behandlung. Bei Patienten mit Rotatorenmanschettenläsionen spielen Knorpeldefekte eine untergeordnete Rolle. Was die Auswahl an therapeutischen Optionen betrifft, so gibt es eine Reihe von regenerativen und nichtregenerativen Operationstechniken. Es hat sich hier noch kein klarer Favorit herausgearbeitet, dementsprechend macht es im klinischen Alltag Sinn, die Verfahren anzuwenden, für die die meiste Erfahrung und der beste Zugang bestehen. Komplikationen, vor allem im Sinne von Reoperationen, sind nicht selten (ein Drittel aller Patienten) und eine entsprechende Aufklärung ist gerechtfertigt.
Literatur:
bei den Verfassern
Das könnte Sie auch interessieren:
Frühe Unterwassertherapie nach totaler Hüft- und Knieendoprothese
Eine frühzeitige Durchführung der Unterwassertherapie mit wasserdichtem Folienverband ab dem vierten postoperativen Tag ist im Allgemeinen sicher, wirksam und ohne Nebenwirkungen.
Aktuelles zur anteromedialen Knieinstabilität
Kombinierte Verletzungen des medialen Kollateral- (MCL) und des vorderen Kreuzbandes (VKB) zählen zu den häufigsten multiligamentären Knieverletzungen. Bei vermeintlich isolierten VKB- ...
Arthroskopische Behandlung von Glenoidrandfrakturen
In der Literatur werden die Begriffe knöcherne Bankart-Läsion und Glenoidrandfraktur häufig synonym verwendet, obwohl sie sich hinsichtlich Pathomechanismus und Therapie deutlich ...