Wie wird sich das Management des Nierenzellkarzinoms verändern?
Autorin:
Prof. Dr. med. Manuela Schmidinger
Universitätsklinik für Urologie
Medizinische Universität Wien
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Immuntherapiekombinationen haben die Prognose des metastasierten Nierenzellkarzinoms (RCC) in den letzten Jahren dramatisch verbessert: Nun ist auch die adjuvante Therapie im Management fest verankert. Sowohl im frühen als auch im späteren Krankheitsstadium des RCC verbleiben jedoch viele offene Fragen. Diese umfassen die Selektion von Patienten für eine adjuvante Therapie, den Stellenwert der zytoreduktiven Nephrektomie, die Auswahl der Erst- und Spätlinientherapien sowie die Therapie des nicht klarzelligen RCC.
Keypoints
-
Der Benefit der adjuvanten Therapie mit Pembrolizumab bestätigt sich auch nach einem längeren Beobachtungszeitraum.
-
Zytoreduktive Nephrektomie scheint in der ICI-Ära mit einem besseren Outcome assoziiert zu sein.
-
Aktive Überwachung bleibt bei ausgewählten Patienten eine Strategie im Metastasenstadium.
-
Erstlinienkombinationen sind auch nach längerem Follow-up wirksam und mit einer anhaltenden Verbesserung der Lebensqualität assoziiert.
-
Lenvatinib plus Everolimus und Cabozantinib sind in späteren Therapielinien besonders wirksam.
-
Immuntherapie ist auch beim nicht klarzelligen RCC eine gute Wahl.
-
Neue therapeutische Ansätze erscheinen nach frühen Ergebnissen interessant.
Adjuvante Therapie
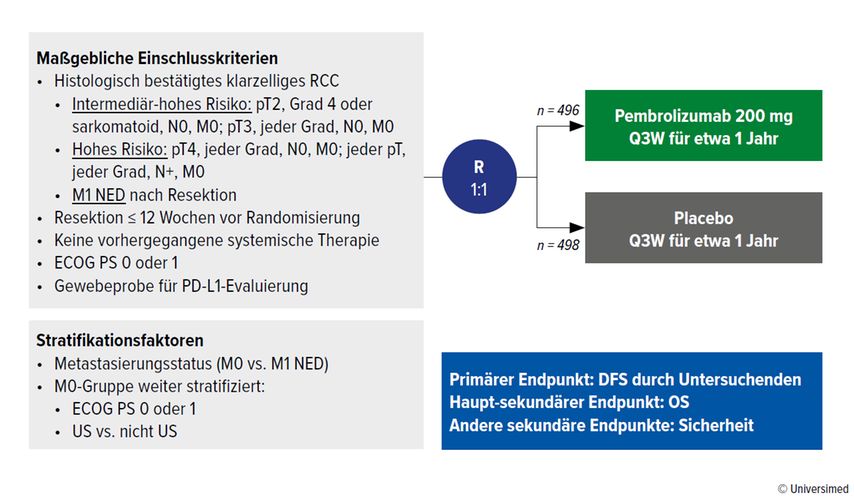
2021 wurde erstmals die Empfehlung für eine adjuvante Therapie beim Nierenzellkarzinom (RCC) in den Therapierichtlinien verankert. Dies geht auf die KEYNOTE-564-Studie zurück, deren Ergebnisse am ASCO Meeting 2021 präsentiert wurden. In dieser Studie konnte gezeigt werden, dass der Immuncheckpoint-Inhibitor (ICI) Pembrolizumab im Vergleich zu Placebo das krankheitsfreie Überleben («disease-free survival», DFS) signifikant verlängert.1 Die Population bestand aus Patienten mit 1)intermediär-hohem Rückfallsrisiko, 2) hohem Rückfallsrisiko und 3) St.n. Resektion von Metastasen (M1-Resektion, «no evidence of disease», NED) (Abb. 1).
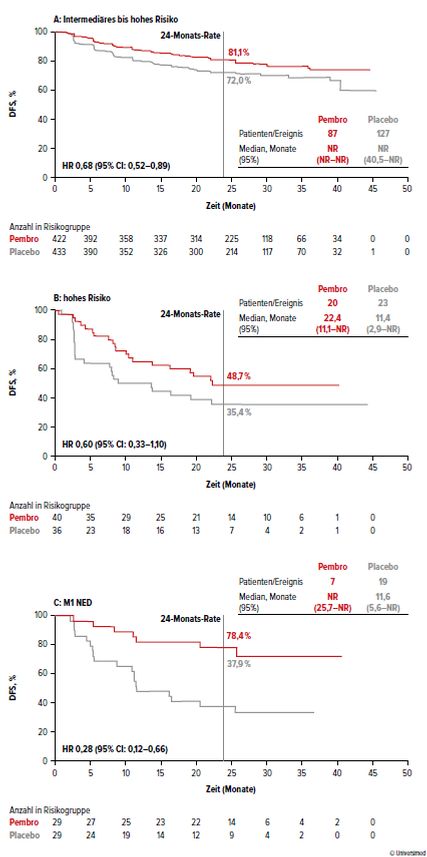
Am ASCO GU Meeting 2022 wurde nun das 30-Monate-Follow-up dieser Studie präsentiert, das die Ergebnisse der Erstbeobachtung bestätigt.2 Nach 30,1 Monaten Follow-up blieb die Rate an Patienten, die krankheitsfrei sind, im Pembrolizumab-Arm signifikant höher als im Placebo-Arm (78,3% vs. 67,3%; Hazard-Ratio [HR] 0,63; 95% CI: 0,50–0,80). Die Risikoreduktion war in allen Subgruppen gegeben, unterschied sich aber in Bezug auf das Ausmass der Risikoreduktion (Abb. 2). Den grössten Benefit hatten Patienten der M1-NED-Gruppe, in der die DFS-Rate bei 78,4% vs. 37,9% lag (HR: 0,28; 95% CI: 0,12–0,66); auch Patienten mit sarkomatoiden Tumoren profitierten besonders (DFS-Rate 71,8% vs. 52%; HR: 0,54; 95% CI: 0,29–1,0). In der Population der Patienten mit hohem Risiko lag die DFS-Rate mit und ohne Pembrolizumab bei 48,7% vs. 35,4% (HR: 0,60; 95% CI: 0,33–1,10); am geringsten war der Benefit bei Patienten mit intermediär-hohem Risiko (DFS-Rate 81,1% vs. 72%; HR: 0,68; 95% CI: 0,52–0,89). Das Gesamtüberleben (OS) ist aufgrund der geringen Zahl an Ereignissen noch nicht signifikant, der initial berichtete Trend einer Verlängerung des Überlebens hält jedoch weiterhin an (HR: 0,52; 95% CI: 0,31–0,86). Es wurden keine neuen Toxizitäten und keine erhöhte Inzidenz bekannter Toxizitäten beobachtet.
TKI + Pembrolizumab
Qurat Ul Ain und Kollegen präsentierten die Ergebnisse einer Metaanalyse, welche adjuvante Studien mit Tyrosinkinase-Inhibitoren (TKI) und Pembrolizumab einschloss. TKI werden seitens der europäischen Guidelines nicht im adjuvanten Setting empfohlen.3 Die Ergebnisse dieser Analyse bestätigten, dass der risikostratifizierte absolute Benefit einer adjuvanten Therapie mit TKI gering ist (selbst für Hochrisikopatienten). Im Gegensatz dazu war der absolute Benefit von Pembrolizumab umso höher, je höher der Leibovich-Score war.
Molekulare Charakterisierung
Der Leibovich-Score kann dennoch für die Selektion von Patienten für eine adjuvante Therapie unzureichend sein, vor allem bei Patienten mit intermediär-hohem Risiko. Cotta und Kollegen haben daher den Benefit einer molekularen Charakterisierung zur Optimierung der Risikostratifizierung bei lokalisierter Erkrankung untersucht.4 In einer Multivariatanalyse und unter Korrektur für klinisch-pathologische Eigenschaften erzielten Patienten mit einem hohen 22-Gen-«epithelial to mesenchymal transition»(EMT)-Score eine signifikante Verlängerung des DFS (HR: 7,2; 95% CI: 1,15–44,8; p=0,035). Ein weiterer Score, der in Bezug auf Risikostratifizierung geeignet scheint, insbesondere bei Patienten mit intermediär-hohem Risiko, ist der 16-Gen-«Transcriptom-Recurrence Score».5
Aktive Überwachung im Stadium der Metastasierung
Durch die Einführung von Immuntherapiekombinationen ist es zu einer dramatischen Verlängerung des Überlebens im Stadium der Metastasierung gekommen. Dennoch stellt sich die Frage, ob wirklich alle Patienten zeitnahe, also zum Zeitpunkt der Diagnose der Metastasierung, sofort mit einer Therapie beginnen müssen. Bereits in der Vergangenheit konnte gezeigt werden, dass ein späterer Therapiebeginn mit einem TKI nicht notwendigerweise mit einer Verkürzung des Überlebens assoziiert ist.6
Schwartzman und Kollegen haben in einer am ASCO GU Meeting präsentierten Analyse versucht, das Profil eines Patienten, der für die aktive Überwachung infrage kommt, besser zu charakterisieren.7 Aus einer elektronischen Datenbank wurden 37 Patienten identifiziert, die trotz Metastasierung keine Therapie (bei gleichzeitig gegebener Therapiefähigkeit) erhalten hatten. Die mediane Zeit bis zum Bedarf einer systemischen Therapie lag bei 37 Monaten (95% CI: 24,3–94,9) und das Überleben ab Initiierung einer systemischen Therapie bei 132,5 Monaten (95% CI: 97,3 bis nicht erreicht). Die Zahl an Metastasen war erwartungsgemäss signifikant mit der Zeit bis zum Therapiebeginn assoziiert. Nach einem medianen Follow-up von 62,5 Monaten hatten immerhin 29% der Patienten noch nicht mit einer systemischen Therapie begonnen.
Die Autoren bestätigen damit frühere Beobachtungen, dass es eine Subgruppe von Patienten gibt, die keine sofortige Therapieeinleitung benötigen.
Zytoreduktive Nephrektomie (CN) in der Ära der Immuncheckpoint-Inhibitoren
Da die Ergebnisse der CARMENA-Studie die Rolle der zytoreduktiven Nephrektomie (CN) in der Ära der TKI infrage gestellt haben, werden Patienten mit intermediärem oder ungünstigem Risiko seltener als früher einer CN zugeführt. Ob die Nichtunterlegenheit einer alleinigen systemischen Therapie vs. CN gefolgt von systemischer Therapie aber auch in der Ära der Immuncheckpoint-Inhibitoren (ICI) zutrifft, ist unklar.
Perimbeti und Kollegen gingen dieser Frage in einer retrospektiven Analyse von Patienten aus einer nationalen Krebsdatenbank, die zwischen 2015 und 2018 eine ICI-Therapie erhalten hatten, nach.8 4369 Patienten wurden identifiziert, davon hatten 36,4% eine CN erhalten (85,3% vor systemischer Therapie, 13,8% danach). Patienten mit grossen Nierentumoren und jene ohne klinischen Verdacht auf Lymphknotenbeteiligung waren häufiger operiert worden. Nach einem Jahr war die Überlebensrate von Patienten mit CN signifikant höher als jene der Patienten ohne CN. In der Multivariatanalyse war die CN ein unabhängiger Risikofaktor für das Überleben (HR: 0,53; 95% CI: 0,41–0,68). Die Autoren schlussfolgerten, dass die CN in der Ära der ICI weiterhin eine wichtige Rolle spielt.
Interessant ist in diesem Zusammenhang auch eine Analyse von Mittal und Kollegen bei 226 Patienten.9 Die Autoren haben die Rolle der CN und der systemischen Therapie (TKI-Therapie) bei Patienten mit oder ohne Tumorthrombus untersucht. Bei jenen, die nur eine systemische Therapie erhielten, waren das mediane progressionsfreie Überleben (PFS) und das OS in Bezug auf Vorhandensein oder Fehlen eines Tumorthrombus nicht signifikant unterschiedlich. Bei Patienten mit Thrombus gab es keinen Unterschied im PFS in Bezug auf CN plus systemische Therapie oder systemische Therapie allein. Jedoch war das OS in der Thrombuspopulation signifikant länger bei jenen, die einer CN zugeführt wurden (29,4 vs. 12,1 Monate, p=0,01). Auch hier schlussfolgerten die Autoren, dass die CN ein wichtiger Pfeiler bleibt, wenngleich dies in der Ära der ICI noch nicht prospektiv untersucht wurde.
Erstlinientherapie beim klarzelligen Nierenzellkarzinom
Das ASCO GU Meeting 2022 hat zu keinen Veränderungen der aktuellen Therapieempfehlungen in der Erstlinie geführt (Abb.3). Es ist weiterhin so wie im Therapiealgorithmus dargestellt: 4 verschiedene Erstlinientherapien stehen für Patienten mit intermediärem oder ungünstigem Risiko zur Verfügung und 3 Strategien für Patienten aller Risikogruppen. Am ASCO GU Meeting wurden die existierenden Daten um einige neue Informationen erweitert. Dies betrifft Aspekte wie Lebensqualität und Effektivität nach längerer Beobachtungszeit.
CheckMate 9ER
Eine finale OS-Analyse der Studie CheckMate 9ER (NC: Nivolumab + Cabozantinib vs. Sunitinib) wurde präsentiert.10 Nach einem medianen Follow-up von 32,9 Monaten zeigte sich anhaltend eine statistisch signifikante Verlängerung des OS für Patienten im NC-Arm (median 37,7 vs. 34,3 Monate; HR: 0,70; 95% CI: 0,55–0,90); das Gleiche galt auch für das PFS (median 16,6 vs. 8,3 Monate; 95% CI: 0,46–0,68) und die Ansprechraten (55,7% vs. 28,4%, Komplettremissionsrate 12,4% vs. 5,2%). Auch in Bezug auf die Lebensqualität zeigte sich weiterhin eine Verbesserung durch Nivolumab plus Cabozantinib vs. Sunitinib: Die Behandlung mit Nivolumab plus Cabozantinib reduzierte das Risiko für eine Verschlechterung der Lebensqualität und das Risiko, dass Patienten mit Nebenwirkungen zu kämpfen hatten.11
CheckMate 214
Ein 5-Jahres-Update der CheckMate-214-Studie (Nivolumab plus Ipilimumab vs. Sunitinib) kam betreffend die Lebensqualität zu den gleichen Erkenntnissen wie zuvor für CheckMate 9ER beschrieben, mit einem klaren Vorteil für Patienten im Nivolumab+Ipilimumab-Arm.12
Ein weiteres Update dieser Studie betraf die Subgruppe der Patienten mit sarkomatoid entdifferenzierten Tumoren.13 139 der 1096 Patienten in der CheckMate-214-Studie hatten sarkomatoide Nierenzellkarzinome. Das 5-Jahres-Follow-up ergab eine beeindruckende Wirkung von Nivolumab plus Ipilimumab in dieser Population: Die Ansprechrate betrug 61% (vs. 23%), das mediane PFS 26 Monate (vs. 5 Monate) und das Gesamtüberleben 49 Monate (vs. 14 Monate; HR: 0,46). Noch bessere Ergebnisse erzielten jene Patienten, die neben der sarkomatoiden Komponente auch zusätzliche PD-L1(«Programmed-death ligand 1»)-positive Tumoren hatten: Hier lag die Ansprechrate bei 69% und das mediane PFS und OS waren noch nicht erreicht.
HCRN GU16-260
In Bezug auf die Kombination Nivolumab plus Ipilimumab wurden auch die finalen Daten der HCRN-GU16-260-Studie präsentiert, die sich damit befasst hatte, dass Patienten mit einer Nivolumab-Monotherapie beginnen (Teil A) und nur jene mit Progression oder Stabilisierung als bestes Ergebnis 4-mal eine Kombination mit Ipilimumab erhalten sollen (Teil B). 123 Patienten wurden eingeschlossen, das mediane Follow-up war 26,9 Monate. Die Ansprechraten lagen bei 34,1%, mit einer Komplettremissionsrate von 6,5%. Die mediane Remissionsdauer betrug 27,6 Monate und das mediane PFS 8,2 Monate. 78% der Patienten waren nach 24 Monaten noch am Leben. Von den 65 Patienten, die durch Nivolumab-Monotherapie keine objektive Remission erreicht hatten («stable disease» oder «progressive disease») und sich somit für die Kombinationsgabe qualifiziert hätten, konnten 25 nicht in diesen Abschnitt der Studie eintreten, vorwiegend wegen symptomatischer Progression. Insgesamt besteht die Empfehlung, die Kombination zu Beginn der Therapie einzusetzen.
KEYNOTE-426
Updates aus der KEYNOTE-426-Studie (Pembrolizumab plus Axitinib vs. Sunitinib) betrafen die Möglichkeit der 6- statt 3-wöchentlichen Gabe von Pembrolizumab (in doppelter Dosierung).14 In einer schottischen Studie wurde aufgrund der Covid-19-Pandemie Pembrolizumab in einer Dosierung von 400mg alle 6 Wochen gegeben. Die Autoren berichteten, dass es in Bezug auf die Wirkung keinen Unterschied zu den Ergebnissen der KEYNOTE-426-Studie gab, mit dem Vorteil, dass die Patienten nicht so oft ins Krankenhaus kommen mussten.
Biomarker und Prädiktion
Alle Erstlinientherapien beim mRCC sind ICI-Kombinationen, es gibt bislang keine Vergleiche untereinander, da alle mit dem TKI Sunitinib verglichen wurden. Biomarker zur besseren Auswahl haben sich bislang noch nicht im klinischen Alltag etabliert. Viele retrospektive Analysen mit «Cross-Trial»-Vergleichen wurden publiziert, jedoch eignen sich diese nicht, um daraus die beste Therapie für den Patienten abzulesen. Auch befassen sich die meisten Analysen mit der Frage, ob ein bestimmtes Biomarkerprofil das Ansprechen auf Immuntherapie vorhersagen kann, nicht aber damit, welche Therapie die bessere für den individuellen Patienten wäre. Dennoch sind die Daten interessant und tragen generell zu einem enormen Wissenszuwachs auf dem Gebiet der Immuntherapie bei.
Nephrektomie, Lungenmetastasen und günstiges IMDC-Profil
Eine der grössten Populationen (n=1084), die in dieser Weise untersucht wurden, sind Patienten aus dem International Metastatic Renal Cell Database Consortium (IMDC). Mit einem besseren Ansprechen auf eine ICI-basierte Therapie waren in der Multivariatanalyse die Nephrektomie (Odds-Ratio: [OR] 1,57; 1,13–2,19; p=0,007), das Vorhandensein von Lungenmetastasen (OR: 1,71; 1,26–2,31; p<0,001) und eine günstige IMDC-Risikogruppe (OR für ungünstig vs. günstig: 0,45; p<0,001; OR für ungünstig vs. intermediär: 0,65; p=0,006) assoziiert.15
Intratumorales Mikrobiom
Ein neuartiges Konzept in Bezug auf die Prädiktion des Ansprechens auf die Immuntherapie (wenngleich nicht auf die Auswahl einer bestimmten Immuntherapiekombination) ist die Analyse der Assoziation des intratumoralen Mikrobioms mit dem Ansprechen. In einer kleinen Studie mit vorerst nur 28 Patienten zeigten Responder auf Immuntherapie einen höheren relativen Reichtum an Stenotrophomonas maltophilia und Corynebacterium sp.zg-917. In diesem Zusammenhang ist darauf hinzuweisen, dass das Corynebacterium spp. seit Dekaden als eine eventuelle Ergänzung zu Immuntherapien wie mit Bacillus Calmette-Guérin (BCG) studiert wird.
Eosinophile und Ratio Neutrophile/Eosinophile
Ein hoher absoluter Eosinophilenwert und eine niedrige Neutrophile-zu-Eosinophile-Ratio unter laufender Therapie wurden als Prädiktoren für ein gutes Ansprechen auf Nivolumab plus Ipilimumab identifiziert.16
Metastasenlokalisation
Auch die Metastasenlokalisation bleibt als Driver für Therapieentscheidungen interessant: Demnach sind zum Beispiel adrenale Metastasen mit einem deutlich schlechteren Ansprechen auf Nivolumab assoziiert (HR ja vs. nein: 1,65; CI: 1,29–2,10; p<0,0001).17
Periphere Zytokine und Outcome von Nivolumab
In einer translationalen Studie bei Patienten aus der Studie NIVOREN GETUG-AFU 26 wurden 80 Patienten (40 Responder und 40 Nicht-Responder) in Bezug auf den prädiktiven und/oder prognostischen Wert bestimmter Plasmazytokine untersucht.18 Hohe Baseline-Plasma-Spiegel an Interleukin-6 (IL-6), IL-7, IL-8 und «vascular endothelial growth factor» (VEGF) waren mit einem signifikant kürzeren Überleben assoziiert.
Im Gegensatz dazu war der Marker 4-1BB mit einem signifikant längeren Überleben assoziiert. 4-1BB (oder CD137) ist ein Aktivierungs-induzierendes kostimulatorisches Molekül und ein wichtiger Regulator der Immunantwort. 4-1BB-mediierte antitumoröse Effekte basieren auf dessen Fähigkeit, zytotoxische T-Zellen zu aktivieren und für einen hohen IFN(Interferon)-γ-Spiegel zu sorgen.
Zweitlinie und spätere Linien
Es gibt bislang keine randomisierte Phase-III-Studie, die einen Standard nach Versagen von ICI-Kombinationen etabliert hätte; die Empfehlungen der Guidelines beschränken sich auf die Aussage, einen TKI zu verwenden, der nicht in der Erstlinie verwendet wurde. Die Empfehlungen sind allesamt IIIB-Empfehlungen.
CABOSEQ
In einer retrospektiven Analyse von Patienten der IMDC-Datenbank wurde die Wirksamkeit von Cabozantinib nach Versagen einer dualen ICI- (Nivolumab plus Ipilimumab) oder ICI-plus-TKI-Therapie untersucht.19 346 Patienten wurden analysiert, wovon 78 eine duale ICI-Therapie und 46 eine ICI+TKI-Kombination erhalten hatten, weitere 222 Patienten hatten andere Vortherapien. Die Ansprechraten mit Cabozantinib lagen für die Gesamtpopulation, unabhängig von der Art der Vortherapie, bei 26,2%. Die mediane Zeit bis zum Therapieversagen lag bei 7,59 Monaten und das Gesamtüberleben bei median 18,12 Monaten. Die Autoren schlussfolgerten, dass Cabozantinib in der Zweitlinie aktiv ist, unabhängig von der Vortherapie.
CaboCHECK
Diese Studie von Grünwald und Kollegen kam zu vergleichbaren Ergebnissen wie CABOSEQ, nur in einer kleineren Population (n=56);20 zudem konnten die Autoren keinen Unterschied im Outcome in Abhängigkeit von der Cabozantinib-Dosis (40mg oder 60mg) beobachten.
Metaanalyse zu Zweitlinientherapien
In einer Metaanalyse verglichen Recio-Boiles und Kollegen alle Zweitlinientherapien, die in einer randomisierten Studie geprüft worden waren, in Bezug auf ihre Wirksamkeit.21 Alle acht Therapien, die in der Analyse berücksichtigt wurden, zeigten einen Benefit im Vergleich zu Placebo. In Bezug auf Reduktion des Risikos für Tod oder Progression schnitten die Kombination Lenvatinib plus Everolimus (Fibroblastenwachstums-Faktor-Rezeptor[FGFR]-VEGFR-Inhibitor mit mTOR-Inhibitor) sowie eine Therapie mit Cabozantinib am besten ab (HR Lenvatinib + Everolimus im Vergleich zu Placebo: 0,13; 95% CI: 0,07–0,24; HR Cabozantinib: 0,17; 95% CI: 0,12–0,24). Am wenigsten wirksam war der TKI Pazopanib (HR: 0,54; 95% CI: 0,35–0,84).
Nicht klarzelliges RCC
In einer kanadischen Studie analysierten Laramee und Kollegen die Effektivität unterschiedlicher Erstlinientherapien (VEGFR-TKI, mTOR-Inhibitoren, ICI-basierte Therapie) bei Patienten mit nicht klarzelligem RCC (non-cc-RCC).22 Erwähnenswert ist hierbei der Umstand, dass die Therapie der analysierten Patienten in einen Behandlungszeitraum fiel, zu dem Cabozantinib noch nicht zur Verfügung stand. 265 Patienten wurden in Bezug auf ihr Outcome mit den erwähnten Therapien untersucht. Die Remissionsraten waren für TKI 17%, für mTOR-Inhibitoren 5% und für die ICI-basierte Therapie 37%. Das 1-Jahres-Überleben lag bei 65,2%, 57,9% und 69%, je nach Behandlungsgruppe. Die Autoren schlussfolgerten, dass eine ICI-Therapie bei Patienten mit non-cc-RCC mit einem verbesserten Outcome assoziiert ist.
Auch eine portugiesische Forschergruppe befasste sich mit der Thematik der ICI-Therapie beim non-cc-RCC.23 Die Autoren analysierten dazu Daten aus 14 Publikationen und berichteten a) über eine vergleichbare Aktivität innerhalb der einzelnen histologischen Subtypen und b) über eine höhere Aktivität unter Kombinationstherapien, vor allem im Bereich der papillären und sarkomatoiden/rhabdoiden Differenzierungen. Nach einer Analyse von Alhalabi ist auch eine duale ICI-Therapie mit Nivolumab plus Ipilimumab beim non-cc-RCC aktiv;24 bei insgesamt 27 Patienten betrug die Ansprechrate 30%. Den grössten Benefit erzielten Patienten mit papillären Karzinomen, während jene mit chromophobem und unklassifiziertem RCC am schlechtesten abschnitten.
In einer internationalen, retrospektiven Multicenter-Studie wurden 29 Patienten mit familiärem Translokationskarzinom mit nachgewiesener TFE3- oder TFEB-Translokation im Tumor identifiziert.25 Die Patienten wurden entweder mit einer dualen ICI-Kombination oder mit ICI+TKI behandelt. Die Ansprechraten und das PFS betrugen 5,5% und 2,8 Monate in der dualen ICI-Therapie-Gruppe und 36% bzw. 5,4 Monate in der ICI-TKI-Gruppe.
Therapieerfolge beim Xp11.2-Translokationskarzinom wurden bei 45 Patienten aus einer Kohorte von 1113 Patienten in China analysiert. In diesem Fall erhielten die Patienten eine reine TKI-Therapie (Sunitinib, Sorafenib, Axitinib und Pazopanib); das numerisch längste PFS wurde bei Axitinib-behandelten Patienten berichtet (median 9,4 Monate). Nur 2 Patienten in der Population wurden mit einer ICI-TKI-Kombination behandelt; hier betrug das PFS 16,6 bzw. 25,6 Monate.26
Abb. 3: ESMO-Empfehlungen zur Erstlinientherapie des fortgeschrittenen klarzelligen Nierenzellkarzinoms (nach Powles, Schmidinger et al.)
Neue Therapiestrategien
Nemvaleukin-α: ein Revival von IL-2
Nemvaleukin-α ist ein IL-2, das selektiv den «intermediate affinity receptor» (IL-2R) bindet, wodurch präferenziell CD8+-T-Zellen und natürliche Killerzellen (NK-Zellen) aktiviert werden, aber kaum regulatorische T-Zellen. RCC-Patienten mit Versagen auf vorangehende Therapien wurden in der ARTISTRY-1-Studie zunächst mit Nemvaleukin allein behandelt und konnten im Falle einer Progression oder Stabilisierung als bestes Ansprechen Nemvaleukin in Kombination mit Pembrolizumab erhalten.27 Nemvaleukin induzierte eine robuste Expansion von CD8+- und NK-Zellen mit minimalem Effekt auf regulatorische T-Zellen. Bei 8 von 11 mit ICI vorbehandelten Patienten konnte in der Monotherapie eine partielle Remission oder Stabilisierung erreicht werden.
Axitinib plus Nivolumab bei vorbehandelten Patienten
In einer Phase-I/II-Studie wurde die Kombination aus Axitininib und Nivolumab bei vorbehandelten Patienten geprüft.28 44 Patienten wurden eingeschlossen, die objektive Ansprechrate lag bei 59,5% und die Krankheitskontrollrate (DCR, Ansprechen und Stabilisierung) bei 97,6%. Das mediane PFS betrug 16,4 Monate (95% CI: 10,6–21,9). Ein sehr hoher Anteil der Patienten (41,9%) hatte ein günstiges Risikoprofil nach IMDC. Die Nebenwirkungen waren vergleichbar mit denen bei jeder anderen ICI-TKI-Kombination.
CD70 als vielversprechendes CAR-T-Zell-Target beim RCC
Ye und Kollegen untersuchten die Expression von CD7029, einem Target für eine CAR(«chimeric antigen receptor»)-T-Zell-Therapie, bei Tumoren von Patienten mit fortgeschrittenem RCC. Die Ergebnisse der Analysen zeigten, dass beim cc-RCC sowohl im Primärtumor als auch in korrespondierenden Metastasen eine hohe CD70-Expression zu finden ist. Die Autoren schlussfolgerten, dass eine Anti-CD70-CAR-T-Cell-Therapie bei einem Grossteil der RCC-Patienten sinnvoll sein könnte.
Quelle:
ASCO Genitourinary Cancer Symposium, 17. bis 19. Februar 2022, San Francisco
Literatur:
1 Choueiri TK et al.: N Engl J Med 2021; 384: 829-41 2Choueiri TK et al.: ASCO GU 2022; Abstr. #290 3 Sipra QUAR et al.: ASCO GU 2022; Abstr. #360 4 Cotta B et al.: ASCO GU 2022; Abstr. #377 5 Shuch B et al.: ASCO GU 2022; Abstr. #383 6 Rini BI et al.: Lancet Oncol 2016; 17: 1317-24 7Schwartzman W et al.: ASCO GU 2022; Abstr. #389 8 Perimbeti S et al.: ASCO GU 2022; Abstr. #359 9Mittal A et al.: ASCO GU 2022; Abstr. #345 10 Powles T et al.: ASCO GU 2022; Abstr. #350 11 Cella D et al.: ASCO GU 2022; Abstr. #323 12Cella D et al.: ASCO GU 2022; Abstr. #307 13 Tannir NM et al.: ASCO GU 2022; Abstr. #352 14 Ansel S et al.: ASCO GU 2022; Abstr. #309 15 Navani V et al.: ASCO GU 2022; Abstr. #310 16 Chen MS et al.: ASCO GU 2022; Abstr. #364 17 Billon E et al.: ASCO GU 2022; Abstr. #348 18 Carril L et al.: ASCO GU 2022; Abstr. #379 19 Navani V et al.: ASCO GU 2022; Abstr. #318 20 Grünwald V et al.: ASCO GU 2022; Abstr. #357 21 Recio-Boiles V et al.: ASCO GU 2022; Abstr. #337 22 Laramee S et al.: ASCO GU 2022; Abstr. #304 23 Rreis AF et al.: ASCO GU 2022; Abstr. #353 24 Alhalabi O et al.: ASCO GU 2022; Abstr. #356 25 Alhalabi O et al.: ASCO GU 2022; Abstr. #343 26 Yan X et al.: ASCO GU 2022; Abstr. #341 27 Calvo E et al.: ASCO GU 2022; Abstr. #330 28 Zibelman M et al.: ASCO GU 2022; Abstr. #291 29 Ye H et al.: ASCO GU 2022; Abstr. #384
Das könnte Sie auch interessieren:
Brain Working Recursive Therapy
Die «brain working recursive therapy» ist eine neue psychotherapeutische Methode für effiziente Kurzzeitinterventionen bei Trauma, Angststörungen und Stresserkrankungen.
Arthritiden bei Psoriasispatienten
Circa ein Viertel aller Psoriasispatienten entwickelt im Lauf des Lebens eine Gelenkbeteiligung. Doch es gibt erfolgreiche Strategien, dem entgegenzuwirken oder zumindest die weitere ...
Patientenedukation bei Acne inversa
Die Patientenedukation trägt einen wesentlichen Teil zu einem erfolgreichen Behandlungskonzept bei Acne inversa bei. Für Behandelnde kann es dabei entscheidend sein, sich zu ...