Traitement chirurgical du cancer du poumon à un stade précoce
Auteurs:
Prof. Dre méd. Isabelle Opitz
PD Dr méd. Sven Hillinger
Klinik für Thoraxchirurgie
Universitätsspital Zürich
E-mail: isabelle.schmitt-opitz@usz.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
L’ablation chirurgicale de la tumeur primaire et des ganglions lymphatiques associés est le traitement du CBNPC au stade précoce conforme aux directives. Les techniques peu invasives sont aujourd’hui considérées comme la norme pour le traitement chirurgical. Les segmentectomies d’épargne parenchymateuse sont déjà pratiquées actuellement chez des patients présentant une limitation fonctionnelle pour les tumeurs de petit diamètre situées en périphérie. La mortalité postopératoire est <1% dans les centres traitant un grand nombre de cas et le résultat oncologique des procédures peu invasives est au moins égal à celui de la procédure ouverte. Le dépistage précoce du cancer du poumon par tomodensitométrie à faible dose fera son entrée dans la médecine préventive à l’avenir, ce qui permettra probablement d’augmenter encore les taux de survie grâce à un diagnostic précoce.
Keypoints
-
Le traitement chirurgical est la prise en charge du CBNPC au stade précoce conforme aux directives.
-
Des procédures peu invasives – VATS ou RATS – sont utilisées de manière standard, la mortalité est inférieure à 1% et la durée d’hospitalisation n’est que de quelques jours. Selon les sociétés spécialisées internationales, au moins 70 résections anatomiques sont nécessaires chaque année, il serait souhaitable d’en réaliser plus de 150 pour obtenir d’excellents résultats.
-
La segmentectomie en cas de cancer du poumon <2cm à ganglion lymphatique négatif est probablement équivalente sur le plan oncologique et préserve la fonction pulmonaire des patients.
-
Le dépistage précoce du cancer du poumon par TDM chez les candidats à risque devrait contribuer à améliorer la survie à long terme des patients atteints de cancer du poumon.
La résection chirurgicale, y compris la lymphadénectomie, est un élément central du traitement curatif du cancer bronchique non à petites cellules (CBNPC), en particulier aux stades précoces. La discussion du cas de chaque patient chez lequel un CBNPC est nouvellement diagnostiqué au sein d’un comité interdisciplinaire de prise en charge des tumeurs est aujourd’hui indispensable. Dans ce contexte, des certifications et une assurance qualité standardisée sont exigées pour les modalités diagnostiques et thérapeutiques. Selon la Deutsche Krebsgesellschaft (Société allemande de lutte contre le cancer), au moins 75 résections anatomiques par an sont nécessaires pour obtenir une certification. Un chiffre qui correspond à la tendance à la mise en place de centres dits «à haut volume», dans lesquels les taux de morbidité et de mortalité peuvent être maintenus à un niveau aussi bas que possible grâce à la grande expertise de tous les spécialistes impliqués, y compris dans la prise en charge du cancer du poumon.1–3
Développement de techniques peu invasives
La chirurgie thoracoscopique vidéo-assistée (VATS) est aujourd’hui utilisée de manière standard dans la plupart des centres.1,4–7 Les patients âgés et ceux dont la capacité pulmonaire est réduite en profitent tout particulièrement et des taux de mortalité <1% sont atteints.5,7
Des études comparatives démontrent la supériorité de la VATS par rapport à la procédure ouverte, surtout lors de la phase postopératoire précoce.5 Grâce à l’invasivité minimale, le traumatisme tissulaire, l’inflammation et les douleurs postopératoires sont réduits et la guérison est accélérée.8 La mobilisation plus précoce qui y est associée et les réductions de coûts qui en découlent grâce à la réinsertion sociale compensent les coûts à première vue plus élevés liés à l’utilisation d’une technologie plus moderne.8 On a même pu démontrer une meilleure observance thérapeutique des patients aux traitements adjuvants éventuellement nécessaires.9 Une étude prospective randomisée réalisée chez plus de 500 patients de Grande-Bretagne (étude VIOLET) démontre un net avantage de la VATS par rapport à la technique ouverte en ce qui concerne les douleurs postopératoires, le taux de complications, la durée d’hospitalisation sans compromis en termes de résultats oncologiques précoces, y compris l’absence de récidive et la survie à un an. De plus, de meilleures capacités fonctionnelles associées à moins de réhospitalisations ont été observées chez les patients ayant bénéficié d’une intervention chirurgicale peu invasive.10
Les résultats oncologiques à long terme ne diffèrent pas significativement entre la VATS et la résection ouverte. Dans une analyse «appariée sur score de propension» menée chez plus de 1000 patients, on a même constaté une «survie spécifique au cancer» significativement meilleure chez les patients ayant bénéficié d’une intervention chirurgicale par voie peu invasive. D’autres études comparatives ont montré que la technique VATS était au moins équivalente à la technique ouverte.4, 8
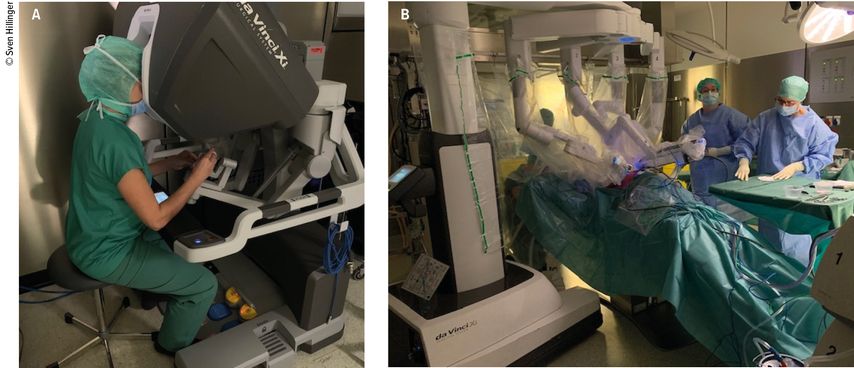
Il faut voir un progrès supplémentaire dans l’introduction de la résection thoracoscopique assistée par robot (RATS), qui permet de réaliser des résections anatomiques encore plus précises11 (et plus ergonomiques pour le chirurgien). La visualisation en trois dimensions, les degrés de liberté supplémentaires des instruments ainsi que deux consoles opératoires avec un simulateur couplé ouvrent de nouvelles dimensions pour le travail quotidien et pour la formation continue (Fig. 1). Il convient de mentionner ici l’utilisation intuitive d’une technique peu invasive, qui facilite le passage de la chirurgie ouverte à l’utilisation de technologies modernes.12
Fig. 1: Chirurgie thoracoscopique assistée par robot. A) Chirurgien opérant sur la console. B) Télémanipulateur et assistants intervenant sur le patient
Les collègues de Shanghai sont parvenus à démontrer, dans le cadre d’une vaste méta-analyse portant sur plus de 11000 patients, que la RATS est au moins équivalente à la VATS concernant les paramètres pertinents tels que la survie, l’absence de récidive et la durée de l’intervention chirurgicale, mais des études prospectives randomisées font défaut.13 Une analyse multicentrique rétrospective de la base de données de la Society of Thoracic Surgeons portant sur plus de 13000 patients atteints de CBNPC de stade I et II a également confirmé cette équivalence entre la RATS et les résections VATS.14
L’expertise spécifique et l’expérience du chirurgien sont toutefois essentielles pour le choix de la voie d’accès. Les sociétés européennes de chirurgie thoracique confirment le nombre minimum de 70 lobectomies par an, il serait souhaitable d’en réaliser plus de 150 pour obtenir d’excellents résultats.15 La durée de l’intervention chirurgicale, les complications et la durée d’hospitalisation peuvent ainsi être considérablement réduites.2,3
Une stadification précise pour optimiser le traitement individualisé
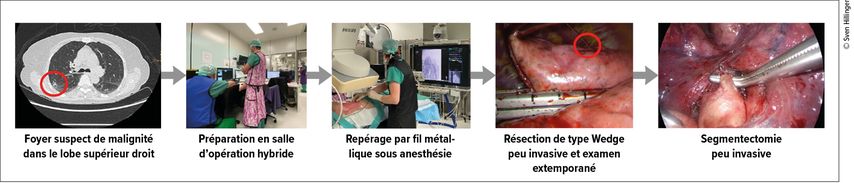
Une stadification pré/peropératoire précise est indispensable pour un traitement correct et réussi du CBNPC. Outre les méthodes d’imagerie non invasives connues comme la TDM, l’IRM et la PET, des méthodes de biopsie peu invasives sont également utilisées. Il convient de mentionner ici en particulier l’échographie endobronchique (EBUS). Grâce à des sondes d’échographie miniaturisées (EBUS radiaire), il est possible de détecter des foyers périphériques avec un taux de réussite élevé (80%).16 L’examen cytologique rapide sur place raccourcit les parcours diagnostiques et les délais d’attente, permettant ainsi un traitement plus efficace du patient. De plus, grâce à l’instauration d’une salle d’opération hybride, il est possible de suivre le parcours complet, des examens diagnostiques au traitement oncologique adéquat, dans le cadre d’une procédure «à guichet unique» confortable pour les patients et en effectuant une seule anesthésie (Fig. 2).
Fig. 2: Bloc opératoire hybride, clinique de chirurgie thoracique, Hôpital universitaire de Zurich: salle d’opération hybride comme «guichet unique» pour le diagnostic et le traitement du cancer du poumon
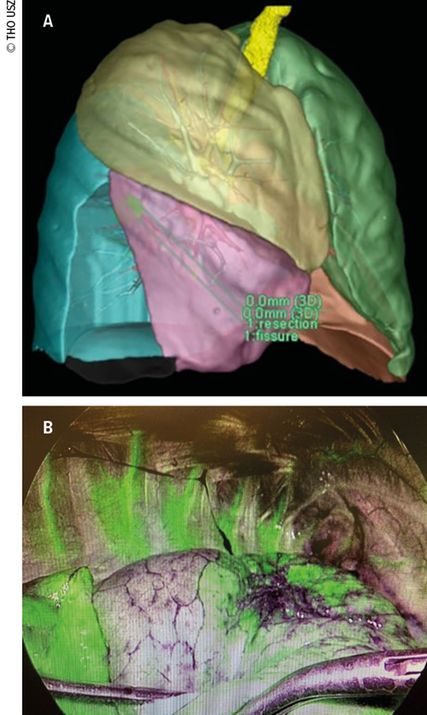
Fig. 3: Nouvelles technologies utilisées pour l’évaluation des limites des segments. A: programmes de réalité virtuelle. B: Firefly (colorant fluorescent injecté)
La question de savoir si une résection anatomique sous-lobaire (segmentectomie) est suffisante du point de vue oncologique au stade précoce du CBNPC fait actuellement l’objet de nombreuses études randomisées contrôlées, mais une analyse approfondie des données de l’European Society of Thoracic Surgeons (ESTS) a démontré que les taux de morbidité et de mortalité après des segmentectomies sont au moins aussi faibles qu’à l’issue de lobectomies.17
Pour définir avec précision les limites de la résection, on dispose aussi bien de reconstructions anatomiques matricées par TDM en phase préopératoire que d’injections peropératoires (intraveineuses ou endobronchiques) de colorants fluorescents (Fig. 3).18
Dans le cadre d’une étude prospective, les collègues de la société japonaise sont parvenus à démontrer l’innocuité19 et un avantage significatif en termes de survie des segmentectomies par rapport aux lobectomies chez des patients atteints de CBNPC périphérique à ganglion négatif <2cm de diamètre et dont la proportion de tumeurs solides est <50%. Les résultats d’autres études prospectives randomisées menées aux États-Unis et en Europe sont attendus prochainement.
Dépistage du cancer du poumon
Le dépistage précoce du cancer du poumon est également un sujet d’actualité et, selon deux études internationales, il semble très prometteur en termes d’amélioration des taux de survie au cancer du poumon. Ainsi, dans une cohorte à risque comprenant plus de 53000 candidats aux États-Unis (essai NLST), le dépistage par TDM à faible dose a permis de réduire de 20% la mortalité liée au cancer.20
Dans le cadre de l’étude européenne correspondante portant sur plus de 15000 candidats à risque (essai NELSON), ce taux a été réduit de 26% chez les hommes et même de plus de 40% chez les femmes grâce à la TDM volumétrique.21 Des programmes systématiques doivent maintenant être mis en place dans les centres afférents.
Dans le cadre d’une étude d’observation ouverte, nous réalisons à l’Hôpital universitaire de Zurich (USZ) une tomodensitométrie chez les fumeuses et fumeurs qui satisfont aux critères d’inclusion (âge: 55 à 74 ans, au moins un paquet par jour pendant 30 ans) afin de dépister les formes précoces de tumeurs pulmonaires:
https://www.usz.ch/app/uploads/2020/11/Lungenkrebs-Screening.pdf (contact: Lungenkrebs-Screening@usz.ch ).
Une initiative nationale impliquant toutes les disciplines concernées (CH-LSIG) prévoit une mise en œuvre coordonnée pour la Suisse.
Littérature:
1 Hoffmann H et al.: Surgical therapy for lung cancer: why it should be performed in high volume centers. Pneumologie 2020; 74: 670-7 2 Wang S et al.: Type and case volume of health care facility influences survival and surgery selection in cases with early-stage non-small cell lung cancer. Cancer 2019; 125: 4252-9 3 Stahel RA et al.: Survival outcome of non-small cell lung cancer patients: comparing results between the database of the Comprehensive Cancer Center Zürich and the Epidemiological Cancer Registry Zurich and Zug. Lung Cancer 2020; 146: 217-23 4 Petersen RH, Hansen HJ: Learning thoracoscopic lobectomy. Eur J Cardiothorac Surg 2010; 37: 516-20 5 Burt BM et al.: Thoracoscopic lobectomy is associated with acceptable morbidity and mortality in patients with predicted postoperative forced expiratory volume in 1 second or diffusing capacity for carbon monoxide less than 40% of normal. J Thorac Cardiovasc Surg 2014; 148: 19-29 6 Bendixen M et al.: Postoperative pain and quality of life after lobectomy via video-assisted thoracoscopic surgery or anterolateral thoracotomy for early stage lung cancer: a randomised controlled trial. Lancet Oncol 2016; 17: 836-44 7 Nasir BS et al.: Performing robotic lobectomy and segmentectomy: cost, profitability, and outcomes. Ann Thorac Surg 2014; 98: 203-8 8 Hartwig MG, D’Amico TA: Thoracoscopic lobectomy: the gold standard for early-stage lung cancer? Ann Thorac Surg 2010; 89: 2098-101 9 Petersen RP et al.: Thoracoscopic lobectomy facilitates the delivery of chemotherapy after resection for lung cancer. Ann Thorac Surg 2007; 83: 1245-9 10 Lim E et al.: Video-assisted thoracoscopic versus open lobectomy in patients with early-stage lung cancer: one-year results from a randomized controlled trial (VIOLET). J Clin Oncol 2021; 39(15 Suppl): 8504 11 Gallina FT et al.: Nodal upstaging evaluation after robotic-assisted lobectomy for early-stage non-small cell lung cancer compared to video-assisted thoracic surgery and thoracotomy: a retrospective single center analysis. Front Surg 2021; 8: 666158 12 Veronesi G et al.: Robot-assisted surgery for lung cancer: state of the art and perspectives. Lung Cancer 2016; 101: 28-34 13 Ma J et al.: Robot-assisted thoracic surgery versus video-assisted thoracic surgery for lung lobectomy or segmentectomy in patients with non-small cell lung cancer: a meta-analysis. BMC Cancer 2021; 21: 498-515 14 Louie BE et al.: Comparison of video-assisted thoracoscopic surgery and robotic approaches for clinical stage I and stage II non-small cell lung cancer using the Society of Thoracic Surgeons database. Ann Thorac Surg 2016; 102: 917-24 15 D’Amico T et al.: European guidelines on structure and qualification of general thoracic surgery. Eur J Cardiothorac Surg 2014; 45: 779-86 16 Herth FJ et al.: Endobronchial ultrasound-guided transbronchial lung biopsy in solitary pulmonary nodules and peripheral lesions. Eur Respir J 2002; 20: 972-4 17 Brunelli A et al.: Perioperative outcomes of segmentectomies versus lobectomies in high-risk patients: an ESTS database analysis. Eur J Cardiothorac Surg 2021; 59: 389-94 18 Wada H et al.: Near-infrared-guided pulmonary segmentectomy after endobronchial indocyanine green injection. Ann Thorac Surg 2020; 109: 396-403 19 Suzuki K et al.: Comparison of pulmonary segmentectomy and lobectomy: safety results of a randomized trial. J Thorac Cardiovasc Surg 2019; 158: 895-907 20 Aberle DR et al.: Reduced lung-cancer mortality with low-dose computed tomographic screening. N Engl J Med 2011; 365: 395-409 21 de Koning HJ et al.: Reduced lung-cancer mortality with volume CT screening in a randomized trial. N Engl J Med 2020; 382: 503-13
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...