Une nouvelle classification pour plus de clarté
Compte-rendu:
Regina Scharf, MPH
Rédactrice
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
La glomérulonéphrite est un cas compliqué. Cela est également dû au fait que les maladies à médiation immunitaire sont décrites à l’aide de modèles histopathologiques qui ne permettent pas de tirer des conclusions sur la cause et le traitement. Une nouvelle classification proposée devrait désormais changer la donne.
Laglomérulonéphrite (GN) est un terme générique désignant des maladies à médiation immunitaire relativement rares, qui entraînent des lésions glomérulaires, une maladie rénale chronique et une perte irréversible de la fonction rénale. Les signes cliniques sont relativement peu spécifiques, avec une hypertension artérielle, une protéinurie et une hématurie. Le diagnostic est confirmé par une biopsie rénale. La classification des GN en sous-groupes est basée sur la description des lésions histopathologiques, par exemple GN mésangio- ou membrano-proliférative, GN membraneuse, etc., et a des origines historiques – notamment l’introduction de la biopsie rénale et la microscopie optique.1,2
Sur la base des connaissances actuelles ainsi que des méthodes diagnostiques et thérapeutiques disponibles, cette approche semble dépassée. «Nous observons toujours les mêmes inflammation et fibrose au microscope», a déclaré le Pr Dr méd. Hans-Joachim Anders, de l’Université Ludwig-Maximilian à Munich, lors du congrès annuel de la Société Suisse de Néphrologie (SSN). Il ne s’agit là que des conséquences de la maladie. La nomenclature et la classification actuelles ne fournissent cependant aucun élément de réponse concernant la pathogenèse. Cela était acceptable tant qu’il n’existait aucun autre traitement que les glucocorticoïdes. «La raison la plus fréquente de la réalisation d’une biopsie rénale était de déterminer si les corticoïdes étaient indiqués ou non», a déclaré le spécialiste. Entre-temps, les choses ont changé: grâce à des méthodes telles que l’immunophénotypage et l’analyse génétique, il a été démontré que des lésions histologiques similaires peuvent être causées par diverses maladies nécessitant un traitement complètement différent.1 De plus, il existe aujourd’hui un grand nombre de médicaments spécifiques pour le traitement des différentes entités de la GN.
Classification GN-AC
H.-J. Anders a proposé une classification simple, directement liée à l’immunothérapie (Tab.1).1 En fonction des principaux mécanismes immunologiques sous-jacents, la GN peut être divisée en 5 catégories.
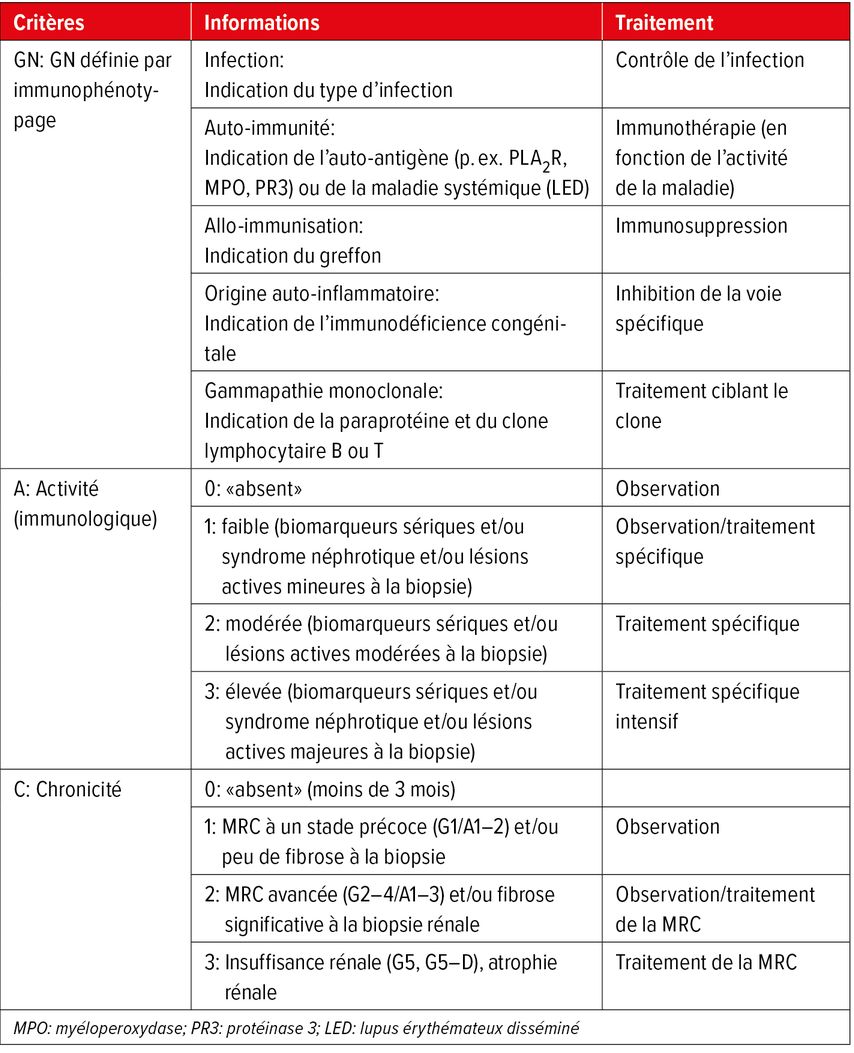
Tab. 1: Classification GN-AC proposée, y compris le système d’information en cas de glomérulonéphrite (adapté selon Romagnani P et al.)1
GN post-infectieuse
Il s’agit de la forme de GN la plus répandue dans le monde. Les virus de l’hépatite, les bactéries telles que les streptocoques et les staphylocoques ainsi que les parasites tels que les plasmodiums et les schistosomes en sont les déclencheurs. La GN survient à la suite d’une réaction immunitaire à une infection aiguë, subaiguë ou persistante. Il existe trois mécanismes immunologiques principaux.1 «En cas d’infection persistante, il faut toujours penser à une immunodéficience primaire ou secondaire», explique H.-J. Anders. Cela est également important dans la perspective d’un traitement immunosuppresseur.
Pour le traitement de la GN post-infectieuse, l’agent pathogène doit être identifié. «Si nous parvenons à l’identifier, nous pouvons traiter la maladie avec succès», a déclaré H.-J. Anders, en faisant référence aux expériences positives chez les patient·es atteint·es de l’hépatite C et du VIH.
GN liée à une gammapathie monoclonale
Cette forme de glomérulonéphrite est globalement rare. «Chez les personnes âgées de plus de 50 ans atteintes de glomérulonéphrite, il faut cependant toujours rechercher une gammapathie monoclonale, car c’est une cause fréquente à cet âge», a-t-il précisé.
Le facteur déclenchant est un clone lymphocytaire B ou plasmocytaire dans la moelle osseuse, qui produit des immunoglobulines ou des composants d’immunoglobulines néphrotoxiques. Le traitement de ces «monoclonal gammopathies of renal significance» (MGRS) cible le clone et s’inspire de l’algorithme thérapeutique du myélome multiple.1
GN d’origine auto-inflammatoire
La GN d’origine auto-inflammatoire est la conséquence d’un dysfonctionnement congénital du système immunitaire, qui entraîne une augmentation de l’activité des cytokines, par exemple de l’interleukine (IL-)1, du facteur de nécrose tumorale alpha (TNF-α) ou de l’interféron de type 1. Celles-ci peuvent provoquer des réactions inflammatoires avec lésions organiques, par exemple une néphrite lupique. Les maladies médiées par le complément, telles que la glomérulonéphrite à dépôts de C3 (C3GN), font également partie de ce groupe.1 Le diagnostic est posé sur la base d’une analyse génétique. Le traitement consiste en une immunothérapie ciblée: «on n’utilise aucun corticoïde ni mycophénolate mofétil, mais une inhibition sélective de la voie dérégulée et la maladie est sous contrôle», a déclaré H.-J. Anders.
GN d’origine auto-immune
Cette forme de GN survient à la suite d’une réponse immunitaire adaptative à un ou plusieurs auto-antigènes. L’auto-immunité est la conséquence d’une perte de tolérance à laquelle contribuent des facteurs génétiques et environnementaux. Dès la perte de tolérance, une auto-immunité à médiation cellulaire ou humorale se développe. Celle-ci peut être transitoire ou conduire à la formation de cellules T et B à mémoire autoréactives et à une mémoire immunitaire à long terme. Une exposition renouvelée ou prolongée à l’antigène entraîne une activité immunologique spécifique qui se manifeste sous la forme d’une activité pathologique persistante ou récidivante.1
Bien que la présentation clinique varie et que les schémas des lésions histologiques diffèrent en fonction de la localisation des antigènes, les mécanismes de la réaction immunitaire sous-jacente présentent des points communs. «Nombre de collègues pensent que la GN à IgA, la GN avec ANCA ou la néphrite lupique constituent des maladies différentes. D’un point de vue immunologique, elles fonctionnent toutefois exactement de la même manière», a déclaré l’intervenant. Ce sont les antigènes et la présentation clinique qui les différencient. Le traitement repose sur des médicaments ciblant des éléments individuels du système immunitaire adaptatif qui jouent un rôle dans la GN d’origine auto-immune, tels que l’azathioprine, le MMF, les inhibiteurs de la calcineurine, les agents dépléteurs de lymphocytes B et le bélimumab, ainsi que les glucocorticoïdes.
GN par allo-immunisation
La réponse immunitaire adaptative dans cette forme de GN présente des similitudes avec la GN d’origine auto-immune décrite ci-dessus. Elle survient chez les personnes ayant subi une allogreffe d’organes, de moelle osseuse ou de cellules. La réponse immunitaire est dirigée contre les antigènes HLA et non-HLA.1 Pour le traitement de l’allo-immunisation en général et en cas de GN par allo-immunisation, on utilise actuellement les mêmes médicaments que pour le contrôle de l’auto-immunité.
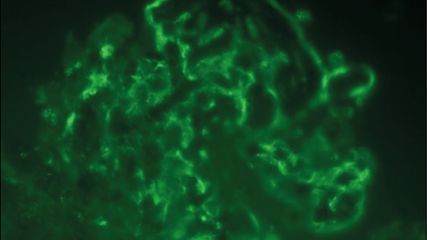
Détermination de l’activité de la maladie
La classification de la GN sur la base de sa pathogenèse nécessite un immunophénotypage approfondi au moyen d’analyses génétiques, microbiologiques et sérologiques, d’une recherche élargie d’auto-anticorps, d’analyses du complément dans le sérum, d’une ponction de la moelle osseuse, etc.1 La biopsie rénale reste un outil diagnostique important: «elle confirme la présence ou l’absence d’une GN et fournit des informations fiables sur l’activité ainsi que la chronicité de la maladie en l’absence de biomarqueurs sériques spécifiques», explique H.-J. Anders. Ce dernier point est déterminant pour l’intensité de l’immunothérapie et du traitement de la maladie rénale chronique (MRC). Plusieurs options thérapeutiques sont aujourd’hui disponibles pour ces deux indications.
Le spécialiste a déconseillé d’utiliser la valeur de protéinurie pour évaluer l’activité de la maladie en cas de GN, car elle constituerait un mauvais biomarqueur. Les causes typiques de protéinurie chez les personnes présentant une GN inactive sont par exemple l’obésité, un apport élevé en sel ou en protéines, un nombre réduit de néphrons, des lésions glomérulaires, le diabète sucré et un traitement par des vasodilatateurs. Tous ces facteurs doivent toujours être contrôlés avant d’interpréter une protéinurie comme un marqueur de l’activité immunologique.
Source:
Congrès annuel de la Société Suisse de Néphrologie (SGN/SSN), du 5 au 6 décembre 2024, à Bâle
Littérature:
1 Romagnani P et al.: Nephrol Dial Transplant 2023; 38: ii3-10 2 Anders HJ et al.: Nat Rev Immunol 2023; 23: 453-71
Das könnte Sie auch interessieren:
Néphrite lupique: détection en temps voulu et traitement adéquat
La néphrite lupique est l’une des principales manifestations organiques du lupus érythémateux systémique, car elle contribue de manière décisive à la morbidité et à la mortalité de la ...
Petites voies respiratoires, grands effets: «small airways disease»
La maladie des petites voies respiratoires («small airways disease», SAD) joue un rôle central dans les maladies respiratoires chroniques telles que la BPCO et l’asthme. Outre le ...
Réactivation du VHB sous traitement immunosuppresseur
En raison des dynamiques migratoires actuelles, la prévalence de l’infection par le virus de l’hépatite B (VHB) est également en hausse en Autriche. Il faut donc être particulièrement ...