Nierenzellkarzinom: Paradigmenwechsel und mysteriöse Mikrobiome
Autorin:
Univ.-Prof. Dr. Manuela Schmidinger
Universitätsklinik für Urologie
Medizinische Universität Wien
Am ASCO-Jahrestreffen 2023 gab es wieder zahlreiche Updates zumThema Nierenzellkarzinom, sowohl im adjuvanten als auch im metastasierten Setting. Beim klarzelligen Nierenzellkarzinom gibt es keinen Paradigmenwechsel, beim nichtklarzelligen Nierenzellkarzinom könnte man das aber durchaus so sehen. Updates gab es zudem zur Zweitlinientherapie, zur Mikrobiommanipulation und zum Stellenwert der zytoreduktiven Nephrektomie.
Keypoints
-
Der Benefit einer adjuvanten ICI-Therapie in speziellen Gruppen wird durch die CM-914-Daten bestätigt.
-
Update der First-Line-Studien: Updates bestätigen die robusten Daten in der ITT-Population, die Rolle der ICI-TKI-Therapie bei Patient:innen mit günstigem Risiko bleibt offen.
-
Mikrobiommanipulation: Es bleibt schwierig, zu verstehen, warum sie so gut wirkt, denn sie verändert weder den relativen Reichtum an Bifidobakterien noch die Stuhl-Mikrobiom-Diversität … aber sie wirkt.
-
Zweitlinientherapie: Atezolizumab+Cabozantinib ist in der Zweitlinientherapie nicht besser als Cabozantinib allein; aber Atezolizumab ist nicht relevant beim RCC.
-
„Non-clear-cell“: ICI-basierte Therapie sollte beim non-ccRCC eine „Standard of Care“-Rolle haben.
-
Zytoreduktion in der ICI-Ära: Ja! Der Zeitpunkt ist variabel.
Adjuvante Therapie
Bislang ist Pembrolizumab beim Nierenzellkarzinom (RCC) der einzige Immuncheckpoint-Inhibitor (ICI) mit statistisch signifikanter Verlängerung des krankheitsfreien Überlebens (DFS);1 andere adjuvante ICI-Studien wurden am ESMO-Kongress gezeigt und waren allesamt negativ.
Eine dieser negativen Studien ist die Studie CheckMate-914, die die ICI-Kombination Nivolumab+Ipilimumab vs. Placebo untersucht hat. Zu ihr gab es beim ASCO-Jahrestreffen eine interessante Subgruppenanalyse:2 Wenngleich die Studie in Bezug auf die Gesamtpopulation beim DFS negativ war, konnte in Subgruppen ein deutlicher DFS-Benefit für die ICI-Therapie gezeigt werden (Tab. 1).
Tab. 1: Risikoreduktion des krankheitsfreien Überlebens (DFS) mit Nivolumab+Ipilimumab vs. Placebo in speziellen Subgruppen in der Studie CheckMate-914. Modifiziert nach Motzer RJ et al.2
Auch wenn diese ICI-Kombination nicht im adjuvanten Setting zugelassen ist, bestärken die Daten generell die Sinnhaftigkeit des immuntherapeutischen Konzeptes, insbesondere in diesen Hochrisiko-Kategorien.
Erstlinientherapie: Updates aus zwei Phase-III-Studien
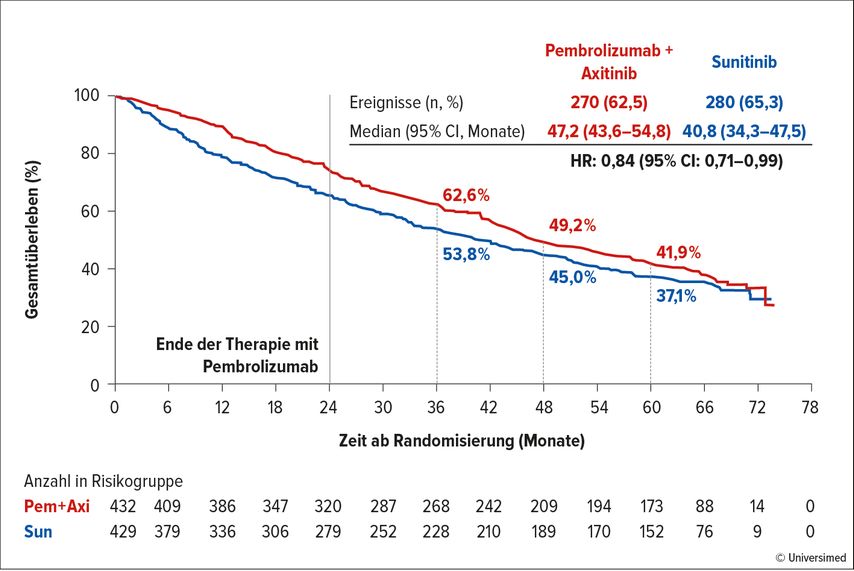
Rini BI et al. haben die Ergebnisse der Studie KEYNOTE-426 (Axitinib+Pembrolizumab vs. Sunitinib) nach einem medianen Follow-up von 67,2 Monaten vorgestellt.3 Das progressionsfreie Überleben (PFS), die Gesamtansprechraten (ORR) und die Dauer des Ansprechens (DoR) bleiben in der „Intention to treat“(ITT)-Population auch nach dieser langen Beobachtungszeit weiter signifikant und therapeutisch relevant.
Das Gesamtüberleben (OS) in der ITT-Population zeigt nach diesem Beobachtungszeitraum median keine großen Unterschiede (47,2 vs. 40,8 Monate; HR: 0,84; Abb. 1). Der therapeutische Stellenwert dieser Kombinationstherapie in Bezug auf das OS ist tatsächlich in dem Zeitraum davor besser erkennbar.
Weiterhin kein Überlebensvorteil lässt sich bei Patient:innen mit günstigem IMDC- („International Metastatic Renal Cell Carcinoma Database Consortium“)-Risiko erkennen, jedoch ist in dieser Population die Zahl der Komplettremissionen doppelt so hoch (13% vs. 6,1%) und auch das PFS ist im experimentellen Arm länger (HR: 0,76).
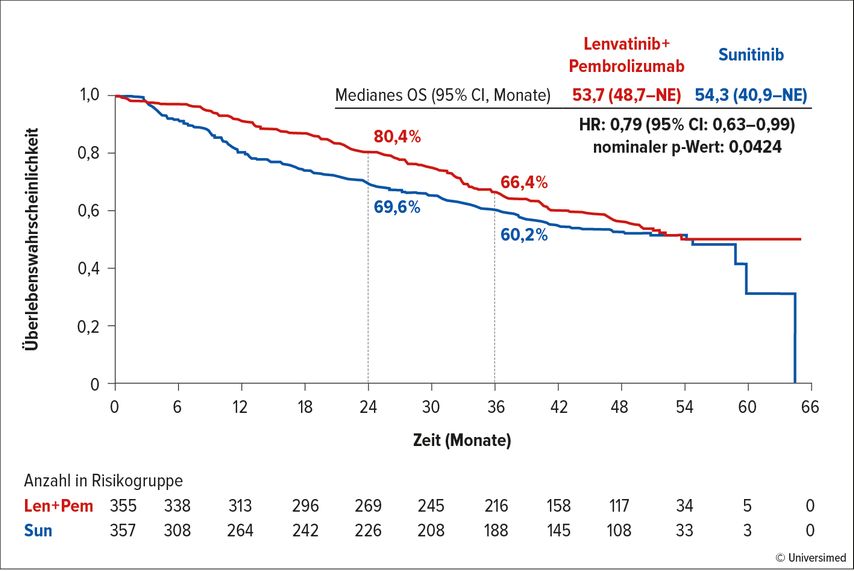
Motzer RJ et al. präsentierten ein Update der CLEAR-Studie (Lenvatinib+Pembrolizumab vs. Sunitinib) nach einem medianen Beobachtungszeitraum von vier Jahren.4 In der ITT-Population erkennt man auch hier in Bezug auf das mediane OS nach vier Jahren keinen allzu großen Benefit mehr für die Kombination (HR: 0,79), der große Unterschied zwischen den beiden Strategien ist vor allem in den ersten 42 Monaten erkennbar (Abb. 2).
Die Dauer des Ansprechens war für Patient:innen im experimentellen Arm erwartungsgemäß weiterhin deutlich länger (26,7 vs. 14,7 Monate; HR: 0–57). Eine OS-Verlängerung für Patient:innen mit günstigem IMDC-Risiko wurde nicht erreicht, jedoch ist auch hier ein eindeutiger Vorteil in Bezug auf das PFS (HR: 0,50) zu erkennen.
Die Updates der beiden Studien ändern nichts an den aktuellen Erstlinienoptionen, es bleibt bei den bisher möglichen Kombinationen für Patient:innen mit intermediärem und ungünstigem Risiko (Nivo+Ipi oder Pembro+Axi oder Nivo+Cabo oder Lenvatinib+Pembro) und drei Optionen (die genannten ohne Nivo+Ipi) für Patient:innen mit günstigem IMDC-Risiko.
Mikrobiommanipulation
Nicht die Phase-III-Studien betreffend, aber gesondert untersucht wurde der Stellenwert einer Mikrobiommanipulation mit dem Produkt CBM-588.5 Patient:innen wurden zu Nivo+Cabo+CBM-588 oder Nivo+Cabo alleine randomisiert. Es wurde durch Zugabe des Bakterienproduktes kein signifikanter Unterschied im Reichtum an Bifidobacterium spp. zwischen den Gruppen beobachtet. Auch die Alpha-Diversität zwischen Baseline und Woche 12 war nicht signifikant verändert.
Dennoch bewirkt die Zugabe von CBM-588 eine signifikante Verlängerung des PFS (p=0,042; nicht erreicht vs. 5,8 Monate) und der Ansprechraten (56% vs. 25%).
Zweitlinientherapie
Die Ergebnisse der Studie CONTACT-03 wurden von Choueiri TK et al. präsentiert. In dieser Phase-III-Studie wurden Patient:innen nach Versagen einer vorangehenden ICI-basierten Therapie zu Atezolizumab+Cabozantinib oder Cabozantinib allein randomisiert. Der primäre Endpunkt war das PFS.6 Im Konkreten ging es darum, die Frage zu klären, ob eine ICI-Fortführung in der Zweitlinie nach einer ICI-basierten Erstlinientherapie sinnvoll ist.
Die Studie war negativ in Bezug auf das PFS und auch betreffend die Remissionsraten. Es darf jedoch bezweifelt werden, ob der Einsatz von Atezolizumab, einem PD-L1-Antikörper, geeignet ist, diese Frage zu beantworten, da dieser als Monotherapie nicht die gleiche Wirkung wie PD-1-Inhibitoren gezeigt hat.
Auch besteht die Annahme, dass möglicherweise die ICI-Therapie aus der Erstlinie noch nachgewirkt haben könnte, sodass letztendlich Patient:innen beider Arme eine ICI-Wirkung in sich trugen. Ein Rückschluss auf die Wirkung von PD-1-Inhibitoren in der Zweitlinie ist in dieser Studie somit eher nicht möglich.
Nichtklarzelliges RCC
Studie KEYNOTE-B61
In der Studie KEYNOTE-B61 wurde der Einsatz von Lenvatinib+Pembrolizumab beim nichtklarzelligen RCC (non-ccRCC) untersucht.7 Nach einem medianen Follow-up von 14,9 Monaten konnte in dieser Phase-II-Studie eine hohe Wirksamkeit der ICI-Tyrosinkinaseinhibitor(TKI)-Kombination gezeigt werden (ORR: 49%; PFS: 17,9 Monate).
Interessant ist, dass ein Benefit bei allen non-ccRCC-Subgruppen gezeigt werden konnte, sogar beim chromophoben RCC, das eigentlich nicht als immunresponsiv eingeschätzt wird. Zu ähnlich guten Ergebnissen kommt auch eine Phase-II-Studie mit Nivolumab+Cabozantinib.8
ICI-Therapie beim rhabdoiden/sarkomatoiden non-ccRCC
Labaki C et al. haben die Ergebnisse einer ICI-basierten Therapie bei Patien-t:innen mit sarkomatoiden und rhabdoiden Elementen beim non-ccRCC präsentiert. Patient:innen der IMDC-Kohorte mit rhabdoidem oder sarkomatoidem non-ccRCC wurden in Bezug auf ICI-basierte Therapieergebnisse untersucht.9
Im Vergleich zu den TKI Sunitinib oder Pazopanib war das Überleben bei Patient:innen, die mit ICI-basierten Therapien behandelt wurden, in dieser Population signifikant länger (nicht erreicht vs. 7,0 Monate; HR: 0,25). Auch die Zeit bis zum Versagen der Therapie war deutlich länger (9,4 vs. 2,9 Monate; HR: 0,34).
Tripeltherapie mit Nivolumab+Ipilimumab+Cabozantinib
McGregor BA et al.stellten die Phase-II-Studie CaNi zur Tripeltherapie mit Nivolumab+Ipilimumab+Cabozantinib vor.10 Die Ergebnisse waren eher enttäuschend: Die Gesamtansprechrate war nur 18% und die PFS-Rate nach sechs Monaten 68%. Nur 44% der Patient:innen konnten alle vier Gaben von Ipilimumab erhalten, und nur 61,5% waren in der Lage, in die Nivolumab-Erhaltungsphase überzugehen. Zudem kam es bei 89,7% zu einer Dosisreduktion von Cabozantinib.
Die Toxizität war nicht unerheblich: 74% der Patient:innen hatten Nebenwirkungen von Grad 3 oder 4, 10% erlitten auch kardiale Ereignisse. Insgesamt ist aber der Beobachtungszeitraum noch sehr kurz und es bleibt abzuwarten, ob es für die Tripeltherapie bei non-ccRCC-Patient:innen vielleicht doch noch einen therapeutischen Stellenwert für einzelne Patient:innen gibt.
Zytoreduktive Nephrektomie
Der Stellenwert der zytoreduktiven Nephrektomie (CN) in der Ära der ICI-Therapie ist bislang nicht prospektiv untersucht.11 Die Autor:innen einer präsentierten retrospektiven Studie verglichen Patient:innen mit alleiniger ICI-Therapie (Gruppe m1), ICI-Therapie gefolgt von CN (Gruppe 2)und CN gefolgt von ICI-Therapie (Gruppe 3).
7367 Patient:innen wurden untersucht: Patient:innen der Gruppen 2 und 3 hatten ein signifikant längeres Überleben als jene mit alleiniger ICI-Therapie (Risikoreduktion Gruppe 2: 63%, Gruppe 3: 47%; p=0,001).
Literatur:
1 Choueiri TK et al.: New Engl J Med 2021; 385: 683-94 2 Motzer RJ et al.: ASCO 2023; Abstr. #4506 3 Rini BI et al.: ASCO 2023; Abstr. #LBA4501 4 Motzer RJ et al.: ASCO 2023; Abstr. #4502 5 Ebrahimi H et al.: ASCO 2023; Abstr. #LBA104 6 Choueiri TK et al.: ASCO 2023; Abstr. #LBA4500 7 Lee CH et al.: ASCO 2023; Abstr. #4518 8 Lee CH et al.: ASCO 2023; Abstr. #4537 9 Labaki C et al.: ASCO 2023; Abstr. #4519 10 McGregor BA et al.: ASCO 2023; Abstr. #4520 11 Zerdan MB et al.: ASCO 2023; Abstr. #4552
Das könnte Sie auch interessieren:
Brain Working Recursive Therapy
Die «brain working recursive therapy» ist eine neue psychotherapeutische Methode für effiziente Kurzzeitinterventionen bei Trauma, Angststörungen und Stresserkrankungen.
Arthritiden bei Psoriasispatienten
Circa ein Viertel aller Psoriasispatienten entwickelt im Lauf des Lebens eine Gelenkbeteiligung. Doch es gibt erfolgreiche Strategien, dem entgegenzuwirken oder zumindest die weitere ...
Patientenedukation bei Acne inversa
Die Patientenedukation trägt einen wesentlichen Teil zu einem erfolgreichen Behandlungskonzept bei Acne inversa bei. Für Behandelnde kann es dabei entscheidend sein, sich zu ...