Sphingosin-1-Phosphat-Rezeptormodulatoren in der MS-Therapie
Bericht: Felix Schmidtner, MSc
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Sphingosin-1-Phosphat-Rezeptormodulatoren stellen eine vielversprechende Medikamentenklasse für das Second-Line-Treatment bei Multipler Sklerose (MS) dar. In zwei kürzlich erschienenen Studien wurden die Bindungsaffinitäten und Sicherheitsprofile dieser krankheitsmodifzierenden Medikamente verglichen.
Sphingosine sind eine Klasse von Lipiden, die im ganzen Körper vorkommen. Besonders häufig sind sie im Gehirn. Sie stellen das Grundgerüst für das Sphingomyelin dar, mit dem die Myelinscheiden aufgebaut werden. Sphingosinphosphate binden zudem an den Sphingosin-1-Phosphat(S1P)-Rezeptoren der T-Zellen. S1P-Rezeptormodulatoren können dadurch T-Zellen in den Lymphknoten binden und die Zahl der autoreaktiven T-Zellen bei MS reduzieren.
Entscheidend unterschiedliche Bindungsaffinitäten
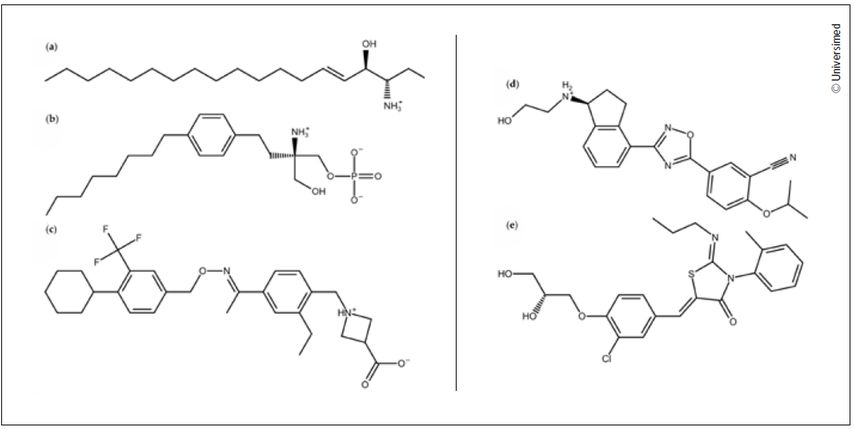
Kores et al. 2024 analysierten die Bin-dungsaffinitäten der vier in der EU zugelassenen S1P-Rezeptormodulatoren in molekularen Simulationen. Auch wenn alle vier Modulatoren niedermolekulare Verbindungen sind, unterscheiden sie sich deutlich in ihrer chemischen Struktur. Ist der erste zugelassene Wirkstoff Fingolimod mit seinem Phosphorsäurerest dem Sphingosin noch am ähnlichsten, sehen die anderen Modulatoren deutlich anders aus (Abb.1).1
Die Autor:innen fokussierten sich auf die in der Bevölkerung vorkommenden Mutationen im S1P-Rezeptor-Gen, sogenannte „single nucleotide polymorphisms“ (SNP), und simulierten deren Einfluss auf das Bindungsverhalten der Modulatoren gegenüber dem Rezeptor. Diese SNP führten alle zu einer veränderten Bindungsaffinität. Das natürlich vorkommende S1P bindet am besten, wenn keiner der SNP im Rezeptor vorkommt. Die Modulatoren zeigten aber eine höhere Bindungsaffinität, wenn zumindest ein SNP im Rezeptorgen vorkam. Siponimod bindet bei allen untersuchten Genvarianten am besten. Ozanimod und Ponesimod zeigen aber ebenfalls über alle Genvarianten hinweg ein besseres Bindungsverhalten als beim Wildtyp-Rezeptor. Fingolimod zeigte bei drei Genvarianten eine bessere Bindungsaffinität. Dabei ist zu beachten, dass es sich um seltene genetische Varianten handelte und die Effektivität eines Medikaments nicht nur von der Bindungsaffinität abhängt, sondern auch von anderen Faktoren wie Pharmakokinetik und Verträglichkeit.
Abb. 1: Chemische Strukturen des natürlich vorkommenden Sphingosin-1-Phosphats (a) und der S1P-Rezeptormodulatoren, die für die Behandlung von Multipler Sklerose verwendet werden. b: Fingolomid, c: Siponimod, d: Ozanimod, e: Ponesimod1
Basierend auf diesen Ergebnissen empfehlen die Autor:innen folgende Wirkstoffe bei den unterschiedlichen Mutationen:
-
bei M1243.32T- oder V1323.40M-Mutation: Ozanimod
-
bei F2055.42L-Mutation: Siponimod (alternativ: Ozanimod oder Posenimod)
-
bei T2075.44I-Mutation: Siponimod oder Ponesimod
-
bei T2115.48P-Mutation: Fingolimod
-
bei A2937.35T oder A2937.35V: Siponimod, Ponesimod oder Fingolimod (alternativ: Ozanimod)
Wirksamkeit von Sphingosin-1-Phosphat-Rezeptormodulatoren
Eine 2024 publizierte Arbeit von Coyle et al. gibt einen Überblick über die Wirksamkeit und Verträglichkeit der vier zuvor vorgestellten S1P-Rezeptormodulatoren. Das Ziel war es, Gemeinsamkeiten und Unterschiede der Substanzen aufzuzeigen, die im praktischen Einsatz bei individuellen Patiet:innen eine Rolle spielen könnten.2
Alle S1P-Rezeptormodulatoren zeigten in den Zulassungsstudien eine vergleichbare Wirksamkeit und reduzierten die jährliche Rückfallrate (ARR) im Vergleich zu Placebo. Beim Einsatz von Fingolimod, Ozanimod und Ponesimod war die ARR auch niedriger im Vergleich zum Einsatz des Immunsuppressivums Teriflunomid.
Es gibt bisher keine Studien, die das Wirkungsprofil der verschiedenen zugelassenen SP1-Rezeptormodulatoren untereinander vergleichen.
Verträglichkeit und Nebenwirkungsprofil
Diese Modulatoren unterscheiden sich wie zuvor beschrieben in der Bindungsaffinität zu den verschiedenen Rezeptoren-Subklassen und in der Halbwertszeit. Aufgrund der Tatsache, dass der Rezeptor in verschiedensten Organen exprimiert wird, ergeben sich dadurch verschiedene Nebenwirkungsprofile, was ein genaues Monitoring der Patient:innen erfordert. Hervorzuheben sind insbesondere kardiovaskuläre Nebenwirkungen, Lymphopenie und eine Neigung zu schweren Infektionen.
Alle vier Rezeptormodulatoren modulieren die Herzrate und können zu Bradykardie führen: Fingolimod mit einer Reduktion von 8–10bpm, Ponesimod von 6bpm, Siponimod von 5–6bpm und Ozanimod von 1,2bpm. Zudem können alle vier Wirkstoffe auch zur Hypertonie führen. Bei Fingolimod ist der Effekt am stärksten und bei Ozanimod am geringsten. Aufgrund dieses Nebenwirkungsprofils wird ein kardiologisches Monitoring mit EKG und Blutdruckmessung empfohlen, insbesondere bei der Initiation von Fingolimod, Ponesimod und Siponimod.
Alle bisher zugelassenen S1P-Rezeptormodulatoren reduzieren die Anzahl an Lymphozyten im Blut, was die Neigung zu Infektionen erhöhen kann. Diese Reduktion der Lymphozytenanzahl reichte von 57% bei Ozanomid (∼760 Zellen/μl) bis 70% bei Fingolimod (∼500 Zellen/μl), Siponimod (∼560 Zellen/μl) und Ponesimod (∼650 Zellen/μl). Der Einsatz der Modulatoren ging in allen Fällen mit einem gestiegenen Risiko für Infekte einher. Hier sind insbesondere respiratorische Infekte der oberen Atemwege und Herpesinfekte zu nennen. Bei Fingolimod häuften sich Pneumonien, bei Siponimod Pilzinfektionen. Bei der Initiation sollten hier also auftretende Infektionen im Blick behalten und die Lymphozyt-Level beobachtetet werden.
Zu beachten ist auch, dass das Tumorrisiko steigen kann. Basalzellkarzinome wurden bei allen Zulassungsstudien im niedrigen Prozentbereich beobachtet: Fingolimod 2% vs. 1% unter Placebo, Ponesimod 0,4% vs. 0,2% unter Teriflunomid), Siponimod 1,1%, bei Ozanimod wurden keine genauen Prozentangaben gemacht. Zudem wurden einzelne Fälle von Lymphomen nach der Markteinführung von Fingolimod berichtet.
Alle S1P-Rezeptormodulatoren haben bei der Initiation einen dosisabhängigen negativen Effekt auf die Lungenfunktion. In der Regel ist kein pneumologisches Routinemonitoring erforderlich, da sich die Lungenfunktion nach 1–3 Monaten wieder normalisiert.
Bezüglich der Leberfunktion zeigten sich erhöhte Werte der Alanin- und Aspartattransaminasen. Unter der Verwendung von Ozanimod und Ponesimod normalisierten sich die Werte innerhalb von 2–4 Wochen, bei Fingolimod und Siponimod erst 1–2 Monate nach Beendigung der Behandlung. Zusammengefasst sind die häufigsten Nebenwirkungen bei den S1P-Rezeptormodulatoren respiratorische Infekte, Kopfschmerzen, Bluthochdruck, Lymphopenie und Entzündungen des Nasen- und Rachenraums.
S1P-Rezeptormodulatoren sollten nicht während Schwangerschaften oder bei Kinderwunsch eingesetzt werden. Es wurden zwar keine Schwangerschaftsstudien durchgeführt, die präklinischen Daten weisen aber auf eine mögliche Gefährdung des Kindes bei Anwendung hin. Bei Schwangerschaften, die bei der Zulassungsstudie von Fingolimod stattfanden und bei Studieneinschluss nicht bekannt waren, fiel auf, dass es eine In-utero-Exposition gab. In 6% der Schwangerschaften gab es Malformationen. Zudem führte der Einsatz von Fingolimod, Ozanimod, Ponesimod und Siponimod zu Aborten.
Was ist in der täglichen Arbeit zu beachten?
Behandelnde Mediziner:innen sollten über die möglichen kardiologischen Effekte der S1P-Rezeptormodulatoren Bescheid wissen. Vorsicht ist hier geboten bei der gleichzeitigen Gabe von Betablockern, Digoxin, Ca2+-Kanal-Blockern und QT-verlängernden Therapien wegen der kardiovaskulären Effekte.
Die klinischen Guidelines zur Initiierung für die Titrierung sind einzuhalten.
Während des Einsatzes von S1P-Rezeptormodulatoren sollte auf attenuierte Lebendimpfstoffe verzichtet werden. Eventuell ausstehende Impfungen mit Lebendimpfstoffen sollten idealerweise vor dem Einsatz von S1P-Rezeptormodulatoren nachgeholt werden. Vor dem Einsatz von S1P-Rezeptormodulatoren wird auch die vollständige Varizella-zoster-Impfung empfohlen.
Patient:innen sollten über das Risiko für eine progressive multifokale Leukenzephalopathie (PML) aufgeklärt werden. Diese kann sich durch Reaktivierung des weitverbreiteten John-Cunningham-Virus bei Menschen mit Immunsuppression entwickeln und wurde vor allem bei der Behandlung mit Fingolimod beobachtet (Fälle, die in Zulassungsstudien oder Open-Label-Extension-Trials beobachtet wurden: Fingolimod 64, Siponimod 3, Ozanimod 1 Fall nach der Zulassung, Ponesimod 0 bekannte Fälle).
Zudem sollten die Patient:innen beim Einsatz von Fingolimod darüber aufgeklärt werden, dass das Absetzen mit schweren Rückfällen einhergehen kann, die mitunter zur Behinderung führen können. Beim Einsatz von Ponesimod, Siponimod oder Ozanimod wurden solche Rückfälle nach dem Absätzen nicht beobachtet.
Empfohlene Untersuchungen vor dem Einsatz
-
Angesichts der kardiovaskulären Effekte der S1P-Rezeptormodulatoren sollte vorher ein EKG durchgeführt werden. Bei allen Patient:innen mit kardiologischen Beschwerden in der Vergangenheit wie einem verlängerten QT-Intervall, Arrhythmie, Ischämie oder einem Myokardinfarkt sollte der Einsatz vorher auch mit einem Kardiologen abgeklärt werden.
-
Ein Blutbild sollte gemacht werden, um das Blutzell-Level sowie die Transaminase- und Bilirubin-Level zu bestimmen.
-
Eine ophthalmologische Evaluierung vor dem Einsatz wird bei praktisch allen Modulatoren empfohlen. Bei Ozanimod ist diese nur bei Hochrisikopatient:innen notwendig.
-
Vor dem Einsatz von Siponimod sollte der CYP2C9-Genotyp bestimmt werden.
-
Eine dermatologische Untersuchung wird bei allen Patient:innen empfohlen, bevor eine Behandlung mit Siponimod gestartet wird.
Kontinuierliches Monitoring
Der Fokus für das Monitoring sollte auf Blutdruck, Ophthalmologie, Blutbild (u.a. weise Blutzellen, Lymphozyten, Leber-Aminotransferase-Spiegel), Hautveränderungen und möglichen schwerwiegenden Infektionen liegen. Es sollte auch eine jährliche Hautkrebskontrolle durchgeführt werden. Eine laufende ophthalmologische Evaluierung ist besonders empfohlen bei allen Patient:innen mit einem Makulaödem oder Uveitis in der Vergangenheit, und mit Diabetes. Wenn die Therapie beendet wird, sollte das Monitoring zumindest noch so lange fortgesetzt werden, bis sich das Lymphozyt-Level normalisiert hat.
Kontraindikationen und Interaktionen
-
Fingolimod ist bei Patient:innen mit einem Baseline-QT-Intervall von ≤500msec kontraindiziert, genauso wie bei Arrhythmien, die Klasse-Ia- oder Klasse-III-Anti-Arrhythmie-Medikamente erfordern.
-
Ozanimod ist bei Patient:innen mit sino-artiellem Block, und bei unbehandelter Schlafapnoe kontraindiziert sowie beim Einsatz von MAO-Inhibitoren nicht empfohlen; laut Schweizer Zulassung stellen MAO-Inhibitoren aber keine Kontaindikation dar.
-
Siponimod ist bei Patient:innen mit CYP2C9*3/*3-Genotyp kontraindiziert.
-
Koadministration von Ozanimod mit Opioden, SSRI, SNRI, trizyklischen Antidepressiva und Tyraminen ist nicht empfohlen. Dies stellt aber laut Schweizer Zulassung keine Kontraindikation dar.
-
Ponesimod ist nicht empfohlen zusammen mit starken CYP3A4- und UGT1A1-Induktoren (z.B.: Rifampin, Phenytoin, Carmazepin).
-
Siponimod sollte nicht zusammen mit Modafinil und jeder Art von CYP2C9- und CYP3A4-Inhibitoren oder -Induktoren eingesetzt werden.
Progressive multifokale Leukenzephalopathie (PML)
Tritt eine PML auf, sollte die Behandlung mit einem S1P-Rezeptormodulator beendet werden.
Erste Anzeichen einer PML sind Symptome wie Sprachstörungen und Demenz. Eine Differenzialdiagnostik mit PCR-Nachweis von Virus im Liquor kombiniert mit einem MRT ist möglich, aber schwierig. Viele gesunde Patient:innen sind ebenfalls infiziert und das Bild im MRT ähnelt den Demyeliniserungsherden bei MS.
Sollte der Verdacht bestehen, muss auf eine andere Medikamentenklasse zur Behandlung der MS zurückgegriffen werden. Generell ist die PML eine seltene Erkrankung, die in erster Linie bei Patient:innen mit mittlerer bis schwerer Lymphopenie und älteren Patient:innen vorkommt.
Bei Patient:innen mit PML wurde auch vom Auftreten des Immunrekonstitutionssyndroms (IRIS) berichtet. In der Regel trat dieses innerhalb weniger Monate nach Beendigung der Behandlung mit S1P-Rezeptormodulatoren auf.
Posteriores reversibles Enzephalopathie-Syndrom (PRES)
Bei der Gabe von Fingolimod gab es auch eine geringe Anzahl an Fällen von PRES. Zu den Symptomen gehören Kopfschmerzen, visuelle Störungen, Verwirrtheit und epileptische Anfälle. Wenn das PRES nicht rechtzeitig behandelt wird, kann es zu ischämischen Schlaganfällen und zerebralen Blutungen führen.
Literatur:
1 Coyle PK et al.: Sphingosine 1-phosphate receptor modulators in multiple sclerosis treatment: a practical review. Ann Clin Transl Neurol 2024; 11(4): 842-855
2 Kores K et al.: Computational analysis of S1PR1 SNPs reveals drug binding modes relevant to multiple sclerosis treatment. Pharmaceutics 2024; 16(11): 1413
Das könnte Sie auch interessieren:
Wie lässt sich die Zeit bis zur Diagnose der amyotrophen Lateralsklerose verkürzen?
Die amyotrophe Lateralsklerose (ALS) gilt als unaufhaltsam fortschreitende neurodegenerative Erkrankung, die im Durchscnitt drei bis vier Jahre nach Symptombeginn mit dem Tod durch ...
Diagnose der ALS: von Biomarkern bis Kognition und Verhalten
Die Heterogenität der ALS macht eine Diagnose nicht leicht. Dazu kommt, dass die Pathogenese immer noch nicht richtig verstanden ist und dass sich die Frühsymptome mit jenen anderer ...
Neues aus der Alzheimer’s Disease Drug Development Pipeline
Mit der weltweiten Zulassung der Amyloidantikörper Lecanemab und Donanemab ist erstmals eine kausale Behandlung der Alzheimerkrankheit möglich geworden. Die Behandlung setzt an der ...