Eine neue Ära der Nephroprotektion
Bericht:
Dr. med. Sabina Ludin
Chefredaktorin
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Eine der absoluten Topstorys der letzten eineinhalb Jahre in der Nephrologie ist der Einsatz der SGLT2-Hemmer als neue nephroprotektive Therapie. Im Rahmen des Update Refresher Innere Medizin im Dezember 2020 liess der Nephrologe Prof. Dr. med. Thomas Fehr, Ärztlicher Direktor, Chefarzt und Departementsleiter Innere Medizin am Kantonsspital Graubünden in Chur, die Geschichte der Nephroprotektion Revue passieren und präsentierte die neusten Daten zu den SGLT2-Hemmern in diesem Zusammenhang.
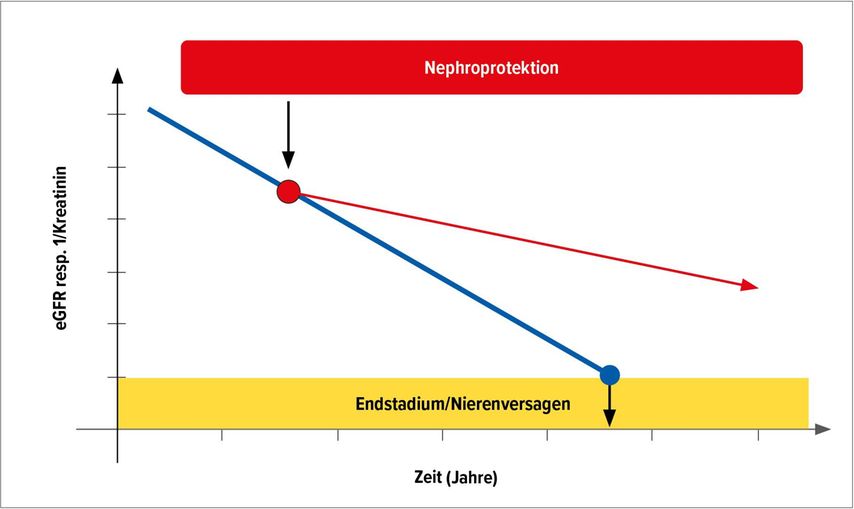
Bei chronischen Nierenerkrankungen wie beispielsweise der diabetischen Nephropathie nimmt die Nierenfunktion stetig ab. Mithilfe der Mitch-Kurve lässt sich für jeden Patienten die individuelle Progression der Niereninsuffizienz darstellen und abschätzen, wann das Nierenversagen das Endstadium erreichen wird.1 Werden die geschätzte glomeruläre Filtrationsrate (eGFR) oder der Wert 1/Kreatinin über die Zeit aufgetragen, ergibt sich eine linear abfallende Kurve (Abb. 1). Ziel der Nephroprotektion ist es, diese Kurve mit einer Intervention abzuflachen und die Progression der Niereninsuffizienz zu verlangsamen. «Wenn es gelingt, die Neigung der Kurve um ein paar Grad zu verringern, gewinnt man auf der Zeitachse rasch 5 bis 10 Jahre bis zum Erreichen des Endstadiums», erklärte Fehr.
Abb. 1: Ziel der Nephroprotektion: Der lineare Abfall der Nierenfunktion (blaue Linie) soll mithilfe einer Intervention abgeflacht resp. gebremst werden (rote Linie)
Nephroprotektion
Eine wirksame Nephroprotektion gelang erstmals in den 1990er-Jahren mittels Blockade des Renin-Angiotensin-Systems (RAS). RAS-Blocker, wie ACE-Hemmer (ACE-I) und Typ-1-Angiotensin-Rezeptorblocker (ARB), bewirken am Glomerulum eine Dilatation des Vas efferens, wodurch der glomeruläre Perfusionsdruck gesenkt und das glomeruläre Kapillarbett geschont wird. Die nephroprotektive Wirkung der ACE-I und der ARB wurde in verschiedenen Studien nachgewiesen, sowohl bei diabetischer als auch bei nichtdiabetischer Nephropathie.2 «Die RAS-Blockade bildet auch heute die Grundlage jeder nephroprotektiven Massnahme», betonte der Nephrologe.
Die 2. Generation der nephroprotektiven Massnahmen wurde in den 2000er-Jahren eingeführt. In mehreren randomisierten Studien wurde gezeigt, dass die progrediente Verschlechterung der Nierenfunktion verzögert werden kann, wenn die metabolische Azidose, die bei fast allen Patienten mit fortgeschrittener chronischer Niereninsuffizienz auftritt, mit der Gabe von Natriumbikarbonat korrigiert wird.3
Seit einigen Jahren wird das Thema nun von der 3. Generation von Nephroprotektiva, den SGLT2-Hemmern (SGLT2-I), dominiert. Für diese neue Gruppe von Antidiabetika wurde in mehreren grossen Studien eine nephroprotektive Wirkung nachgewiesen. Diese Substanzen blockieren im proximalen Tubulus den Natrium-Glukose-Kotransporter («sodium-glucose transporter 2», SGLT2), wodurch sowohl eine Glukosurie als auch eine Natriurese induziert wird. «SGLT2-I wirken also nicht nur antidiabetisch, sondern auch diuretisch und sind gewissermassen eine neue Klasse von Diuretika», sagte Fehr.
Zusätzliche Nephroprotektion durch SGLT2-Hemmer
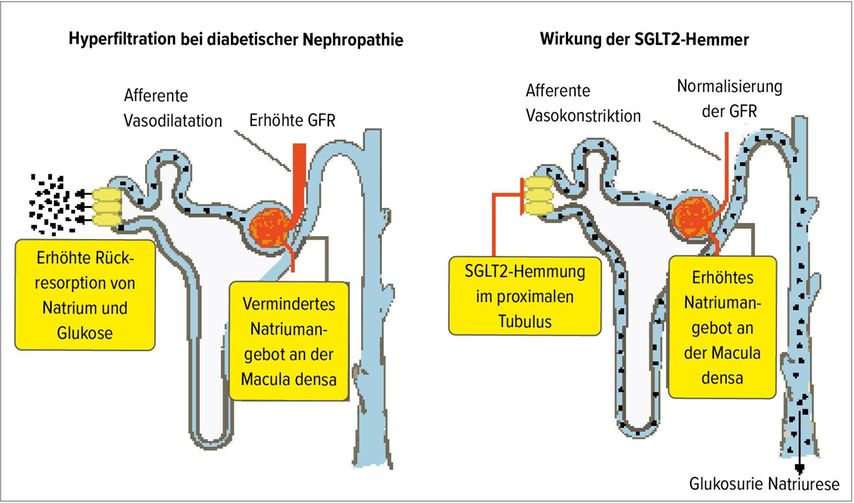
Bei Diabetes führt die Glukosurie zu einer vermehrten Rückresorption von Natrium und Glukose im proximalen Tubulus. Dadurch gelangt weniger Natrium in den distalen Tubulus, was eine Vasodilatation des Vas afferens und eine glomeruläre Hyperfiltration zur Folge hat. Die Blockade von SGLT2 verhindert die Rückresorption von Natrium und Glukose im proximalen Tubulus und stellt damit das tubuloglomeruläre Feedback wieder her: Das vermehrte Angebot an Natrium im distalen Tubulus bewirkt eine Vasokonstriktion vor dem Glomerulum und eine Reduktion der glomerulären Hyperfiltration (Abb. 2).4 Gleich wie die Senkung des glomerulären Afterloads durch eine RAS-Blockade führt die Hemmung von SGLT2 über die Normalisierung des tubuloglomerulären Feedbacks auf der afferenten Seite zu einer Druckentlastung im Glomerulum und letztlich einer Nephroprotektion.
Abb. 2: Bei der diabetischen Nephropathie kommt es zu einer glomerulären Hyperfiltration (links), die durch SGLT2-Hemmer über die Wiederherstellung des tubuloglomerulären Feedbacks normalisiert werden kann (rechts) (adaptiert nach Heerspink et al.)4
«Als mit der EMPA-REG-OUTCOME-Studie erstmals die nephroprotektive Wirkung eines SGLT2-I nachgewiesen wurde, waren die Resultate so eindrücklich, dass sie kaum zu glauben waren», berichtete Fehr. In die randomisierte, doppelblinde, placebokontrollierte Studie waren circa 7000 Patienten mit Typ-2-Diabetes und einer kardiovaskulären Erkrankung eingeschlossen worden. Praktisch alle Patienten hatten schon eine ausgebaute Therapie mit einem ACE-I oder einem ARB, erhielten also bereits eine optimale nephroprotektive Behandlung. Trotzdem konnte das Risiko für das Eintreten des kombinierten renalen Endpunkts (Makroalbuminurie, Verdoppelung des Kreatinins, terminales Nierenversagen) durch die Gabe von Empagliflozin um eindrückliche 31% reduziert werden.5
Es folgten weitere Studien, die gleich wie die EMPA-REG-Outcome-Studie als sekundäre Endpunkte auch renale Endpunkte untersucht und ähnliche Resultate erbracht haben.
Studien mit renalem Endpunkt
2019 wurde mit der CREDENCE-Studie die erste SGLT2-I-Studie mit primärem renalem Endpunkt publiziert. Die Studienpopulation der randomisierten, doppelblinden, placebokontrollierten Studie waren Typ-2-Diabetiker mit einer Nephropathie und einer ausgebauten RAS-Inhibition. Der kombinierte primäre Endpunkt umfasste terminale Niereninsuffizienz, Verdoppelung des Kreatinins oder kardiovaskulär oder renal bedingten Tod. Nach Einschluss von 4400 Patienten wurde die Studie vorzeitig abgebrochen, weil sich in der mit Canagliflozin behandelten Gruppe eine klare Überlegenheit gegenüber Placebo gezeigt hat. In der Verumgruppe war das Risiko für das Eintreten des primären Endpunkts 30% geringer als unter Placebo. Die Risikoreduktion in Bezug auf den nierenspezifischen kombinierten Endpunkt betrug sogar 34%.6
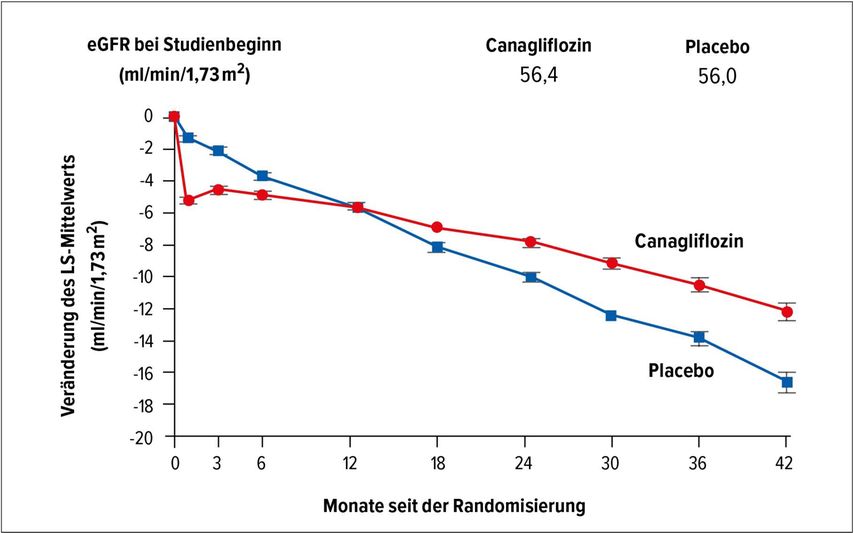
Zusätzlich wurde gezeigt, dass mit dem SGLT2-I tatsächlich die Hyperfiltration blockiert wurde. Die Proteinurie war bereits nach 6 Monaten signifikant geringer als bei Studienbeginn und auch der GFR-Verlust wurde deutlich vermindert.6 Bei Beginn der SGLT2-I-Therapie kommt es initial zu einem Abfall der GFR – davon darf man sich nicht irritieren lassen –, danach stabilisiert sich die GFR und es zeigt sich im Vergleich mit Placebo das gleiche Bild wie bei der eingangs erwähnten Mitch-Kurve (Abb. 3). «Das ist Nephroprotektion und das ist exakt der gleiche Effekt, den wir vor 25 Jahren mit den ACE-Hemmern gesehen haben. Dabei muss betont werden, dass die nephroprotektive Wirkung der SGLT2-Hemmer zusätzlich zu einer bereits etablierten optimalen RAS-Blockade hinzugekommen ist», so Fehr.
Abb. 3: Verlauf der eGFR unter Canagliflozin im Vergleich zu Placebo (adaptiert nach Perkovic et al.)5
Wie eine Metaanalyse der Outcomestudien mit Empagliflozin (EMPA-REG OUTCOME), Canagliflozin (CANVAS-Programm und CREDENCE) und Dapagliflozin (DECLARE-TIMI 58) mit insgesamt fast 40000 Probanden zeigte, handelt es sich bei der Nephroprotektion unter SGLT2-I um einen konsistenten Klasseneffekt.7
Noch einen Schritt weiter ging die erst vor Kurzem publizierte DAPA-CKD-Studie. Es ist die erste Studie, in welcher ein SGLT2-I bei Patienten mit chronischer Niereninsuffizienz (CKD) untersucht wurde, unabhängig davon, ob diese einen Diabetes hatten oder nicht. Wie bereits in den zuvor genannten Studien standen alle Patienten bereits unter einer RAS-I-Behandlung. Primärer Endpunkt der randomisierten, doppelblinden, placebokontrollierten Studie war ein Kompositum aus anhaltendem GFR-Verlust von ≥50%, terminalem Nierenversagen oder renal oder kardiovaskulär bedingtem Tod.
Auch diese Studie wurde nach Einschluss von 4300 Probanden wegen einer «überwältigenden» Wirksamkeit in der Verumgruppe vorzeitig beendet. Unter der Behandlung mit Dapagliflozin war eine Reduktion des primären Endpunkts um 39% und des nierenspezifischen Endpunkts um 44% zu verzeichnen.8 Dabei waren die renalen Effekte über sämtliche der vordefinierten Subgruppen konsistent und insbesondere unabhängig davon, ob ein Diabetes vorlag oder nicht. Eindrücklich ist auch die Risikoreduktion für Tod jeglicher Ursache um 31%.8 «Das ist wirklich ein sehr eindrückliches Resultat. Vor allem wenn man bedenkt, dass es sich bei der Studienpopulation um sehr kranke Patienten mit schwerer oder sehr schwerer chronischer Niereninsuffizienz gehandelt hat», betonte Fehr.
Fazit
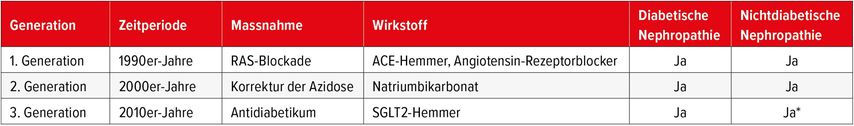
Damit steht nun fest, dass auch die SGLT2-I, gleich wie die Substanzen der 1. und 2. Generation, ihre nephroprotektive Wirkung sowohl bei diabetischer als auch bei nichtdiabetischer Nephropathie entfalten (Tab. 1). «Mit dieser neuen Medikamentengruppe, die den gleichen Effekt auf harte Endpunkte zeigt wie die ACE-Hemmer – aber dies zusätzlich zu einer etablierten RAS-Blockade –, sind wir in der Therapie des chronischen Nierenversagens definitiv in einer neuen Ära angekommen», resümierte Fehr.
Tab. 1: Drei Generationen von nephroprotektiven Massnahmen, * Beruht auf neusten Daten von 2020; noch keine Zulassung für CKD ohne Diabetes
Quelle:
FomF Update Refresher Innere Medizin, 1. bis 5. Dezember 2020 (virtuell)
Literatur:
1 Mitch WE et al.: A simple method of estimating progression of chronic renal failure. Lancet 1976; 308: 1326-8 2 Lewis EJ et al.: The effect of angiotensin-converting-enzyme inhibition on diabetic nephropathy. The Collaborative Study Group. N Engl J Med 1993; 329: 1456-62 3 de Brito-Ashurst I et al.: Bicarbonate supplementation slows progression of CKD and improves nutritional status. J Am Soc Nephrol 2009; 20: 2075-84 4 Heerspink HJ et al.: Sodium glucose cotransporter 2 inhibitors in the treatment of diabetes mellitus: cardiovascular and kidney effects, potential mechanisms, and clinical applications. Circulation 2016; 134: 752-72 5 Wanner C et al.: Empagliflozin and progression of kidney disease in type 2 diabetes. N Engl J Med 2016; 375: 323-34 6 Perkovic V et al.: Canagliflozin and renal outcomes in type 2 diabetes and nephropathy. N Engl J Med 2019; 380: 2295-306 7 Neuen BL et al.: SGLT2 inhibitors for the prevention of kidney failure in patients with type 2 diabetes: a systematic review and meta-analysis. Lancet Diabetes Endocrinol 2019; 7: 845-54 8 Heerspink HJL et al.: Dapagliflozin in patients with chronic kidney disease. N Engl J Med 2020; 383: 1436-46
Das könnte Sie auch interessieren:
«Die Nephrologie erlebt aktuell eine kleine Revolution»
Pietro Cippà ist seit April 2025 Chefarzt Nephrologie und Transplantationsimmunologie am Universitätsspital Basel – und seit dem Jahreskongress der Schweizerischen Gesellschaft für ...
Intensivierte Hämodialyse eröffnet neue Perspektiven
Eine Schwangerschaft galt bei Patientinnen mit terminaler Niereninsuffizienz jahrzehntelang als Ausnahme und war mit erheblichen Risiken für Mutter und Kind verbunden. Die intensivierte ...
Aktuelles zu Nierensteinen, Lupusnephritis und chronischer Nierenkrankheit
Am Jahreskongress der Schweizerischen Gesellschaft für Nephrologie (SGN-SSN) in Interlaken stellten junge Forschungsteams im Rahmen der Posterpräsentationen ihre Ergebnisse vor. Wir ...