Polymyalgie rhumatismale: que rechercher? Quel traitement?
Auteure:
Dre méd. Stella Mollet
FMH Rheumatologie und Allgemeine Innere Medizin
RheumaClinic Bethanien, Zürich
E-mail: rheumaclinic@hin.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
La polymyalgie rhumatismale (PMR) fait partie des maladies rhumatismales auto-immunes/inflammatoires les plus fréquentes chez les personnes âgées de >50 ans, avec une incidence de 111/100000 personnes.1,2 Il n’est cependant pas rare qu’une autre maladie sous-jacente se cache derrière les troubles polymyalgiques, de sorte qu’il faut d’abord parler de «syndrome polymyalgique» comme diagnostic de travail avant de poser le diagnostic définitif de PMR. Quels sont les diagnostics différentiels à rechercher en cas de suspicion de PMR? Quel traitement doit être initié si le diagnostic de PMR est confirmé après avoir exclu les diagnostics différentiels? L’article suivant tente de répondre à ces questions.
Keypoints
Que rechercher en cas de suspicion de polymyalgie rhumatismale?
-
Arthropathie à cristaux de pyrophosphate de calcium dihydraté (CPPD)
-
Polyarthrite rhumatoïde ou signes d’arthrite psoriasique
-
Vascularite des gros vaisseaux (au moins une anamnèse et un examen clinique ciblés)
-
Les diagnostics différentiels possibles sont nombreux. Recherche d’un autre diagnostic en cas de réponse insuffisante à la prednisone
Quel traitement en cas de diagnostic de polymyalgie rhumatismale?
-
Commencer la prednisone à une dose initiale <25mg/j
-
Évaluation d’un traitement d’épargne en glucocorticoïdes en cas d’effets secondaires liés aux glucocorticoïdes, de comorbidités ou de réduction insuffisante de la dose de prednisone
-
Les traitements d’épargne en glucocorticoïdes de référence sont les antagonistes du récepteur de l’interleukine 6, ou encore le méthotrexate ou le rituximab.
Tableau clinique de la polymyalgie rhumatismale
Les caractéristiques clés de la PMR sont caractérisées par des douleurs proximales au niveau de l’épaule et de la ceinture pelvienne, typiquement associées à une raideur matinale pendant >45 minutes et à une activité inflammatoire humorale accrue avec une CRP élevée et/ou une VS élevée. Il existe parfois aussi des symptômes constitutionnels comme la fièvre, les sueurs nocturnes, la fatigue et, plus rarement, la perte de poids.
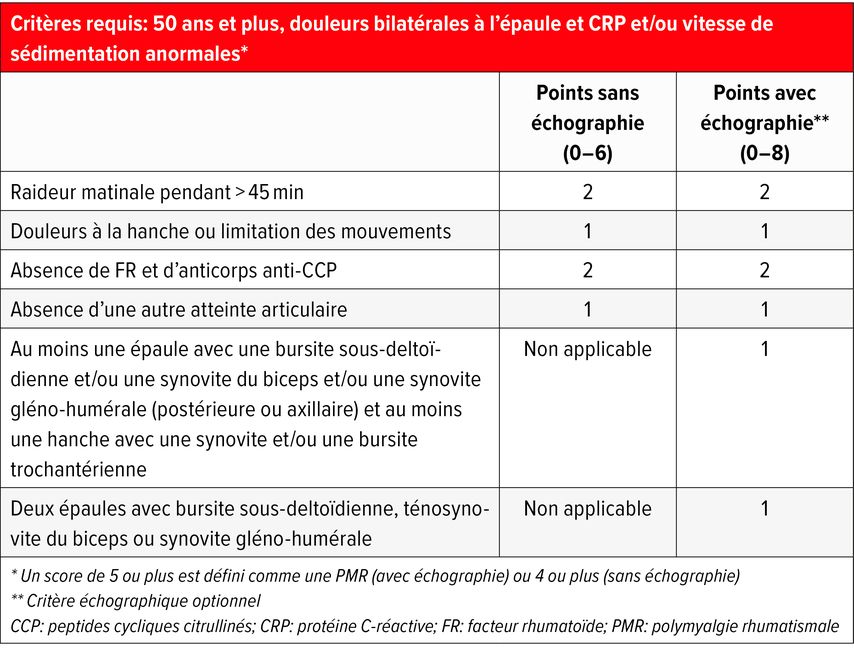
L’European Alliance of Associations for Rheumatology (EULAR) a établi en 2012 des critères de classification3, qui incluent ces caractéristiques clés (Tab.1). Outre ces dernières, des points sont également attribués en cas d’absence de facteur rhumatoïde et d’anticorps anti-CCP, ainsi qu’en l’absence d’autres douleurs articulaires. Il convient toutefois de noter qu’il s’agit de critères de classification généralement utilisés dans les études pour l’inclusion de participant·es. Il ne s’agit pas de critères diagnostiques permettant de poser un diagnostic au sens d’une liste de contrôle lorsque les critères sont remplis. La sensibilité de 68% et la spécificité de 78% sont donc plutôt faibles. L’ajout d’une échographie des épaules et des hanches n’a qu’une influence minime sur la sensibilité (66%) et la spécificité (81%). Les signes typiques d’une PMR à l’échographie sont une bursite sous-deltoïdienne généralement bilatérale, une ténosynovite du biceps en cas de synovite gléno-humérale, ainsi qu’une bursite trochantérienne ou une synovite fémoro-acétabulaire au niveau de l’articulation de la hanche.
Tab.1: Critères de classification de l’EULAR/ACR pour la polymyalgie rhumatismale (adapté selon Dasgupta B et al. 2012)3
Enfin, la PMR constitue un diagnostic d’exclusion. Sur la base du diagnostic de travail de «syndrome polymyalgique», il convient de rechercher les diagnostics différentiels principaux avant de poser un diagnostic définitif.
Diagnostics différentiels les plus fréquents de la PMR
Arthropathie à cristaux de pyrophosphate de calcium dihydraté (CPPD)
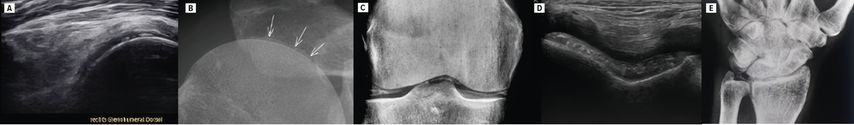
En cas de syndrome polymyalgique, il faut toujours envisager une CPPD. La prévalence de la CPPD (5%) est ainsi encore plus élevée que celle de la PMR (1%).4 Également appelée pseudogoutte, elle se caractérise par des dépôts de cristaux de pyrophosphate de calcium dihydraté sur le cartilage, les articulations, les ligaments, les tendons et les bourses. Ces dépôts peuvent être observés sous forme de calcifications à la radiographie conventionnelle et à l’échographie des articulations (Fig.1). Ce résultat radiologique, qui peut être détecté chez 15% des personnes âgées de >60 ans asymptomatiques, est appelé chondrocalcinose. On trouve typiquement des dépôts sur les articulations de l’épaule (sur le cartilage hyalin de la tête humérale et sur le fibrocartilage du labrum glénoïdal ainsi que du disque articulaire de l’articulation acromio-claviculaire), de la hanche (sur le fibrocartilage du labrum acétabulaire), du genou (sur le cartilage hyalin du fémur et du tibia, sur le fibrocartilage des ménisques) ainsi que du poignet sur le «triangular fibrocartilage complex» (TFCC). Une arthrose scapho-trapézo-trapézoïdienne (STT) dominante avec une rizarthrose comparativement faible, des ostéophytes au niveau des articulations métacarpophalangiennes (MCP) II et III sont également des signes typiques à la radiographie ainsi qu’à l’échographie. La colonne cervicale peut également être touchée dans des cas plus rares, avec des calcifications au niveau du ligament transverse de l’atlas autour de la dent de l’axis, ce qui peut conduire à un «crowned dens syndrome» accompagné de douleurs cervicales aiguës. Dans 20% des cas, la radiographie ne révèle aucune calcification au sens d’une chondrocalcinose. La recherche de cristaux de pyrophosphate de calcium dans le liquide synovial est plus sensible, de sorte qu’une ponction articulaire à visée diagnostique doit être effectuée chaque fois que possible en cas d’épanchement articulaire.
Fig.1: Radiographies et échographies de patients présentant une CPPD en tant que diagnostic différentiel principal de la polymyalgie rhumatismale. Calcifications au niveau du cartilage hyalin de la tête humérale à l’échographie (A) et à la radiographie (B); calcifications au niveau du cartilage hyalin du fémur ainsi que du fibrocartilage du ménisque à la radiographie (C) et du cartilage hyalin du fémur à l’échographie (D); calcifications au niveau du TFCC à la radiographie (E)
Polyarthrite rhumatoïde à début tardif (LORA)
Il convient également de rechercher de manière ciblée une polyarthrite rhumatoïde qui, lorsqu’elle survient à un âge avancé, est appelée polyarthrite rhumatoïde à début tardif (LORA). Les signes évocateurs sont une polyarthrite symétrique qui, en règle générale, touche également les articulations des mains et des doigts, en particulier les articulations MCP et interphalangiennes proximales (PIP). Les articulations métatarsophalangiennes (MTP) des orteils sont parfois également affectées. La sérologie permet parfois de mettre en évidence la présence d’un facteur rhumatoïde et d’anticorps anti-CCP. La détection de taux très élevés d’anticorps anti-CCP ainsi que d’érosions marginales au niveau des mains et des pieds à la radiographie sont très spécifiques de la présence d’une polyarthrite rhumatoïde et excluent clairement une PMR.
Spondyloarthrite périphérique/arthrite psoriasique
Moins fréquente, mais tout aussi importante, la spondylarthrite périphérique, en particulier l’arthrite psoriasique, peut également se manifester pour la première fois après 50 ans. Il convient donc d’interroger les patient·es sur leurs antécédents personnels et familiaux de psoriasis. Un examen clinique précis permet parfois de trouver des foyers de psoriasis cachés au niveau du sillon interfessier, du nombril, du conduit auditif ou du cuir chevelu.
Vascularite des gros vaisseaux
La polymyalgie rhumatismale est associée dans 20% des cas à une vascularite des gros vaisseaux (artérite à cellules géantes)2, de sorte que les signes évocateurs d’une telle vascularite doivent toujours être recherchés lors de l’anamnèse. Ils comprennent des symptômes crâniens tels que des céphalées temporales, des troubles de la vision (p.ex. amaurose fugace), une claudication de la mâchoire ou une dysesthésie du cuir chevelu. Les signes évocateurs d’une vascularite des gros vaisseaux extracrâniens sont une différence de pression artérielle bras droit/gauche (>20mmHg systolique) et/ou une réponse insuffisante à une dose de prednisone de 15–25mg/j.
En cas de symptômes crâniens, il faut immédiatement effectuer une échographie des artères temporale et axillaire pour détecter un signe de halo indiquant un épaississement de la paroi vasculaire. Une IRM crânienne peut également être réalisée pour rechercher une vascularite avec atteinte crânienne. Pour ce faire, il faut toutefois procéder à une «MR vessel wall imaging» ciblée, qui utilise les séquences «black blood» pour rendre les parois des vaisseaux visibles. En cas de suspicion, une vascularite des gros vaisseaux de l’aorte et des branches aortiques doit être recherchée rapidement (dans les 3 jours suivant le début du traitement par la prednisone) au moyen d’une TEP-TDM ou d’une angiographie par résonance magnétique thoraco-abdominale. Le choix de l’imagerie dépend de la méthode étant disponible le plus rapidement. Le diagnostic ne doit pas retarder l’initiation du traitement.
Autres diagnostics différentiels
Les autres diagnostics différentiels fréquents de la PMR sont le syndrome cervico- et lombo-spondylogène et la fibromyalgie.5
Ceux-ci se manifestent toutefois généralement par des douleurs mécaniques, qui se caractérisent par des douleurs liées à l’effort, toute la journée ou en soirée, sans raideur matinale accentuée. De même, une arthrose symptomatique ou une bursite sous-deltoïdienne des épaules d’origine mécanique peut généralement être différenciée à l’anamnèse et sur le plan clinique par les douleurs liées à l’effort.
En revanche, les myopathies auto-immunes ou induites par les statines présentent des symptômes cliniques très similaires à ceux de la PMR et doivent être différenciées par des analyses de laboratoire visant à déterminer la créatine kinase. Les myalgies associées à une infection ou les paranéoplasies, notamment les lymphomes, peuvent également imiter le tableau clinique d’une PMR. Dans les cas réfractaires, il convient de les rechercher.
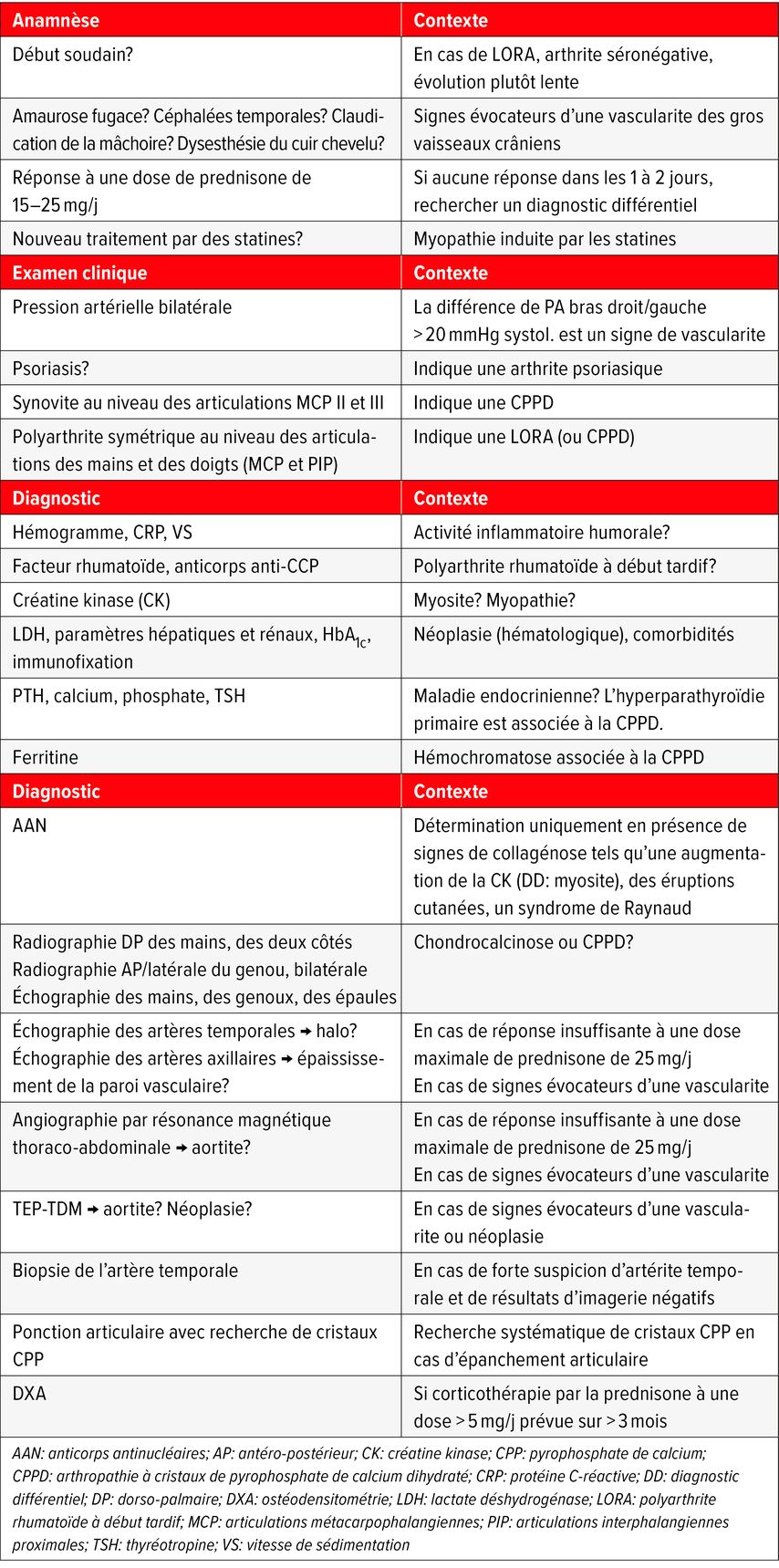
On observe typiquement une réponse rapide à la prednisone à une dose <25mg/j en un à deux jours dans la PMR. En l’absence de réponse, il convient de rechercher d’autres diagnostics, notamment une vascularite des gros vaisseaux, une néoplasie ou une infection. Une biopsie de l’artère temporale peut être utile en cas de forte suspicion de vascularite des gros vaisseaux crâniens, mais de résultats d’imagerie négatifs. Les principaux diagnostics différentiels ainsi que la liste de contrôle pour les rechercher sont résumés dans le tableau 2.
Traitement de la PMR
Glucocorticoïdes/prednisone
Les sociétés européenne et américaine de rhumatologie (EULAR – European Alliance of Associations for Rheumatology et ACR – American College of Rheumatology) ont publié en 2015 des directives sur le traitement de la PMR.6
Les glucocorticoïdes, comme la prednisone, restent le traitement de référence. Pour ne pas masquer la présence d’une éventuelle vascularite des gros vaisseaux associée, la dose initiale de prednisone ne doit pas dépasser 15–25mg/j. Une réponse immédiate à la prednisone, généralement dans un délai d’un à deux jours, est typique d’une PMR et confirme le diagnostic clinique. En cas de réponse rapide, il convient de réduire la dose de prednisone à 10mg/j dans les 4 à 8 semaines suivant la normalisation de l’activité inflammatoire humorale. En cas de rémission (aucun symptôme, paramètres inflammatoires normaux), la dose de 10mg/j doit être réduite de 1,25mg toutes les 4 semaines (couper les comprimés de 5mg en quatre).
En cas de rechute, il est recommandé de revenir à la dose précédente à laquelle les symptômes étaient encore contrôlés. Si elle est administrée en monothérapie, la prednisone doit être poursuivie pendant 1 an au maximum.
Les effets secondaires liés aux glucocorticoïdes sont fréquents. 65% des patient·es présentent au moins un tel effet secondaire. Il est donc recommandé de faire surveiller les effets secondaires les plus fréquents pendant le traitement et de rechercher les comorbidités pour lesquelles un traitement prolongé par des glucocorticoïde doit être évité. Il s’agit notamment d’évaluer le diabète et la prise de poids, les maladies cardiovasculaires concomitantes, l’ostéoporose, les infections, la cataracte, le glaucome, la myopathie liée aux corticoïdes, la fragilité cutanée, les troubles du sommeil ou la psychose associée aux corticoïdes.
De plus en plus d’études ont montré ces dernières années que les alternatives à la prednisone, sous forme de traitements d’épargne en glucocorticoïdes, étaient efficaces. Les sociétés allemande, autrichienne et suisse de rhumatologie (DGRh, ÖGR, SSR) ont publié en 2024 une mise à jour sur le traitement de la PMR dans le cadre de la directive S2.7
Traitements d’épargne en glucocorticoïdes
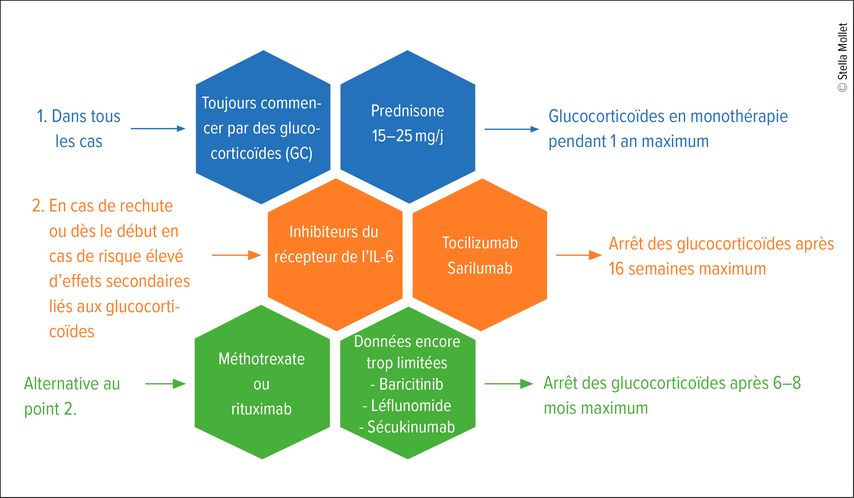
L’utilisation de traitements d’épargne en glucocorticoïdes est recommandée en présence de comorbidités (p.ex. ostéoporose, diabète, antécédents d’événements cardiovasculaires), lorsqu’une réduction de la dose de prednisone <5mg/j n’est pas possible, lorsqu’il existe en outre une arthrite périphérique ou lorsque des effets secondaires liés aux glucocorticoïdes surviennent au cours de l’évolution. Comme une récidive est fréquente chez les femmes et en cas de VS élevée >40mm/h, l’utilisation de traitements d’épargne en glucocorticoïdes doit également être envisagée à un stade précoce (Fig.2).
La modification la plus significative des directives 2024 est la recommandation de l’initiation d’une biothérapie par un antagoniste du récepteur de l’interleukine (IL-)6 en cas de récidive ou de risque élevé d’effets secondaires liés aux glucocorticoïdes. Grâce à de nouvelles études avec un haut niveau de preuve, ces traitements sont même privilégiés au méthotrexate.
Les inhibiteurs de l’IL-6 tocilizumab et sarilumab ont montré une supériorité par rapport au placebo pour l’obtention d’une rémission sans glucocorticoïdes et en termes de dose cumulée des glucocorticoïdes dans des essais randomisés contrôlés. Sur la base des études disponibles, il est recommandé d’arrêter les glucocorticoïdes après 16 semaines en utilisant des inhibiteurs du récepteur IL-6.
Le sarilumab est autorisé dans la PMR aux États-Unis (par la FDA) et dans l’UE (par l’EMA). En Suisse, son utilisation est toujours considérée comme «off-label», mais on peut espérer une autorisation prochaine.
Le méthotrexate (MTX) et le rituximab sont des alternatives aux antagonistes du récepteur de l’IL-6.
Par rapport aux directives précédentes, le MTX a donc été repositionné et ne constitue plus le traitement d’épargne en glucocorticoïdes de référence. Cela s’explique par l’effet modéré du MTX, alors que celui des inhibiteurs de l’IL-6 est constant et significatif. Le MTX peut être administré par voie sous-cutanée (dose cible de 10–20mg/semaine) ou orale (dans les études, généralement 10mg 1 fois/semaine). Cela est particulièrement utile en cas de contre-indications aux inhibiteurs de l’IL-6, comme des antécédents de diverticulites ou de phobie des aiguilles.
Dans la PMR, une étude randomisée portant sur le rituximab a mis en évidence une différence significative par rapport au placebo en ce qui concerne l’obtention d’une faible activité de la maladie, après une perfusion unique de 1000mg de rituximab. Le nombre de participant·es était toutefois faible et sa durée courte, ce qui explique que le niveau de preuve et la gradation de la recommandation soient plus faibles par rapport à ceux des inhibiteurs de l’IL-6.
Si le méthotrexate ou le rituximab sont utilisés, il est recommandé d’arrêter les glucocorticoïdes dans un délai de 6 à 8 mois.
L’inhibiteur de JAK baricitinib a montré dans une étude randomisée, contrôlée par placebo qu’une dose de glucocorticoïdes de 4mg/j par voie orale permettait d’obtenir une faible activité de la maladie, de sorte qu’une recommandation pour ce médicament est également attendue à l’avenir. Cependant, l’autorisation fait encore défaut à ce jour.
Le fait que l’inhibiteur de JAK upadacitinib ait été récemment autorisé en Suisse dans le traitement de l’artérite à cellules géantes laisse espérer que l’utilisation d’inhibiteurs de JAK en cas de PMR seule sera bientôt possible.
Les données sur le léflunomide ou l’inhibiteur de l’IL-17 sécukinumab sont insuffisantes. Il reste à attendre le résultat d’études de plus grande envergure.
Au moins une co-évaluation par un rhumatologue est recommandé afin de ne pas retarder l’évaluation des traitements d’épargne en glucocorticoïdes.
Des contrôles cliniques doivent être effectués toutes les 1 à 4 semaines jusqu’à l’obtention d’une rémission et tous les 3 à 6 mois en cas de rémission stable.
Traitements non médicamenteux
Il ne faut pas oublier les mesures thérapeutiques non médicamenteuses qui doivent être utilisées chez l’ensemble des patient·es atteint·es de PMR. Un entraînement de renforcement musculaire, éventuellement avec un physiothérapeute, permet de maintenir la masse musculaire, de prévenir les chutes et donc de prévenir les fractures ostéoporotiques.
Littérature:
1 Schmidt WA et al.: Frequency, diagnosis, and management of polymyalgia rheumatica in Germany-database analysis of medical insurance data. Rheumatology 2025; keaf367 2 Dejaco C et al.: Diagnostik und Therapie der Polymyalgia rheumatica. Z Rheumatol 2016; 75: 687-700 3 Dasgupta B et al.: 2012 classification criteria for polymyalgia rheumatica: a European League Against Rheumatism/American College of Rheumatology collaborative initiative. Ann Rheum Dis 2012; 71: 484-92 4 Hameed M et al.: Prevalence and incidence of non-gout crystal arthropathy in southern Sweden. Arthritis Res Ther 2019; 21: 29 5 Salvarani C et al.: Polymyalgia rheumatica and giant-cell arteritis. Lancet 2008; 372: 234-45 6 Dejaco C et al.: 2015 Recommendations for the management of polymyalgia rheumatica. Ann Rheum Dis 2015; 74: 1799-807 7 Buttgereit F et al.: [S2e guidelines on the treatment of polymyalgia rheumatica: update 2024 : Evidence-based guidelines of the German Society for Rheumatology and Clinical Immunology (DGRh), the Austrian Society for Rheumatology and Rehabilitation (ÖGR) and the Swiss Society for Rheumatology (SGR) and the participating medical scientific specialist societies and other organizations]. Z Rheumatol 2025; 84: 494-505
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...