Nephrokalzinose, Mutationen, Nierensteine – und was dies mit dem Alter zu tun hat
Bericht:
Moana Mika, PhD
Redaktorin
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Prof. Martin Konrad leitet die Pädiatrische Nephrologie an der Universitätsklinik für Kinder- und Jugendmedizin in Münster. An der Jahrestagung der Schweizerischen Gesellschaft für Nephrologie (SGN) hielt er eine State of the Art Lecture mit dem Titel «Phenotypic Expression of Kidney Tubular Disorders. Age Matters!»
Keypoints
-
Die idiopathische infantile Hyperkalzämie zeigt sich in stark erhöhten Kalziumwerten in Blut und Urin. Symptome sind unter anderem: Nephrokalzinose, Gedeihstörung, Muskelschwäche und Dehydrierung.
-
Die Stoffwechselstörung kann durch verschiedene Gendefekte hervorgerufen werden, die direkt oder indirekt den Abbau von Vitamin D3 stören.
-
Mildere Varianten der Gendefekte treten in der Bevölkerung häufiger auf. Sie beeinflussen den Kalzium-Phosphat-Haushalt und tragen damit zur Bildung von Nierensteinen bei.
-
Einfache medizinische Massnahmen, wie zum Beispiel eine Substitution mit Phosphat oder die Sistierung der Vitamin-D3-Prophylaxe, scheinen effektiv zu sein.
Die beiden Kinder, die der Kindernephrologe Konrad in seinem Vortrag vorstellte, waren erst drei respektive vier Monate alt, als bei ihnen eine infantile primäre Hyperoxalurie des Typs 1 (PH1) diagnostiziert wurde. Für die Kinder bedeutete dies fortan eine wahre Odyssee an Behandlungen: Nebst der täglichen Peritonealdialyse kam alle paar Tage eine Hämodialyse hinzu. Das Ziel: das Oxalat aus dem Körper zu filtern. Im Alter von rund einem halben Jahr wurde den beiden zudem eine doppelte RNA-Interferenztherapie verabreicht. Die Therapie hemmt die Translation eines Gens, das für die Produktion von Glyoxylat – einem Substrat für die Bildung von Oxalat – zuständig ist.1
PH1 ist eine seltene Erkrankung – und lebensbedrohlich für Betroffene. Ihnen fehlt genetisch bedingt ein Enzym zum Abbau von Glyoxylat. Ohne das Enzym wird Glyoxylat in Oxalat umgewandelt. Dieses verbindet sich im Körper mit Kalzium, es bilden sich unlösliche Kristalle, die die Nieren verkalken und zu Nierensteinen wachsen. Eine longitudinale Studie zeigte, dass bei 192 Teilnehmenden mit PH1 das Nierenüberleben zehn Jahre nach Diagnose bei 79% lag, 20 Jahre nach Diagnose noch bei 51%.2
Trotz RNA-Therapie: Die Nieren der beiden Kinder mit PH1 waren durch das Oxalat stark geschädigt. Das eine Kind erhielt im Alter von zwei Jahren eine Nierentransplantation und ist seitdem nicht mehr auf die Dialyse angewiesen.1 Für das andere Kind sei bislang noch kein passendes Spenderorgan gefunden worden, erzählte Konrad.
Nephrokalzinose bei Kindern
Nebst der Hyperoxalurie, wie sie die Kinder aus dem Fallbericht von Konrad haben, stellt auch die Hyperkalzurie ein Risiko für verkalkte Nieren – eine sogenannte Nephrokalzinose – und Nierensteine dar. «Kinder sind suszeptibler, eine Nephrokalzinose zu entwickeln», so Konrad. Bei Erwachsenen träten hingegen häufiger Nierensteine auf. Das Alter, in dem sich eine genetische Nierenerkrankung manifestiere, scheine die phänotypische Ausprägung zu beeinflussen. «Age matters!», sagte Konrad dazu.
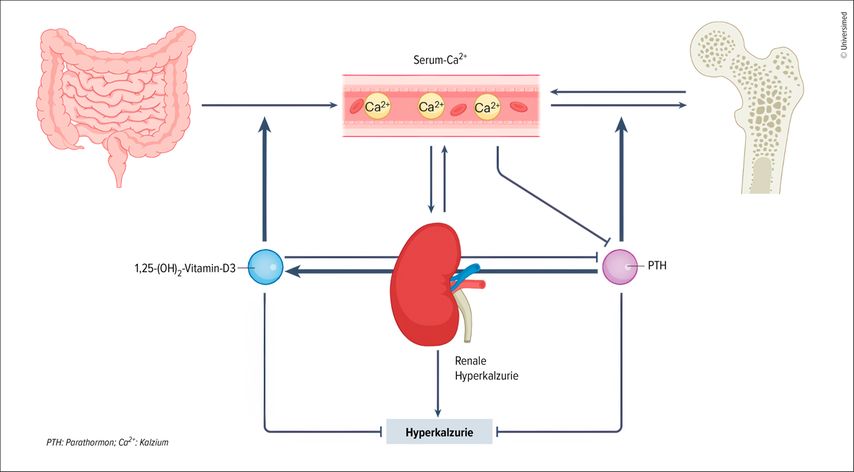
Kalzium wird in der Niere zurückresorbiert, rund zwei Drittel über einen passiven Transport im proximalen Tubulus, der Rest im distalen Tubulus, insbesondere im dicken aufsteigenden Ast.3 Die Rückresorption im distalen Tubulus wird über das Parathormon reguliert: Das Hormon aus der Nebenschilddrüse zielt auf eine rasche Erhöhung der Kalziumkonzentration im Plasma ab und steigert daher nicht nur die Resorption in der Niere, sondern stimuliert auch die Synthese von Calcitriol (1,25-[OH]2-Vitamin-D3), der aktiven Form von Vitamin D3. Calcitriol wiederum begünstigt die Aufnahme von Kalzium aus dem Darm und reguliert die Knochenhomöostase (Abb. 1).4
Abb. 1: Pathophysiologie der Hyperkalzurie. Die Rückresorption von Kalzium in der Niere erfolgt über einen passiven Transport im proximalen Tubulus und einen Parathormon-gesteuerten Transport im distalen Tubulus. Parathormon stimuliert zudem die Synthese von Calcitriol (1,25-[OH]2-Vitamin-D3), der aktiven Form von Vitamin D3. Calcitriol wiederum begünstigt die Aufnahme von Kalzium aus dem Darm und reguliert die Knochenhomöostase (modifiziert nach Bargagli M et al. 2025)4
Transporter, die an der Rückgewinnung von Kalzium beteiligt sind, können genetische Mutationen aufweisen. Je nach Transporter sind unterschiedliche Tubulus-Abschnitte beeinträchtigt, beim Bartter-Syndrom beispielsweise der dicke aufsteigende Ast, beim Gitelman-Syndrom der konvolute Teil. «Es ist daher nicht erstaunlich, dass diese Mutationen die Entstehung der Nephrokalzinose oder die Bildung von Nierensteinen beeinflussen», sagte Konrad. Eine Patientin mit Nephrokalzinose blieb Konrad in besonderer Erinnerung. Dieser Fall hat seine eigene Forschung massgeblich beeinflusst.
Was ist die Ursache der idiopathischen Hyperkalzämie?
Vor fast 20 Jahren sah Konrad das damals sechsmonatige Mädchen zum ersten Mal in seiner Sprechstunde. Nebst einer Nephrokalzinose wurde bei dem Kind eine Polyurie diagnostiziert, es war dehydriert, hatte eine muskuläre Hypotonie und war für sein Alter unterentwickelt. «Es hatte signifikant hohe Kalziumwerte im Serum und Urin, dafür aber ein niedriges Parathormon», sagte Konrad. Welche Mutation für das Krankheitsbild verantwortlich war – oder ob es sich überhaupt um eine vererbte Krankheit handelte –, war zu jener Zeit nicht bekannt. Und so wurde bei dem Mädchen die Diagnose idiopathische infantile Hyperkalzämie (IIH) gestellt. «Wir haben Pamidronat verabreicht, die Vitamin-D3-Gabe gestoppt und die Kalziumaufnahme über die Ernährung reduziert», sagte Konrad. Die Kalziumwerte senkten sich und der Zustand des Kindes habe sich daraufhin verbessert.
Auch wenn es dem Kind besser ging – Konrad liess die IIH keine Ruhe. «Die Krankheit wurde in den 1950er-Jahren zum ersten Mal beschrieben», sagte er. «In dieser Zeit kam es in Grossbritannien zu einer endemischen Häufung von IIH.» Die britische Gesundheitsbehörde empfahl damals, Kindern hochdosiertes Vitamin D3 zu verabreichen, und zwar 4000IE pro Tag. In anderen Ländern galt die Empfehlung von 400IE pro Tag. Aufgrund der Häufung von IIH in Grossbritannien ging man davon aus, dass eine Vitamin-D3-Hypersensitivität die IIH verursachte.5
«Uns hat die IIH interessiert, daher haben wir eine Kohorte von betroffenen Kindern zusammengestellt», erzählte Konrad. Basierend auf den Erkenntnissen aus Grossbritannien vermutete Konrad, dass die Krankheit durch eine Genmutation im Vitamin-D3-Metabolismus entstand. Konrad und sein Team versuchten mittels «candidate gene approach» das entsprechende Gen zu finden. Calcitriol, die aktive Form von Vitamin D3, wird in den Nieren aus Calcidiol hergestellt. Calcidiol entsteht in der Leber aus Cholecalciferol, das wiederum durch UV-B-Strahlung in der Haut isomerisiert wird und von dort in den Blutkreislauf gelangt.6
«Damit haben wir zwei Rätsel gelöst»
Konrad und sein Team hatten Glück: Tatsächlich fanden sie bei sechs Kindern mit IIH eine Mutation im CYP24A1-Gen. Das Gen kodiert für ein Enzym – die 25-Hydroxyvitamin-D-24-Hydroxylase. Das Enzym baut Calcitriol ab, verliert aber seine Funktion bei einer Mutation.7 «Wenn man Kindern mit dieser Mutation dann auch noch Vitamin D3 verabreicht, akkumuliert dieses und führt zu Hyperkalzämie», erklärte Konrad. Dazu kommt: Auch in einer zweiten Kohorte von vier Kindern fanden die Forschenden die Mutation im CYP24A1-Gen. Die Kinder dieser Kohorte hatten eine hochdosierte Bolus-Prophylaxe mit Vitamin D3 erhalten und entwickelten daraufhin eine symptomatische Hyperkalzämie. Konrad schlussfolgerte, dass die Mutation nicht nur ein genetischer Risikofaktor für Hyperkalzämie sei, sondern dass die Hyperkalzämie auch durch eine Vitamin-D3-Prophylaxe ausgelöst werden könne.7 «Damit haben wir gleich zwei Rätsel gelöst: die ‹nun nicht mehr idiopathische› infantile Hyperkalzämie und die Vitamin-D3-Hypersensitivität», sagte Konrad.
Bei der CYP24A1-Mutation können sowohl ein Allel als auch beide Allele zusammen betroffen sein.8 Bei einer biallelischen Mutation sei das Risiko gross, eine IIH zu entwickeln, sagte Konrad. «Ist aber nur ein Allel betroffen, scheinen die Symptome etwas später aufzutreten und dann eher zu Nierensteinen zu führen», so Konrad weiter. «Auch hier gilt: Das Alter hat einen Einfluss auf den Phänotyp.» Nun gab es in Konrads Kohorten aber auch Patient:innen, die zwar mit IIH diagnostiziert waren, im CYP24A1-Gen aber keine Mutation aufwiesen, weder heterozygot noch biallelisch. Allerdings war das klinische Bild bei diesen Betroffenen in einem Punkt anders: Sie alle hatten eine Hypophosphatämie.9
Die Rolle von Phosphat
In den Nieren wird Phosphat zu 80 bis 90% rückresorbiert. Die dazu notwendigen Transportproteine befinden sich hauptsächlich im proximalen Tubulus. Das zurückgewonnene Phosphat wirkt auf den Vitamin-D3-Metabolismus: Es hemmt die Bildung von Calcitriol, der aktiven Form von Vitamin D3, und begünstigt dessen Abbau. NaPi-2a steht für Natrium-abhängiges-Phosphat-Transportprotein-2a. Es ist einer der zentralen Symporter zur Reabsorption von Phosphat. «Bei IIH-Betroffenen ohne CYP24A1-Mutation fanden wir eine Mutation im Gen, das für NaPi-2a kodiert», sagte Konrad. Dies erkläre sowohl die Hypophosphatämie als auch die Hyperkalzämie, so Konrad weiter. Zur Behandlung hätten sie zuerst nur die Vitamin-D3-Supplemente gestoppt. «Aber das bewirkte nicht viel», sagte er. Erst die Verabreichung von Phosphat habe schliesslich die Serumkonzentration erhöht und gleichzeitig das Kalzium gesenkt.9
Bei der NaPi-2a-Mutation handelt es sich um einen Defekt des Gens SLC34A1. Wie bei der CYP24A1-Mutation kann auch der SLC34A1-Defekt auf einem oder auf beiden Allelen auftreten. Und auch hier scheint dies den klinischen Phänotypen zu beeinflussen: Ist der Defekt auf beiden Allelen zu finden, birgt dies ein grosses Risiko für eine IIH. Ist allerdings nur ein Allel defekt, so manifestiert sich die Krankheit eher in einer Nephrokalzinose und Nierensteinen.10 «Ganz generell lässt sich sagen, dass sich Mutationen mit grosser Effektstärke in Krankheiten manifestieren», sagte Konrad. «Hingegen führen Varianten eher zu subklinischen oder gar gesunden Phänotypen, dafür sind sie in der Bevölkerung auch häufiger vertreten als starke Mutationen.»
Quelle:
Jahrestagung der Schweizerischen Gesellschaft für Nephrologie, 4. bis 5. Dezember 2025, Interlaken
Literatur:
1 Metry EL et al.: Successful kidney-alone transplantation in a patient with PH1 on combination RNA-interference therapy. Kidney Int 2023; 104: 203-4 2 Zhao F et al.: Predictors of incident ESRD among patients with primary hyperoxaluria presenting prior to kidney failure. Clin J Am Soc Nephrol 2015; 11: 119-26 3 Hanna RM et al.: Calcium transport in the kidney and disease processes. Front Endocrinol (Lausanne) 2022; 12: 762130 4 Bargagli M et al.: Kidney stone disease: risk factors, pathophysiology and management. Nat Rev Nephrol 2025; 21: 794-808 5 Hypercalcaemia in infants and vitamin D. Br Med J 1956; 2: 149 6 Delrue C et al.: Vitamin D and vitamin D-binding protein in health and disease. Int J Mol Sci 2023; 24 :4642 7 Schlingmann KP et al.: Mutations in CYP24A1 and idiopathic infantile hypercalcemia. N Engl J Med 2011; 365: 410-21 8 Molin A et al.: CYP24A1 mutations in a cohort of hypercalcemic patients: evidence for a recessive trait. J Clin Endocrinol Metab 2015; 100: E1343-52 9 Schlingmann KP et al.: Autosomal-recessive mutations in SLC34A1 encoding sodium-phosphate cotransporter 2A cause idiopathic infantile hypercalcemia. J Am Soc Nephrol 2016; 27: 604-14 10 Lapointe JY et al.: NPT2a gene variation in calcium nephrolithiasis with renal phosphate leak. Kidney Int 2006; 69: 2261-7
Das könnte Sie auch interessieren:
Aktuelles zu Nierensteinen, Lupusnephritis und chronischer Nierenkrankheit
Am Jahreskongress der Schweizerischen Gesellschaft für Nephrologie (SGN-SSN) in Interlaken stellten junge Forschungsteams im Rahmen der Posterpräsentationen ihre Ergebnisse vor. Wir ...
Adipositas und ihre Folgen für die Niere
Die Adipositas ist zu einem der wichtigsten weltweiten Gesundheitsprobleme geworden. Diese hat direkte und indirekte Folgen für die Niere. Neben der Gefahr einer Glomerulopathie und der ...
Inkrementelle Dialyse: Weniger kann mehr sein
Die inkrementelle Dialyse rückt zunehmend in den Fokus moderner Therapiekonzepte – nicht zuletzt, weil sie gleich mehrere Vorteile vereint: Flexibilität, eine geringere Glukosebelastung ...