Mise à jour sur la gestion des lipides
Auteures:
Dre méd. Simona Danioth
KD Dre méd. Lea Slahor
Endokrinologie/Diabetologie
Luzerner Kantonsspital, Luzern
Correspondance:
E-mail: simona.danioth@luks.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Les maladies cardiovasculaires (CV) représentent la première cause de mortalité en Suisse et dans le monde, les troubles du métabolisme des lipides étant considérés comme un facteur de risque majeur. Dans la pratique clinique, de plus en plus d’options sont disponibles pour diagnostiquer et traiter ces troubles du métabolisme des lipides.
Keypoints
-
Les troubles du métabolisme des lipides font partie des principaux facteurs de risque de maladies CV.
-
L’accent doit être mis sur l’identification précoce des facteurs de risque correspondants.
-
Pour améliorer la stratification des risques, le «phenotype assessment» (détermination du nombre de particules athérogènes) présente un intérêt croissant.
-
Un traitement hypolipémiant précoce, puissant et durable est essentiel dans la prévention et le traitement des maladies CV. Un nombre croissant de nouvelles classes de médicaments sont disponibles à cet effet, en plus des statines établies depuis longtemps.
Les maladies cardiovasculaires (CV) sont la principale cause d’augmentation de la morbidité et de la mortalité dans le monde.1 La prévention ainsi que le traitement des facteurs de risque CV (hypercholestérolémie, hypertension artérielle, diabète, obésité, consommation de tabac, activité physique insuffisante) revêtent une importance capitale à cet égard. Des traitements hypolipémiants très efficaces peuvent réduire le taux de cholestérol LDL (LDL-C) et donc la morbidité ainsi que la mortalité CV. Sur la base des études menées jusqu’à présent, l’accent a été mis sur l’obtention de la meilleure baisse possible du LDL-C. D’autres approches diagnostiques et thérapeutiques, résumées dans cet article, présentent toutefois un intérêt croissant. L’article se concentre sur les aspects cliniquement pertinents.
Diagnostic
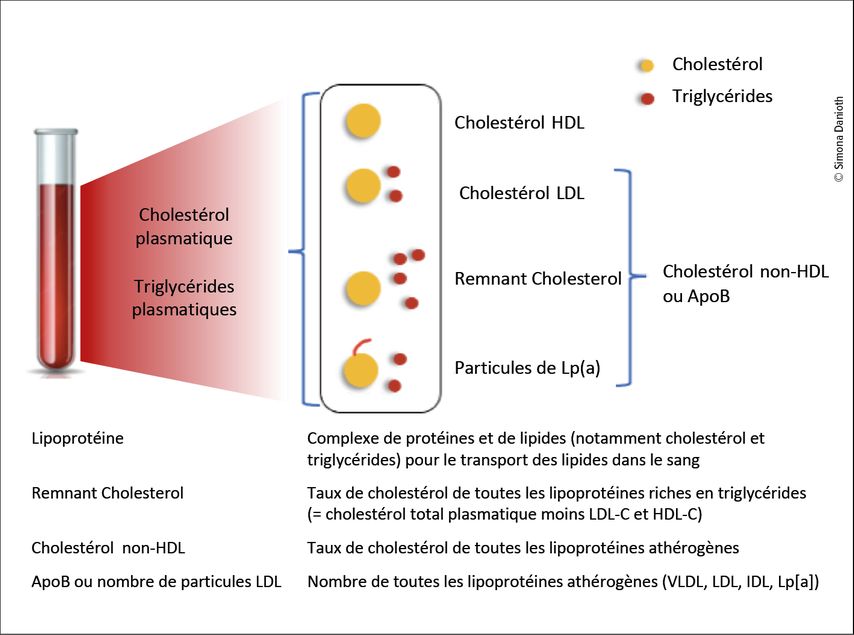
Le transport des lipides dans le sang est assuré par les lipoprotéines (Fig. 1). Les complexes qui en résultent, notamment la lipoprotéine(a), les VLDL, les IDL, présentent des propriétés athérogènes différentes en fonction de leur densité. Dans la pratique, le métabolisme des lipides est évalué de manière routinière par la détermination d’un profil lipidique normal (cholestérol total, LDL-C, HDL-C, triglycérides). Une prise de sang à jeun n’est pas forcément nécessaire pour mesurer le taux de cholestérol (à l’exception du taux de triglycérides). Cependant, une stratification des risques basée uniquement sur le LDL-C peut être insuffisante, par exemple chez les patients souffrant d’un syndrome métabolique (obésité abdominale, résistance à l’insuline).2–3 Cela est dû à une variation interindividuelle du nombre et de la taille des particules LDL. Ainsi, un nombre élevé de petites particules LDL par rapport à un faible nombre de grandes particules LDL est associé à un risque cardiovasculaire plus élevé, malgré un taux de LDL-C identique. Pour détecter une telle discordance, le «phenotype assessment» (détermination des particules athérogènes) présente un intérêt croissant. Selon les preuves actuelles, on suppose que le cholestérol total lié aux particules de lipoprotéines athérogènes (jugé comme cholestérol non-HDL) ou la concentration de ces lipoprotéines athérogènes (mesurée comme ApoB ou nombre de particules LDL) est supérieur à la mesure du LDL-C comme marqueur du risque à long terme de développer une coronaropathie.4,5
Fig. 1: Lipides et lipoprotéines plasmatiques (adapté selon Nordestgaard BG et al.: Eur Heart J 2016; 37: 1944-58)
«Remnant Cholesterol»
Différentes études ont par ailleurs montré qu’un taux élevé de «remnant cholesterol» (= cholestérol total plasmatique moins le LDL-C et le HDL-C) est associé à un risque de maladies cardiovasculaires athéroscléreuses ainsi qu’à une mortalité accrus.6 Un taux de «remnant cholesterol» élevé semble en outre contribuer à une mortalité globale accrue ainsi qu’à la survenue d’infarctus du myocarde chez les patients sous traitement par une statine déjà établi et est discuté comme facteur de risque indépendant pour les critères d’évaluation CV dans la prévention primaire.4–5,7
Lipoprotéine(a)
Une autre lipoprotéine importante est la lipoprotéine(a), qui se caractérise par ses propriétés pro-athérogènes (notamment la régulation positive des cyto- et chimiokines, le dysfonctionnement endothélial, la migration et la prolifération des cellules musculaires lisses, la calcification des valves). Sa concentration est associée de manière linéaire à l’apparition de maladies cardiovasculaires athéroscléreuses chez les adultes d’âge moyen.8 La lipoprotéine(a) est considérée comme un facteur de risque CV héréditaire. Malgré des concentrations variables dans différents sous-groupes ethniques, la lipoprotéine(a) semble modifier le risque de maladies cardiovasculaires athéroscléreuses, indépendamment du groupe ethnique et de la présence ou non de diabète.
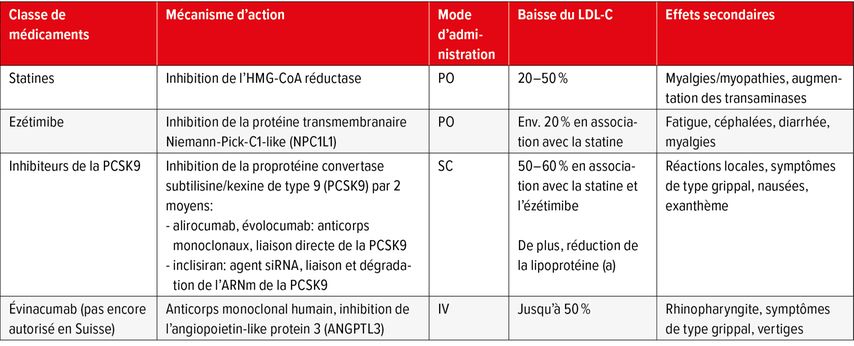
Traitements (Tab.1)
Statines et ézétimibe
Malgré le nombre croissant d’options thérapeutiques hypolipémiantes, les statines continuent, pour des raisons historiques notamment, à jouer le rôle de précurseur dans le traitement de l’hypercholestérolémie. L’inhibition de l’HMG-CoA réductase permet d’obtenir, outre une baisse du cholestérol (puissance: baisse de 20–50% du LDL-C), une réduction des VLDL-C ou une augmentation de la synthèse des récepteurs LDL, avec un effet positif sur les critères CV.9 Les effets secondaires les plus fréquents sont des myalgies/myopathies ainsi qu’une augmentation des transaminases.
En cas de réponse thérapeutique insuffisante à la dose maximale tolérée de statine (selon la stratification des risques) ou comme traitement combiné primaire chez les patients à haut risque CV, l’ajout d’ézétimibe est recommandé (puissance: baisse de 18–22% du LDL-C en association avec la statine). Le mécanisme d’action est basé sur l’inhibition de la protéine transmembranaire Niemann-Pick-C1-like (NPC1L1) avec une diminution consécutive de l’absorption intestinale du cholestérol/des micelles. Une réduction significative du nombre d’événements CV a été démontrée en cas de traitement combiné avec une statine.10 Les effets indésirables les plus fréquents sont la fatigue, les céphalées, la diarrhée et les myalgies.
Acide bempédoïque
En tant que traitement de troisième ligne ou en cas d’intolérance aux statines, un traitement par l’acide bempédoïque est recommandé (puissance: baisse d’environ 20% du LDL-C). Il s’agit d’un précurseur sous forme inactive (prodrogue) qui est absorbé de manière sélective dans les hépatocytes et qui, après activation, entraîne une inhibition de l’ATP-citrate lyase. Le site d’action étant similaire à celui des statines, il en résulte également une réduction du VLDL-C et une augmentation de la synthèse des récepteurs LDL. L’activation ayant lieu majoritairement au sein des hépatocytes, l’acide bempédoïque n’entraîne toutefois aucune myotoxicité. L’hyperuricémie/la goutte est un effet indésirable important. En outre, des troubles abdominaux, une anémie et une augmentation des transaminases peuvent survenir. En Suisse, l’acide bempédoïque est disponible en monothérapie ou en association avec l’ézétimibe. En cas de traitement par la simvastatine, il faut impérativement réduire la dose de statine de 50%. Les critères de limitation sont remplis en cas de traitement dans le cadre d’une prévention secondaire et lorsque le LDL-C est ≥1,8mmol/l ou dans le cadre d’une prévention primaire chez les patients présentant une hypercholestérolémie familiale et un LDL-C ≥2,6mmol/l. Si les critères mentionnés ne sont pas remplis, il est judicieux de consulter un spécialiste pour la demande d’une garantie de prise en charge des coûts (pour une prescription en dehors des critères de limitation). Une réponse thérapeutique adéquate (baisse d’au moins 10% du LDL-C) doit être démontrée après 6 mois.
Inhibiteurs de la PCSK9
L’approbation des inhibiteurs de la PCSK9 (puissance: baisse de 50–60% du LDL-C en association avec la statine et l’ézétimibe) a marqué une nouvelle ère dans le traitement de l’hypercholestérolémie. La proprotéine convertase subtilisine/kexine de type 9 (PCSK9) est normalement absorbée par les hépatocytes dans le cadre de l’absorption des LDL dans le sang, où elle entraîne une dégradation des récepteurs LDL. L’inhibition de la PCSK9 entraîne un recyclage des récepteurs LDL, et donc une augmentation du nombre de récepteurs au niveau de la membrane cellulaire. Cette inhibition est obtenue par la prise de médicaments: soit des anticorps monoclonaux (alirocumab, évolocumab) qui se lient directement à la PCSK9, soit un agent siRNA (inclisiran) qui est absorbé de manière ciblée dans les hépatocytes (via les endosomes) par le biais du récepteur ASGP, où il se lie à l’ARNm de la PCSK9 et le dégrade. Les inhibiteurs de la PCSK9 constituent également le seul traitement hypolipémiant autorisé à ce jour qui entraîne une réduction de la lipoprotéine(a). Ils sont administrés par voie sous-cutanée (alirocumab/évolocumab tous les 14 à 30 jours, inclisiran tous les 6 mois), l’effet secondaire le plus fréquent étant des réactions locales. Les autres effets indésirables sont des symptômes de type grippal, des nausées et un exanthème. Dans le cadre de la première prescription, le traitement par un inhibiteur de la PCSK9 nécessite une demande de garantie de prise en charge par un spécialiste. La prescription dans le cadre d’une indication de prévention secondaire et d’un LDL-C ≥1,8mmol/l ou dans le cadre d’une prévention primaire chez les patients présentant une hypercholestérolémie familiale hétéro/homozygote et un LDL-C ≥2,6mmol/l constitue une exception. La condition pour la poursuite du traitement dans le cadre de la limitation est remplie en cas de baisse d’au moins 40% du LDL-C ou d’un LDL-C <1,4mmol/l après 6 mois. Il existe une autre indication thérapeutique en cas d’intolérance aux statines, définie par l’apparition de myalgies, l’augmentation de la créatine kinase jusqu’à une valeur au moins 5 fois supérieure à la normale ou l’apparition d’une hépatopathie sévère en cas de tentative de traitement par au moins deux statines différentes avec ou sans ajout d’ézétimibe à la dose maximale tolérée pendant au moins trois mois, sans atteindre les valeurs cibles de LDL-C susmentionnées.
Perspectives
Les traitements les plus récents se concentrent sur d’autres points d’attaque du métabolisme des lipides. L’évinacumab (Evkeeza®; autorisation aux États-Unis et dans l’UE en 2021, aucune autorisation en Suisse) est un anticorps monoclonal humain qui inhibe l’angiopoietin-like protein3 (ANGPTL3) et qui a été développé spécifiquement pour le traitement de l’hypercholestérolémie familiale homozygote. Le mécanisme d’action n’est pas entièrement clair, on discute d’un effet renforcé de la lipoprotéine lipase et de la lipase endothéliale. Cela se produit indépendamment des récepteurs LDL. Des études ont mis en évidence une baisse allant jusqu’à 50% du LDL-C.11 Il n’existe aucune donnée sur les critères d’évaluation CV.
D’autres traitements visent à réduire la lipoprotéine(a) (pelacarsen, olpasiran).12 Les résultats des études de phase III sur le pelacarsen sont attendus dans le courant de l’année 2024.
Littérature:
1 Office fédérale de la statistique: Causes spécifiques de décès. https://www.bfs.admin.ch/bfs/fr/home/statistiques/sante/etat-sante/mortalite-causes-deces/specifiques.html ; dernier accès 16.4.2024 2 Mora S et al.: Discordance of low-density lipoprotein (LDL) cholesterol with alternative LDL-related measures and future coronary events. Circulation 2014; 129: 553-61 3 Lawler PR et al.: Discordance between circulating atherogenic cholesterol mass and lipoprotein particle concentration in relation to future coronary events in women. Clin Chem 2017; 63: 870-9 4 Castañer O et al.: Remnant cholesterol, not LDL cholesterol, is associated with incident cardiovascular disease. J Am Coll Cardiol 2020; 76: 2712-24 5 Quispe R et al.: Remnant cholesterol predicts cardiovascular disease beyond LDL and ApoB: a primary prevention study. Eur Heart J 2021; 42: 4324-32 6 Tybjaerg-Hansen A: Do triglycerides contribute to residual cardiovascular disease risk in diabetes? ADA Congress 2023 7 Johannesen CDL et al.: Apolipoprotein B and non-HDL cholesterol better reflect residual risk than LDL cholesterol in statin-treated patients. J Am Coll Cardiol 2021; 77: 1439-50 8 Patel AP et al.: Lp(a) (Lipoprotein[a]) concentrations and incident atherosclerotic cardiovascular disease: New insights from a large national biobank. Arterioscler Thromb Vasc Biol 2021; 41: 465-74 9 Chou R et al.: Statin use for the primary prevention of cardiovascular disease in adults: Updated evidence report and systematic review for the US Preventive Services Task Force. JAMA 2022; 328: 754-71 10 Cannon CP et al.: Ezetimibe added to statin therapy after acute coronary syndromes. N Engl J Med 2015; 372: 2387-97 11 Raal FJ et al.: Evinacumab for homozygous familial hypercholesterolemia. N Engl J Med 2020; 383: 711-20 12 Yeang C et al.: Effect of pelacarsen on lipoprotein(a) cholesterol and corrected low-density lipoprotein cholesterol. J Am Coll Cardiol 2022; 79: 1035-46
Das könnte Sie auch interessieren:
Études actuelles sur le traitement de l’ILD
Le terme pneumopathie interstitielle (ILD) est un terme générique désignant un groupe important et hétérogène de maladies qui se manifestent principalement dans l’espace broncho- ...
Mise à jour 2026: vers la modification de la maladie
Un grand nombre de médicaments biologiques immunomodulateurs et de «small molecules» ont considérablement élargi l’éventail des options thérapeutiques dans les maladies inflammatoires ...
Schémas thérapeutiques de référence plus courts dans la tuberculose
La tuberculose (TB) constitue toujours un défi majeur à l’échelle mondiale. Malgré les progrès, le besoin de schémas thérapeutiques plus efficaces, plus courts et mieux tolérés reste ...