Doubles et triples agonistes en cas de diabète et/ou d’obésité
Auteurs:
Dr méd. Michael Resl
Dr méd. Matthias Heinzl
Abteilung für Innere Medizin
Barmherzige Brüder Linz
E-mail:
De nouveaux développements sur les doubles et triples agonistes ont été présentés dans le cadre du congrès 2023 de l’EASD. Le tirzépatide n’était-il qu’un début? Cet article présente les perspectives d’avenir.
Agonistes des récepteurs du GLP-1
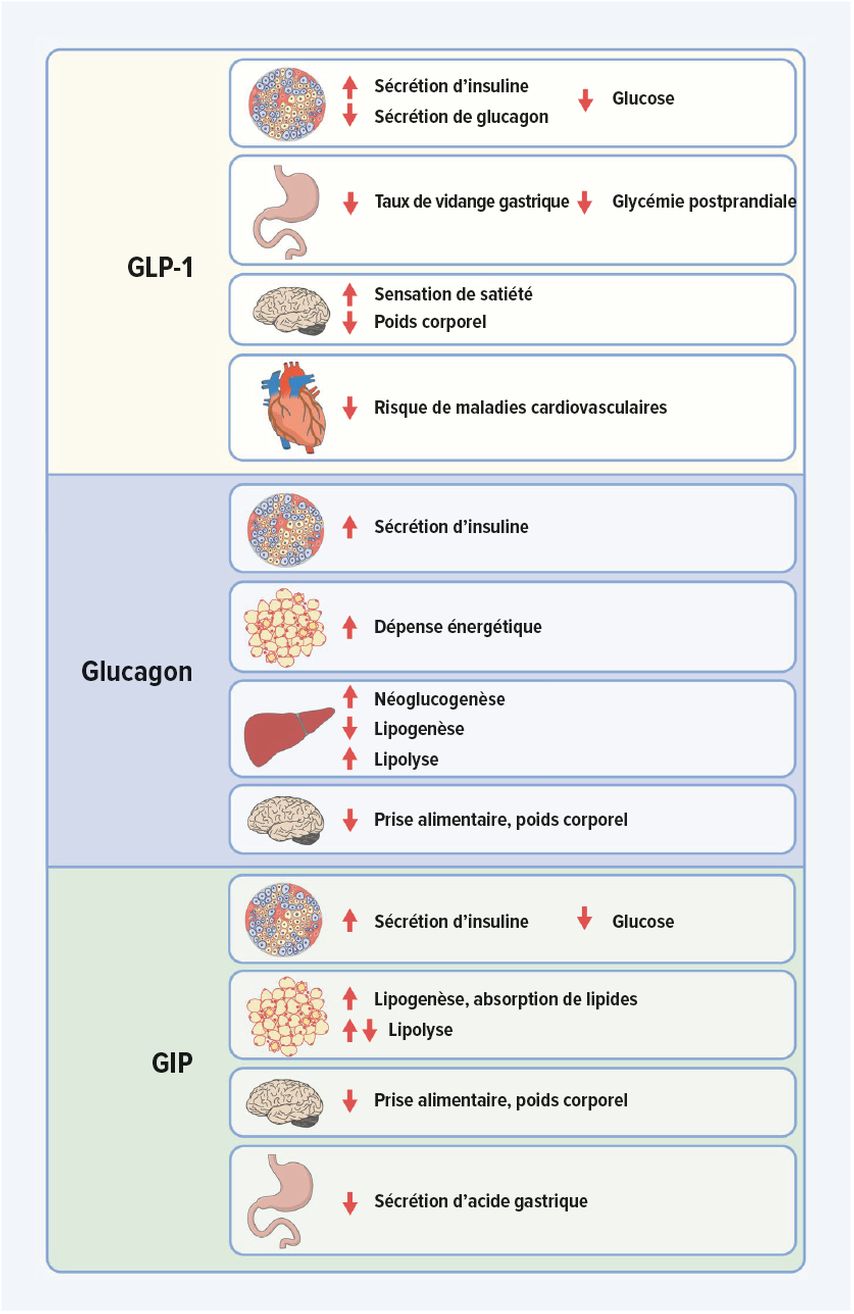
Établis depuis plusieurs années déjà, les analogues du GLP-1 du groupe des incrétines constituent l’un des principaux piliers du traitement moderne du diabète. Outre l’effet hypoglycémiant, la perte de poids significative ainsi que les effets positifs sur la stéatose hépatique et une réduction des événements cardiovasculaires sont particulièrement avantageux (Fig.1).
Fig. 1: Les principaux mécanismes d’action cliniques du GLP-1, du glucagon et du GIP. Ceux-ci constituent la base principale de l’action des agonistes des récepteurs du GLP-1 ainsi que des doubles et des triples agonistes des récepteurs dans le traitement du diabète de type 2 tout comme de l’obésité (modifié d’après Tschöp M et al., 2023)1 (Creative Commons Licence 4.0)
L’étude SELECT, présentée dans le cadre du congrès de l’American Heart Association (AHA) et publiée en parallèle, démontre de manière convaincante la réduction des critères d’évaluation cardiovasculaires par le sémaglutide (2,4mg/semaine SC) dans un groupe de patients souffrant d’obésité non diabétiques, ce qui constitue une nouveauté dans le traitement de l’obésité.
La plupart des incrétines sont administrées par voie sous-cutanée, seul le sémaglutide existe aussi sous forme orale. L’étude porte actuellement sur l’orforglipron, un agoniste non peptidique des récepteurs du GLP-1, également administré par voie orale. Dans une récente étude de phase II sur le traitement de l’obésité, l’orforglipron a entraîné une perte de poids de 15,4kg en 36 semaines. Les résultats des études de phase III encore en cours sont donc attendus avec impatience.
Agonistes des récepteurs du GIP/GLP-1
L’activation médicamenteuse d’autres récepteurs aux incrétines semble avoir un effet positif sur le diabète et l’obésité (Fig.1). Comparé aux analogues du GLP-1 uniquement, le double agoniste des récepteurs du GIP/GLP-1 tirzépatide s’avère significativement plus efficace pour réduire la glycémie et le poids. Le GIP ou «glucose-dependent insulinotropic polypeptide» était auparavant connu sous le nom de «gastric inhibitory peptide». Outre les effets connus des incrétines, l’action agoniste supplémentaire sur le GIP présente entre autres des effets positifs sur le tissu adipeux.
Le tirzépatide est autorisé dans l’UE et en Suisse pour le traitement du diabète de type 2. Dans le cadre du programme d’étude SURPASS mené sur les patients diabétiques, le tirzépatide a été étudié aux doses de 5mg, 10mg et 15mg une fois par semaine. Après 72 semaines, il a permis de réduire le poids corporel jusqu’à 20,9%. Les effets secondaires les plus significatifs sur le plan clinique sont les nausées et la diarrhée, qui surviennent à une fréquence similaire à celle des analogues du GLP-1. Les résultats de l’étude sur les critères d’évaluation cardiovasculaires SURPASS-CVOT seront publiés à l’automne 2024.
Agonistes des récepteurs du glucagon et du GLP-1
Une action agoniste médicamenteuse sur le récepteur du glucagon devrait également avoir des effets très positifs chez les patients diabétiques (Fig.1). L’activation du récepteur du glucagon semble à première vue contre-productive, car le glucagon est connu pour être une puissante hormone antagoniste de l’insuline. Il a des effets cataboliques très puissants, stimule la lipolyse dans les adipocytes, réduit la prise alimentaire et ralentit la vidange gastrique. Une action agoniste sur les récepteurs du glucagon devrait également entraîner une augmentation des besoins énergétiques, contrairement aux autres incrétines mentionnées. Ainsi, plusieurs agonistes des récepteurs du glucagon/GLP-1 (survodutide, cotadutide, éfinopegdutide) ont déjà été testés dans le cadre d’études cliniques, le survodutide ayant entraîné une perte de poids de 13,8% en 16 semaines chez des patients souffrant d’obésité.
Triples agonistes
Le rétatrutide a une action agoniste sur les 3 récepteurs mentionnés, il s’agit donc d’un triple agoniste des récepteurs GIP/GLP-1/glucagon («Triple-G»). Il a entraîné une perte de poids de 24% en 48 semaines chez des patients souffrant d’obésité ou de surpoids dans le cadre d’une étude de phase II. Comme pour les agonistes des récepteurs du GLP-1, les effets secondaires les plus importants ont été les nausées et les vomissements, qui sont survenus chez 45 à 60% des participants à l’étude. Les données relatives au rétatrutide peuvent sans doute être considérées comme très optimistes, mais il faut bien entendu attendre les résultats des études de phase III. Dans un sous-groupe de 98 patients atteints de maladie hépatique stéatosique associée à un dysfonctionnement métabolique (MASLD), le rétatrutide a montré une normalisation de la teneur en graisse du foie chez 90% des patients. D’une manière générale, des études cliniques portant sur diverses préparations à base d’incrétines sont attendues dans le cadre de la MASLD, de sorte que, outre le diabète de type 2 et l’obésité, la stéatosique hépatique pourrait éventuellement constituer une indication supplémentaire à l’utilisation d’analogues des incrétines.
Analogues de l’amyline/agonistes des récepteurs du GPL-1
Connu depuis longtemps, le concept des analogues de l’amyline est également en cours d’étude en association avec le sémaglutide. L’amyline est une hormone peptidique neuroendocrine qui est sécrétée par les cellules bêta pancréatiques en même temps que l’insuline. L’appétit est réduit par des effets centraux directs au niveau du «centre de vomissement» et du noyau arqué. Aux États-Unis, le pramlintide est autorisé pour le traitement du diabète de type 1 et 2 en tant que traitement adjuvant à l’insulinothérapie. Le cagrilintide, un nouvel analogue de l’amyline à longue durée d’action avec une demi-vie prolongée (environ 180h), est en cours d’évaluation clinique en association avec le sémaglutide (CagriSema). Chez 92 patients atteints de diabète de type 2 et ayant un IMC >27kg/m2, l’HbA1c a baissé de 2,2% sous CagriSema. La réduction de l’HbA1c a été similaire à celle observée avec le sémaglutide à forte dose en monothérapie (–1,8%), mais CagriSema a entraîné une perte de poids nettement plus importante (–15,6%) par rapport au sémaglutide en monothérapie. CagriSema a toutefois également provoqué une augmentation significative des effets secondaires gastro-intestinaux, même s’ils étaient légers.
Conclusion
Dans l’état actuel des choses, il semblerait que le tirzépatide annonce en effet seulement le début de toute une série de médicaments révolutionnaires contre le diabète. Associée à une perte de poids significative, la rémission du diabète et de la stéatose hépatique est à portée de main.
Source:
59th EASD Annual Meeting, du 2 au 6 octobre 2023, Hamburg
Littérature:
1 Tschöp M et al.: Gut hormone-based pharmacology: novel formulations and future possibilities for metabolic disease therapy. Diabetologia 2023; 66: 1796-808
Littérature supplémentaire auprès des auteurs