Dépistage du cancer du poumon – évolutions actuelles en Suisse et approche possible de mise en place
Auteurs:
Lisa Jungblut
Prof. Dr méd. Thomas Frauenfelder
Radiologisches Institut
Universitätsspital Zürich
E-mail:
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Le cancer du poumon est souvent découvert seulement à un stade avancé. La mortalité est en conséquence élevée. Grâce à un programme de dépistage ciblé sur la population à haut risque, les carcinomes du poumon peuvent être diagnostiqués de manière avérée à des stades nettement plus précoces, ce qui a pour conséquence une augmentation considérable du taux de survie à 5 ans.
Keypoints
-
Plus de 4000 nouveaux cas de cancer du poumon sont diagnostiqués chaque année en Suisse. Avec plus de 3000 décès par an, le cancer du poumon est devenu la principale cause de mortalité due au cancer en Suisse.
-
En 2011, le dépistage par TDM a permis de réduire de 20% la mortalité due au cancer du poumon et de 6,7% la mortalité globale totale dans le cadre de la première étude randomisée de grande envergure (étude américaine «National Lung Screening Trial NLST») dans un collectif de patients à haut risque clairement défini composé de fumeurs et d’anciens fumeurs (au moins 30 paquets-années) asymptomatiques âgés de 55 à 74 ans.
-
Un dépistage pulmonaire en Suisse, un pays européen à hauts revenus où la prévalence de fumeurs est élevée, pourrait présenter d’autres avantages que l’économicité; on dispose déjà de résultats provisoires d’une étude pilote suisse prometteuse. Une évaluation des technologies de la santé comprenant des procédures et des recommandations a déjà été publiée et a donné lieu à des entretiens avec la commission de dépistage précoce du cancer.
Le cancer du poumon est responsable, chaque année, de 1,6 à 1,8 million de décès à l’échelle mondiale1 et de près de 3200 décès en Suisse.2 Plus de 20% des décès dus à un cancer en Suisse sont attribuables à un cancer du poumon.2 En raison de l’absence de symptômes pendant une longue période, la progression du cancer du poumon passe en règle générale inaperçue jusqu’aux stades avancés de la maladie, ce qui peut compromettre considérablement les possibilités de traitement et le succès thérapeutique. Le taux de survie à 5 ans chez les patients présentant un cancer à un stade avancé est d’environ 5%, alors que le taux de survie à 5 ans aux stades précoces peut atteindre jusqu’à 50%.3 De plus en plus d’études confirment les données probantes en termes de diminution du taux de mortalité du cancer du poumon au moyen d’un dépistage par tomodensitométrie à faible dose (LDCT).4,5 Le dépistage précoce du cancer du poumon dans une population à haut risque a donc le potentiel de permettre la détection et le traitement du cancer à des stades plus précoces et d’induire une diminution de la mortalité due au cancer.
Études actuelles: dépistage et premières tentatives de mise en place en Europe
La publication des résultats de l’étude américaine «National Lung Screening Trial» réalisée en 2011 a permis de réduire de 20% la mortalité due au cancer du poumon et de 6,7% la mortalité globale (réduction relative du risque) dans un collectif de patients à haut risque clairement défini, composé de fumeurs et d’anciens fumeurs (au moins 30 paquets-années) asymptomatiques et âgés de 55 à 74 ans.4 En chiffres absolus: dans le groupe LDCT, 13 des 1000 fumeurs dépistés sont décédés du cancer du poumon contre 17 sur 1000 dans le groupe radiographie du thorax. En raison de ces données prometteuses, les coûts engendrés par le programme de dépistage sont remboursés depuis 2015 en Amérique, aussi bien par les caisses maladie privées que publiques.
Des résultats similaires ont pu être obtenus dans le cadre de l’étude NELSON, qui est à ce jour avec >13000 hommes et >2500 femmes, la plus vaste étude réalisée en Europe portant sur le dépistage du cancer du poumon (LCS, «lung cancer screening»). Dans cette étude également, la mortalité due au cancer du poumon était nettement plus faible chez ceux qui ont subi un dépistage par TDM volumétrique que chez ceux qui n’ont pas subi de dépistage. Les carcinomes du poumon découverts lors du dépistage ont été en outre diagnostiqués beaucoup plus fréquemment au stade IA ou IB. En revanche, dans le groupe non dépisté, presque la moitié des carcinomes ont été diagnostiqués au stade IV, alors que dans le groupe dépisté, seuls 9,4% des patients ont été diagnostiqués au stade IV.6
Afin d’éviter une stigmatisation, un programme de dépistage se basant sur un concept de «bilan de santé pulmonaire» comprenant une approche holistique a été conçu dans le cadre de l’étude pilote réalisée à Manchester. L’accès à ces services a pu être élargi en ayant recours à des scanners mobiles et les obstacles à une participation ont pu être minimisés.7
L’étude allemande «Lung Cancer ScreeningIntervention (LUSI)» portant sur le dépistage du cancer du poumon est une étude randomisée incluant 4052 fumeurs de longue date âgés de 50 à 69 ans qui ont été recrutés dans la population générale. Les données sur l’incidence du cancer du poumon, sur sa mortalité et sur le statut vital, ont été recueillies auprès d’hôpitaux, de médecins exerçant en cabinet, de registres du cancer, de registres de population et d’offices de la santé. Pendant une phase d’observation moyenne de 8,8 ans après la randomisation, une diminution statistiquement significative de la mortalité due au cancer du poumon a été mise en évidence chez les femmes, mais pas chez les hommes.8
En janvier 2020, la Croatie a été le premier pays européen à lancer un programme national de dépistage du cancer du poumon qui s’adressait à tous les fumeurs actifs (ou à ceux qui avaient arrêté de fumer lors des 15 dernières années) et âgés de 50 à 70 ans. Au total, onze établissements de santé dans toute la Croatie proposent ce dépistage. La Pologne a également mis en place un programme de dépistage précoce du cancer du poumon, dans le cadre d’un programme national contre le cancer, financé par le ministère de la santé.9 Les expériences et les rapports issus de ces pays qui sont actuellement chargés de l’extension de ces établissements plaident clairement en faveur de la mise en place d’un dépistage du cancer du poumon.10 Le Royaume-Uni a aussi déjà présenté des programmes régionaux et une très grande observance a pu être obtenue au moyen d’un camion de dépistage mobile, en particulier dans les régions excentrées.11 Field et al. ont publié les résultats d’un panel d’experts concernant la mise en place de dépistages du cancer du poumon en Europe, document dans lequel les auteurs ont recommandé aux instances nationales de politiques de santé de commencer les dépistages par LDCT dès que l’on disposera de preuves de leur efficacité.12
Parcours de dépistage
Un entretien de conseil approfondi avec un (ancien) fumeur doit avoir lieu avant de l’envoyer effectuer un dépistage par LDCT. Dans un premier temps, il s’agit de déterminer si le patient remplit les critères d’inclusion (âge compris entre 55 et 74 ans, au moins 30 paquets-années et fumeur actuel ou abstinent depuis moins de 15 ans). En effet, un bénéfice en termes de survie a pu être mis en évidence uniquement dans cette population à risque. Dans un deuxième temps, le patient doit être informé du risque de résultats faussement négatifs et de la découverte fortuite potentielle d’autres maladies. En outre, le patient doit être informé des procédures, notamment en cas de diagnostic potentiel d’un cancer. Les patients chez lesquels le dépistage révèle des indices faisant suspecter la présence d’une maladie cancéreuse devront subir des examens plus approfondis, une intervention chirurgicale, une radiothérapie et/ou un traitement médicamenteux qui peuvent entraîner un stress important selon l’état physique et psychique du patient.
Le compte-rendu radiologique doit comporter une section sur les paramètres de l’imagerie, tels que la dose et le protocole utilisé, mais aussi la description des observations et des recommandations thérapeutiques spécifiques. Des documents types standardisés sont privilégiés afin de garantir que les résultats soient rapportés de manière uniforme et que les directives soient respectées. Des systèmes de reconnaissance assistés par ordinateur et basés sur des procédés d’intelligence artificielle doivent être utilisés afin de réduire la variabilité des mesures effectuées. Chaque nodule est catégorisé selon des systèmes de classification établis, tels que LungRADS ou NELSON;6,13 en outre, des recommandations thérapeutiques et/ou les intervalles entre les examens de contrôle seront déterminés en conséquence. Les patients qui présentent des résultats nécessitant un traitement peuvent être soit informés des résultats par leur médecin assignant, soit être mis directement en contact avec le service de consultation du département interne de chirurgie thoracique.
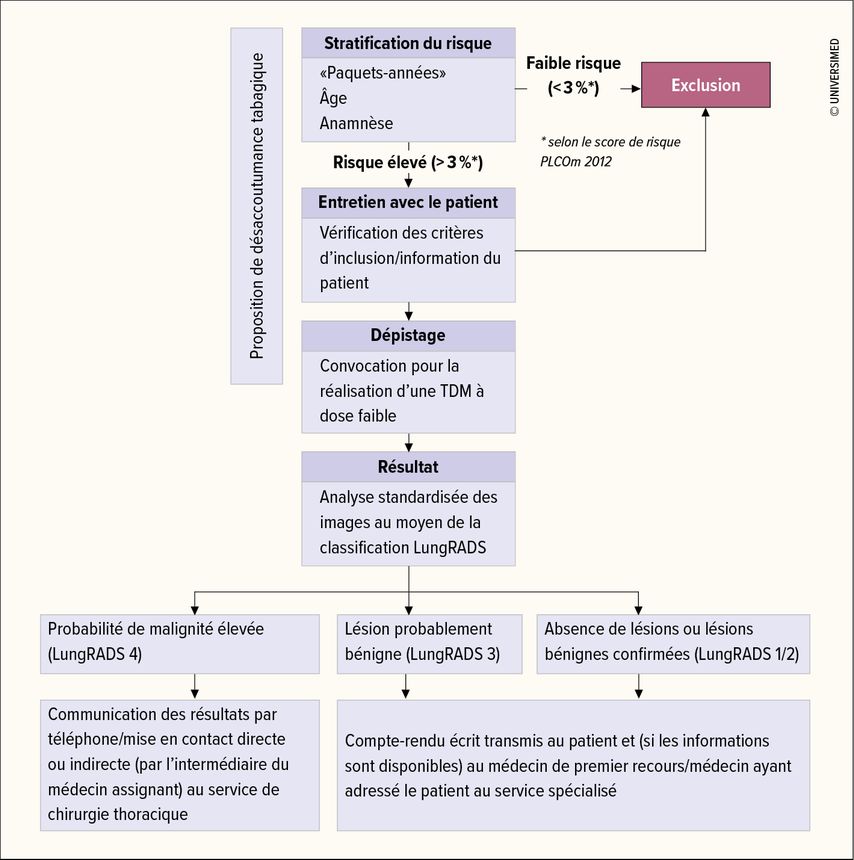
La littérature fournit des données controversées concernant l’intervalle entre les dépistages en cas de résultats négatifs; alors qu’un suivi annuel était effectué dans les études de grande envergure réalisées jusqu’ici, l’étude MILD a prouvé pour la première fois qu’une LDCT tous les deux ans permet d’obtenir une diminution comparable de la mortalité chez les personnes présentant un examen initial négatif.14 À l’avenir, les scores qui se basent sur l’évaluation individuelle du risque pourraient encore plus stratifier le suivi du dépistage.5 La Figure 1 en donne un aperçu.
Dépistage du cancer du poumon en Suisse
Le bénéfice en termes de mortalité obtenu grâce au dépistage précoce d’un cancer du poumon à l’aide de la LDCT n’a pas seulement rencontré un grand écho auprès des spécialistes, mais il a aussi été relayé par les médias non spécialisés et sur Internet. Deux sociétés médicales prestigieuses, la société européenne de pneumologie (ERS) et la société européenne de radiologie (ESR), ont conçu en commun un livre blanc en se basant sur les données probantes actuelles. Elles recommandent un dépistage complet du cancer du poumon basé sur des critères de qualité définis dans le cadre d’études longitudinales ou dans la pratique de routine clinique dans des centres multidisciplinaires certifiés.15 Un programme de dépistage ne peut toutefois être couronné de succès que s’il est accessible à autant de personnes éligibles que possible. Une limitation du nombre d’établissements proposant ce dépistage peut être utile afin d’en garantir la qualité, mais elle augmente néanmoins la distance jusqu’au centre de dépistage le plus proche. Ceci peut à son tour avoir un impact négatif sur le taux de participation. Plusieurs groupes d’intérêt se sont prononcés en faveur d’un dépistage mobile. La densité des scanners de TDM à disposition en Suisse étant toutefois estimée comme étant élevée, le degré de centralisation pourrait varier selon l’envergure du pré-dépistage, du dépistage et de l’évaluation. Une approche possible consiste à décentraliser la réalisation des examens diagnostiques et à centraliser la lecture des résultats et le traitement. Les «bilans de santé pulmonaire» réalisés à Manchester mentionnés plus haut, qui sont effectués avec un scanner mobile, sont exemplaires à cet égard. L’approche holistique du bilan pulmonaire, afin d’éviter la stigmatisation, serait également un concept possible de mise en place en Suisse. Un organisme indépendant d’évaluation de la qualité (p.ex. composé d’experts internationaux en radiologie, en pneumologie et en épidémiologie) contrôlerait toutes les étapes du dépistage, en particulier le dépistage par tomodensitométrie et son évaluation.
Des incertitudes concernant le financement subsistent encore aujourd’hui. À l’heure actuelle, les caisses-maladie obligatoires ne remboursent pas les frais de dépistage. Les sources de financement potentielles sont l’Office fédéral de la santé publique (OFSP), les régions (cantons), les associations actives dans le domaine de la santé, Promotion Santé Suisse et le Fonds de prévention du tabagisme. En outre, le prélèvement d’impôts sur les produits du tabac, pour aider à la création d’un fonds pour le dépistage, pourrait être examiné afin de couvrir les coûts d’un futur programme de dépistage. Tomonaga et al.16 ont déjà attiré l’attention sur le fait que le dépistage pulmonaire en Suisse, un pays européen à hauts revenus où la prévalence de fumeurs est élevée, pourrait être économique. Ils ont évalué l’économicité du dépistage du cancer du poumon par LDCT à moins de 50000 euros par année de vie gagnée.
Pour garantir la durabilité du dépistage pulmonaire, il serait important que le dépistage soit à long terme pris en charge par l’assurance obligatoire des soins (LAMal). Selon l’art. 12d de l’OPAS, l’assurance obligatoire des soins couvre certaines mesures de prévention en vue du dépistage précoce de maladies chez certains groupes à risque. La liste des mesures énumérées à l’article 12d de l’OPAS est toutefois exhaustive, à savoir que seules les mesures mentionnées sont prises en charge par l’assurance obligatoire des soins. Chaque nouvelle mesure de dépistage précoce doit être examinée par l’assurance obligatoire des soins en termes d’efficacité, d’adéquation et d’économicité avant d’être acceptée. Cette évaluation est effectuée par la Commission fédérale des prestations générales et des principes (CFPP) après la remise d’une demande auprès de l’OFSP. Cette demande doit se baser sur des recommandations concrètes d’action. Les sociétés médicales impliquées y œuvrent en coopération avec les organisations de patients Ligue pulmonaire suisse et Ligue contre le cancer suisse. Une ETS (évaluation des technologies de la santé) comprenant des procédures et des recommandations a été récemment publiée et a donné lieu à des entretiens avec la Commission de dépistage précoce du cancer. Quelques rares points, tels que le pronostic en termes de survie globale, ne sont pas encore élucidés.
L’indication médicale d’un dépistage par LDCT doit dans tous les cas être posée par un médecin afin d’être acceptée par l’assurance obligatoire des soins. Il faut tenir compte des inconvénients, tels que les résultats faussement positifs associés aux coûts subséquents qui en résultent, mais aussi du stress psychique du patient; éléments qui doivent être pris en considération lors du processus de décision aboutissant à une recommandation potentielle de dépistage. Les résultats provisoires d’une étude pilote interne incluant des patients à haut risque (se basant sur les critères NELSON ou calculé selon un score de risque PLCOm2012 >3%) sont prometteurs. Cette étude a suscité un grand intérêt au sein de la population générale et un cancer du poumon a été diagnostiqué chez près de 5% des participants. Tous les carcinomes pulmonaires détectés ont pu être pris en charge dans le cadre d’une approche curative.
Illustration du dépistage se basant sur un exemple de patient
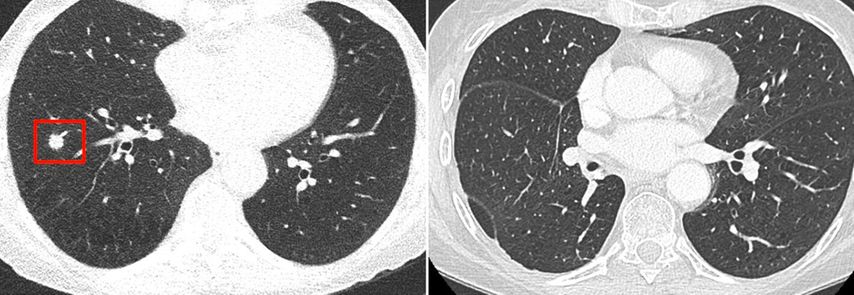
Madame X, une patiente alerte, âgée de 59 ans, a vu par hasard au cabinet de son médecin de premier recours un dépliant sur le dépistage pulmonaire. Mis à part un toussotement matinal, elle ne présente aucun symptôme pulmonaire. L’interrogation de la patiente révèle l’absence de symptômes B. Au cours d’un entretien bref avec Madame X, son médecin de premier recours lui expose le pour et le contre d’un dépistage et la patiente manifestant toujours son intérêt, il l’inscrit par courrier électronique à un dépistage. Une semaine plus tard, un médecin du centre de dépistage vérifie les critères d’inclusion dans le cadre d’un entretien téléphonique. Toutes les informations importantes sur les procédures à venir sont également fournies à la patiente lors de cet entretien. Une semaine plus tard, Madame X reçoit par courrier postal une convocation pour la réalisation d’une tomodensitométrie, une brochure sur la désaccoutumance tabagique et un formulaire de consentement. La LDCT est effectuée deux semaines plus tard. Dans le cas de Madame X, la dose correspond à un indice de dose tomodensitométrique (CTDI) de 0,4mGy (soit l’équivalent d’une exposition aux rayonnements correspondant à environ 4 vols transatlantiques ou d’une radiographie du thorax en deux plans). Un nodule de 11mm de catégorie 4b selon les critères du système de classification LungRADS (lésion suspecte, probabilité de la présence d’une tumeur de 5 à 15%) est détecté dans le poumon droit. Des métastases à distance ou des ganglions lymphatiques suspectés d’être métastatiques ne sont pas décelés. Le compte-rendu est vérifié par un radiologue sous-spécialisé en imagerie thoracique et la patiente est informée par téléphone le jour même de l’examen. Une biopsie transbronchique confirme la suspicion d’adénocarcinome pulmonaire primitif. Trois jours plus tard, une procédure chirurgicale est discutée avec la patiente lors de la consultation dans le service de chirurgie thoracique. Environ trois mois après la TDM initiale, Madame X subit une lobectomie. Après 4 cycles de chimiothérapie adjuvante à base de cisplatine/pémétrexed, le traitement a pu être achevé six mois plus tard. L’examen de contrôle réalisé un an plus tard révèle l’absence persistante de tumeurs. La Figure 2 présente La TDM de dépistage initiale et la dernière TDM de contrôle.
Fig. 2: À gauche: Nodule (entouré en rouge) de Madame X sur l’imagerie initiale. À droite: Examen de contrôle un an plus tard, une lobectomie ayant été entretemps effectuée et une chimiothérapie adjuvante ayant été administrée. Des modifications cicatricielles sont visibles sans indice de résidu tumoral ou de récidive
Fig. 3: Grâce à un programme de dépistage ciblé sur la population à haut risque, les carcinomes du poumon peuvent être diagnostiqués à des stades plus précoces. La mortalité peut être réduite de manière significative grâce aux meilleures possibilités de traitement à ces stades
Littérature:
1 Ferlay J et al.: Int J Cancer 2015; 136: E359-86 2 Office SFS: Specific causes of death in 2016 [ https://www.bfs.admin.ch/bfs/en/home/statistics/health/state-health/mortality-causes-death/specific.html ] 3 National Cancer Institute: Cancer stat facts: lung and bronchus cancer [ https://seer.cancer.gov/statfacts/html/lungb.html ] 4 National Lung Screening Trial Research Team; Aberle DR et al.: N Engl J Med 2011; 365: 395-409 5 Oudkerk M et al.: Nat Rev Clin Oncol 2021; 18: 135-51 6 de Koning HJ et al.: N Engl J Med 2020; 382: 503-13 7 Crosbie PA et al.: Thorax 2019; 74: 405-9 8 Becker N et al.: Int J Cancer 2020; 146: 1503-13 9 Rzyman WS et al.: Transl Lung Cancer Res 2019; 8(Suppl 1): S95-105 10 Breathing in a new era. A comparative analysis of lung cancer policies across Europe. The Economist Intelligence Unit Healthcare 2020 [ https://pages.eiu.com/rs/753-RIQ-438/images/EIU%20MSD%20lung%20cancer%20in%20Europe%20final%202020%206%2029.pdf ] 11 Field JK et al.: Health Technol Assess 2016; 20: 1-146 12 Field JK et al.: ESMO Open 2019; 4: e000577 13 Chelala L et al.: AJR Am J Roentgenol 2021; 216: 1411-22 14 Pastorino U et al.: Eur J Cancer 2019; 118: 142-8 15 Kauczor HU et al.: Eur Respir J 2015; 46: 28-39 16 Tomonaga Y et al.: Lung Cancer 2018; 121: 61-9
Das könnte Sie auch interessieren:
Revue de presse: L’importance d’objectifs thérapeutiques centrés sur les patient·es dans la SLA
Dans une revue récente, Chio et al., mettent en lumière la nécessité de repenser les critères d’évaluation dans les essais cliniques portant sur la sclérose latérale amyotrophique (SLA ...
L’asthme et le rythme circadien
Le rythme circadien ne joue pas seulement un rôle important dans le sommeil, il a également une influence considérable sur les crises d’asthme et la fonction pulmonaire. Le ciblage ...
Les défis du diabète de type 1
Dans le cas du diabète de type 1, surtout s’il ne se déclare qu’à l’âge adulte, la pose du diagnostic peut déjà constituer un défi. Le risque d’hypoglycémie, qu’il faut minimiser, et le ...