Coronaropathie: Nouvelles technologies dans le traitement interventionnel
Auteurs:
Dr méd. Peter Dietrich
Oberarzt m.e.V. Kardiologie
PD Dr méd. Gregor Fahrni
Leitender Arzt Kardiologie, Leiter Koronarinterventionen
Klinik für Kardiologie
Stadtspital Zürich Triemli
E-mail: gregor.fahrni@stadtspital.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Depuis la première dilatation par ballonnet pour le traitement de la coronaropathie en 1977, de nombreux autres jalons ont été posés. Le développement des endoprothèses à élution médicamenteuse, les progrès de la technologie par fils et des microcathéters ainsi que la possibilité d’athérectomie ont considérablement amélioré le taux de revascularisation interventionnelle et les résultats à long terme. Nous décrivons dans cet article quelques technologies récentes qui, en raison de leur grande utilité, ont rapidement fait leur entrée dans le traitement des coronaropathies et sont devenues incontournables dans le quotidien de la cardiologie interventionnelle.
Physiologie coronaire: pertinence hémodynamique d’une sténose coronaire et angor microvasculaire
FFR, iFR, RFR
L’évaluation angiographique de la pertinence hémodynamique d’une sténose coronaire intermédiaire n’est pas fiable,1 car, en plus de la gravité de la sténose, la zone à perfuser joue un rôle.
La détermination invasive de la fraction de flux de réserve («fractional flow reserve», FFR) pour évaluer la pertinence hémodynamique d’une sténose coronaire intermédiaire est largement répandue depuis longtemps en raison de son utilité clinique bien établie.2 Pour ce faire, on introduit un fil coronaire muni d’un capteur de pression intégré à l’extrémité du fil dans la périphérie du vaisseau en passant par la sténose et on mesure la chute de pression au niveau de la sténose sous flux coronaire maximal. L’administration par voie intraveineuse d’adénosine permet d’atteindre le flux coronaire maximal par une vasodilatation de la microcirculation. En présence d’une chute de pression au niveau de la sténose de >20% (FFR ≤0,80), une revascularisation est indiquée en raison de l’atténuation des symptômes qu’elle permet et de la réduction du risque d’intervention coronarienne non planifiée.
L’administration d’adénosine provoque toutefois une sensation désagréable d’oppression thoracique et de dyspnée. Étant donné qu’une hyperémie maximale est physiologiquement présente pendant la phase diastolique du cycle cardiaque, la chute de pression au niveau de la sténose coronaire pendant la diastole est corrélée de manière fiable à la FFR, même sans administration d’adénosine. Deux grandes études cliniques randomisées ont pu confirmer, au moyen d’indices «instantaneous wave-free ratio» (iFR) ou un «resting full-cycle ratio» (RFR) ≤0,89, le bénéfice d’une revascularisation en ce qui concerne les critères cliniques (décès, infarctus du myocarde et revascularisation non planifiée); ce bénéfice n’est pas inférieur à la revascularisation guidée par la FFR.3,4 L’expérience clinique montre que la détermination de la valeur diastolique au repos est moins constante que la mesure de la FFR, raison pour laquelle nous effectuons une mesure supplémentaire de la FFR (en hyperémie) avec le même fil de capteur de pression chez une partie des patient·es, notamment en présence d’un trouble du rythme cardiaque ou de résultats de mesure limites.
CFR et IMR
Malgré l’exclusion d’une sténose coronarienne épicardique hémodynamiquement significative, les patient·es peuvent présenter une angine de poitrine typique. L’angine dite microvasculaire a pour origine un dysfonctionnement endothélial. La microcirculation perd sa capacité de vasodilatation ou d’augmentation du flux malgré une stimulation adéquate. Pour déterminer la fonction microvasculaire, le même fil de capteur de pression susmentionné dispose d’un capteur de température qui permet de mesurer la vitesse du flux dans le vaisseau coronaire à l’aide de la thermodilution. L’application répétée d’un bolus de sérum physiologique à température ambiante dans les vaisseaux coronaires permet de déterminer le temps de transition du bolus et donc la vitesse du flux. L’augmentation du temps de transition du bolus lors de l’administration d’adénosine est corrélée à la capacité d’augmenter le flux coronaire, appelée réserve de flux coronaire («coronary flow reserve», CFR), et reflète la fonction endothéliale. Un CFR normal est >2. L’indice de résistance microcirculatoire («index of microcirculatory resistance», IMR) est le quotient de la pression coronaire distale et du temps de transit en hyperémie et reflète la résistance de la microcirculation. Un IMR <25 est considéré comme une résistance microvasculaire normale.5
Ainsi, l’angine microvasculaire, considérée jusqu’à présent comme un diagnostic d’exclusion, peut être diagnostiquée directement au laboratoire de cathétérisme cardiaque et un traitement anti-ischémique efficace peut être initié.6 Inversement, nous évitons aux patient·es d’essayer un traitement non prometteur lorsque les valeurs mesurées de la microcirculation sont normales.
Cas pratique sur la physiologie coronaire
Une femme de 58 ans se plaint depuis quelques mois d’une sensation d’oppression thoracique à l’effort et d’une dyspnée. Elle présente un facteur de risque cardiovasculaire: des antécédents de tabagisme de longue date.
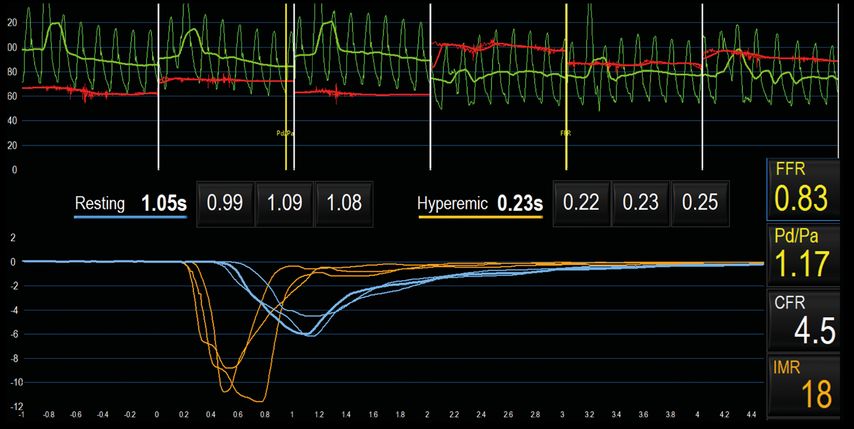
La tomodensitométrie des artères coronaires réalisée au préalable évoque une sclérose coronarienne diffuse avec une sténose intermédiaire focale dans l’artère interventriculaire antérieure (IVA). L’angiographie coronaire confirme la sténose susmentionnée et la pression de remplissage télédiastolique du ventricule gauche est de 13mmHg, ce qui est dans la norme. La mesure invasive de la pression en hyperémie permet d’exclure une pertinence hémodynamique de la sténose de l’IVA (FFR: 0,83) et donc un bénéfice d’une revascularisation dans cette zone.
La détermination simultanée de la fonction microvasculaire par thermodilution permet d’exclure largement, avec un IMR de 18 (et un CFR de 4,5), un trouble de la microcirculation et donc une cause cardiaque des troubles décrits (Fig.1).
Fig. 1: Détermination de la fraction de flux de réserve (FFR), du flux de réserve coronaire («coronary flow reserve», CFR) et de l’indice de résistance microcirculatoire (IMR) à l’aide de la pression coronaire distale (Pd), de la pression aortique (Pa) et du temps de transition (s) moyenné sur 3 injections au repos («resting» en bleu) et pendant l’hyperémie («hyperemic» en orange)
Imagerie intravasculaire: comprendre ce qui était invisible jusqu’à présent
L’angiographie coronaire peut nous donner rapidement une vue d’ensemble des artères coronaires et des sténoses éventuellement présentes. La radiographie plane n’est toutefois qu’une représentation simplifiée de la lumière coronaire tridimensionnelle et ne donne que peu d’informations sur la composition de la paroi vasculaire atteinte. L’imagerie intracoronaire – qu’il s’agisse de l’échographie intravasculaire (IVUS) ou de la tomographie par cohérence optique (OCT) – peut fournir des informations supplémentaires. La résolution spectaculaire de ces techniques, de l’ordre du micromètre, permet quasiment une «histologie in vivo». Ainsi, la structure d’une plaque peut être différenciée en lipomateuse, fibreuse ou calcifiée. Un thrombus intravasculaire peut également être facilement détecté, ce qui peut être utile dans la pratique clinique quotidienne dans le contexte d’un infarctus du myocarde, car la plaque activée ou la lésion responsable est ainsi clairement identifiée. Outre un diagnostic affiné, l’imagerie coronaire est également très précieuse en appui à une intervention: elle nous aide par exemple à choisir la stratégie d’intervention et les outils de prétraitement, principalement pour les sténoses calcifiées. Il est également possible de mesurer avec précision la longueur et le diamètre de l’endoprothèse à implanter et de définir des zones de réception saines. Enfin, après la pose d’une endoprothèse, il est possible d’examiner l’apposition de l’endoprothèse (l’appui de l’endoprothèse sur la paroi du vaisseau) ainsi que l’expansion de l’endoprothèse (dilatation adéquate de l’endoprothèse). Ces deux éléments sont des prédicteurs importants d’un bon résultat à court et à long terme. Une large méta-analyse récemment publiée a montré les bénéfices cliniques de l’intervention coronarienne assistée par imagerie intracoronaire.7
Toutes les interventions coronariennes ne nécessitent pas une imagerie supplémentaire. En cas de sténose à courte distance non compliquée ou de sténose dans de petits vaisseaux, les bénéfices potentiels ne l’emportent pas sur les coûts. Toutefois, en présence de facteurs de risque de défaillance de l’endoprothèse (diabète, interventions coronariennes complexes, bifurcations), l’imagerie intracoronaire est de plus en plus utilisée. En cas d’intervention majeure sur le tronc commun, le contrôle est renforcé par une imagerie intravasculaire conformément aux directives européennes actuelles en matière de cardiologie, avec une recommandation de classe IIa.2
Cas pratique sur l’imagerie intravasculaire
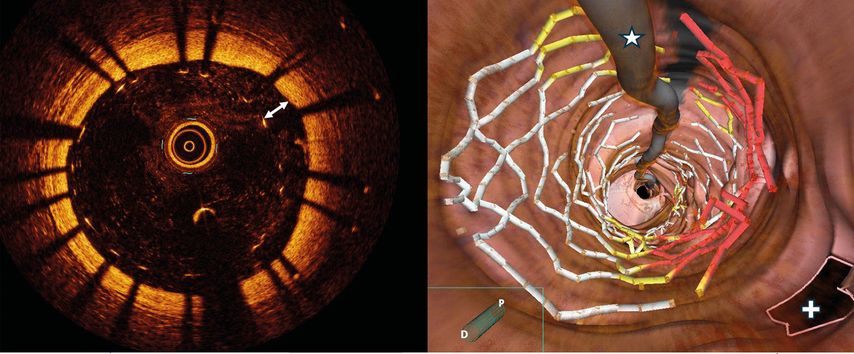
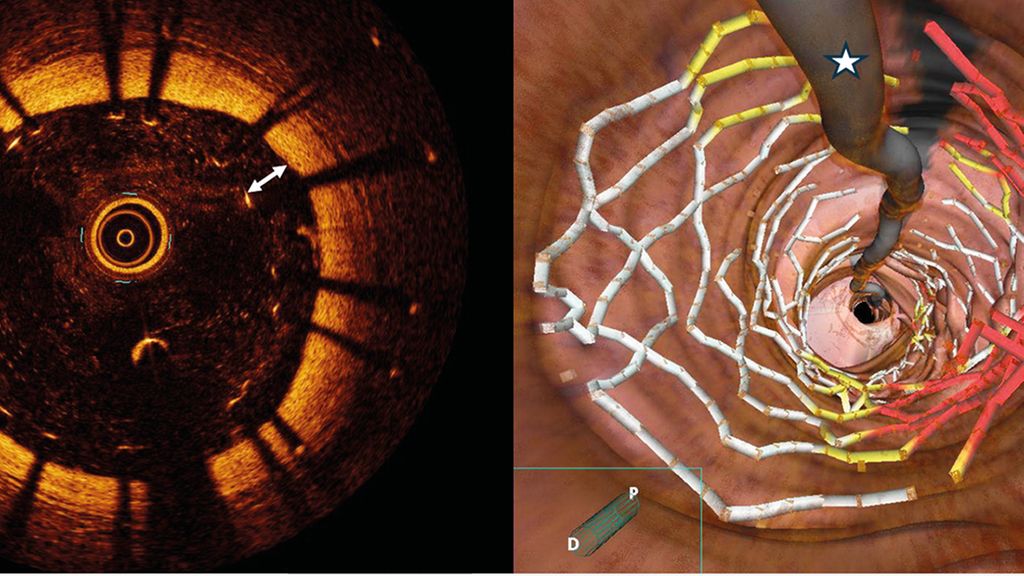
Un patient de 45 ans se présente avec un infarctus aigu du myocarde sans sus-décalage du segment ST et l’angiographie coronaire révèle une ectasie coronaire avec une occlusion subtotale de l’IVA proximale. Après la revascularisation avec implantation d’une endoprothèse, l’angiographie montre un bon résultat. L’OCT montre cependant une apposition d’endoprothèse inadéquate en raison de la dilatation ectasique des vaisseaux (Fig. 2). Après une nouvelle dilatation avec un ballonnet de taille supérieure, il est possible de corriger l’apposition de l’endoprothèse et d’améliorer ainsi le pronostic à court et à long terme.
Fig. 2: Tomographie par cohérence optique en coupe (à gauche) et reconstruction 3D simultanée (à droite) avec apposition de l’endoprothèse (à gauche: double flèche; à droite: coloré en rouge par le système) à l’extrémité proximale de l’endoprothèse. Étoile: fil coronal; croix: départ d’une branche latérale
Intervention coronarienne «leave nothing behind»
L’introduction des endoprothèses dans les années 1990 a constitué une étape importante dans le développement de l’intervention coronarienne percutanée et a entraîné une nette diminution des occlusions vasculaires aiguës et des resténoses. Même si chaque nouvelle itération de la technologie des endoprothèses a entraîné une nouvelle réduction des complications liées aux endoprothèses au cours de la première année après l’implantation, le taux de complications un an après l’implantation est resté constant à 1–2% par année, indépendamment de la génération d’endoprothèse.8 La réduction des complications à court terme fait que l’on s’intéresse de plus en plus au succès à long terme du traitement percutané. C’est pourquoi les technologies qui ne nécessitent pas l’implantation de métal – considéré comme centre lésionnel en cas de complications ultérieures aussi – gagnent de plus en plus d’attrait. Le ballonnet à élution médicamenteuse («drug-coated balloon», DCB) est une technologie de ce type. Si, après une prédilatation d’une sténose, on obtient un résultat satisfaisant sans dissection vasculaire importante ni recul élastique, il n’est pas forcément nécessaire d’implanter une endoprothèse. Dans ce cas, des médicaments antiprolifératifs peuvent être administrés au niveau de la paroi vasculaire à l’aide d’un DCB qui reste gonflé pendant 45 à 60 secondes sur la zone traitée, empêchant ainsi une cicatrisation excessive (hyperplasie) et donc une resténose. L’étude la plus vaste et la plus importante au monde dans ce domaine a été menée par Raban Jeger et al.9 L’étude BASKET-SMALL-2 a montré que le traitement des sténoses coronaires par un DCB dans un vaisseau de diamètre <3mm n’était pas inférieur à l’implantation d’une endoprothèse en termes de critères cliniques après trois ans. Dans diverses autres situations, les DCB présentent également des avantages par rapport au traitement par endoprothèse: p.ex., chez les patients présentant un risque élevé d’hémorragie ou devant subir une intervention chirurgicale à court terme, la double inhibition plaquettaire raccourcie à 4 semaines est très appréciée. En cas d’intervention par bifurcation, l’utilisation d’un DCB permet souvent de renoncer à la pose d’endoprothèse dans la branche latérale, évitant ainsi les couches superposées d’endoprothèses, qui ont tendance à se resténoser. Enfin, les DCB sont utiles dans le cas des resténoses intra-endoprothèse, permettant également d’éviter la superposition de plusieurs couches d’endoprothèses.
Pour éviter d’avoir à laisser un matériau étranger dans le corps («leave nothing behind»), des supports vasculaires qui se dissolvent d’eux-mêmes avec le temps ont été développés dans le passé. L’endoprothèse Absorb a été la première à avoir cette capacité et a été utilisée entre 2011 et 2017. Comme le support vasculaire ne se dégradait pas de manière uniforme et que les parties de l’endoprothèse situées dans le vaisseau entraînaient un taux de thrombose d’endoprothèse plus élevé, il a dû être retiré du marché. Actuellement, nous testons nous aussi, dans le cadre d’études strictement contrôlées, la dernière génération d’une telle endoprothèse biorésorbable, qui est désormais à base de magnésium. Les résultats obtenus jusqu’à présent sont encourageants, mais avant que cette technologie puisse être considérée comme l’avenir de l’intervention coronarienne, d’autres grandes études randomisées à long terme sont nécessaires, dans lesquelles l’avantage théorique se manifeste également sur des critères cliniques.
Cas pratique sur le traitement par ballonnet à élution médicamenteuse
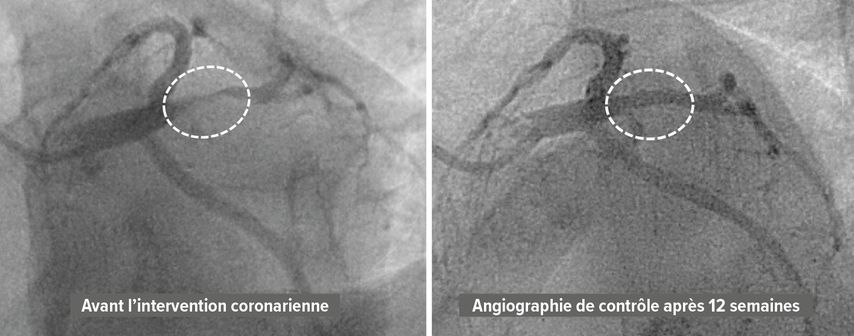
La coronarographie révèle une sténose de très haut grade dans la branche atriale intermédiaire chez un patient de 29 ans ayant des antécédents familiaux de maladie coronarienne précoce et une angine de poitrine typique (Fig. 3, à gauche). Chez ce patient jeune, le traitement est effectué à l’aide d’un ballonnet à élution médicamenteuse. L’angiographie de contrôle, réalisée en raison de symptômes atypiques, donne un bon résultat à 3 mois sans sténose résiduelle (Fig.3, à droite).
Fig. 3: Angiographie coronaire de référence montrant une sténose de branche intermédiaire de très haut grade avant traitement par ballonnet à élution médicamenteuse (à gauche) et angiographie de contrôle après 12 semaines sans sténose résiduelle (à droite)
Conclusion
Les techniques décrites témoignent des vastes progrès technologiques réalisés dans notre domaine au cours des dernières décennies. Nous disposons d’outils de plus en plus nombreux et de meilleure qualité. L’art de l’intervention coronarienne moderne consiste à développer une stratégie sur mesure en fonction des facteurs du patient et des caractéristiques de la lésion à traiter, afin d’obtenir un résultat optimal à long terme pour nos patient·es.
Littérature:
1 Toth G et al.: Eur Heart J 2014; 35: 2831-8 2 Knuuti J et al.: Eur Heart J 2020; 41: 407-7 3 Götberg M et al.: N Engl J Med 2017; 376: 1813-23 4 Davies JE et al.: N Engl J Med 2017; 376: 1824-34 5 Luo et al.: Circ Cardiovasc Interv 2014; 7: 43-8 6 Ford Th J et al.: J Am Coll Cardiol 2018; 72: 2841-55 7 Stone GW et al.: Lancet 2024; 403: 824-37 8 Madhavan MV et al.: J Am Coll Cardiol 2020; 75: 590-604 9 Jeger R et al.: Lancet 2020; 396: 1504-10