Les conjugués anticorps-médicament ont le vent en poupe
Auteure:
Noemi Reguart, MD, PhD
Department of Medical Oncology
Hospital Clínic de Barcelona, Spanien
E-mail: nreguart@clinic.cat
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Actuellement, de nombreux conjugués anticorps-médicament sont en cours d’évaluation dans le cancer du poumon. Qu’ils soient utilisés seuls ou en combinaison avec d’autres thérapies antitumorales, ces agents présentent un fort potentiel.
Données sur les tumeurs mutéesEGFR
Un grand nombre de conjugués anticorps-médicament (ADC) sont actuellement en développement clinique chez des patient·es atteint·es de cancer du poumon non à petites cellules (NSCLC). Certains ont déjà obtenu la «Breakthrough Therapy Designation» de la FDA aux États-Unis. L’Izalontamab Brengitecan (Iza-Bren), un ADC bispécifique ciblant EGFRxHER3, a montré un taux de réponse objective (ORR) de 47%, une médiane de survie sans progression (PFS) de 6,9 mois et une médiane de survie globale (OS) de 24,8 mois chez les patient·es prétraité·es atteint·es de NSCLC EGFR muté, en monothérapie.1 Dans le même contexte, l’étude OptiTROP-Lung03 a démontré l’efficacité du sacituzumab tiumotécan, un ADC ciblant TROP2: par rapport au docétaxel, une prolongation de la PFS (HR: 0,30; p<0,0001) et de l’OS (HR: 0,49; p=0,007) a été observée.2
Une amélioration supplémentaire peut être obtenue via les combinaisons. Dans l’étude LUMINOSITY, l’ajout du Télisotuzumab vedotin (Téliso-v), un ADC ciblant c-Met, à l’osimertinib a permis d’obtenir un ROR de 50% après progression sous osimertinib de première ligne.3 Actuellement, l’étude de phaseIII TROPION-Lung14 évalue la combinaison de première ligne osimertinib + datopotamab deruxtecan (Dato-DXd), un ADC ciblant TROP2. Il reste à déterminer comment les ADC s’intègrent idéalement dans le paysage thérapeutique du NSCLC EGFR-positif avancé. La question du séquençage optimal, de la sélection des patient·es, l’activité du SNC et du profil de sécurité sera déterminante.
Maladie non oncogène
Les ADC sont également évalués dans le NSCLC non oncogène-dépendant. Deux stratégies de sélection des patient·es sont possibles. Une approche non sélective sur les biomarqueurs en cas de forte expression (TROP2, EGFR, ITB-6, B7-H3); une approche sélective en cas d’expression modérée ou faible (CEACAM5, c-MET, HER2, HER3).
Les études EVOKE-01 et TROPION-Lung01 et ont donné des résultats décevants pour le Dato-DXd et le sacituzumab govitecan dans un setting non sélectionné: aucun bénéfice d’OS par rapport au docetaxel.4,5 La troisième étude de phaseIII négative est CARMEN LC03, qui n’a pas atteint ses critères d’évaluation coprimaires (PFS et OS).6 Ici, le tusamitamab ravtansine était comparé au docétaxel chez des patient·es avec forte expression de CEACAM5.
D’autre part, des études réussies reposant sur des approches sélectionnées selon des biomarqueurs ont constitué la base de l’approbation par la FDA du Téliso-v et du trastuzumab déruxthécan (T-DXd) pour les tumeurs surexprimant respectivement la protéine c-Met et HER2, dans un contexte de prétraitement, bien que les cohortes de patient·es aient été de petite taille.7,8 Dans LUMINOSITY, le Téliso-v a induit un ORR de 35% et une PFS médiane de 5,5 mois en cas de forte expression de c-MET.7 Dans l’étude DESTINY-Lung01, le groupe avec forte expression HER2 (IHC 3+) a obtenu un ORR de 53% sous T-DXd.8
Un exemple d’ADC à cible innovante est le Sigvotatug Vedotin (SV), dirigé contre l’intégrine bêta 6. Les données préliminaires font état d’un ORR de 32,5% et d’une PFS médiane de 6,4 mois chez des patient·es atteint·es de NSCLC non épidermoïde.9 L’étude de phaseIII Be6A Lung-01 évalue SV dans ce cadre en deuxième ligne. D’autres études de phaseIII de deuxième ligne incluent TeliMET NSCLC-01, évaluant Téliso-v chez des patient·es sélectionné·es surexprimant c-MET, et une étude sur Iza-Bren dans l’EGFR de type sauvage. Dans toutes ces études, le docétaxel est utilisé comme traitement de contrôle.
Intensification du traitement enpremière ligne
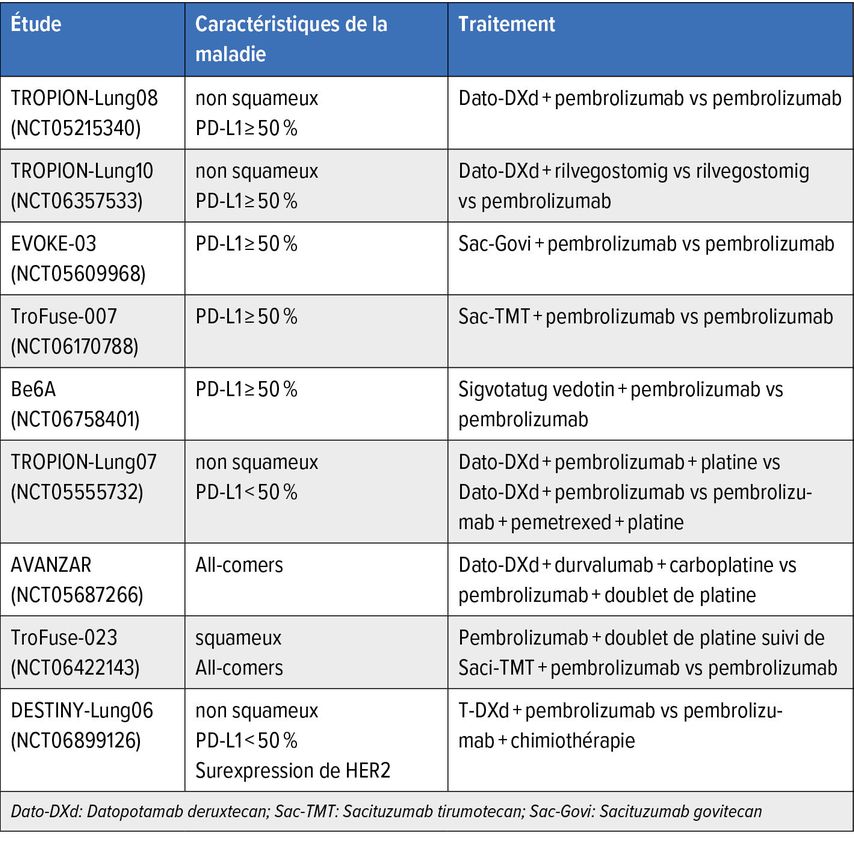
Plusieurs études de phaseI/II ont testé des combinaisons de première ligne associant ADC et chimiothérapie, immunothérapie ou les deux approches (TROPION-Lung02, TROPION-Lung04 avec Dato-DXd; EVOKE-02 avec Saci-Govitecan). Les doublets comme les triplets ont montré une activité antitumorale soutenue, mais également des taux substantiels d’effets indésirables.10 Actuellement, de nombreuses études de phaseIII évaluent des combinaisons d’ADC + inhibiteurs de points de contrôle immunitaire en première ligne dans le NSCLC métastatique avec une expression élevée de PD-L1 (≥50%), PD-L1<50% ou all-comers (Tab.1).
Tab.1: Études de phaseIII en cours sur les combinaisons d’ADC en première ligne dans le NSCLC métastatique sans altération du driver génomique
Des réponses dans le contexte de l’utilisation d’ADC en première ligne sont encore attendues concernant la durée optimale du traitement, la qualité de vie et la sécurité. Des études supplémentaires seront nécessaires pour affiner la sélection des patient·es susceptibles de bénéficier d’une intensification thérapeutique.
Résultats du setting périopératoire
La phase précoce de la maladie constitue un autre champ de recherche majeur. L’étude de plateforme de phaseII NEOCOAST-2 évalue l’administration périopératoire de durvalumab + chimiothérapie + agents innovants dans le NSCLC résécable. Dans le bras 4 (durvalumab + dato-DXd + chimiothérapie à base de platine), des taux encourageants de rémission pathologique complète (pCR) et de rémission pathologique majeure ont été observés: 35,2% et 63,0% respectivement.11 Même chez les patient·es PD-L1-négatif·ves, le taux de pCR était élevé. Les données indiquent également une clairance pertinente de l’ADNc dans le bras 4.
Des stratégies d’intensification basées sur l’ADC pourraient être utiles en phase précoce. Cependant, un équilibre adéquat entre efficacité et sécurité devra être maintenu. La question du recours aux doublets vs triplets et de la meilleure sélection des patient·es (PD-L1 all-comers vs PD-L1 négatifs) reste ouverte. Il en va de même pour l’utilisation adjuvante des ADC. Reste à déterminer s’il faut privilégier les monothérapies ou les combinaisons avec immunothérapie, et si la pCR, la maladie résiduelle minimale ou d’autres biomarqueurs doivent guider la sélection des patient·es.
Dans l’ensemble, de nombreux paramètres doivent être considérés pour définir la stratégie de traitement optimale basée sur les ADC. Il nous appartient également d’identifier les domaines d’application idéaux pour toutes les nombreuses combinaisons actuellement évaluées.
Littérature:
1 Zhao H et al.: Phase I/II Study of iza-bren(BL-B01D1) as monotherapy in patients with locally advanced or metastatic EGFR mutated NSCLC. WCLC 2025; Abstr. #OA10 2 Zhang L et al.: Sacituzumab tirumotecan (sac-TMT) in patients (pts) with previously treated advanced EGFR-mutated non-small cell lung cancer (NSCLC): results from the randomized OptiTROP-Lung03 study. J Clin Oncol 2025; 43(Suppl. 16): 8507 3 Horinouchi H et al.: Results from a phase Ib study of telisotuzumab vedotin in combination with osimertinib in patients with c-Met protein-overexpressing, EGFR-mutated locally advanced/metastatic non-small-cell lung cancer (NSCLC) after progression on prior osimertinib. Ann Oncol 2025; 36(5): 583-91 4 Ahn M et al.: Datopotamab deruxtecan versus docetaxel for previously treated advanced or metastatic non-small cell lung cancer: the randomized, open-label phase III TROPION-Lung01 study. J Clin Oncol 2025; 43(3): 260-72 5 Paz-Ares L et al.: Sacituzumab govitecan versus docetaxel for previously treated advanced or metastatic non-small cell lung cancer: the randomized, open-label phase III EVOKE-01 study. J Clin Oncol 2024; 42(24): 2860-72 6 Besse B et al.: Tusamitamab ravtansine vs docetaxel in previously treated advanced nonsquamous NSCLC: results from phase 3 CARMEN-LC03 trial. WCLC 2024; Abstr. #OA08.05 7 Camidge DR et al.: Telisotuzumab vedotin monotherapy in patients with previously treated c-Met–overexpressing non-squamous EGFR wildtype advanced NSCLC: primary analysis of the LUMINOSITY trial. JClin Oncol 2024; 42(Suppl. 16): Abstr. #103 8 Smit EF et al.: Trastuzumab deruxtecan in patients with metastatic non-small-cell lung cancer (DESTINY-Lung01): primary results of the HER2-overexpressing cohorts from a single-arm, phase 2 trial. Lancet Oncol 2024; 25(4): 439-54 9 Peters S et al.: Efficacy and safety of sigvotatug vedotin, an investigational ADC, in NSCLC: updated phase 1 results (SGNB6A-001). J Clin Oncol 2024; 42(Suppl. 16): Abstr. #8521 10 Levy B et al.: TROPION-Lung02: datopotamab deruxtecan (Dato-DXd) plus pembrolizumab (pembro) with or without platinum chemotherapy (Pt-CT) as first-line (1L) therapy for advanced non-small cell lung cancer (aNSCLC). J Clin Oncol 2025; 43(Suppl. 16): Abstr. #8501 11 Cascone T et al.: Perioperative durvalumab plus chemotherapy plus new agents for resectable non-small-cell lung cancer: the platform phase 2 NeoCOAST-2 trial. Nat Med 2025; 31(8): 2788-96
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...