Asthme sévère
Compte-rendu:
Dre méd. Sabina Ludin
Rédactrice en chef
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Comment éviter qu’un patient souffrant d’asthme sévère doive être traité par corticostéroïdes oraux? Quel médicament biologique convient à quel patient? Des experts internationaux ont répondu à ces questions et à d’autres concernant le traitement de l’asthme sévère lors du congrès de la SSP. En outre, le Prof. Jörg Leuppi a donné un premier aperçu du Swiss Severe Asthma Register.
Effets secondaires à long terme des corticostéroïdes oraux
Dans le monde, 15 à 57% des patients souffrant d’asthme sévère prennent régulièrement des corticostéroïdes oraux (CSO), selon les études.1–5 Les problèmes à long terme causés par cette situation sont multiples. Un risque accru de diabète, d’obésité et de comorbidités associées, de complications osseuses et musculaires, d’hypertension, d’hypercholestérolémie et de maladies cardiovasculaires, de complications psychiatriques ainsi que de cataracte figure parmi les effets secondaires du traitement par CSO.6 Dans une étude britannique, 93% des patients souffrant d’asthme sévère présentaient au moins une comorbidité associée à l’utilisation de CSO, et la prévalence de ces affections était significativement plus élevée chez les patients asthmatiques traités par CSO que chez ceux qui ne l’étaient pas.7
Le risque de complications aiguës et chroniques dépend de la dose quotidienne de CSO et de la dose cumulée.8, 9 «Il est toutefois intéressant de noter que le risque de complications à long terme augmente après seulement deux ou trois traitements de CSO de courte durée. Ceci montre l’importance d’utiliser les CSO le moins souvent possible et, lorsque c’est inévitable, à la dose la plus faible possible»,9 a déclaré le Prof. Dr méd. Louis-Philippe Boulet, Québec.
Stratégies visant à éviter les CSO
Les mesures non médicamenteuses visant à prévenir les CSO comprennent notamment la confirmation du diagnostic d’asthme, l’évitement des facteurs déclenchants, dans la mesure du possible, ainsi que l’éducation du patient et l’encouragement de l’observance thérapeutique. Pour réduire le risque d’exacerbations, il faut non seulement un bon traitement par inhalation, mais aussi une technique d’inhalation correcte.
«Les stéroïdes inhalés (CSI) font désormais partie du traitement de l’asthme dès le départ»,10 a souligné L.-M. Boulet. Le traitement régulier par CSI peut réduire de manière significative le besoin de CSO.11 Chez les patients souffrant d’asthme sévère, l’utilisation de CSO peut également être réduite efficacement par un traitement par médicaments biologiques.
Réduction graduelle des CSO
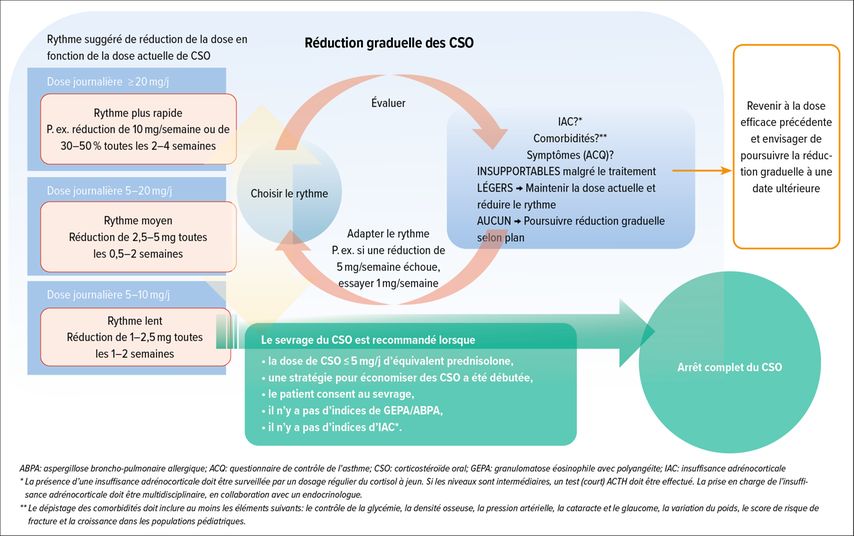
Une des difficultés lors du sevrage des CSO est de réduire la dose au bon rythme pour éviter à la fois la réapparition des symptômes d’asthme et le développement d’une insuffisance adrénocorticale (IAC). Une déclaration de consensus a récemment été publiée; elle propose une procédure selon un algorithme personnalisé.12 Le rythme et l’ampleur de la réduction de la dose sont basés sur la dose initiale de CSO, les signes d’IAC et la survenue de symptômes d’asthme, entre autres facteurs (Fig.1).
Fig. 1: Diminution progressive des corticostéroïdes oraux (CSO) chez les patients souffrant d’asthme sévère (adapté d’après Suehs et al., 2021)12
Médicaments biologiques pour le traitement de l’asthme sévère
Pour le traitement de l’asthme sévère, les lignes directrices de GINA (niveau 5) recommandent l’utilisation d’un médicament biologique lorsque le contrôle de l’asthme est insuffisant malgré une triple association inhalée (CSI + LABA + LAMA).10 Les CSO à faible dose ne sont désormais recommandés que lorsque toutes les autres options ont été épuisées.10 Actuellement, cinq médicaments biologiques différents avec des cibles distinctes sont disponibles:
-
Anticorps (Ac) anti-IgE: omalizumab (Xolair®)
-
Ac anti-interleukine (IL)-5: mépolizumab (Nucala®), reslizumab (Cinqaero®)
-
Ac anti-récepteur IL-5: benralizumab (Fasenra®)
-
Ac anti-récepteur IL-4: dupilumab (Dupixent®)
«L’une des questions les plus fréquentes que l’on me pose dans ce contexte est la suivante: lequel de ces médicaments biologiques dois-je prescrire à mon patient?», a déclaré le Prof. Dr méd. Roland Buhl, de Mayence. Tout d’abord, il convient de déterminer si le patient remplit les conditions requises pour recevoir un traitement biologique, c’est-à-dire s’il présente un asthme allergique ou éosinophilique, des taux élevés de FeNO (oxyde nitrique exhalé fractionné) et/ou un traitement d’entretien par CSO. Le choix du médicament biologique peut alors être guidé par les lignes directrices de GINA, qui proposent un algorithme simple accompagné de critères de décision clairs (Fig. 2).10 Chez les patients présentant un asthme clairement allergique, un Ac anti-IgE constitue le premier choix. Dans l’asthme éosinophilique sévère avec exacerbations fréquentes, un Ac anti-(récepteur) IL-5 ou, si les taux de FeNO sont très élevés, un Ac anti-récepteur IL-4 est indiqué. Le succès du traitement peut être évalué au plus tôt après quatre à six mois.
Fig. 2: Algorithme de GINA pour la sélection du médicament biologique pour le traitement (ttt) l’asthme sévère10
Données actuelles sur les médicaments biologiques
Ces derniers mois, plusieurs études en situation réelle sur l’utilisation des médicaments biologiques contre l’asthme sévère ont été publiées, confortant les résultats des essais cliniques. Un exemple est l’étude REALITI-A, qui montre que le mépolizumab réduit significativement la fréquence des exacerbations et la dose du traitement d’entretien de CSO, même en conditions réelles.13
Une autre étude en situation réelle s’est intéressée à la proportion de patients asthmatiques qui ont eu une réponse à long terme aux médicaments biologiques anti-IL-5.14 Après un suivi de 2 ans, un total de 83% des patients ont présenté une bonne réponse au médicament biologique. 69% d’entre eux présentaient encore des résidues – le plus souvent une altération de la fonction pulmonaire, des symptômes sinusaux incontrôlés et des symptômes d’asthme. 14% étaient des «super-répondants», qui n’avaient plus aucun symptôme. «Ces patients viennent consulter et nous disent qu’ils sont guéris et n’ont plus d’asthme. Notre tâche consiste à les convaincre qu’ils doivent au moins poursuivre la thérapie par inhalation», a déclaré R. Buhl. 17% des patients de cette étude n’ont pas répondu au médicament biologique et ont arrêté le traitement en raison de la détérioration de la maîtrise de l’asthme ou pour d’autres raisons.14
Les médicaments biologiques agissent non seulement sur l’asthme, mais aussi sur un certain nombre de comorbidités. Ainsi, l’omalizumab, un Ac anti-IgE, est également efficace contre l’urticaire et la rhinosinusite chronique avec polypose nasale.15,16 Le mépolizumab, un Ac anti-IL-5, s’est également avéré efficace chez les patients atteints de syndrome hyperéosinophilique et ceux souffrant de rhinosinusite chronique avec polypose nasale.17,18 Le dupilumab, Ac anti-récepteur de l’IL-4, affiche également une bonne efficacité face à la dermatite atopique et à la rhinosinusite chronique avec polypose nasale et est également autorisé pour ces deux indications.19,20 «L’efficacité dans ces comorbidités typiques de l’asthme peut influencer le choix du médicament biologique dans certaines circonstances», déclare l’expert.
Nouveau médicament biologique en préparation
Le tézépélumab, un nouvel anticorps monoclonal humain actuellement en cours d’essais cliniques, est dirigé contre une cible totalement nouvelle, à savoir la cytokine TSLP («thymic stromal lymphopoietin»). La TSLP est une «alarmine» et est sécrétée, en cas d’asthme, par les cellules épithéliales des voies aériennes lorsqu’elles sont exposées à un stimulus. «La TSLP joue un rôle dans la pathogenèse de l’asthme allergique et éosinophilique, de sorte qu’un anticorps anti-TSLP constitue une nouvelle option thérapeutique très intéressante», a expliqué R. Buhl. L’essai NAVIGATOR, publié en mai 2021, est la première étude de phase III avec le tézépélumab.21 Chez les adultes et les adolescents souffrant d’asthme sévère non contrôlé, le tézépélumab a significativement réduit le taux annuel d’exacerbations par rapport au placebo (critère d’évaluation primaire) à la fois dans la population globale (0,93 contre 2,1; RR: 0,44; IC à 95%: 0,37–0,53; p<0,001) et dans tous les sous-groupes dont le nombre d’éosinophiles sanguins variait (<300, ≥300, <150 et ≥150cellules/μl). Dans le groupe sous traitement actif, la fonction pulmonaire, la maîtrise de l’asthme et la qualité de vie se sont en outre améliorés. La fréquence et le type d’effets secondaires étaient comparables dans les deux groupes (traitement actif et placebo). «Ces résultats nous donnent l’espoir que nous aurons bientôt un autre médicament biologique disponible pour le traitement de l’asthme sévère», a conclu R. Buhl.
Registre suisse pour les patients souffrant d’asthme sévère
En Suisse, environ 5 à 10% des patients asthmatiques souffrent d’asthme sévère, mais il existe encore relativement peu de données sur cette population en situation réelle. Pour y remédier, en 2018, un registre clinique pour les patients souffrant d’asthme sévère (Swiss Severe Asthma Registry, SSAR) a été lancé.22 «Notre objectif est d’en savoir plus sur la maladie et son évolution, de découvrir des corrélations entre différentes variables qui ont un impact sur l’asthme sévère, et de faire un inventaire prenant en compte différents aspects de la maladie», a expliqué le Prof. Dr méd. Jörg D. Leuppi, Liestal.
Jusqu’à présent, un peu plus de 200 patients de toutes les régions de Suisse ont été inclus dans le registre. Afin d’obtenir un tableau aussi complet que possible des patients, outre les antécédents d’asthme, les antécédents familiaux, le type d’asthme, le statut tabagique, etc., les symptômes, les résultats des questionnaires spécifiques à l’asthme et une grande variété d’examens (fonction pulmonaire, laboratoire, imagerie, etc.), les médicaments actuels et antérieurs, les allergies et les comorbidités sont recueillis. «Nous collaborons du reste avec d’autres réseaux européens de lutte contre l’asthme, nous avons un aperçu de leurs données et nous partageons nos données avec eux», a précisé J. Leuppi.
Analyse des 200 premiers patients
Lors du congrès, le Prof. Leuppi a présenté des données inédites provenant des 200 premiers patients inclus dans le registre. 114 d’entre eux sont des hommes et 86 des femmes, l’âge moyen est de 55,6 ans, le patient le plus jeune a 13 ans, le plus âgé 87 ans. Quelque 50% des patients souffrent d’asthme allergique, 35% d’asthme non allergique et le reste d’une forme mixte. Au cours de l’année précédant l’inclusion dans le registre, 40% des patients n’ont eu aucune exacerbation et environ la moitié en ont eu une ou plusieurs. Quelques-uns ont eu plus d’une exacerbation par mois. «Près de 80% des patients sont traités par une association CSI/LABA et 40% utilisent en outre un anticholinergique. Presque tous les patients sont en outre traités avec un médicament biologique», précise J. Leuppi. La proportion élevée de patients sous traitement d’entretien par CSO, 17,5%, n’est pas une bonne nouvelle.
«Le recrutement de patients et de centres se poursuit et nous espérons que le registre va devenir une évidence. Veuillez demeurer actives et actifs et inscrire vos patients souffrant d’asthme sévère dans le registre», a exhorté J. Leuppi.
Source:
Assemblée annuelle de la Société Suisse de Pneumologie (SSP), 17 et 18 juin 2021
Littérature:
1 Broder MS et al.: Cost and health care utilization in patients with asthma and high oral corticosteroid use. Ann Allergy Asthma Immunol 2017; 118: 638-9 2 Phipatanakul W et al.: Effects of age and disease severity on systemic corticosteroid responses in asthma. Am J Respir Crit Care Med 2017; 195: 1439-48 3 Shaw DE et al.: Clinical and inflammatory characteristics of the European U-BIOPRED adult severe asthma cohort. Eur Respir J 2015; 46: 1308-21 4 Sweeney J et al.: Clinical management and outcome of refractory asthma in the UK from the British Thoracic Society Difficult Asthma Registry. Thorax 2012; 67: 754-6 5 Heffler E et al.: The Severe Asthma Network in Italy: findings and perspectives. J Allergy Clin Immunol Pract 2019; 7: 1462-8 6 Bleecker ER et al.: Systematic literature review of systemic corticosteroid use for asthma management. Am J Respir Crit Care Med 2020; 201: 279-93 7 Sweeney J et al.: Comorbidity in severe asthma requiring systemic corticosteroid therapy: cross-sectional data from the Optimum Patient Care Research Database and the British Thoracic Difficult Asthma Registry. Thorax 2016; 71: 339-46 8 Volmer T et al.: Consequences of long-term oral corticosteroid therapy and its side-effects in severe asthma in adults: a focused review of the impact data in the literature. Eur Respir J 2018; 52: 1800703 9 Price DS et al.: Adverse outcomes from initiation of systemic corticosteroids for asthma: long-term observational study. J Asthma Allergy 2018; 11: 193-204 10 Global Initiative for Asthma, GINA: Global strategy for asthma management and prevention. 2021; www.ginasthma.org 11 Ververeli K, Chipps B: Oral corticosteroid-sparing effects of inhaled corticosteroids in the treatment of persistent and acute asthma. Ann Allergy Asthma Immunol 2004; 92: 512-22 12 Suehs CM et al.; Oral Corticosteroids Tapering Delphi Expert Panel: Expert consensus on the tapering of oral corticosteroids for the treatment of asthma. A Delphi study. Am J Respir Crit Care Med 2021; 203: 871-81 13 Harrison T et al.: Real-world mepolizumab in the prospective severe asthma REALITI-A study: initial analysis. Eur Respir J 2020; 56: 2000151 14 Eger K et al.: Long-term therapy response to anti-IL-5 biologics in severe asthma-a real-life evaluation. J Allergy Clin Immunol Pract 2021; 9: 1194-200 15 Maurer M et al.: Omalizumab for the treatment of chronic idiopathic or spontaneous urticaria. N Engl J Med 2013; 368: 924-35 16 Gevaert P et al.: Efficacy and safety of omalizumab in nasal polyposis: 2 randomized phase 3 trials. J Allergy Clin Immunol 2020; 146: 595-605 17 Roufosse F et al.: Efficacy and safety of mepolizumab in hypereosinophilic syndrome: a phase III, randomized, placebo-controlled trial. J Allergy Clin Immunol 2020; 146: 1397-405 18 Han JK et al.; SYNAPSE study investigators: Mepolizumab for chronic rhinosinusitis with nasal polyps (SYNAPSE): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Respir Med 2021: S2213-2600(21)00097-7 19 Simpson EL et al.; SOLO 1 and SOLO 2 Investigators: Two phase 3 trials of dupilumab versus placebo in atopic dermatitis. N Engl J Med 2016; 375: 2335-48 20 Boyle JV et al.: Dupilumab in the treatment of chronic rhinosinusitis with nasal polyposis. Immunotherapy 2020; 12: 111-21 21 Menzies-Gow A et al.: Tezepelumab in adults and adolescents with severe, uncontrolled asthma. N Engl J Med 2021; 384: 1800-9 22Swiss Severe Asthma Register. ClinicalTrials.gov Identifier: NCT03984253
Das könnte Sie auch interessieren:
Revue de presse: L’importance d’objectifs thérapeutiques centrés sur les patient·es dans la SLA
Dans une revue récente, Chio et al., mettent en lumière la nécessité de repenser les critères d’évaluation dans les essais cliniques portant sur la sclérose latérale amyotrophique (SLA ...
L’asthme et le rythme circadien
Le rythme circadien ne joue pas seulement un rôle important dans le sommeil, il a également une influence considérable sur les crises d’asthme et la fonction pulmonaire. Le ciblage ...
Les défis du diabète de type 1
Dans le cas du diabète de type 1, surtout s’il ne se déclare qu’à l’âge adulte, la pose du diagnostic peut déjà constituer un défi. Le risque d’hypoglycémie, qu’il faut minimiser, et le ...