Herzfunktion unter Tafamidis bei Transthyretin-Amyloid-Kardiomyopathie
Bericht: Christian Fexa
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Tafamidis verlängert das Überleben von Patienten mit Transthyretin- Amyloid-Kardiomyopathie (ATTR-CM) im Vergleich zu Placebo. Offen sind Fragen zur Wirkung des Medikaments auf die Herzfunktion. Kürzlich sind Publikationen erschienen, die mit spannenden Daten aufwarten und einiges zur Klärung beitragen.
Keypoints
-
Tafamidis reduziert bei Patienten mit ATTR-CM die Mortalität sowie weitere schwerwiegende Ereignisse.
-
Unter Tafamidis kommt es zumindest zu einer geringeren Verschlechterung der LEVF, bei Patienten mit Wildtyp-ATTR-CM kommt es möglicherweise sogar zu gar keiner Verschlechterung.
-
Bestimmte echokardiografische Parameter können sich als nützlich in der Bestimmung der Krankheitsprogression zeigen.
Bei ATTR-CM infiltriert Transthyretin(TTR)-Amyloid den Herzmuskel und lagert sich ab. Dies führt zu einer Kardiomyopathie mit Herzinsuffizienzsymptomatik. Die häufigste Form der ATTR-CM ist die Wildtyp-ATTR-CM (ATTRwt-CM), eine zweite Form ist hereditär (ATTRv-CM). Bei Letzterer liegt eine pathogene TTR-Variante vor, was bei ATTRwt-CM nicht der Fall ist.1 Von der Erkrankung sind beide Geschlechter betroffen. Die Diagnose der ATTRwt-CM wird meist bei Männern zwischen dem 70. und 80. Lebensjahr gestellt, während die Diagnose einer ATTRv-CM hinsichtlich des Lebensalters variabel ist. Die ATTRwt-CM präsentiert sich vorwiegend kardial, die ATTRv-CM mit neurologischer Symptomatik. Die Prognose bei unbehandelter ATTR-CM ist mit einer mittleren Überlebenszeit von 2 bis 6 Jahren nach der Diagnose schlecht.2 Die Studie ATTR-ACT zeigte, dass Tafamidis das Überleben von ATTR-CM-Patienten verlängert.3 Die EMA erteilte 2020 die Zulassung zur Therapie beider ATTR-Formen. Kürzlich wurden zwei Metaanalysen zur Behandlung mit dieser Substanz bei ATTR-CM publiziert. Eine weitere rezente Arbeit, eine Post-hoc-Analyse der ATTR-ACT-Studie, befasst sich mit der kardialen Funktion unter der Therapie und wieder eine andere rezente Arbeit mit der Überwachung der Progression der Erkrankung.
Mortaliät und LV-Funktion analysiert
In eine Metaanalyse von Sukaina M et al. flossen zwei klinische randomisierte sowie eine retrospektive Studie ein. Basis der Metaanalyse waren die Selektionskriterien: Patientenalter >18 Jahre und Patienten randomisiert unter 80mg Tafamidis versus eine Kontrollgruppe. Analysiert wurde die Wirksamkeit von Tafamidis im Vergleich zur Kontrollgruppe bei Patienten mit ATTR-CM. Insgesamt waren 876 Patienten in der Metaanalyse. Es zeigte sich, dass Tafamidis die kardiovaskuläre Mortalität und die Gesamtmortalität bei Patienten mit ATTR-CM in allen Subgruppen senkt. Patienten mit Herztransplantation bzw. mechanischen Herzunterstützungssystemen profitierten jedoch nicht.4
Eine 2023 publizierte Metaanalyse von 15 Studien mit insgesamt 2765 Patienten analysierte auch die Veränderung der linksventrikulären Auswurffraktion (LVEF). Es zeigte sich zwar eine leichte Abnahme der LVEF im Krankheitsverlauf auch unter Tafamidis mit einem standardisierten mittleren Unterschied von −0,17; (p = 0,02), es wurden jedoch keine signifikanten Unterschiede in der Dicke des intraventrikulären Septums oder des globalen longitudinalen Strains (GLS) vor und nach der Tafamidis-Behandlung gefunden. Bei Patienten mit ATTRwt-CM zeigte eine Subgruppenanalyse gar keine signifikante Verschlechterung der LVEF. Insgesamt kam es unter Tafamidis zu einer Risikoreduktion (RR) in Bezug auf Gesamtmortalität oder Herztransplantation versus Patienten ohne Behandlung (gepoolte RR: 0,44; p < 0,01). Es profitierten sowohl Patienten mit ATTRwt-CM als auch solche mit ATTRv-CM. Ebenso zeigte sich für das Eintreten des zusammengesetzten Endpunkts bestehend aus Gesamtmortalität, Herztransplantation, Implantation von Herzunterstützungsgeräten, Herzinsuffizienzexazerbationen und Krankenhausaufenthalt unter Tafamidis ein geringeres Risiko (RR: 0,57; p<0,01). Die Ergebnisse deuten darauf hin, dass es bei den Patienten mit ATTRwt-CM im Laufe der Behandlung mit Tafamidis zu keiner signifikanten Verschlechterung der LVEF mehr kommt. Außerdem war die Behandlung mit Tafamidis mit einem geringen Risiko für Todesfälle insgesamt und für kardiovaskuläre Nebenwirkungen verbunden.5
Verschlechterung der LV-Funktion reduziert
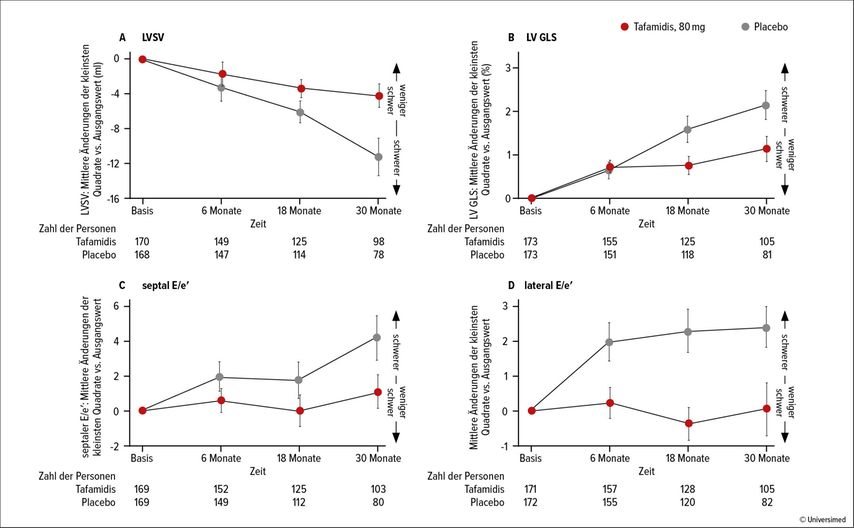
Zur Wirkung von Tafamidis auf die Herzfunktion bei Patienten mit ATTR-CM wurde 2024 eine Post-hoc-Analyse der Zulassungsstudie ATTR-ACT publiziert; aus dieser lagen von 436 Patienten echokardiografische Daten vor.6 Eine Herzinsuffizienz mit erhaltener LEVF hatten 220 (50,5%), eine mit leicht reduzierter LVEF 119 (27,3%) und eine mit reduzierter LVEF hatten 97 Patienten (22,2%). Im Follow-up von 30 Monaten kam es bei 4 echokardiografischen Parametern zu einer geringeren Verschlechterung bei Patienten, die Tafamidis 80mg (n=176) erhalten hatten, verglichen mit jenen unter Placebo (n=177): LV-Schlagvolumen: 7,02ml (p=0,002), GLS: –1,02% (p=0,005); septale E/e´: –3,11 (p=0,01), laterale E/e´ –2,35; (p=0,006). Die Abbildung 1 zeigt die Veränderungen im Laufe des Follow-ups.
Abb. 1: Mittlere Änderungen der kleinsten Quadrate gegenüber dem Ausgangswert über die Zeit mit Tafamidis 80 mg im Vergleich zu Placebo. A) linksventrikuläres Schlagvolumen (LVSV), B) linksventrikulärer (LV) globaler longitudinaler Strain (GLS), C) septaler E/e′ und D) lateraler E/e′. Die mittleren LS-Differenzen stellen Tafamidis 80 mg minus Placebo dar. LV GLS wird als negative Zahl ausgedrückt, daher bedeutet eine Veränderung in positiver Richtung eine Verschlechterung des Wertes
Im Vergleich zu Placebo verringerte Tafamidis 80mg also die Verschlechterung der systolischen und diastolischen LV-Funktion bei Patienten mit ATTR-CM über das Follow-up von 30 Monaten hinweg. Bemerkenswert ist, dass etwa die Hälfte der Patienten bei Studieneinschluss eine leicht reduzierte oder reduzierte LEVF aufwies, was darauf hinweist, dass ATTR-CM als mögliche Diagnose bei Patienten mit Herzinsuffizienz unabhängig von der zugrunde liegenden LEVF in Betracht gezogen werden sollte, so die Studienautoren.6
Parameter zur Beobachtung der Krankheitsprogression
Ein aktueller Expertenkonsensus empfiehlt drei klinische Bereiche (klinisch, Biomarker und EKG/Bildgebung), die anhand mehrerer messbarer Merkmale bewertet werden, um das Fortschreiten der ATTR-CM zu definieren.7 Nun analysierten Ney et al. retrospektiv Daten von wtATTR-CM-Patienten, die eine Tafamidis-Therapie begonnen hatten, hinsichtlich der Krankheitsprogession. Die Patienten waren im Rahmen eines Routineprotokolls zu Beginn und nach 6 Monaten auf die Häufigkeit von Werten jenseits der im Konsensus vorgeschlagenen Schwellenwerte zur Definition des Fortschreitens der Krankheit untersucht worden. Außerdem wurde die Assoziation der kardialen Magnetresonanztomografie (CMR) mit klinischen Bereichen innerhalb einer Untergruppe untersucht. Die Studie wurde ebenfalls im Jänner 2024 publiziert.8
In die Studie wurden 62 ATTR-CM-Patienten eingeschlossen (88,7% männlich, durchschnittlich 79 Jahre alt). Bei 16,1% der Patienten fand sich eine Krankheitsprogression im klinischen und funktionellen Bereich, bei 33,9% im Bereich der Biomarker und bei 43,5% im Bereich der Bildgebung/des EKG. Letzteres wurde durch eine Verschlechterung des Grades der diastolischen Dysfunktion und des GLS bestimmt. Bei 35,5% der Patienten zeigten sich Fortschritte in keinem, bei 35,5% in einem, bei 29,0% in zwei und bei keinem Patienten in drei Bereichen. Eine Subgruppenanalyse von 22 Patienten mit verfügbaren Basis- und Nachuntersuchungsdaten der CMR zeigte eine Zunahme des extrazellulären Volumens um >5% bei 18,2% der Patienten, wobei sich keine signifikante Korrelation in Bezug auf die klinischen Bereiche fand. Die häufigsten Merkmale mit nachgewiesenem kurzfristigem Fortschritt waren somit echokardiografische Parameter der LVEF wie der Grad der diastolischen Dysfunktion und GLS.8
Literatur:
1 Ruberg FL et al.: Transthyretin amyloid cardiomyopathy: JACC state-of-the-art review. J AmColl Cardiol 2019;73 (22): 2872-91 2 Lane T et al.: Natural history, quality of life, and outcome in cardiac transthyretin amyloidosis. Circulation. 2019; 140(1): 16-26 3 Maurer MS et al.: Tafamidis treatment for patients with transthyretin amyloid cardiomyopathy. N Engl J Med 2018; 379(11): 1007-16 4 Mahnoor S et al.: Efficacy of tafamidis in transthyretin amyloid cardiomyopathy: a systematic review and meta-analysis. Ann Med Surg 2023; 86(1): 433-8 5 Wang J et al.: Tafamidis treatment in patients with transthyretin amyloid cardiomyopathy: a systematic review and meta-analysis. EClinicalMedicine 2023; 63: 102172 6 Shah SJ et al.: Effect of tafamidis on cardiac function in patients with transthyretin amyloid cardiomyopathy: a post hoc analysis of the ATTR-ACT randomized clinical trial. JAMA Cardiol 2024; 9(1): 25-34 7 Garcia-Pavia P et al.: Expert consensus on the monitoring of transthyretin amyloid cardiomyopathy. Eur J Heart Fail 2021; 23: 895-905 8 Ney S et al.: Multiparametric monitoring of disease progression in Contemporary Patients with wild-type transthyretin amyloid cardiomyopathy initiating tafamidis treatment. J Clin Med 2024; 13(1): 284
Das könnte Sie auch interessieren:
Asbestbedingtes Larynx- und Lungen-karzinom – Primär- oder Sekundärtumor?
Im Folgenden wird der Fall eines deutschen Facharbeiters vorgestellt, der während seiner Berufstätigkeit asbesthaltigen Stäuben ausgesetzt war und dadurch an einem Plattenepithelkarzinom ...
Alpha-1-Antitrypsin-Mangel: blinder Fleck auch in der Pneumologie?
Der Alpha-1-Antitrypsinmangel (AATM) gilt als seltene genetische Erkrankung und betrifft überwiegend die Lunge und die Leber,jedoch mithoher klinischer Variabilität. Doch AATM ist nicht ...
Sjögren-Syndrom: ein Update
Prof. Dr. Stephan Gadola, MD, PhD, gab im Rahmen der Webinar-Reihe von Rheuma Schweiz einen Überblick über aktuelle Diagnose- und Klassifikationskriterien des Sjögren-Syndroms (SjS), ...