Stellenwert der Immuntherapie
Autor:
Univ.-Prof. Prim. Dr. Martin Burian
Abteilung für Hals-Nasen-Ohrenheilkunde, Kopf- und Halschirurgie
Ordensklinikum Linz
E-Mail: martin.burian@ordensklinikum.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Bei Kopf-Hals-Tumoren spielt die Immuntherapie in der klinischen Praxis erst seit Kurzem eine Rolle. Derzeit sind drei Substanzen für die Behandlung von Plattenepithelkarzinomen des Kopf-Hals-Bereiches zugelassen. Zwei Antikörper sind Checkpoint-Inhibitoren und binden an den „Programmed cell death protein 1 (PD-1)“-Rezeptor, ein Antikörper ist gegen den epidermalen Wachstumsfaktorrezeptor (EGFR) gerichtet.
Keypoints
-
Der Einsatz von Immuntherapien bei Kopf-Hals-Tumoren ist im klinischen Alltag angekommen. Die Zulassung eines Checkpoint-Inhibitors in der Erstlinientherapie hat die Behandlung von Tumorrezidiven deutlich verändert.
-
Die bessere Verträglichkeit von Immuntherapien im Vergleich zu zytotoxischen Chemotherapien verringert die Nebenwirkungsrate und führt zu einer besseren Lebensqualität der Patienten im Rezidivfall.
-
Ziel muss sein, die Immuntherapie Prognose-verbessernd in der Primärbehandlung von Kopf-Hals-Tumoren einzusetzen.
Über etliche Jahrzehnte war die chirurgische Therapie von Kopf-Hals-Tumoren die einzige Möglichkeit eines kurativen Behandlungsansatzes. Nach dem Zweiten Weltkrieg ist die Strahlentherapie als zweite Säule im Behandlungskonzept hinzugekommen. Die Kombination beider Therapieformen im Sinne der adjuvanten Radiotherapie hat die Prognose dieser Erkrankungen deutlich verbessert. Die Chemotherapie war die letzte und dritte Säule, die Ende der 1980er-Jahre in das Therapiekonzept aufgenommen wurde. Nach wie vor sind die Platine (Cisplatin und Carboplatin) die am häufigsten eingesetzten Präparate in den verschiedensten Kombinationen. Durch Verbesserungen im Bereich aller dieser drei Säulen (z.B. die minimalinvasive CO2-Laser-Chirurgie und transorale Roboterchirurgie oder die intensitätsmodulierte Strahlentherapie [IMRT]) konnte die Prognose bei akzeptabler Lebensqualität etwas angehoben werden. Trotz allem sind die Früh- und Spättoxizitäten, vor allem wenn alle drei Therapieformen bei der Primärbehandlung zum Einsatz kommen müssen, sehr hoch. Neben dem Ziel der Verbesserung der onkologischen Ergebnisse steht daher die Minimierung von Nebenwirkungen sowie Früh- und Spättoxizitäten im Vordergrund der Anstrengungen um neue Therapieformen.
Zielgerichtete Therapien
Die erste zielgerichtete Therapie, die bei Kopf-Hals-Tumoren zum Einsatz kam, war Cetuximab. Dieser gegen den epidermalen Wachstumsfaktorrezeptor (EGFR) gerichtete Antikörper wurde erstmals 2004 in Kombination mit einer Strahlentherapie bei lokal fortgeschrittenen Erkrankungen oder in Kombination mit einer platinbasierten Chemotherapie bei rezidivierenden/metastasierenden Erkrankungen zugelassen. Vor allem bei Patienten, die platinrefraktär waren oder ein Platin nicht bekommen konnten, war Cetuximab eine sinnvolle Alternative. Die Ansprechrate konnte von 64% mit der alleinigen Radiotherapie auf 74% mit der Kombinationstherapie gesteigert werden. 2008 wurde gezeigt, dass die Zugabe von Cetuximab zu der bis dahin üblichen Standardtherapie bei rezidivierten/metastasierten Tumoren mit Cisplatin und 5-Fluorouracil (5-FU) eine Verbesserung des rezidivfreien Überlebens bringt. Seit diesem Zeitpunkt war die als EXTREME-Schema bezeichnete Erstlinientherapie der Standard. Vor Kurzem konnte gezeigt werden, dass eine Dosisreduktion des Platins und der Ersatz von 5-FU durch Docetaxel in Kombination mit Erbitux besser verträglich und im onkologischen Ergebnis nicht schlechter als das ursprüngliche EXTREME-Schema sind.
Checkpoint-Inhibitoren
Vor drei Jahren wurde nun erstmals ein Checkpoint-Inhibitor als Monotherapie zur Behandlung des rezidivierten oder metastasierten Plattenepithelkarzinoms des Kopf-Hals-Bereichs mit einer Progression während oder innerhalb von sechs Monaten nach einer platinbasierten Therapie für den klinischen Einsatz zugelassen. Nivolumab ist ein monoklonaler Antikörper, der an den „Programmed cell death protein1 (PD-1)“-Rezeptor auf T-Zellen und anderen Immunzellen bindet und auf diese Weise die Interaktion mit den Liganden PD-L1 und PD-L2 verhindert. Da manche Tumoren PD-L1 reichlich exprimieren, kann durch die Gabe von Nivolumab die immunsupprimierende Wirkung des Tumors unterdrückt werden und die T-Zell-Aktivierung erhöht werden. Die Ansprechrate wird in der Zulassungsstudie mit 13,3% angegeben.1 Im Gegensatz zu dem weiter unten beschriebenen, zweiten zugelassenen Checkpoint-Inhibitor Pembrolizumab ist Nivolumab unabhängig von der PD-L1-Expression des Tumors einsetzbar.
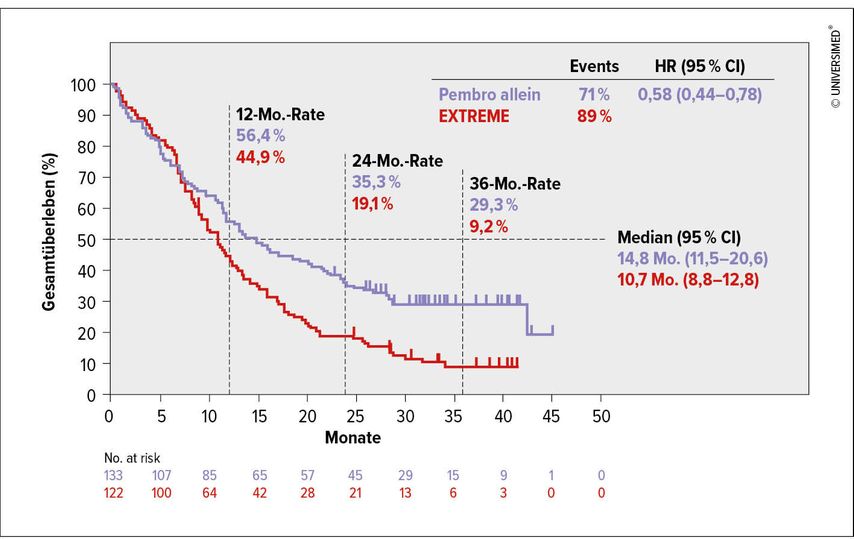
Vor einem Jahr wurde schließlich ein weiterer PD-1-Antikörper in Europa für die Erstlinientherapie zugelassen. Pembrolizumab kann nun bei rezidivierenden oder metastasierenden Kopf-Hals-Tumoren als Monotherapie oder in Kombination mit einer Chemotherapie angewendet werden, wenn eine PD-L1-Expression vorliegt und der Combined Positive Score (CPS) einen Wert über 1 zeigt. Die Bestimmung des CPS-Wertes ist derzeit nur bei Kopf-Hals-Tumoren gefordert. Bei den meisten anderen Tumoren wird der Tumor Proportion Score (TPS) bestimmt, dessen Wert als Prognose für das Ansprechen gedeutet werden kann. Während der TPS-Wert die Expression von PD-L1 nur an den Tumorzellen reflektiert, ist der CPS-Wert eine Kombination der PD-L1-Expression der Tumorzellen und der Zellen in der Tumorumgebung, nämlich hauptsächlich der Entzündungszellen. In der KEYNOTE-048-Studie, die für die Zulassung verantwortlich war, wurde die CPS-Expression nochmals unterteilt.2 Die höchsten Ansprechraten waren bei einem CPS von über 20 gegeben (Abb. 2). So ist es nun im klinischen Alltag üblich, bei CPS-Werten von 1 bis 19 die Pembrolizumab-Therapie mit einer Chemotherapie zu kombinieren. Auch hier steht derzeit Cisplatin im Vordergrund. Bei CPS-Werten über 20 oder deutlich höher, wird eine Pembrolizumab-Monotherapie empfohlen. Die Daten bezüglich des Überlebensvorteils konnten nun vor Kurzem in einer Folgestudie, die den Progressionsverlauf bei Patienten nach Pembrolizumab-Therapie und der Gabe einer weiteren Therapielinie beobachtete, bestätigt werden.3
Abb. 2: Gesamtüberleben von Patienten mit einem CPS ≥20 mit einer Pembrolizumab-Therapie versus Patienten, die mit einem EXTREME-Schema in der Erstlinie behandelt wurden (adaptiert nach Rischin D et al.: J Clin Oncol 2019; doi:10.1200/JCO.2019.37.15_suppl.6000)
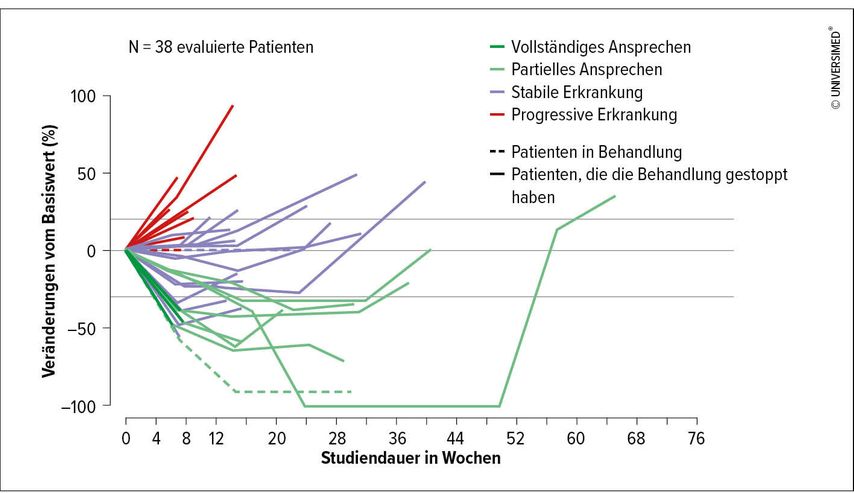
Abb. 3: Veränderung der Tumormasse nach Therapie mit Monalizumab und Cetuximab bei mit Platin und Checkpoint-Inhibitoren vorbehandelten Patienten (adaptiert nach Cohen RB et al.: J Clin Oncol 2020; doi: 10.1200/JCO.2020.38.15_suppl.6516)
Die Einführung der Checkpoint-Inhibitoren in die Erstlinientherapie hat den Praxisalltag durchaus verändert. Verglichen mit den Toxizitäten, die im Rahmen des EXTREME-Schemas auftreten, stellt die Monotherapie mit Pembrolizumab eine gut verträgliche Therapie dar. Der Benefit für den Patienten ist daher durch eine bessere Lebensqualität während und nach dieser Erstlinientherapie gegeben.Die Ansprechrate ist mit 14,1% vergleichbar mit dem zweiten zugelassenen Checkpoint-Inhibitor Nivolumab. Diese Ansprechraten sind derzeit niedrig, da verlässliche Biomarker, die ein gutes Ansprechen voraussagen und jene Patienten herausfiltern würden, die von der Therapie profitieren, derzeit noch nicht vorhanden sind. Die Bestimmung des CPS-Wertes geht in diese Richtung, erfüllt aber eine verlässliche Praktikabilität im klinischen Alltag noch nicht. Wenn allerdings ein Patient ein gutes Ansprechen zeigt, so hält dieses Ansprechen auch relativ lange an. Daten über einen Zeitraum von fünf Jahren sind dazu nun verfügbar (Abb. 2).
Trotz der guten Verträglichkeit muss darauf hingewiesen werden, dass schwerwiegende, potenziell tödliche Autoimmunnebenwirkungen auftreten können. Neben der gefürchteten Pneumonitis, welche letal verlaufen kann, sind auch gastrointestinale Nebenwirkungen sowie die Beeinflussung des Hormonhaushaltes über Hypophyse oder Bauchspeicheldrüse zu beachten.
Ausblick
Wie wird es nun weitergehen? Derzeit laufen bei Kopf-Hals-Tumoren über 120 Studien, die eine Immuntherapie in Kombination mit anderen Therapieformen zum Inhalt haben. Der größte Anteil dieser Studien beschäftigt sich mit einer Kombination verschiedener zielgerichteter Therapien. So wurde heuer bei der virtuellen ASCO-Präsentation eine Phase-II-Studie mit Monalizumab, einem gegen den NKG2A-Rezeptor gerichteten Antikörper, der an tumorinfiltrierendeT-Zellen und NK-Zellen bindet, in Kombination mit Cetuximab vorgestellt (Abb. 3).4 Die Gesamtansprechrate von 20% bei mehrfach vortherapierten Patienten hat nun zu der Erstellung einer Phase-III-Studie, die im Herbst 2020 startet, geführt. Des Weiteren beschäftigen sich viele Studien mit der Kombination von Antikörpern, die gegen verschiedenste Rezeptoren gerichtet sind. Als Beispiel hierfür sei eine Kombination eines Anti-ICOS-Antikörpers mit Pembrolizumab erwähnt. Aber auch verschiedene Applikationswege werden getestet. So wird die Wirkung eines „Stimulator of interferon genes (STING)“-Agonisten als Monotherapie gegen eine Kombination mit Pembrolizumab getestet. Die lokale Infiltration in das Tumorgewebe soll neben der lokalen Wirkung auch eine systemische Wirkung entfalten.
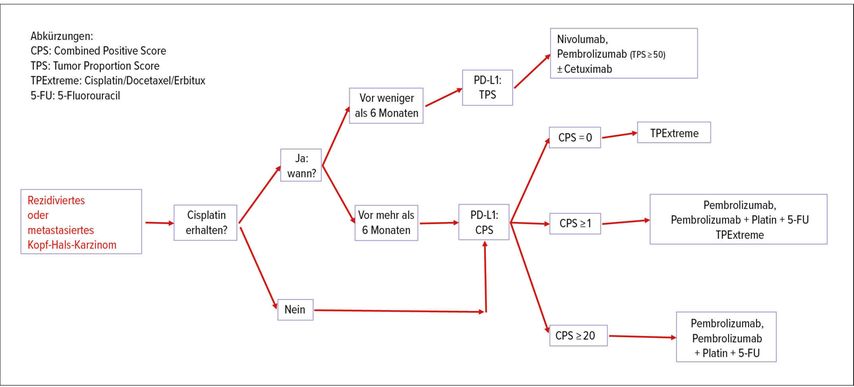
Zusammenfassend kann daher gesagt werden, dass sich durch die Einführung der Immuntherapie bei rezidivierten/metastasierten Kopf-Hals-Tumoren eine neue Therapierichtlinie etabliert hat. Einen Vorschlag für ein Vorgehen in der Praxis zeigt Abbildung
Abb. 4: Vorschlag für einen Behandlungspfad bei Patienten mit einem rezidivierten oder metastasierten Plattenepithelkarzinom des Kopf-Hals-Bereiches
Literatur:
1 Ferris RL et al.: Nivolumab for recurrent squamous-cell carcinoma of the head and neck. N Engl J Med 2016; 375(19): 1856-67 2 Burtness B et al.: Pembrolizumab alone or with chemotherapy versus cetuximab with chemotherapy for recurrent or metastatic squamous cell carcinoma of the head and neck (KEYNOTE-048): a randomised, open-label, phase 3 study. Lancet 2019; 394(10212): 1915-28 3 Harrington KJ et al.: KEYNOTE-048: progression after the next line of therapy following pembrolizumab (P) or P plus chemotherapy (P+C) vs EXTREME (E) as first-line (1L) therapy for recurrent/metastatic (R/M) head and neck squamous cell carcinoma (HNSCC). J Clin Oncol 2020; 38(no. 15_suppl): 6505 4 Cohen RB et al.: Combination of monalizumab and cetuximab in recurrent or metastatic head and neck cancer patients previously treated with platinum-based chemotherapy and PD-(L)1 inhibitors. J Clin Oncol2020; 38(no. 15_suppl): 6516
Das könnte Sie auch interessieren:
Morbus Menière – der Pathomechanismus des Hydrops
Schon im 19. Jahrhundert sah man einen Zusammenhang zwischen Schwindel, Hörverlust und Tinnitus, verursacht von pathologischen Vorgängen im Innenohr. Knapp 80 Jahre später wurde der ...
Wie Coaching den Fachärztemangel an medizinischen Abteilungen angehen kann
Hohe Arbeitsbelastung, Stress, schlechte Stimmung: An vielen Spitalskliniken ist das die tägliche Realität. Es ist daher nicht verwunderlich, dass viele Fachärzt:innen den Weg in die ...
AC102: ein vielversprechender Wirkstoffkandidat bei Hörsturz
Hörsturz führt häufig zu dauerhaftem Hörverlust und Begleiterkrankungen wie Tinnitus. Glukokortikoide werden für den Off-Label-Einsatz verschrieben, obwohl es keine klinischen Beweise ...