Innovationen in der Diagnostik schlafbezogener Atmungsstörungen
Autor:innen:
Nora-Maria Burian
HNO-Zentrum Mangfall-Inn
Bad Aibling
Prof. Dr. J. Ulrich Sommer
HNO-Zentrum Mangfall-Inn
Bad Aibling
Klinik für HNO-Heilkunde
Klinikum rechts der Isar
München
Korrespondierende Autorin:
Nora-Maria Burian
E-Mail: noramaria.burian@gmail.com
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Gruppe der schlafbezogenen Atmungsstörungen (SBAS) betrifft weltweit aktuell ca. 900 Millionen Menschen, von denen ca. die Hälfte an einer obstruktiven Schlafapnoe (OSA) leiden. In Österreich sind im Alter von 30–69 Jahren 28,4% der Menschen betroffen.1 In diesem Artikel werden die Neuerungen der Diagnostik jenseits der klassischen Polygrafie/Polysomnografie in der Diagnostik der SBAS vorgestellt.
Keypoints
-
Der Goldstandard in der Diagnostik der schlafbezogenen Atmungsstörungen ist weiterhin die Polysomnografie. Diese ist aber aufwendig und kommt daher, trotz einer bekannten hohen Nacht-zu-Nacht-Variabilität, meist nur für 1 Nacht zur Anwendung.
-
In den vergangenen Jahren sind immer mehr alternative portable Systeme (z.B. WatchPAT) verfügbar geworden, welche in der deutschen S3-Leitlinie der Polygrafie gleichgestellt wurden.
-
Patienteneigene Messgeräte (Wearables) wie z.B. die Apple Watch ermöglichen eine Messung des Schlafs über mehrere Nächte. Obwohl diese Geräte relativ genau sind, erweisen sich Validierungsstudien aufgrund der unablässigen Erneuerungen jedoch als schwierig.
-
Apps (z.B. Somnofox/Snorefox) bieten die Möglichkeit einer akustischen Analyse mit minimaler Invasivität, finden immer mehr Verwendung im Screening-Prozess und erhöhen so die Prätestwahrscheinlichkeit.
Eine obstruktive Schlafapnoe (OSA) stellt nicht nur ein erhöhtes Risiko für das Auftreten von Herz-Kreislauf-Erkrankungen, sondern mit der resultierenden Tagesmüdigkeit ein eindeutig erhöhtes Risiko für Sekundenschlaf dar. Daraus resultiert, dass im Straßenverkehr doppelt so viele Menschen an den Folgen des Sekundenschlafs als an den Folgen von Alkohol am Steuer sterben.2 Umso wichtiger sind einfache und zugängliche Möglichkeiten zur Diagnostik einer schlafbezogenen Atmungsstörung (SBAS).
Kein anderer Bereich der Schlafmedizin hat in den letzten Jahren so stark von den Fortschritten in der digitalen Signalver-arbeitung und der Verkleinerung und Verbesserung der Sensorik profitiert. In den vergangenen 10 Jahren ist in Europa die Verwendung von Geräten zur Diagnostik dieser Erkrankung zu Hause, mehrheitlich Polygrafie-Geräte (PG), von 29% auf 42% gestiegen. Trotz der Entwicklung in der Signalverarbeitung und des immer größeren Einsatzes von Machine Learning ist weiterhin sowohl vorher als auch nachher ein hoher personeller Einsatz zur validen Diagnose notwendig.3
Status quo
Der Verdacht auf eine SBAS wird auf verschiedenen Wegen und aufgrund von verschiedenen Leitsymptomen gestellt. Einerseits die vermehrte Tagesmüdigkeit, die den Patienten meist selbst an eine Schlafstörung denken lässt, andererseits die kardiovaskulären Risikofaktoren wie z.B. die fehlende nächtliche Blutdruck-senkung (Non-Dipper) oder eine sehr schwer medikamentös einstellbare arterielle Hypertonie, die den Kardiologen oder Allgemeinarzt an eine OSA denken lässt. Aktuell ist z.B. in Deutschland der Verlauf bis zur Diagnosestellung mittels der Qualitätssicherungsvereinbarung gemäß §135 Abs.2 SGB V zur Diagnostik und Therapie schlafbezogener Atmungsstörungen klar geregelt: angefangen mit der Anamnese und der klinischen Untersuchung, gefolgt von der ambulanten Polygrafie bis hin zur Polysomnografie.
Anamnese und körperliche Untersuchung
Hier sollen vor allem Komorbiditäten wie Herz-Kreislauf-Erkrankungen, arterielle Hypertonie und eine ausgeprägte Tagesschläfrigkeit identifiziert werden. Letztere lässt sich über verschiedenste Fragebögen quantifizieren, u.a.: Epworth-Schläfrigkeitsskala (ESS), Pittsburgh Sleep Quality Index (PSQI), der Berlin Questionnaire, der STOP- und der STOP-BANG-Fragebogen.
Die Polygrafie (PG)
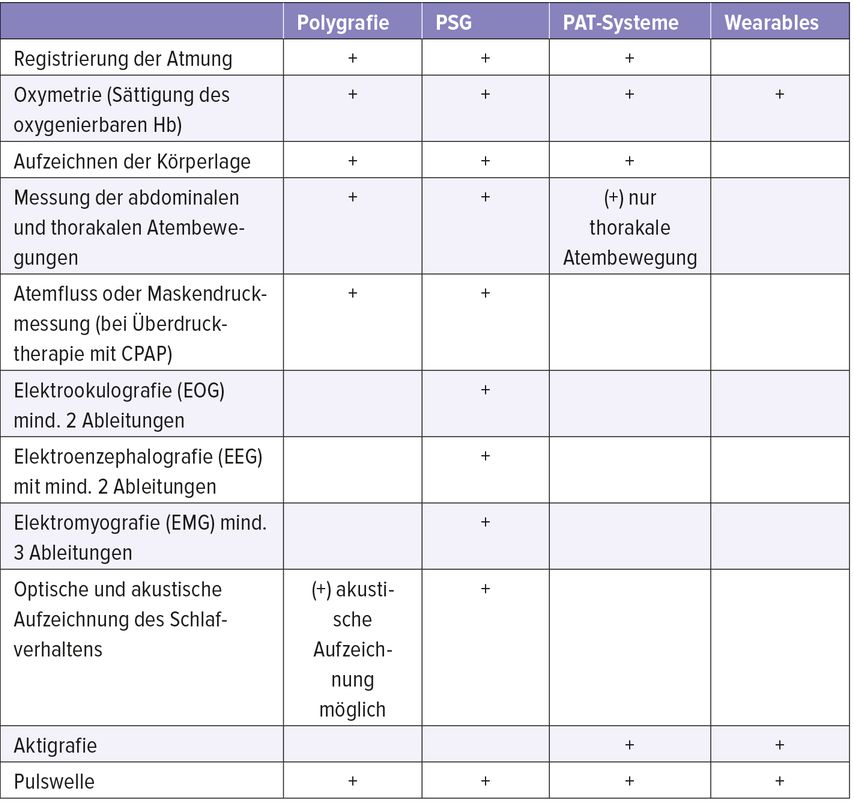
Polygrafie(PG)-Systeme zur Diagnostik der Schlafapnoe lassen sich in verschiedene Klassen einteilen und umfassen im allgemeinen Systeme mit 6 Kanälen ohne EEG. Sie müssen jedoch mindestens die in Tabelle 1 aufgeführten Messdaten liefern.
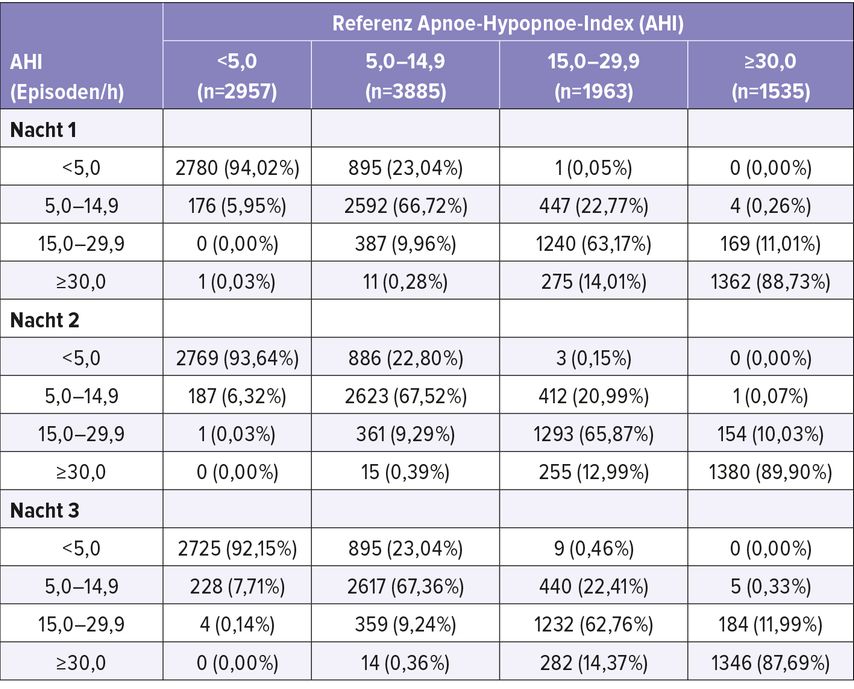
Tab. 1: Darstellung der Nacht-zu-Nacht-Variabilität bei Messungen über 3 Nächte (modifiziert nach Punjabi NM et al. 2020)12
Der Goldstandard – die Polysomnografie (PSG)
Der größte Unterschied zwischen der Polysomnografie (PSG) und der kleinen Schwester Polygrafie ist die Hinzufügung eines Elektroenzephalogramms (EEG), eines Elektrookulogramms (EOG) und eines Elektromyogramms (EMG) zur Schlafstadienbestimmung. Diese ist mittels PG nur schätzungsweise möglich. Die genau abzuleitenden Parameter sind in Tabelle 1 aufgeführt.
Problem der Inter-Nacht-Variabilität der OSA
Gemein ist diesen Messverfahren, dass sie aufgrund des erwähnten hohen personellen und apparativen Aufwandes meist nur für eine Nacht zur Anwendung kommen. Neuesten Forschungsergebnissen zufolge zeigt sich jedoch eine hohe Nacht-zu-Nacht-Variabilität in den Ergebnissen der PG und PSG. Nur bei einem Apnoe-Hypopnoe-Index (AHI) <5/Stunde oder >30/Stunde ist der Schweregrad einer OSA demzufolge konklusiv in einer Nacht ermittelbar (Tab. 1). Bei 1/3 der Patienten mit leichter oder mittelgradiger OSA wird somit durch die Messung über nur eine Nacht ein falscher Schweregrad ermittelt.4
Auch wenn die PSG als diagnostischer Goldstandard besonders für Erkrankungen abseits der SBAS aktuell noch nicht ersetzt werden kann,5 ist sie doch aufgrund der hohen Arbeitsintensität und des finanziellen Aufwandes (technisches Fachpersonal, spezielle Räumlichkeiten, begrenzte Bettenzahl etc.) für Längsschnittmessungen über mehrere Nächte nicht wirklich geeignet. Hier hat vor allem in den letzten Jahren die Bedeutung mobiler Diagnostikgeräte neben der PG auch in Europa zugenommen.3 Derzeit werden immer mehr solcher ambulanten Diagnostikgeräte als Medizinprodukte zugelassen.
Pulsoxymetrie, Pulswelle und peripherer arterieller Tonus als diagnostische Marker
Aktueller Bestandteil jeder PG und PSG ist die Pulsoxymetrie. Aus ihr kann mit ausreichender Erhöhung der Samplingfrequenz die sog. Pulswelle abgeleitet werden. Diese dient sowohl der Qualitätssicherung der Pulsoxymetrie als auch der Analyse kardiovaskulärer Parameter. Mit nur leicht erhöhtem apparativem Aufwand lässt sich zur weiteren Steigerung der Aussagekraft aus den plethysmografischen Daten der Pulsoxymetrie der sog. periphere arterielle Tonus (PAT) ableiten. Dabei macht man sich zunutze, dass Fingerarterien Arterien muskulären Typs sind, welche auf Impulse des sympathischen Nervensystems mit einer Widerstandsänderung reagieren. So kann man z.B. aus dem reziproken Muster von Einschnürung der Pulswelle oder des PAT bei gleichzeitigem Anstieg der Herzfrequenz nicht nur auf eine Erhöhung des Sympathikotonus schließen, sondern auch auf ein sog. vegetatives Arousal.
Ein vegetatives Arousal besteht aus:
-
Änderung des Atemmusters
-
psychogalvanischem Reflex (Haut-widerstand)
-
Anstieg von Herzfrequenz, Blutdruck und Pulsgeschwindigkeit sowie einer
-
Vasokonstriktion (Pulswellenreduktion)
Während mittels Pulswelle vornehmlich Arousals detektiert werden können, kann mittels des peripher arteriellen Tonus auch eine Einteilung in die verschiedenen Schlafstadien erfolgen. Während im Tiefschlaf z.B. ein geringer Sympathikotonus (d.h. hohe PAT-Amplitude) und eine niedrige Herzfrequenz (HF) mit niedriger Variabilität gemessen werden, zeigt sich im Wachzustand und im REM-Schlaf eine hohe Variabilität bei meist hoher HF und hohem Sympathikotonus. Bei aufgezeichneten Körperbewegungen in diesem Stadium lässt sich eher auf einen Wachzustand schließen, während eine Schwankung der Sauerstoffsättigung hier typisch für den REM-Schlaf ist.
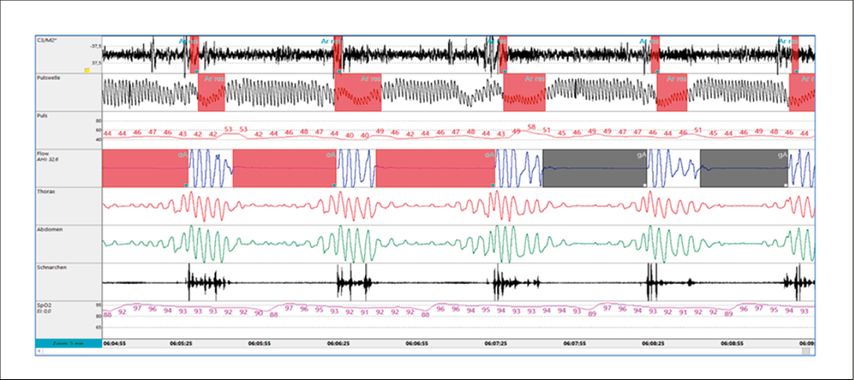
Natürlich lassen die Schwankungen von Pulswelle und Herzfrequenz auch Rückschlüsse auf eine obstruktive Apnoe zu (Abb. 1). Eine Auswertung in Bezug auf respiratorische Ereignisse gelingt jedoch nicht alleine auf der Basis des PAT, sondern nur unter Berücksichtigung weiterer Biosignale wie der Sauerstoffsättigung, Herzfrequenz, Aktigrafie und der Messung der Thoraxexkursion sowie der Körper-lage. Die PAT-basierten Systeme (z.B. WatchPAT) weisen eine gute Evidenz bei hoher Prätestwahrscheinlichkeit für den Nachweis und die Schweregradbestimmung einer SBAS auf.5 Auch lassen sich hier im klinischen Alltag, durch die einfache Möglichkeit, mehrere Nächte beim gleichen Patienten zu messen, die Unsicherheiten der Nacht-zu-Nacht-Variabilität umgehen.
Abb. 1: Darstellung und Erkennung von Apnoen im PAT-Signal (modifiziert nach Schnall RP et al. 2022)13
„Wearables“
Unter „Wearables“ versteht man Geräte, die vom Endverbraucher selbst gekauft und am Körper getragen werden und physiologische Messwerte direkt an intelligente Geräte (z.B. Smartphones oder Tablets) übertragen. Die sicherlich bekanntesten Wearables werden wie eine Uhr (Apple Watch, Garmin, Polar) oder Armband (WHOOP) am Handgelenk getragen. Außerdem gibt es z.B. das Oura-System, welches wie ein Ring am Finger getragen wird, oder das Somfit-System, das als Pflaster auf der Stirn angeklebt wird.
Die physiologischen Messwerte, die von o.g. Wearables gemessen werden, sind zum einen Aktigrafiedaten, generiert über Beschleunigungsmesser (Apple, Garmin, Polar, WHOOP) und zum anderen Photoplethysmografiedaten (Blutvolumen) mithilfe von grünen und/oder roten LED, die mit Photodioden gekoppelt sind. Bei Somfit werden über das Pflaster sowohl Signale der Gehirnaktivität, Augenbewegung als auch des Muskeltonus und des Blutvolumens über Elektroden ermittelt. Diese Wearables unterscheiden sich in ihrer Messgenauigkeit bezüglich der Schlafdiagnostik untereinander sehr.15,16 Die erfassten Daten werden dann von jeweils herstellerspezifischen Algorithmen verarbeitet, die jedoch auch auf Anfrage von Studienautoren bisher nicht offengelegt wurden.
Die Erkennung von Wachheit im Schlaf ist aufgrund der Ähnlichkeit der Bewegungen zwischen ruhigem Wachzustand und Schlaf schwierig. Es ist daher notwendig, dass Geräte, die in der Schlafdiagnostik eine Rolle spielen möchten, ihre proprietären Algorithmen verfeinern, um Wachheit anhand anderer Parameter als nur Bewegung zu erkennen (z.B. Herz-frequenz und Herzfrequenzvariabilität).6
In einer Studie von Miller et al. zeigten sich im Test von 6 verschiedenen Wearables (Apple WatchOS 6, GarminForerunner 245 Music, Polar Vantage V, OuraRing Generation 2, WHOOP 3.0 and Somfit) im Vergleich zur PSG eine hohe relative Übereinstimmung bei der Schätzung der Herzfrequenz und eine mäßige bis hohe relative Übereinstimmung bei der Herzfrequenz-variabilität.7 Da dadurch eine Unterscheidung zwischen Wachzustand und Schlaf gut möglich ist, ist auch die Messung der Schlafdauer sehr akkurat, aber die Unterscheidung der verschiedenen Schlafstadien erfordert noch weitere Verbesserung.
Im Vergleich zur PSG gibt es aktuell nur zwei Systeme (Somfitund Apple WatchOS 9), denen es möglich ist, eine Unterscheidung zwischen 5 Zustandskategorien zu treffen (wach, N1, N2, N3 und REM-Schlaf). Für die restlichen Systeme sowie die Vorgängermodelle bis watchOS 8 ist dies nur bedingt möglich, da die Geräte nur über eine 3-Zustands-Kategorisierung (wach/ leichter Schlaf/Tiefschlaf) bzw. 4-Zustands-Kategorisierung (wach/leichter Schlaf/Tiefschlaf/REM-Schlaf) verfügen.7,8
Die Auswertung des Mehrphasenschlafes nur mithilfe eines Wearables ist schwierig. Hier erreichen die Geräte im Vergleich zur PSG nur eine Übereinstimmung von 50 bis 65%. Lediglich die Apple Watch scheint sich mit dem Update auf watchOS9 von der Konkurrenz abzuheben und erreicht eine überdurchschnittliche Klassifikation des Mehrphasenschlafs.8
Die Wearables aktuell auf dem Markt unterliegen ständiger Verbesserungen und Neuerungen der Systeme. Unter anderem aufgrund dessen ist es aber auch sehr schwierig, hier unabhängige Validierungsstudien durchzuführen.
Akustische Analyse zur SBAS-Diagnostik
Eine weitere vielversprechende Methode zur Diagnostik der SBAS, die nach Jahren der Grundlagenforschung Einzug in die Praxis gehalten hat, ist die akustische Analyse von Atemgeräuschen. Dieser innovative Ansatz ermöglicht eine qualitativ hochwertige Diagnostik mit minimaler Invasivität und teilweise sogar mit patienteneigener Hardware.9
Während einige Produkte auf die Aufzeichnung der Atemgeräusche über ein Bluetooth-basiertes Körperschall-Mikrofon setzen, welches oberhalb des Jugulums angebracht wird (AcuPebble), nutzen andere ausschließlich die in modernen Smartphones eingebauten Mikrofone (Somnofox/Snorefox; als App erhältlich). Allen Ansätzen ist gemein, dass die Analyse der akustischen Eigenschaften der Schlaf-Atemgeräusche nach der Übertragung des Datensatzes am nächsten Morgen in der Cloud mithilfe von trainierten Machine-Learning-Modellen erfolgt.14
Für die Software Somnofox/Snorefox wurde eine der bisher weltweit größten Datenbanken mit Schnarchgeräuschen und korrespondierenden medikamenteninduzierten Schlaf-Videoendoskopien (DISE) verwendet, um ein Machine-Learning-Modell bzgl. der Zuordnung von Schnarchgeräuschen mit der zugehörigen Vibrationsebene zu trainieren. Auf die Auswertung von Schlaf-Videoendoskopien spezialisierte HNO-Ärzte analysierten für diese Datenbank mittels DISE den Ort der Vibrationen der oberen Atemwege. Sowohl das AcuPebble-System als auch das Snorefox/Somnofox-System wurden in klinischen Studien gegen etablierte Systeme (PG/PSG) validiert und haben beide eine CE-Zulassung als Medizinprodukt.10,11
In der Praxis bieten die Messung und Analyse nächtlicher Atemgeräusche zur Diagnose schlafbezogener Atmungsstörungen einige potenzielle Vorteile: Bei der Verwendung eines Smartphone-Mikrofons ist z.B. kein direkt am Körper befestigter Sensor erforderlich, was den Schlafkomfort erhöht und den natürlichen Schlaf nicht beeinflusst. Außerdem ergibt sich durch die Nutzung des eigenen Smartphones die Möglichkeit, mit akustischen Methoden das nächtliche Atemverhalten über mehrere Nächte oder aber auch über einen längeren Zeitraum und in Abhängigkeit von den Tagesaktivitäten zu beobachten. Insbesondere bei kontaktlosen Technologien ist die Hemmschwelle der Patienten, diese über einen längeren Zeitraum zu nutzen, geringer. So können Abweichungen im nächtlichen Atemverhalten beobachtet werden, die bei Messungen über nur eine oder wenige Nächte nicht erfasst werden können.
Die Erhebung von Daten zum Ort der Vibrationen des oberen Atemwegs über mehrere Nächte und nicht nur während eines medikamentös herbeigeführten Schlafs wird zweifelsfrei einen völlig neuen Einblick in das Verhalten des oberen Atemwegs bei OSA-Patienten liefern.
Eine prinzipielle Einschränkung der rein akustischen Messung ist die fehlende Information über die Sauerstoffsättigung, die aber nach den gültigen Definitionen der AASM bzw. DGSM zur Erkennung einer Hypopnoe – und damit zur wichtigen Abgrenzung zur Schlafapnoe – herangezogen werden muss. Eine rein akustische Messung kann daher den Schweregrad einer Schlafapnoe nur approximieren, somit aber eine wertvolle Ergänzung zur leitliniengerechten Diagnostik darstellen.
Literatur:
1 Benjafield AV et al.: Estimation of the global prevalence and burden of obstructive sleep apnoea: a literature-based analysis. Lancet Respir Med 2019; 7(8): 687e98 2 Stuck BA et al.: Praxis der Schlafmedizin. 3. Auflage. Heidelberg: Springer-Verlag, 2017: 317-26 3 Fietze I et al.: Management of obstructive sleep apnea in Europe – A 10-year follow-up. Sleep Medicine 2022; 97: 64-72 4 Lechat B et al.: Multinight prevalence, variability, and diagnostic misclassification of obstructive sleep apnea. Am J Respir Crit Care Med 2022; 205(5): 563-9 5 Stuck BA et al.: Teil-Aktualisierung S3-Leitlinie Schlafbezogene Atmungsstörungen bei Erwachsenen. Somnologie 2020; 24: 176-208 6 Sargent C: How well does a commercially available wearable device measure sleep in young athletes? Chronobiol Int 2018; 35(5): 754-8 7 Miller DJ et al.: A validation of six wearable devices for estimating sleep, heart rate and heart rate variability in healthy adults. Sensors 2022; 22(16): 6317 8 The Quantified Scientist: Validations of Apple Watch‘s new sleep staging as compared to Dreem‘s EEG based sleep staging. 2022; www.youtube.com/watch?v=LPqtfC70QTU ; zuletzt aufgerufen am 4.8.2023 9 Kang C: Age-integrated artificial intelligence framework for sleep stage classification and obstructive sleep apnea screening. Front Neurosci 2023; 17:105918 10 Devani N: Accuracy and usability of AcuPebble SA100 for automated diagnosis of obstructive sleep apnoea in the home environment setting: an evaluation study. BMJ Open 2021; 11: e046803 11 Heiser C.: Evaluierung einer Smartphone-basierten Methode zum Risikoscreening auf obstruktive Schlafapnoe (OSA) basierend auf einem multiparametrischen Modell akustischer und anamnestischer Parameter. Abstractband Laryngo-Rhino-Otologie 2022; doi: 10.1055/s-0042-1747043 12 Punjabi NM et al.: Variability and misclassification of sleep apnea severity based on multi-night testing. Chest 2020; 158(1):365-73 13 Schnall RP et al.: Peripheral arterial tonometry-PAT technology. Sleep Med Rev 2022; 61: 101566 14 Mallick S et al.: Sleep apnea detection system using machine learning on resource-constrained devices. IEEE International Systems Conference (SysCon) 2023; doi: 10.1109/SysCon53073.2023.10131117 15 Task Force of the European Society of Cardiology and the North American Society of Pacing and Electrophysiology: Heart rate variability, standards of measurement, physiological interpretation, and clinical use. Circulation 1996; 93:1043-65 16 Marino M: Measuring sleep: accuracy, sensitivity, and specificity of wrist actigraphy compared to polysomnography. Sleep 2013; 36(11): 1747-55
Das könnte Sie auch interessieren:
Morbus Menière – der Pathomechanismus des Hydrops
Schon im 19. Jahrhundert sah man einen Zusammenhang zwischen Schwindel, Hörverlust und Tinnitus, verursacht von pathologischen Vorgängen im Innenohr. Knapp 80 Jahre später wurde der ...
Wie Coaching den Fachärztemangel an medizinischen Abteilungen angehen kann
Hohe Arbeitsbelastung, Stress, schlechte Stimmung: An vielen Spitalskliniken ist das die tägliche Realität. Es ist daher nicht verwunderlich, dass viele Fachärzt:innen den Weg in die ...
AC102: ein vielversprechender Wirkstoffkandidat bei Hörsturz
Hörsturz führt häufig zu dauerhaftem Hörverlust und Begleiterkrankungen wie Tinnitus. Glukokortikoide werden für den Off-Label-Einsatz verschrieben, obwohl es keine klinischen Beweise ...