Immuncheckpoint-Inhibitoren: eine neue Ära der onkologischen Therapie
Autor:
Dr. med. Raphaël Delaloye
Kaderarzt
Mitglied Tumorzentrum
Onkologie
Universitätsspital Basel
E-Mail: Raphael.Delaloye@usb.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Onkologie ist eines der sich am schnellsten entwickelnden Gebiete der Medizin. Zu den neueren Entwicklungen gehören die Immuncheckpoint-Inhibitoren, die bereits in zahlreichen Indikationen zur Anwendung kommen. Erfahren Sie, was Allgemeininternisten über die Wirkungsweise, mögliche Nebenwirkungen und die Indikationen der aktuell zugelassenen Immuncheckpoint-Inhibitoren wissen sollten.
Keypoints
-
Gewisse Tumorzellen exprimieren Oberflächenrezeptoren, die es ihnen ermöglichen, über den PD-1-Signalweg die zelluläre Immunabwehr zu bremsen und damit die Immunkontrolle zu umgehen.
-
Durch die Blockade dieser Rezeptoren durch Immuncheckpoint-Inhibitoren kann die antitumorale Immunantwort reaktiviert werden.
-
Nebenwirkungen werden oft durch eine überschiessende Reaktion des Immunsystems verursacht.
Vor etwa zehn Jahren begann mit der Markteinführung von Ipilimumab zur Behandlung des metastasierten Melanoms ein neues Zeitalter in der Onkologie. Die Ergebnisse waren verblüffend: Bei Patienten mit einer fortgeschritten metastasierten Erkrankung zeigte sich in knapp 20% der Fälle ein hervorragendes und lang anhaltendes Ansprechen, hin bis zur kompletten Remission.1 Mittlerweile werden durch die Kombination verschiedener Substanzen noch höhere Remissionsraten erreicht, und es kommen jedes Jahr neue Indikationen für die Behandlung onkologischer Erkrankungen mit sogenannten Immuncheckpoint-Inhibitoren (häufig vereinfacht als Immuntherapie bezeichnet) dazu.
Möglich wurde diese Entwicklung durch die Entdeckung und Hemmung der Rezeptoren CTLA-4 und PD-1/PD-L1 durch James Allison und Tasuku Honjo Anfang der 1990er-Jahre, wofür sie 2018 den Nobelpreis für Medizin und Physiologie erhielten. CTLA-4 («cytotoxic T-lymphocyte-associated protein 4») und PD-1/PD-L1 («programmed cell death 1/ligand 1») sind wichtige Oberflächenrezeptoren im Zusammenhang mit der Regulation der Immunantwort. Sie haben eine hemmende Wirkung auf das Immunsystem, sodass eine überschiessende Reaktion vermieden werden kann, wenn das Immunsystem durch Pathogene aktiviert wird. Wenn diese Aktivierung durch maligne Tumorzellen erfolgt, ist eine Hemmung der Immunantwort kontraproduktiv und begünstigt die weitere Vermehrung der bösartigen Zellen.
Immunsystem und Krebsentwicklung
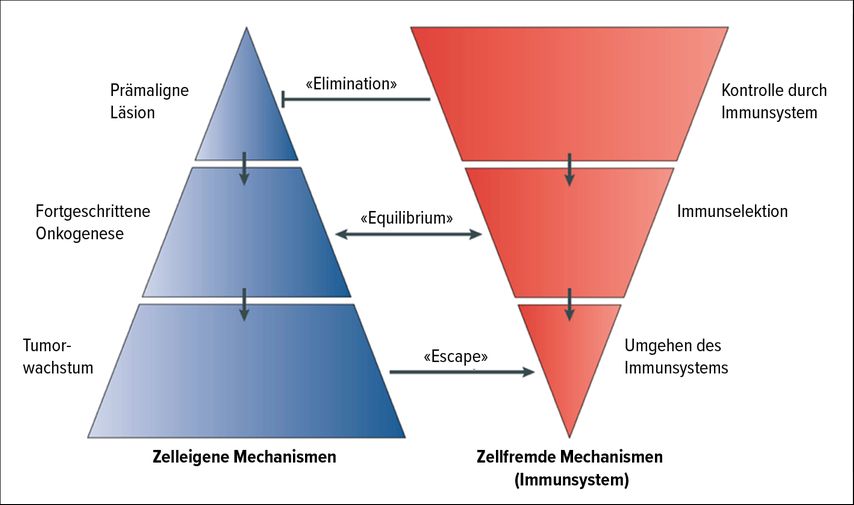
Damit eine Krebserkrankung überhaupt zustande kommt, müssen verschiedene Bedingungen erfüllt sein. Tumorzellen entstehen durch eine Reihe von Mutationen, durch welche sie sich gewisse Fähigkeiten aneignen, wie die Unsterblichkeit (Antiapotose), die unkontrollierte Proliferation sowie die Angiogenese und die Migration ausserhalb des ursprünglichen Gewebes. Diese Entwicklung wird im gut etablierten Modell der Adenom-Karzinom-Sequenz widergespiegelt. Mittlerweile wurde ein weiterer zentraler Aspekt in der Onkogenese beschrieben, nämlich die Fähigkeit, die Kontrolle durch das Immunsystem zu umgehen. Im normalen Zustand der sogenannten «Immunosurveillance» werden mutierte Zellen, bei welchen keine Apoptose stattfindet, durch eine Reihe von Mechanismen von den zytotoxischen T-Zellen erkannt und eliminiert (Abb. 1).2 Dieser Schutz verhindert möglicherweise tagtäglich die Entwicklung von Tumoren, ohne klinisch bemerkbar zu werden («Elimination»). Allerdings kann manchmal die Tumorentwicklung nicht ganz verhindert werden, nämlich dann, wenn eine Präkanzerose in einem Organ oder beispielsweise eine monoklonale Gammopathie unklarer Signifikanz (MGUS) vorliegt. Solche Präkanzerosen oder MGUS können während Jahren stabil bleiben, ohne dass sich daraus ein invasives Karzinom oder ein Plasmazellmyelom entwickelt. Es herrscht hier ein Gleichgewicht zwischen der Onkogenese und der Immunantwort, die Tumorzellen werden jedoch nicht gänzlich eliminiert («Equilibrium»). Aus dieser Situation kann sich ein invasives Karzinom entwickeln, wenn neue Mutationen dazukommen, welche die Kontrolle durch das Immunsystem umgehen, oder wenn eine tumorspezifische Immuntoleranz erreicht wird («Escape»). Angesichts der zentralen Rolle des Immunsystems scheint eine Modulation der Immunantwort als Therapie einer Tumorerkrankung naheliegend.
Wirkungsweise der Immuncheckpoint-Inhibitoren
Immuncheckpoint-Inhibitoren sind spezifische monoklonale Antikörper, die gegen CTLA-4, PD-1 oder PD-L1 gerichtet sind. Diese Rezeptoren befinden sich entweder auf T-Zellen (CTLA-4) oder sowohl auf T-Zellen als auch auf antigenpräsentierenden Zellen (APC) und Tumorzellen (PD-1, PD-L1). Die Blockade dieser Rezeptoren verhindert die Hemmung der Immunantwort, also des natürlichen Kontrollmechanismus. Dadurch wird die Immunreaktion gegen Tumorzellen stimuliert. Das Ziel ist es, von einer «Escape»-Situation zurück in ein Gleichgewicht oder gar eine komplette Elimination der Tumorzellen zu kommen.
Der Erfolg einer solchen Therapie ist von verschiedenen Faktoren abhängig. Erstens hängt die Wirksamkeit mit der Relevanz der involvierten Mechanismen zusammen. Bei Tumorzellen, die keine PD-1 oder PD-L1 an ihrer Oberfläche exprimieren, wird die alleinige Blockade dieser Rezeptoren kaum Wirksamkeit zeigen. Zweitens müssen die Immunzellen in das Tumorgewebe eindringen können, um dort eine Immunantwort auslösen zu können. Dies hängt vom sogenannten «Microenvironment» ab, also vom Stroma und von der Umgebung der Tumorzellen.3 Lymphozyten, die in das Tumorgewebe eindringen können, werden als TIL («tumor infiltrating lymphocyte») bezeichnet. Werden im Tumor keine oder nur wenige TIL festgestellt, dann ist auch hier von keiner grossen Wirksamkeit der Immuntherapie auszugehen (man spricht von einer Immunwüste oder «immune desert»). Lymphozytäre Infiltrate im Tumorgewebe werden insbesondere durch das Vorhandensein multipler Mutationen in den Tumorzellen begünstigt. Je mehr Mutationen vorliegen, desto mehr Neo-Antigene werden produziert, was zu einer erhöhten Mobilisation der T-Lymphozyten führt. Man spricht von einer hohen Mutationlast im Tumor («tumor mutational burden» oder TMB).4
Um die Wirksamkeit der Immuncheckpoint-Inhibitoren zu erhöhen, werden diese entweder mit weiteren Immuncheckpoint-Inhibitoren kombiniert (insbesondere Anti-CTLA-4 mit Anti-PD-1)5 oder zusammen mit einer konventionellen Chemotherapie verabreicht.6,7 Die gleichzeitige Gabe einer Chemotherapie führt zu einer höheren Antigenfreisetzung durch die Zerstörung von Tumorzellen, was eine Entzündungsreaktion und eine Immunantwort begünstigen kann. Durch diese Strategie können deutlich höhere Ansprechraten und ein verlängertes Überleben in verschiedenen metastasierten Situationen erreicht werden.
Nebenwirkungen
Es liegt auf der Hand, dass Nebenwirkungen der Immuncheckpoint-Inhibitoren durch eine überschiessende Reaktion des Immunsystems verursacht werden. Prinzipiell kann jedes Organ autoimmun angegriffen werden, und diese Reaktion kann entweder durch Kreuzantigene oder unspezifisch ausgelöst werden. Der Schweregrad einer immunvermittelten Nebenwirkung wird anhand der CTCAE-Tabelle graduiert («common terminology criteria for adverse events»).8 Die Graduierung geht von milden (Grad 1–2) über schwere Symptome (Grad 3–4) bis zum Tod (Grad 5). Immunvermittelte Nebenwirkungen kommen in 65–85% der Fälle vor und sind meistens mild. Schwerwiegende Nebenwirkungen kommen in 15–30% der Fälle vor.9 Todesfälle sind selten (bis zu 1% der Fälle). Nebenwirkungen sind bei kombinierten Therapien häufiger (Kombination zweier Immuncheckpoint-Inhibitoren oder eines Immuncheckpoint-Inhibitors mit einer Chemotherapie). Typischerweise treten Nebenwirkungen verzögert auf, meist einige Wochen bis wenige Monaten nach der ersten Verabreichung.10 Am häufigsten kommen kutane und gastrointestinale Nebenwirkungen vor. Milde Reaktionen wie ein Exanthem mit oder ohne Juckreiz können topisch mit Antihistaminika oder Steroiden angegangen werden. Milde Durchfälle können mit Loperamid oder Opiumtinktur behandelt werden. Auch hier können Steroide mit topischer Wirkung (z.B. Budenosid) zum Einsatz kommen. Dabei kann die Immuntherapie fortgeführt werden, wenn die Symptome kontrolliert werden können. Schwererwiegende Nebenwirkungen wie eine Erhöhung der Transaminasen oder des Kreatinins, eine Troponinämie oder Atembeschwerden verlangen die sofortige Unterbrechung der Therapie und den raschen Einsatz von Steroiden (meist Prednison 2mg/kgKG, eventuell initial intravenös, insbesondere bei möglicher Resorptionsstörung im Falle einer immunvermittelten Kolitis). Grundsätzlich empfehlen sich in dieser Situation immer die Konsultation eines Fachspezialisten und das Anstreben einer Biopsie zur Bestätigung der Verdachtsdiagnose und zum Ausschluss einer weiteren Ursache für die Befunde (Tumorprogression, Reaktivierung einer viralen Erkrankung usw.). Selten sind immunvermittelte Reaktionen refraktär gegenüber Steroiden und benötigen zusätzlich Immunsuppressiva wie TNF-α-Blocker (Infilximab) oder Mycofenolat mofetil. Darunter, wie auch unter systemischen Steroiden, soll eine Pneumocystis-jirovecii-Pneumonie-Prophylaxe durchgeführt werden (beispielsweise Cotrimoxazol p.o. dreimal wöchentlich). Die Dauer der Therapie richtet sich nach der Kontrolle der immunvermittelten Reaktion. In der Regel werden Steroide innert weniger Wochen langsam reduziert und schliesslich komplett sistiert. Manchmal kann danach eine Reexposition mit dem Immuncheckpoint-Inhibitor versucht werden, je nach klinischer Dringlichkeit.
Eine absolute Kontraindikation für eine Therapie mit Immuncheckpoint-Inhibitoren ist die Transplantation von soliden Organen wie Herz oder Leber. Nierentransplantierte Patienten können im Einzelfall eine Immuntherapie erhalten, im Wissen, dass diese zur Abstossung des Transplantats führen kann (bei 25–50% der Patienten).11 Weitere relative Kontraindikationen sind bestehende, therapiebedürftige Autoimmunerkrankungen und jede medizinische Situation, die den Einsatz von Immunsuppressiva benötigt. Grundsätzlich soll eine Risikoabwägung erfolgen und mit dem Patienten besprochen werden. Die Immunsuppression sollte sistiert werden, bevor Immuncheckpoint-Inhibitoren zum Einsatz kommen. Eine niedrig dosierte Therapie mit Steroiden (bis 10mg Prednison oder Äquivalent täglich) kann beibehalten werden, ohne nennenswerten Einfluss auf die Immuntherapie.
Eine besondere Situation stellt die endokrine Dysfunktion dar. Die häufigste istdie immunvermittelte Thyroiditis.9 Diese kommt in circa 5% der Fälle vor und äussert sich klinisch in Form einer Hypothyreose (selten einer transienten Hyperthyreose). Weitere endokrine Störungen sind deutlich seltener. Beispielsweise können ein immunvermittelter Diabetes mellitus, eine Nebennierenrindeninsuffizienz (Hypokortisolismus) oder ein Panhypopituitarismus vorkommen. In der Regel wird in solchen Fällen die Immuntherapie fortgesetzt und eine Hormonsubstitution etabliert.
Anwendungsbereich
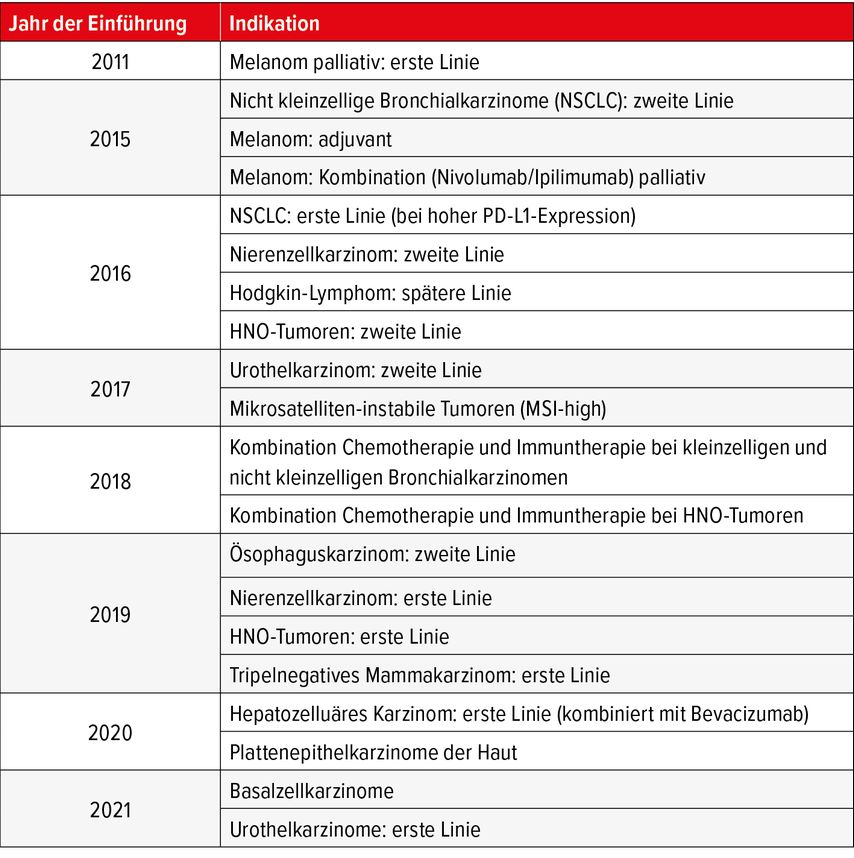
Wie häufig in der Onkologie, wurden Immuncheckpoint-Inhibitoren initial in der Zweitlinientherapie bei metastasierten Tumorerkrankungen untersucht und zugelassen. Rasch rückte aber die Anwendung in die erste Linie vor und hat heute bereits einen Platz in der adjuvanten oder gar neoadjuvanten Situation gefunden.12 Tumoren mit einer naturgemäss hohen Mutationslast («TMB high»), wie das maligne Melanom oder das nicht kleinzellige Bronchialkarzinom, zeigen die höchste Rate des Ansprechens auf eine alleinige Immuntherapie. Das Gleiche gilt für Patienten mit einer Dysfunktion der Reparaturproteine, die für die Korrektur von Kopierfehlern bei der DNA-Replikation zuständig sind. In diesem speziellen Fall akkumulieren sich multiple Mutationen, die schliesslich zur Tumorerkrankung führen. Man spricht von Mikrosatelliten-Instabilität (MSI), was angeboren (im Falle des sogenannten Lynch-Syndroms) oder erworben (nur im Tumorgewebe) vorkommen kann. Auch diese Patienten profitieren von einer alleinigen Immuntherapie.13,14 Tumorerkrankungen, die auf das Rauchen zurückzuführen sind, sprechen ebenfalls häufiger auf eine Therapie mit Immuncheckpoint-Inhibitoren an, da das Rauchen multiple Mutationen und somit eine grosse Anzahl von Neo-Antigenen verursacht. Tabelle 1 präsentiert eine (nicht vollständige) Liste der häufigsten Indikationen für eine Immuntherapie. Laufend ergeben sich aber neue Anwendungsmöglichkeiten und Zulassungen für die Immuncheckpoint-Inhibitoren.
Tab. 1: Die häufigsten Indikationen für eine Therapie mit einem Immuncheckpoint-Inhibitor (eine Auswahl)
Zusammenfassung
Das bessere Verständnis für die Rolle des Immunsystems in der Entstehung bösartiger Erkrankungen hat in den letzten Jahren die Entwicklung neuer immunmodulierender Therapien wie der Immuncheckpoint-Inhibitoren ermöglicht. Dadurch wurden etliche Therapiestandards neu definiert und die Prognose vieler Tumorarten wurde verbessert. Weitere Immuncheckpoints wurden mittlerweile identifiziert und neue Substanzen entwickelt, um diese Wege ebenfalls zu blockieren. Weitere vielversprechende Möglichkeiten, wie Vakzine und genetisch modifizierte T-Lymphozyten (CAR-T), die ebenfalls das Gleichgewicht zwischen Tumor und Immunsystem wiederherzustellen vermögen, werden zugelassen. Neue Therapien bringen aber neue Nebenwirkungen mit sich, die früh erkannt und therapiert werden müssen. Die sich rasch ändernde Therapielandschaft stellt zudem eine grosse Herausforderung für die Zulassungsbehörden, die Kostenträger und die Therapeuten dar, welche den Patienten die bestmögliche Behandlung anbieten wollen. Insgesamt sind diese neuen Therapieansätze grosse Hoffnungsträger in Bezug auf die Verbesserung der Prognose onkologischer Erkrankungen.
Literatur:
1 Hodi FS et al.: N Engl J Med 2010; 363: 711-23 2 Zitvogel L et al.: Nat Rev Immunol 2006; 6: 715-27 3 Hegde PS et al.: Clin Cancer Res 2016; 22: 1865-74 4 Alexandrov LB et al.: Nature 2013; 500: 415-21 5 Postow MA et al.: N Engl J Med 2015; 372: 2006-17 6 Gandhi L et al.: N Engl J Med 2018; 378: 2078-92 7 Paz-Ares L et al.: N Engl J Med 2018; 379: 2040-51 8 National Cancer Institute: Cancer therapy evaluation program. https://ctep.cancer.gov/ 9 Haanen JBAG et al.; ESMO Guidelines Committee: Ann Oncol 2017; 28 (suppl_4): iv119-42 10 Weber JS et al.: J Clin Oncol 2012; 30: 2691-7 11 Owoyemi I et al.: Cancer 2020; 126: 4780-7 12 Antonia SJ et al.: . N Engl J Med 2017; 377: 1919-29 13 Le DT et al.: Science 2017; 357: 409-13 14 André T et al.: N Engl J Med 2020; 383: 2207-18
Das könnte Sie auch interessieren:
Klimakosten im Gesundheitswesen – eine massiv unterschätzte Folge der Erderwärmung
Auch wenn sich viele Konsequenzen erst langfristig zeigen: Die klimatischen Veränderungen haben Folgen für unsere Gesundheit. Dennoch werden die Gesundheit und die Gesundheitskosten in ...
Was tun bei Medikamentenunverträglichkeit?
Wenn Patientinnen und Patienten in die Praxis kommen und über eine Medikamentenunverträglichkeit klagen, gilt es herauszufinden, ob dies tatsächlich der Fall ist. Wie man dabei vorgeht ...
Der Tiefenrausch ist eine häufige Ursache für einen Tauchunfall
Atemgase verändern sich in der Wassertiefe physikalisch, was physiologische und medizinische Folgen bei Taucher:innen haben kann. Sauerstoff beispielsweise wird beim Abtauchen in der ...