Highlights zum Nierenzellkarzinom vom ASCO20 Virtual
Obwohl es auf der diesjährigen virtuellen Jahrestagung der ASCO beim Nierenzellkarzinom (RCC) keinen Paradigmenwechsel gab, wurden viele interessante und klinisch relevante Präsentationen vorgestellt. Darunter waren Themen zur Erstlinientherapie des metastasierten klarzelligen und nicht klarzelligen RCC sowie Therapieergebnisse nach Immuntherapie-Vorbehandlung. Neue Daten wurden auch im Bereich der Lokaltherapie des RCC präsentiert.
First-Line-Standardtherapie des metastasierten Nierenzellkarzinoms
Aktuell stellen Immuntherapie(IO)-Kombinationen die Standardtherapie in der Erstlinie dar. Für Patienten mit intermediärem oder ungünstigem IMDC-Risiko kann eine duale Immuntherapie mit Nivolumab und Ipilimumab gewählt werden. Patienten aller IMDC-Risiko-Scores sind zudem Kandidaten für eine Kombination aus Pembrolizumab und Axitinib (PA). Beide Kombinationen sind für das jeweils erwähnte Patientenprofil zugelassen; einen „Head-to-head“-Vergleich gibt es nicht, daher kann für die große Population der Gruppe mit intermediär-ungünstigemIMDC-Risiko keine Empfehlung für die eine oder andere Wahl in der Erstlinie ausgesprochen werden.
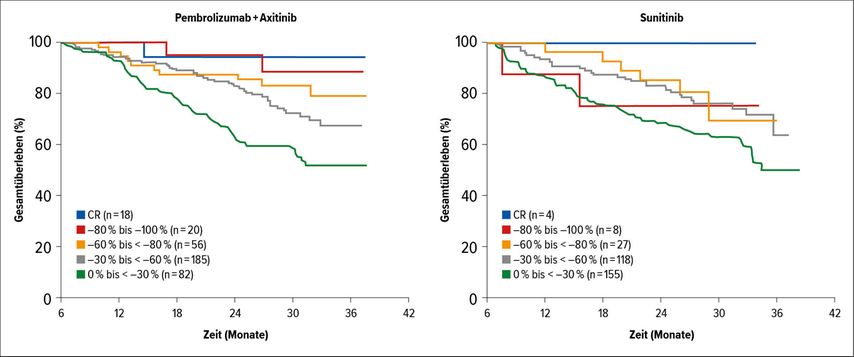
Zur jüngeren Studie, der KEYNOTE-426 mit PA versus Sunitinib (Sun), wurden Daten zum 30-Monate-Follow-up vorgestellt.1 Demnach war der Vorteil beim Gesamtüberleben (OS) (Abb. 1), beim progressionsfreien Überleben (PFS) und bei den Responseraten (ORR) auch bei diesem längeren Follow-up für den Arm PA statistisch signifikant erhalten. Der initiale OS-Benefit der Subgruppe „favorable IMDC risk“ konnte im längeren Follow-up nicht mehr beobachtet werden, jedoch muss eingeschränkt werden, dass diese Analyse nicht gepowert war, um einen OS-Benefit zu erkennen. Bemerkenswert ist jedoch, dass die Rate an Komplettremissionen in dieser Subgruppe bei 11% lag, was die höchste jemals berichtete Komplettremissionsrate bei Patienten mit günstigem IMDC-Risiko darstellt.
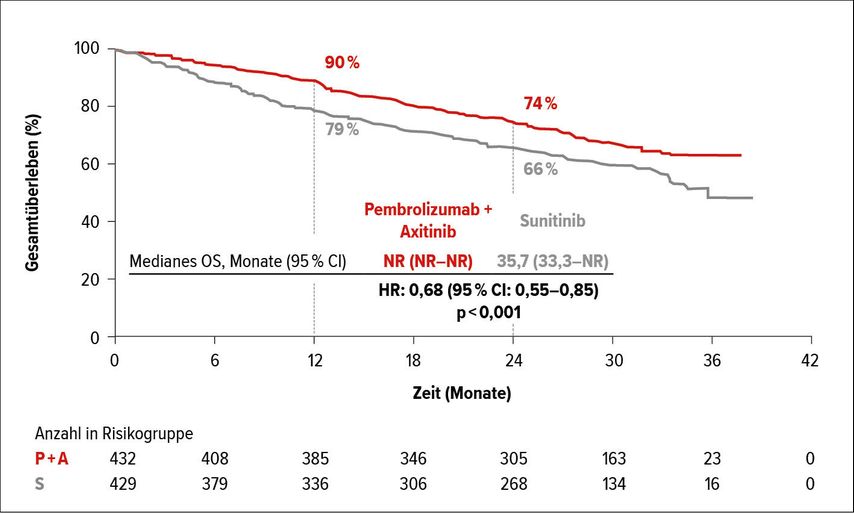
Abb. 1: Gesamtüberleben in der KEYNOTE-426-Studie (nach Plimack ER et al.)1
Interessant sind auch die Daten zur Korrelation der Responsetiefe mit dem OS (Abb. 2). Demzufolge hatten Patienten mit Remission >80% unter PA den gleichen Überlebens-Benefit wie jene mit Komplettremission, während Patienten mit Remissionen >80% im Sun-Arm ein deutlich kürzeres OS als CR-Patienten hatten. Auch Patienten mit einer 60–80%igen Tumorreduktion hatten mit PA gegenüber Sun einen Überlebensvorteil.
Daten zur First-Line-Monotherapie mit Immuncheckpoint-Inhibitoren (Non-Standard)
Die KEYNOTE-427-Studie ist eine Phase-II-Studie mit Pembrolizumab-Monotherapie in der FirstLine bei Patienten mit klarzelligem (Kohorte A) und nicht klarzelligem RCC (Kohorte B). Für beide Kohorten wurde ein Update am ASCO gezeigt; in Kohorte A wurden eine Remissionsrate von 36,4% (27,4–46,1) und eine Clinical-Benefit-Rate (CBR) von 58,2% (48,4–67,5) erreicht.2 Bei Patienten mit sarkomatoider Differenzierung lag die ORR bei 63,6% (30,8–89,1). Enttäuschend ist jedoch die Rate an Komplettremissionen, welche bei der Gesamtpopulation bei 5,8% und bei Patienten mit sarkomatoiden Tumoren bei 0 lag. Eine Aktivität der Monotherapie besteht demnach, jedoch liegt sie im indirekten Vergleich doch unter jener der Kombination mit Axitinib. Aus diesem Grund sollte eine Monotherapie nur bei Patienten mit Kontraindikation für Axitinib in Betracht gezogen werden. Ergebnisse der Kohorte B werden im Abschnitt über nichtccRCC berichtet.
Weitere Studien haben sich damit befasst, ob man mit einer PD1-Checkpoint-Inhibition beginnen kann und nur im Falle eines insuffizienten Ansprechens (stabile Erkrankung oder Progression) mit Ipilimumab ergänzen soll (Abb. 3 und 4, Tab.1).3,4 Durch Zugabe von Ipilimumab konnte bei lediglich 13,3% bzw. 14% ein objektives Ansprechen erreicht werden; Komplettremissionen gab es keine. Diese Daten bestätigen im indirekten Vergleich zur CheckMate-214-Studie, dass Ipilimumab von Anfang an gegeben werden sollte und nicht erst bei insuffizientem Ansprechen auf Nivolumab (Tab. 1).
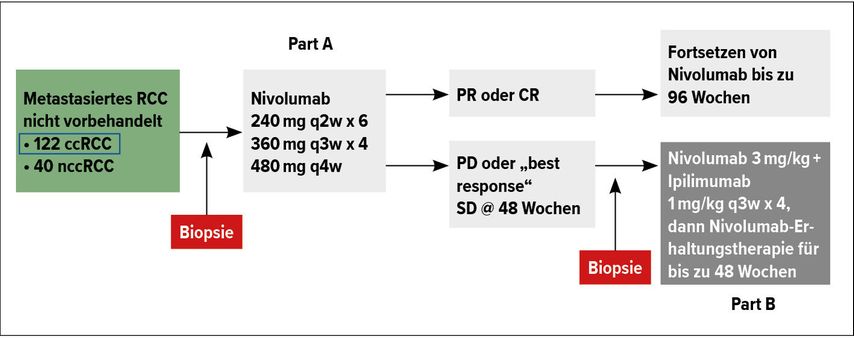
Abb. 3: Design der Studie HCRN GU16-260
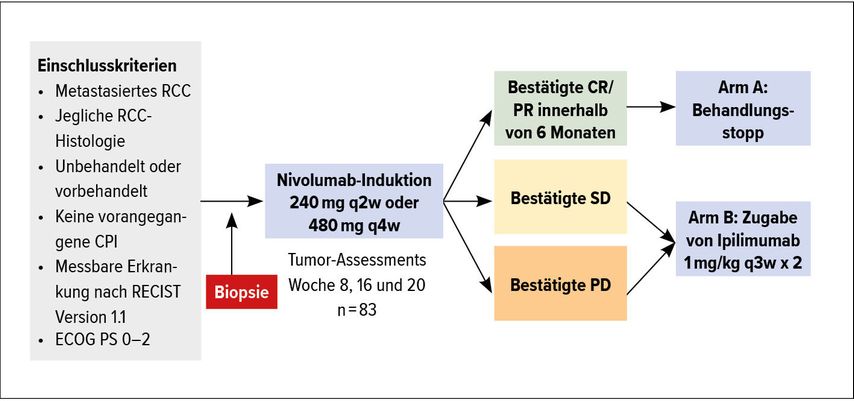
Abb. 4: Studiendesign von OMNIVORE (nach McKay R et al.)5
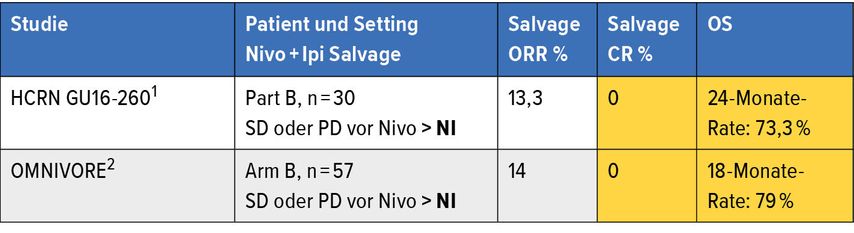
Tab. 1: Ergebnisse der Ipilimumab-Salvage-Studien (nach Atkins MB et al., McKay R et al.)3, 4
SecondLine und spätere Linien der Therapie des metastasierten Nierenzellkarzinoms
Fraction-RCC
In dieser Phase-II-Studie wurden Patienten nach IO-Vorbehandlung (Track 1: Anti-PD[-L1]-1- und Anti-CTLA4-naiv; Track2: Anti-PD[-L1]-1- oder Anti-CTLA4-vorbehandelt) mit Nivolumab+Ipilimumab nach Progression bei der Vortherapie
eingeschlossen. In dieser Analyse wurden die Ergebnisse der Track-2-Patienten präsentiert.5
Zwei Therapiearme standen zur Option: entweder Nivolumab-Ipilimumab oder eine experimentelle Therapie basierend auf einer Rationale aus einer Phase I.46 Patienten wurden in den Nivolumab+Ipilimumab-Arm randomisiert. Alle hatten zuvor eine Anti-PD(-L)-1-Therapie und keiner eine Anti-CTLA4-Therapie erhalten; 37 Patienten hatten außerdem zuvor eine TKI-basierte Therapie erhalten. Nach einem medianen Follow-up von 8,9 Monaten betrug die ORR 15,2%; Komplettremissionen wurden keine berichtet; das mediane PFS betrug 16,1 Wochen.
Lenvatinib+Pembrolizumab
Sehr vielversprechend sind die Ergebnisse einer Phase-II-Studie mit Pembrolizumab+Lenvatinib bei Patienten, die auf diverse vorangehende IO-Vortherapien progredient waren: Die Ansprechraten lagen bei 55% (45–65), die mediane Ansprechdauer lag bei 12 Monaten (9–18) und das PFS bei 11,7 Monaten (9,4–17,7).6 Das Gesamtüberleben war nicht erreicht (16,7–NR). Von den insgesamt 104 eingeschlossenen Patienten hatte der Großteil bereits 2 oder mehr Vortherapien erhalten.
Post-IO-Studien mit Tyrosinkinase-Inhibitoren
Sämtliche Studien mit TKI (Tivozanib, Sunitinib, Cabozantinib) in der späteren Linie nach IO waren deutlich weniger vielversprechend.7–9 Zwar zeigte sich bei allen Studien ein gewisses Ansprechen, jedoch durchwegs unter 30%, und auch das mediane PFS war nicht mit der Kombination Pembrolizumab+Lenvatinib vergleichbar.
Nicht klarzellige Nierenzellkarzinome und VHL-Erkrankung
SAVOIR-Studie
Die SAVOIR-Studie ist eine Phase-III-Studie mit dem selektiven MET-Inhibitor Savolitinib versus Sunitinib bei Patienten mit MET-getriebenem papillärem Nierenzellkarzinom.10 Der MET-Status des Tumors wurde zentral bestimmt; als „MET-driven“ galten Tumoren mit MET- und/oder HGF-Amplifikation, Chromosome 7 Gain und/oder MET-Kinase-Domäne-Mutationen. Die Studie wurde nach 60 Patienten vorzeitig geschlossen.
Die Ansprechraten betrugen für Savolitinib 27% und für Sunitinib 7%, das mediane PFS 7,0 bzw. 5,6 Monate; der Unterschied war nicht statistisch signifikant.
Erlotinib+Bevacizumab bei HLRCC oder sporadischem papillärem RCC
In einer Phase-II-Studie wurde die Kombination Erlotinib+Bevacizumab bei Patienten mit hereditärer Leiomyomatose und RCC (HLRCC) oder sporadischem papillärem RCC untersucht.11 Die Ergebnisse waren äußerst vielversprechend: Bei Patienten mit HLRCC war die Ansprechrate 72,1% (95%CI: 57,2–83,4) und beim sproadischen papillären RCC 35% (95%CI: 22,1–50,6). Die Responsedauer betrug 19,3 Monate. Das mediane PFS betrug in der HLRCC-Gruppe 21,1 Monate (15,6–26,6) und in der sporadischen Gruppe 8,8 Monate (5,5–15,6). Die Autoren schlussfolgerten zu Recht, dass in dieser seltenen Entität des HLRCC diese Kombination als neuer Standard betrachtet werden sollte.
Update KEYNOTE-427, Kohorte B beim nicht klarzelligen RCC
Es gab ein Update der Phase-II-Studie KEYNOTE-427, bei der in der Kohorte B Patienten mit metastasiertem nicht klarzelligem RCC in der Erstlinie mit einer Pembrolizumab-Monotherapie behandelt wurden.12 165 Patienten wurden in dieser Kohorte behandelt; die Ansprechraten betrugen 26,7%, davon erreichten 6,7% eine Komplettremission. Das mediane PFS betrug 4,2 Monate. Wie zuvor in anderen Studien mit Pembrolizumab berichtet, war die Tiefe des Ansprechens maßgeblich mit der Überlebensdauer assoziiert.
HIF-2α-Inhibitor bei VHL-assoziiertem RCC
Eine weitere beachtete Phase-II-Studie war jene mit dem HIF-2α-Inhibitor MK-6482 bei Patienten mit Von-Hippel-Lindau(VHL)-Disease-assoziiertem RCC.13 Diese autosomal dominant vererbte Erkrankung geht mit einem hohen Risiko für RCC einher (25–60%); weiters zeigen diese Patienten häufig retinale Hämangioblastome, neuroendokrine Tumoren und andere Läsionen in diversen Organen inklusive des ZNS. 61 Patienten wurden in diese Studie eingeschlossen; die Ansprechraten betrugen 27,9%.Ein objektives Ansprechen wurde auch in extrarenalen Läsionene wie jenen des ZNS, der Retina und des Pankreas beobachtet. Das mediane PFS war zum Zeitpunkt der Analyse noch nicht erreicht, die 12-Monate-PFS-Rate betrug 98,3%.
Lokaltherapien
Stereotaktische Bestrahlung (SBRT) versus Nephrektomie (TN)
In einer retrospektiven Analyse wurden die Outcomes von Patienten mit T1–T4-, N0-, M0-RCC-Tumoren, die entweder eine SBRT oder eine TN als Behandlung hatten, verglichen.14 Die Daten von 243743 Patienten wurden hierfür analysiert; 243288 wurden einer TN und 266 einer SBRT zugeführt. Die 5-Jahres-Überlebensraten waren für die TN 80% und für die SBRT 53%; in der multivariaten Analyse war die SBRT mit einem höheren Risiko für Tod assoziiert (HR: 2,05; 95%CI: 1,72–2,44; p<0,001). Nach einem Propensity Score Matching der 266 SBRT-Patienten mit 266 TN-Patienten blieb die SBRT mit einem kürzeren Überleben gegenüber TN assoziiert (HR: 1,85; 95%CI: 1,41–2,44; p<0,001). Die Autoren schlussfolgerten, dass die TN für diese Patienten der Standard of Care bleibt und die SBRT jenen Patienten vorbehalten bleiben sollte, die keine Kandidaten für eine Operation sind.
Stereotaktische Bestrahlung von Oligometastasen
Diese Phase-II-Studie beschäftigte sich mit dem Impact einer stereotaktischen Bestrahlung (SRT) bei Patienten mit Oligometastasierung und Progression unter einer 1st- oder 2nd-Line TKI-Therapie.
Patienten konnten in diese Studie eingeschlossen werden, wenn ≤5 Metastasen unter der Therapie radiologisch progredient waren. Diese Läsionen wurden dann unter temporärer Pause des TKI stereotaktisch bestrahlt und die gleiche TKI-Therapie wurde im Anschluss fortgesetzt. Endpunkte der Studie waren die lokale Kontrolle der bestrahlten Regionen, das PFS und das OS sowie die kumulative Inzidenz für einen Therapiewechsel nach Studieneintritt. 37 Patienten wurden eingeschlossen; 35 wurden zu diesem Zeitpunkt mit Sunitinib behandelt und 2 mit Pazopanib. Die mediane Therapiedauer vor Studieneintritt betrug 18,6 Monate. Die mediane biologisch effektive (BED) Dosis betrug 72Gy in 5 Fraktionen, einer SRT-Dosis von 40Gy in 5 Fraktionen entsprechend. Bestrahlte Regionen umfassten Lunge und Pleura, Lymphknoten, Nebenniere, Leber, ZNS, Milz, Knochen und Pankreas. Nach einem medianen Follow-up von 11,6 (1,8–53,5) Monaten betrug das mediane PFS ab Studieneintritt 9,6 Monate (95%CI: 7,4–20,5), wobei die Progression zum überwiegenden Teil in den nicht bestrahlten Regionen auftrat. Die 2-Jahres-Rate an lokaler Kontrolle der bestrahlten Metastasen lag bei 96%. Die 2-Jahres-Überlebensrate betrug 77%. Die kumulative Inzidenz eines Therapiewechsels betrug nach einem Jahr 47%, nach 2 Jahren 75% mit einer medianen Zeit bis zum Therapiewechsel von 12,6 Monaten. Es gab keine SRT-assoziierten Grad-3–5-Toxizitäten. Die Autoren schlussfolgerten, dass die SRT eine effektive Methode ist, um einen Therapiewechsel hinauszuzögern.
Zusammenfassung
Nach dem ASCO 2020 gibt es keine Änderung in der First-Line-Therapie des mRCC; das Follow-up der KEYNOTE-426-Studie bestätigt die Überlegenheit von Pembrolizumab+Axitinib versus Sunitinib und zeigt zudem hohe CR-Raten auch bei Patienten mit günstigem IMDC-Risiko; weiters korreliert die Responsetiefe mit dem Überleben. Wenn die First-Line-Wahl auf Nivolumab+Ipilimumab fällt, sollte Ipilimumab nicht verzögert (bei insuffizientem Ansprechen auf Nivolumab) gegeben werden, sondern „upfront“, wie es auch der Zulassung entspricht; denn die CR-Raten sind dabei im indirekten Vergleich deutlich besser.
Bei der seltenen Konstellation eines HLRCC ist die Kombination aus Bevacizumab und Erlotinib überaus aktiv, die Ansprechraten liegen bei über 70%.
In der Zweitlinie nach IO-Versagen ist die Kombination Pembrolizumab mit Lenvatinib extrem vielversprechend; eine normale TKI-Therapie wirkt bis zu einem gewissen Grad, kommt aber nicht an die eben erwähnte Kombination heran.
Stereotaxie eignet sich sehr gut zur lokalen Kontrolle bei Oligometastasierung und Progression unter einer TKI-Therapie; damit kann auch der Therapiewechsel verzögert werden. Im Falle des lokalisierten RCC bleibt die stereotaktische Bestrahlung jedoch deutlich hinter der Tumornephrektomie zurück.
Autorin:
Univ.-Prof. Dr. Manuela Schmidinger
Universitätsklinik für Innere Medizin I
Medizinische Universität Wien
E-Mail: manuela.schmidinger@meduniwien.ac.at
Literatur:
1 Plimack ER et al.: ASCO 2020, Abstr. #5001 2 McDermott DF et al.: ASCO 2020, Abstr. #5069 3 Atkins MB et al.: ASCO 2020, Abstr. #5006 4 McKay R et al.: ASCO 2020, Abstr. #5005 5 Choueiri T et al.: ASCO 2020, Abstr. #5007 6 Lee CH et al.: ASCO 2020, Abstr. #5008 7 Pal SK et al.: ASCO 2020, Abstr. #5062 8 Grande E et al.: ASCO 2020, Abstr. #5060 9 Motosugu O et al.: ASCO 2020, Abstr. #5084 10 Choueriri T et al.: ASCO 2020, Abstr. #5002 11 Srinivasan R et al.: ASCO 2020, Abstr. #5004 12 Lee et al.: ASCO 2020, Abstr. #5034 13 Jonasch E et al.: ASCO 2020, Abstr. #5003 14 Patel M et al., ASCO 2020, Abstract 5059
Das könnte Sie auch interessieren:
«Können für das Management von Bedeutung sein»
Modic Changes beschreiben Veränderungen in der Wirbelsäulen-MRT, die auf den Radiologen Dr. Michael Modic zurückgehen. Welchen Stellenwert die Veränderungen haben und wann sie ...
Nur eine von vielen Begleiterscheinungen
Warum er MRT-Veränderungen bei unspezifischen Rückenschmerzen wenig Bedeutung beimisst, erklärt Prof. Dr. med. Andreas Seekamp aus Kiel.
Modic Changes bei Rückenschmerzen
Obwohl die Erstbeschreibung fast 40 Jahre her ist, ist immer noch nicht klar, wodurch die MRT-Veränderungen entstehen und welchen Stellenwert sie für Diagnostik und Therapie haben.