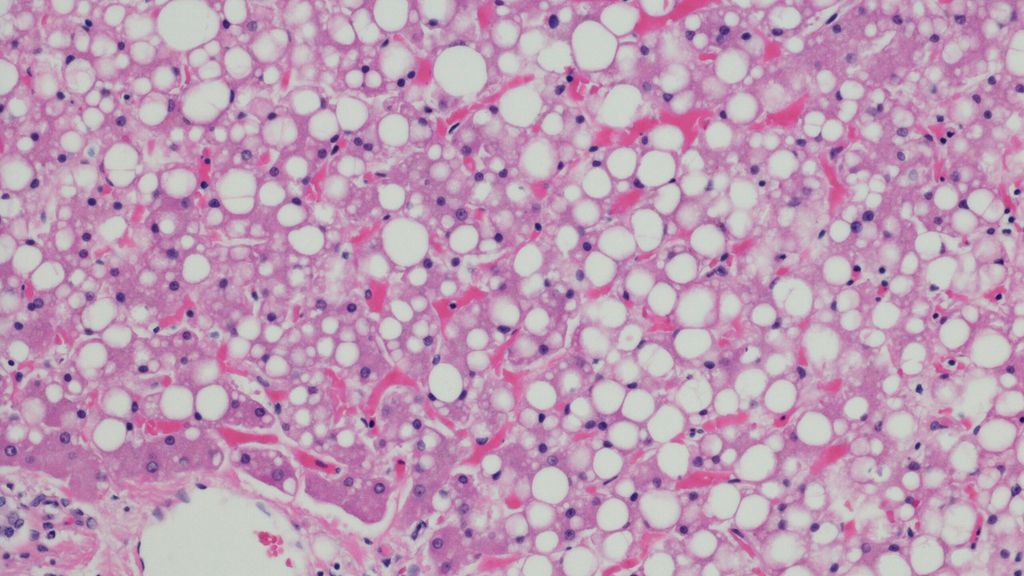
Nichtalkoholische Fettlebererkrankung: unterdiagnostiziert und unterschätzt
Autoren:
Dr. med. Sena Blümel
PD Dr. med. Christoph Jüngst
Klinik für Gastroenterologie und Hepatologie
Universitätsspital Zürich
E-Mail: sena.bluemel@usz.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die nichtalkoholische Fettlebererkrankung (NAFLD) ist eng assoziiert mit dem metabolischen Syndrom und mittlerweile die weltweit häufigste Lebererkrankung. Im Krankheitsverlauf kann die NAFLD zu einer Fibroseentwicklung bis hin zur Leberzirrhose führen. Wichtig ist es, Patienten mit einem höheren Risiko für einen progressiven Verlauf oder bereits vorliegender fortgeschrittener Leberfibrose zu identifizieren, um sie weiterführender Diagnostik und Surveillance zuzuführen.
Keypoints
-
Patienten mit Adipositas und metabolischem Syndrom haben ein hohes Risiko, eine NAFLD zu entwickeln.
-
Ein Screening dieser Risikopopulationen durch die behandelnden Hausärzte auf das Vorliegen einer NAFLD und die Einschätzung des Krankheitsstadiums ist essenziell, um eine fortgeschrittene Lebererkrankung frühzeitig zu erkennen und ihr entgegenwirken zu können.
-
Der NAFLD-Fibrose-Score und FIB-4 sind gute Screening-Methoden zur Beurteilung der Fibrose und können ohne apparativen Aufwand durchgeführt werden.
-
Die Krankheitsbezeichnung NAFLD ist derzeit in Diskussion, da begleitend auch zusätzliche Ursachen für eine Lebererkrankung vorliegen können. Um die Ätiologie zu betonen, gibt es Bestrebungen, die Erkrankung in metabolisch assoziierte Fettlebererkrankung (MAFLD) umzubenennen.
Die NAFLD ist die häufigste Lebererkrankung in der westlichen Welt. In Ländern mit hohem Anteil an Personen mit Übergewicht und Adipositas leiden circa ein Viertel bis ein Drittel der Erwachsenen an einer NAFLD. Mit der steigenden Prävalenz von Übergewicht und damit einhergehenden Erkrankungen wie Diabetes mellitus Typ 2, Dyslipidämie, Hypertonie und obstruktiver Schlafapnoe hat auch die Prävalenz der NAFLD rapide zugenommen. Während beispielsweise in den Vereinigten Staaten 2003 noch 6% der Erwachsenen von einer NAFLD betroffen waren, stieg diese Zahl bis 2011 auf 18% an und liegt aktuell bei knapp 25%.1 In den Risikopopulationen, d.h. bei Patienten mit Übergewicht und Diabetes mellitus Typ 2, liegt die Prävalenz der NAFLD sogar bei über 50%.2 Neben den genannten hauptsächlichen Risikofaktoren können auch ein rapider Gewichtsverlust, eine total parenterale Ernährung, eine Hepatitis-C-Genotyp-3-Infektion, ein Morbus Wilson und bestimmte Medikamente (z.B. Methotrexat) zur Entstehung einer Lebersteatose führen. Darüber hinaus existieren Risikogene, wie PNPLA3 («patatin-like phospholipase domain containing 3»), TM6SF2 («transmembrane 6 superfamily member 2»), HSD17B13 («17-beta hydroxysteroid dehydrogenase 13»), oder MBOAT7 («membrane-bound O-acyltransferase domain-containing 7»), die die Lebersteatose- und Fibroseentwicklung bei einem Teil der NAFLD-Patienten beeinflussen. Bei dem überwiegenden Anteil der NAFLD-Patienten liegt eine reine Lebersteatose vor und bei etwa 15–30% dieser Patienten kann sie zu einer nichtalkoholischen Steatohepatitis (NASH) fortschreiten. Bei einem Teil dieser Patienten kommt es zu einer relevanten Leberfibrose und bis zu 12% der Patienten mit NASH entwickeln in der Folge eine Leberzirrhose.2 Dadurch besteht das Risiko für eine hepatische Dekompensation und die Entwicklung eines hepatozellulären Karzinoms (HCC), was jeweils die Morbidität und Mortalität der Erkrankung deutlich erhöht. Daher ist es wichtig, Patienten mit Risiko für einen progressiven Verlauf bzw. solche mit vorhandener fortgeschrittener Fibrose zu erkennen, um diese frühzeitig zu behandeln und einem HCC-Screening zuzuführen. Die Mortalität von Patienten mit NAFLD wird allerdings im Wesentlichen durch kardiovaskuläre Erkrankungen bestimmt, sodass das kardiovaskuläre Risiko dieser Patienten jährlich überprüft werden sollte (beispielsweise mit dem Risikorechner der Schweizerischen Atherosklerose-Gesellschaft AGLA).
Screening und Diagnostik
Die Verdachtsdiagnose einer NAFLD wird nach Ausschluss anderer Ursachen einer Lebererkrankung (v.a. chronisch-virale Hepatitiden, alkoholische oder autoimmune Lebererkrankungen) und bei vorliegendem metabolischem Risikoprofil mit gleichzeitigen Hinweisen für eine Steatose in der Ultraschalluntersuchung gestellt. Die aktuellen Guidelines führen eine Leberbiopsie zum Nachweis der Steatose auf, wobei sich aufgrund der Invasivität und der hohen Patientenzahlen im klinischen Alltag o.g. Vorgehen durchgesetzt hat.3
Als nächster diagnostischer Schritt ist es wichtig abzuschätzen, ob bereits eine Leberfibrose vorliegt, da diese die Prognose des Patienten bestimmt. Unabhängig vom Vorhandensein einer entzündlichen Aktivität (NASH) haben Patienten mit vorhandener Leberfibrose eine deutlich höhere allgemeine und leberbezogene Langzeitmortalität als Patienten ohne Fibrose.4
Die Leberbiopsie ist der Goldstandard zur Fibrosediagnostik. Histologisch werden 5 Fibrosestadien unterschieden: von F0=keine Fibrose bis F4=Zirrhose. Zudem ist die Histologie die einzige Möglichkeit, um zwischen dem Vorliegen einer NAFLD und einer NASH zu unterscheiden. Bei der NAFLD sind mehr als 5% der Hepatozyten von einer Steatose betroffen.3 Bei der NASH finden sich zusätzlich ballonierte Hepatozyten und Infiltrate mit Entzündungszellen.5 Diese Veränderungen begünstigen eine Fibrosebildung bis hin zur Zirrhose. Die Leberbiopsie wird bei spezieller Fragestellung in der Regel von einem Facharzt für Gastroenterologie und Hepatologie durchgeführt. Sie kann erfolgen bei Verdacht auf eine höhergradige Fibrosierung in der nicht invasiven Fibrosediagnostik (s.u.) oder zur Differenzialdiagnostik bei möglicher gleichzeitig vorhandener anderer Ursache einer Lebererkrankung (s.o.), da dies eine Relevanz für die Therapie und Überwachung des Patienten hat.
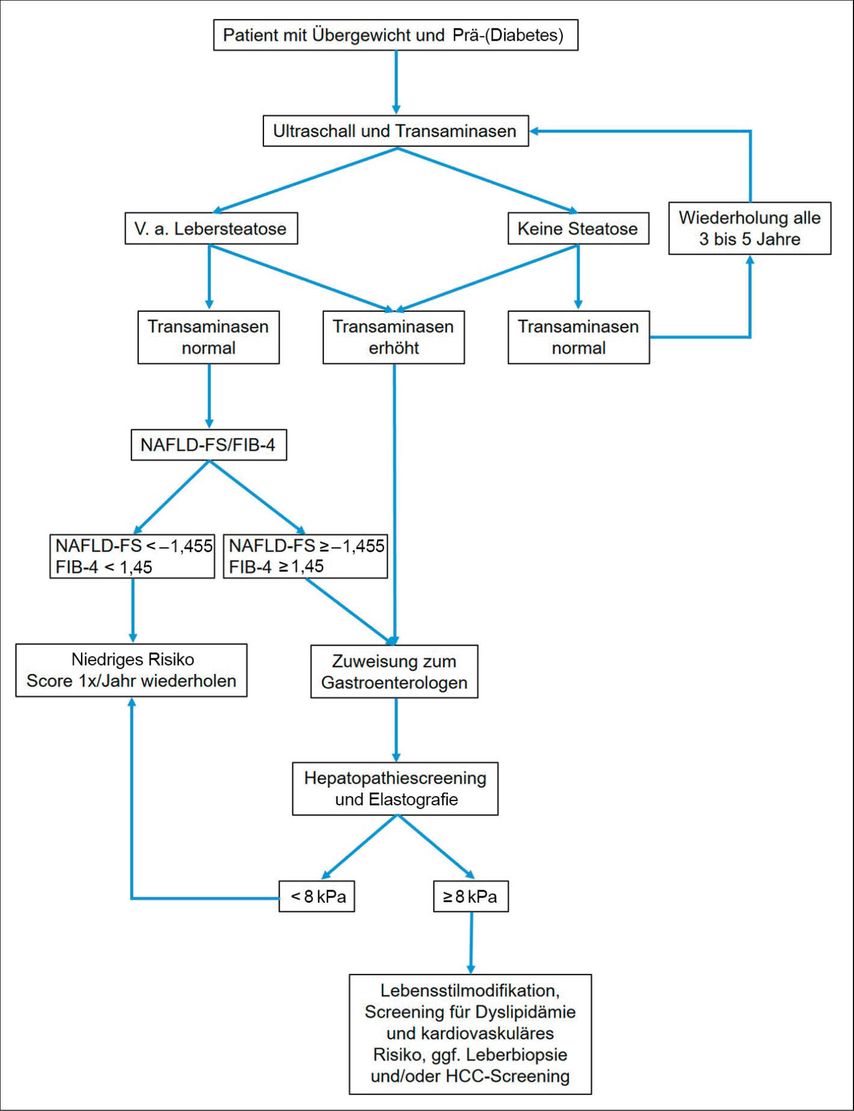
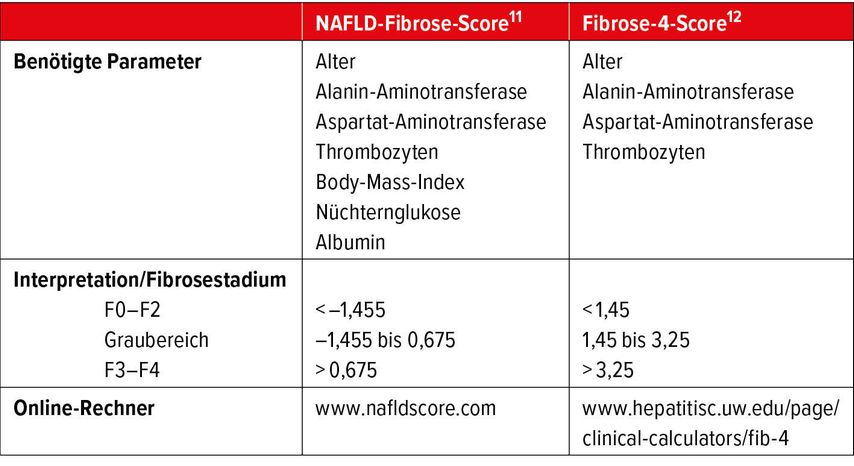
Darüber hinaus gibt es nicht invasive Möglichkeiten, um das Vorhandensein und das Ausmass einer Leberfibrose abzuschätzen. Damit können Kollegen, wie Hausärzte, Diabetologen und Kardiologen, die häufig Patienten der Risikopopulationen für eine NAFLD behandeln, ein einfaches Screening durchführen. Generell wird empfohlen, das NAFLD-Screening bei allen Patienten, die zu einer der Risikopopulation gehören, durch eine Ultraschalluntersuchung zu initiieren (Abb. 1). Wenn sich hier der Verdacht auf eine Lebersteatose ergibt, sollte über die Bestimmung der Transaminasen und weiterer klinischer Parameter, wie beispielsweise Body-Mass-Index, Alter und Blutbild, das Risiko für eine existierende höhergradige Lebererkankung beurteilt werden. Es existieren viele, auf klinischen Zeichen oder Serumwerten basierte Scores, die in erster Linie zum Ausschluss einer fortgeschrittenen Lebererkrankung verwendet werden können. Von diesen sind der NAFLD-Fibrose-Score (NAFLD-FS) und der Fibrose-4-Score (FIB-4) ausreichend validiert, um hier empfohlen zu werden (Tab. 1).
Abb. 1: Algorithmus für Screening und Abklärung einer möglichen NAFLD je nach initialem, in der Hausarztpraxis erhobenem Ultraschallbefund und anhand von NAFLD-Fibrose-Score (NAFLD-FS) und Fibrose-4-Score (FIB-4) (adaptiert nach Angulo et al. und Sterling et al.)11, 12
Werte von NAFLD-FS und FIB-4 im Bereich einer F0- bis F2-Fibrose schliessen eine schwere Lebererkrankung nahezu aus. Sollte sich anhand dieser Scores der Verdacht auf eine höhergradige Leberfibrose (Scores im Graubereich oder im Bereich einer F3-/F4-Fibrose) ergeben, sollte eine Zuweisung an einen Gastroenterologen zur erweiterten Diagnostik mittels transienter Elastografie (FibroScan®) oder Scherwellen-Elastografie und ggf. Leberbiopsie erfolgen (Abb. 1). Über die Ausbreitungsgeschwindigkeit eines Ultraschallimpulses in der Leber kann mithilfe der transienten oder Scherwellen-Elastografie der Grad der Leberfibrose nicht invasiv abgeschätzt werden und auch eine Verlaufsdiagnostik unter Therapie erfolgen. Patienten mit Übergewicht, Typ-2-Diabetes oder Prädiabetes und erhöhten Transaminasen sollten aufgrund der hohen NAFLD-Prävalenz in dieser Population generell für eine Abdomensonografie mit Elastografie einem Facharzt für Gastroenterologie und Hepatologie zugewiesen werden.3,6
Therapiemöglichkeiten
Die Therapie der NAFLD oder NASH soll insbesondere eine Progression der Erkrankung verhindern und das kardiovaskuläre Risiko der Patienten senken. Es wurden und werden zahlreiche medikamentöse Therapiestudien inklusive Phase-III-Studien durchgeführt, eine spezifische Therapie ist aber noch nicht zugelassen. Die untersuchten Substanzen umfassen metabolische, antiinflammatorische und antifibrotische Therapieansätze. In aktuellen Studien wird auch die Kombination verschiedener Präparate untersucht. Eine Verhinderung der Krankheitsprogression scheint einfacher zu erreichen sein als eine Rückbildung der Leberfibrose. Insbesondere für Patienten mit fortgeschrittener Erkrankung könnte eine medikamentöse Therapie sinnvoll sein, bisher ist eine pharmakologische Heilung allerdings noch nicht möglich.3
Im Zentrum der Therapie der NAFLD steht daher eine Gewichtsabnahme mit Veränderung der Lebensgewohnheiten. In Studien konnten hierdurch deutliche Effekte auf den Grad der Leberverfettung und -entzündung und zum Teil auch eine Fibroseregression gezeigt werden. Durch diesen Therapieansatz wird auch ein positiver Effekt auf relevante Komorbiditäten, wie beispielsweise einen Diabetes, ein Schlafapnoe-Syndrom oder ein erhöhtes kardiovaskuläres Risiko, erreicht. Die Deutsche Gesellschaft für Verdauungs- und Stoffwechselerkrankungen und die Europäische Gesellschaft für Lebererkrankungen empfehlen eine Gewichtsreduktion von 7–10%, die durch Ernährungsumstellung und Steigerung der körperlichen Aktivität erreicht werden sollte.3,7 In diesem Sinne wird auch die bariatrische Chirurgie als mögliche Therapie aufgeführt, wenn aufgrund einer vorliegenden Adipositas eine Operationsindikation besteht.
Liegen Komorbiditäten vor, sollten diese nach den aktuellen Empfehlungen der jeweiligen Fachgesellschaften behandelt werden. Für den Einsatz von Lipidsenkern, Statinen, Biguaniden, SGLT2-Inhibitoren oder GLP-1-Agonisten bei Patienten mit einer NAFLD ohne die entsprechende Komorbidität bestehen aktuell noch keine Empfehlungen, es existieren jedoch Daten, die einen Nutzen im Sinne einer Regression von Steatose und Entzündung bei NAFLD-Patienten zeigen.8,9
Patienten mit einer Fettleber und metabolischem Syndrom haben häufig hohe Serumferritin-Werte bei normaler Transferrinsättigung bzw. Abwesenheit einer mit einer Hämochromatose zu vereinbarenden Genmutation. Diese Hyperferritinämie ist in der Regel Ausdruck der Leberinflammation. Bei diesen Patienten ist der Nutzen einer Phlebotomie zur Depletierung der Eisenspeicher umstritten, diese kann aufgrund eingeschränkter Datenlage nicht empfohlen werden.3
MAFLD – was ist das?
Die Abgrenzung zwischen alkoholischer und nichtalkoholischer Fettlebererkrankung ist häufig schwierig. Gemäss Definition sollte der Alkoholkonsum bei einer NAFLD im Rahmen eines im Allgemeinen unbedenklichen Masses liegen, d.h. <20g/d bei Frauen und <30g/d bei Männern.3 Wie oben erwähnt, handelt es sich bei der NAFLD somit um eine Ausschlussdiagnose.
Häufig ist es jedoch nicht möglich, die Rolle von Alkoholkonsum oder einer gleichzeitig vorliegenden anderen Lebererkrankung gegenüber einer NAFLD abzugrenzen, z.B. bei einem Patienten mit Übergewicht, Diabetes und chronischer Hepatitis B. Aus diesem Grund gibt es die Bestrebung mit dem Begriff metabolisch assoziierte Fettlebererkrankung (MAFLD) eine neue Terminologie mit Betonung der Ätiologie einzuführen. Bei dieser Definition werden metabolische Begleiterkrankungen berücksichtigt und das Vorliegen anderer Lebererkrankungen stellt keine Kontraindikation für die Diagnosestellung dar.10 Die MAFLD kann diagnostiziert werden, wenn eine Lebersteatose vorliegt (Bildgebung oder Biopsie) mit zusätzlichem Übergewicht (BMI ≥25kg/m2) oder Typ-2-Diabetes. Bei Normalgewichtigen sollten zusätzlich zwei Faktoren des metabolischen Syndroms vorhanden sein. Diese Definition wird an Zentren zum Teil angewendet, hat sich aber in den vorliegenden Leitlinien der Fachgesellschaften und im klinischen Alltag noch nicht etabliert.
Literatur:
1 Arshad T et al.: Epidemiology of non-alcoholic fatty liver disease in North America. Curr Pharm Des 2020; 26: 993-70 2 Vieira Barbosa J, Lai M: Nonalcoholic fatty liver disease screening in type 2 diabetes mellitus patients in the primary care setting. Hepatol Commun 2021; 5: 158-67 3 European Association for the Study of the Liver, European Association for the Study of Diabetes, and European Association for the Study of Obesity: EASL-EASD-EASO Clinical Practice Guidelines for the management of non-alcoholic fatty liver disease. J Hepatol 2016; 64: 1388-402 4 Angulo P et al.: Liver fibrosis, but no other histologic features, is associated with long-term outcomes of patients with nonalcoholic fatty liver disease. Gastroenterology 2015; 149: 389-97.e10 5 Kleiner DE et al.: Design and validation of a histological scoring system for nonalcoholic fatty liver disease. Hepatology 2005; 41: 1313-21 6 American Diabetes Association: 4. Comprehensive Medical evaluation and assessment of comorbidities: standards of medical care in diabetes - 2021. Diabetes Care 2021; 44: S40-52 7 Roeb E et al.: [S2k Guideline non-alcoholic fatty liver disease]. Z Gastroenterol 2015; 53: 668-723 8 Lai LL et al.: Empagliflozin for the treatment of nonalcoholic steatohepatitis in patients with type 2 diabetes mellitus. Dig Dis Sci 2020; 65: 623-31 9 Newsome PN et al.: A placebo-controlled trial of subcutaneous semaglutide in nonalcoholic steatohepatitis. N Engl J Med 2021; 384: 1113-24 10 Eslam M et al.: A consensus-driven proposed nomenclature for metabolic associated fatty liver disease. Gastroenterology 2020; 158: 1999-2014.e1 11 Angulo P et al.: The NAFLD fibrosis score: a noninvasive system that identifies liver fibrosis in patients with NAFLD. Hepatology 2007; 45: 846-54 12 Sterling RK et al.: Development of a simple noninvasive index to predict significant fibrosis in patients with HIV/HCV coinfection. Hepatology 2006; 43: 1317-25
Das könnte Sie auch interessieren:
Neues aus der Welt der Hepatologie
Kürzlich wurden Arbeiten zu den Risiken nach TIPS-Implantation veröffentlicht und eine neue S3-Leitlinie zu autoimmunen Lebererkrankungen steht nun zur Verfügung. Aktuelles gibt es aber ...
Portale Hypertonie – neue diagnostische und therapeutische Möglichkeiten
Patientinnen und Patienten mit portaler Hypertonie haben ein hohes Risiko, an Komplikationen wie gastroösophagealen Varizen und Blutungen, Aszites oder hepatischer Enzephalopathie zu ...
UEGW 2025: Neues aus der Hepatologie
In der Indikation metabolisch bedingte Lebersteatose bzw. Steatohepatitis scheiterten über viele Jahre zahlreiche Therapieversuche. Seit Kurzem stehen erstmals wirksame Therapien zur ...