Das Potenzial von GLP-1-Rezeptor-Agonisten für die Behandlung neurodegenerativer Erkrankungen
Autor:
Prim. A.o. Univ.-Prof. Dr.
Johann Sellner, MBA, FAAN, FEAN
Abteilung für Neurologie
Landesklinikum Mistelbach-Gänserndorf
Karl Landsteiner Universität für Gesundheitswissenschaften, Krems
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Klinische Studien mit synthetischen GLP-1-Rezeptor-Agonisten bei der Alzheimererkrankung: Stehen wir an der Schwelle eines neuen Zeitalters?
Inkretine sind gastrointestinale Hormone, die nahrungsabhängig sezerniert werden. Sie regulieren den Glukosespiegel über die Stimulation der Insulinausschüttung. Dieser Mechanismus ist bei Patient:innen mit Typ-2-Diabetes (T2D) deutlich eingeschränkt. Inkretin-basierte Therapien wie GLP-1-Rezeptor-Agonisten (GLP-1-RA) und Dipeptidylpeptidase-4-Inhibitoren (DPP-4-Inhibitoren) sind heute etablierte Substanzklassen in der Therapie des T2D und der Adipositas.1 Die GLP-1-RA Liratglutid bzw. Semaglutid wurden 2009 bzw. 2018 für die Behandlung des T2D und 2015 bzw. 2022 für die Behandlung der Adipositas von der Europäischen Arzneimittelagentur (EMA) zugelassen.
Prof. Dr. Lotte Bjerre Knudsen, Chief Scientific Advisor von Novo Nordisk A/S (Måløv, Dänemark) und Trägerin des Lasker-DeBakey-Preises für klinisch-medizinische Forschung des Jahres 2024, hielt einen vielbeachteten Plenarvortrag mit dem Titel „GLP-1R agonist effects in the brain“ beim diesjährigen AD/PD-Kongress in Wien. Sie war grundlegend an der translationalen Entwicklung von GLP-1-RA für die Behandlung des T2D und der Fettleibigkeit beteiligt. Den Lasker-DeBakey-Preis erhielt sie zusammen mit Joel Habener (Harvard Medical School, Boston) und Svetlana Mojsov (Rockefeller University, New York).
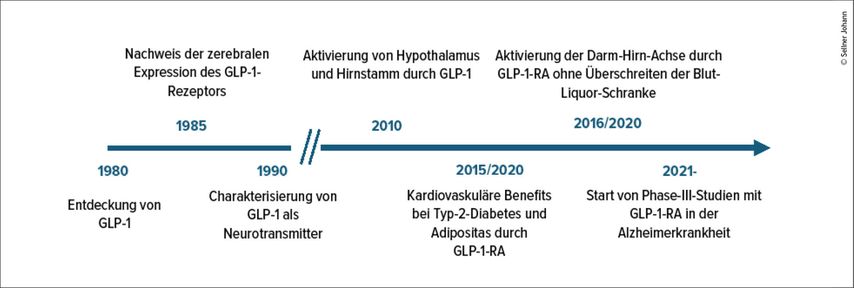
Ihre wissenschaftlichen Projekte der letzten Jahre haben ein tiefergehendes Verständnis für die Wirkung von GLP-1-Rezeptor-Agonisten im Gehirn gebracht, so Knudsen. Sie betonte, dass bezüglich der möglichen zerebralen Effekte von mittelgroßen und kaum liquorgängigen Peptiden wie GLP-1 zunächst große Skepsis bestand und sie Kritiker mit Ergebnissen aus ihren Forschungsarbeiten überzeugen musste.2 Die neurowissenschaftlich relevanten zeitlichen Meilensteine der GLP-1-Entwicklung reichen einige Jahrzehnte zurück (Abb. 1).
Abb. 1: Die wichtigsten neurowissenschaftlichen Erkenntnisse zur therapeutischen Beeinflussung von GLP-1 und dessen Rezeptor im zeitlichen Verlauf
Physiologie und Pathophysiologie von GLP-1
GLP-1 wird zum einen von den L-Zellen im gastrointestinalen (GI) Trakt nahrungsabhängig sezerniert. Zum anderen wird GLP-1 von Neuronen des Nucleus tractus solitarius (NTS) im Rhombencephalon produziert. Dort übt es eine Funktion als Neurotransmitter im zentralen Nervensystem (ZNS) aus. Zuletzt konnte auch die Produktion von GLP-1 im Hypothalamus nachgewiesen werden. Der GLP-1-Rezeptor ist vielerorts exprimiert, u.a. im Pankreas, Gehirn, GI-Trakt, in Herz, Niere und Blutgefäßen. Eine Aktivierung ist mit der Regulation zahlreicher physiologischer Prozesse assoziiert.
In den frühen klinischen Studien wurde nachgewiesen, dass eine Behandlung mit Liraglutid und Semaglutid zur Reduktion der Blutspiegel einiger Biomarker des kardio- und zerebrovaskulären Risikos im Vergleich zu Placebo führt. Zu nennen sind u.a. die Proteine Plasminogen-Aktivator-Inhibitor Typ 1 (PAI-1), B-natriuretisches-Peptid (BNP) und C-reaktives-Protein (CRP). In weiterer Folge wurde in den klinischen Studien konsistent eine signifikant niedrigere Rate an Todesfällen und der vaskulären Endpunkte wie Herzinfarkte und Schlaganfälle bestätigt.
GLP-1 und Inflammation
Ein Meilenstein für das Verständnis der Verhinderung von kardio- und zerebrovaskulären Ereignissen war der Nachweis des Effekts von GLP-1 auf die Atherosklerose über die Modulation von inflammatorischen Prozessen. In einem Tiermodell der Atherosklerose reduzierte Semaglutid dosisabhängig die Surrogatmarker des Cholesterinmetabolismus (ABCA1, PTGID), der Leukozytenrekrutierung (CCL2, IL-1RN, IL-6), der Leukozytenadhäsion und -extravasation (SELE, VCAM-1, OPN) und des Matrix-Remodelings (MMP3, MMP13). Korrespondierend zu den Ergebnissen aus der Laborforschung und aus dem Tiermodell konnte eine Stabilisierung von atherosklerotischen Gefäßplaques im Menschen bestätigt werden.
GLP-1-Effekte durch synthetische Rezeptor-Agonisten im Gehirn
Die ersten Untersuchungen zur zerebralen GLP-1-Funktion und zur Expression der korrespondierenden Rezeptoren mit Nachweis der Regulation von Hungergefühl, die auch als GLP-1-Hirn-Adipositas-Achse bezeichnet wird, stammen von Tiermodellen aus den 1980er-Jahren. Im Zuge der Entwicklung der ersten GLP-1-RA wurde festgestellt, dass diese als mittelgroße Peptide die Blut-Hirn-Schranke nur eingeschränkt überschreiten. Knudsen konnte allerdings zwischenzeitlich zeigen, dass die zerebralen Effekte über Bindung an die GLP-1-Rezeptoren an den zirkumventrikulären Organen des Gehirns vermittelt werden. Peripher verabreichte Agonisten können damit auch in bestimmten Regionen des Hirnstamms und des Hippocampus binden, ohne die Blut-Hirn-Schranke zu überschreiten. Dies wird durch eine besonders hohe Dichte an GLP-1-Rezeptoren in diesen Strukturen unterstützt. Nach der Bindung erfolgen zahlreiche direkte und indirekte Effekte an Neuronen durch Veränderungen des Energiemetabolismus. Durch die auf diesem Wege erfolgte Aktivierung neuronaler Verbindungen werden, so Knudsen, die Effekte der synthetischen GLP-1-RA wie Hunger- und Sättigungsgefühl sowie Gewichtsabnahme vermittelt.
Zerebrale GLP-1-Effekte: Benefit für neurodegenerative Erkrankungen?
Knudsen fasste zunächst die historische Entwicklung der zerebralen GLP-1-Effekte zusammen. Zunächst wurde im Jahr 2002 in der Zellkultur eine Stimulation des Neuritenwachstums durch GLP-1, vergleichbar mit den Effekten des Nervenwachstumsfaktors (NGF), nachgewiesen. Im selben Jahr wurden die neuroprotektive Wirkung von GLP-1 und die Rückbildung exzitotoxizitätsbedingter neuronaler Schäden in vitro beschrieben. Ebenso wurde gezeigt, dass GLP-1 in vitro und in vivo die Inflammation im ZNS abschwächt und die Permeabilität der Blut-Hirn-Schranke reduziert. Dies führte zu weiteren Untersuchungen und zur Exploration des Potenzials von GLP-1 bei neurodegenerativen Erkrankungen. Im Jahr 2012 wurde eine Arbeit veröffentlicht, in der Liraglutid die kognitive Performance in einem Mausmodell der Alzheimerkrankheit (APP[swe]/PS1[ΔE9]) verbesserte. Gleichzeitig wurden die kortikalen β-Amyloid-Plaques um 40–50% reduziert, die löslichen β-Amyloid-Oligomere waren um 25% geringer. Die Neuroinflammation, gemessen am Ausmaß der aktivierten Mikroglia, wurde durch Liraglutid halbiert und die Neurogenese im Gyrus dentatus angeregt.
Im Jahr 2017 wurde in einer klinischen Studie an Patient:innen mit Alzheimerkrankheit gezeigt, dass Liraglutid den bei dieser Krankheit reduzierten Blut-Gehirn-Glukose-Transfer, gemessen mit 18F-FDG-PET, wieder normalisiert. Zwischenzeitlich werden nicht nur die Abschwächung von neurodegenerativen Prozessen, Inflammation und die neurovaskuläre Hirnschädigung als therapeutisches Target von synthetischen GLP-1-Rezeptor-Agonisten gesehen, erklärte Knudsen. Es gebe eine Vielzahl von Hinweisen, dass synthetische GLP-1-Mimetika auch auf den Lipidstoffwechsel, den Metabolismus, die Bioenergetik, neuroendokrine Mechanismen, neuronale Schaltkreise und Synapsen, Autophagie, Endozytose, Immunität und Zelltod wirken. Somit kann diese Substanzklasse aufgrund ihrer pleiotropen Mechanismen für die Behandlung neurodegenerativer Erkrankungen von Nutzen sein, postuliert Knudsen.
Sie selber habe die letzten Jahre die Effekte von Semaglutid auf die Neuroinflammation untersucht, da sie hierfür eine Schlüsselrolle in der Pathogenese der Alzheimererkrankung sehe. Insbesondere wies sie auf das Potenzial der GLP-1-RA durch ihre Wirkung auf die Mikroglia und die Blockade der Transmigration von neutrophilen Granulozyten hin. Darüber hinaus interagiere Semaglutid mit Genen des im Zusammenhang mit Alzheimer viel diskutierten ApoE-Lokus. Ihre Untersuchungen zeigen, dass sich die in den Mikroglia durch Semaglutid herunterregulierten Gene Clptm1, Relb und Bcl3 beim Menschen im ApoE-Lokus auf Chromosom19 befinden.
Kommentar
In den letzten Jahren gab es einen immensen Wissenszuwachs über die vielfältige physiologische Rolle von GLP-1 im GI-Trakt und im ZNS. Im Plenarvortrag wurden vielversprechende wissenschaftliche Daten vorgestellt, in denen eine Modulation pathogenetisch relevanter Prozesse von neurodegenerativen Erkrankungen durch synthetische GLP-1-RA, vorwiegend in vitro und im Tiermodell, gezeigt wurden.
Im Vortrag nicht erwähnt wurden die ersten klinischen Studien zu synthetischen GLP-1-RA bei der Alzheimererkrankung. Bei der American Alzheimer’s Association Conference 2024 wurden erneut die Ergebnisse einer Phase-IIb-Studie mit Liraglutid vs. Placebo vorgestellt.4 In der Studie mit 204 Patient:innen mit milder Alzheimererkrankung, die nicht an T2D erkrankt waren, wurden sowohl der primäre Endpunkt zerebraler Glukosemetabolismus, bestimmt mittels FDG-PET nach 12 Monaten, wie auch die sekundären und explorativen Endpunkte (Kognition mittels verschiedener neuropsychologischer Testbatterien, Hirnatrophie mittels MRT) nicht erreicht. Über die Ergebnisse zu weiteren explorativen Endpunkten wie einer Mikrogliaaktivierung mittels Translokatorprotein-PET (TSPO-PET) und Surrogatmarker der Erkrankung (Amyloid- und Tau-PET) wurde bislang noch nicht berichtet. Die ELAD-Studie ist weiterhin nicht publiziert, Teilaspekte der Untersuchung wurden bereits ab 2020 auf diversen Kongressen vorgestellt. Zu dem fehlenden Therapieeffekt könnte die geringe Patient:innenzahl, aber auch die geringe Blut-Hirn-Schranken-Penetration von Liraglutid beigetragen haben, so die Beurteilung in Expert:innenkreisen.
Im Jahr 2026 werden die Ergebnisse der Phase-III-Studien mit Semaglutid bei leichter kognitiver Störung und milder Alzheimererkrankung erwartet. Große Hoffnung wird auf die klinischen Studien mit den GLP-1-Analoga Lixisenatid und Exenatid gesetzt, die als niedermolekulare Verbindungen eine bessere Penetration der Blut-Hirn-Schranke aufweisen als Semaglutid oder Liraglutid.5,6
Nicht unerwähnt bleiben sollte, dass Lixisenatid in einer placebokontrollierten Phase-II-Studie bei der frühen Parkinsonerkrankung eine Verzögerung der motorischen Progression zeigte.7 Eine kürzlich publizierte Phase-III-Studie aus dem Vereinigten Königreich mit Exenatid bei der Parkinsonerkrankung bestätigte allerdings kein verbessertes motorisches Abschneiden gegenüber Placebo.8
Es erwartet uns somit eine spannende Zeit für neue krankheitsmodifizierende Alzheimertherapien abseits von der auf β-Amyloide gerichteten Behandlungsstrategie. Zumal neue wissenschaftliche Erkenntnisse zur Darm-Hirn-Achse mit Relevanz für die Neurologie erwartet werden.
Literatur:
1 Nauck MA et al.: GIP und GLP-1-Rezeptoragonismus in der Therapie des Typ 2 Diabetes mit Fokus auf Tirzepatid.Diabetol Stoffwechs 2023; 18: 475-87 2 Knudsen LB: GLP-1 for treating obesity - origin, history, and evolution: 2024 Lasker-DeBakey clinical medical research award.JAMA 2024; 332(20): 1697–98 3 Knudsen LB: GLP-1R agonist effects in the brain. AD/PD Conference 2025, Wien. Plenarvortrag am 1.4.2025 4 Shugart J: Liraglutide trial was negative four years ago, still negative today. Alzforum 2024 www.alzforum.org/news/conference-coverage/liraglutide-trial-was-negative-four-years-ago-still-negative-today, zuletzt aufgerufen: 23.05.2025 5 Alzforum Database: Lixisenatide, www.alzforum.org/therapeutics/lixisenatide, zuletzt aufgerufen: 23.05.2025 6 Alzforum Database: Exenatide, www.alzforum.org/therapeutics/exenatide, zuletzt aufgerufen: 23.05.2025 7 Meissner WG et al.: Trial of lixisenatide in early parkinson‘s disease. N Engl J Med 2024; 390(13): 1176-85 8 Vijiaratnam N et al.: Exenatide once a week versus placebo as a potential disease-modifying treatment for people with parkinson‘s disease in the UK: a phase 3, multicentre, double-blind, parallel-group, randomised, placebo-controlled trial. Lancet 2025; 405(10479): 627-36
Das könnte Sie auch interessieren:
Welchen Beitrag kann therapeutisches Drug-Monitoring leisten?
Bariatrische Operationen sind eine wirksame Strategie zur Gewichts-reduktion bei Adipositas. Die damit veränderte Anatomie kann die Bioverfügbarkeit von Arzneimitteln massgeblich ...
Neues zur Diagnostik und Therapie bei akutem und episodischem Schwindel
Schwindel ist eines der häufigsten Leitsymptome sowohl auf der Notfallstation wie auch in der Praxis. Wegen der äusserst breiten Differenzialdiagnose, der oftmals transienten Natur der ...
Wichtige Laborparameter bei Epilepsie: ein aktueller Überblick
Laborkontrollen sind bei Epilepsien aus verschiedensten Gründen erforderlich. Anfallssupprimierende Medikamente können Störwirkungen auf unterschiedliche Organsysteme haben, die unter ...