Bispezifischer Antikörper in Pilotstudie effektiv, aber es sind noch Fragen offen
Bericht:
Dr. Felicitas Witte
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Trotz zielgerichteter Medikamente sprechen manche Patienten mit rheumatoider Arthritis (RA) selbst auf Kombinationsbehandlungen nicht an. Der bispezifische Antikörper Blinatumomab zeigte sich in einer Pilotstudie1 mit sechs Patienten als effektiv. Der Ansatz ist aufgrund der Pathophysiologie der RA sinnvoll; ob sich die Behandlung in der Routine etablieren wird, ist zum jetzigen Zeitpunkt noch unklar.
Die Prognose von Patienten mit RA hat sich mit der Einführung von monoklonalen Antikörpern wie TNF-Hemmern und Interleukin-6-Hemmern sowie „small molecules“ wie den Januskinase-Inhibitoren deutlich verbessert, sodass auch bei Patienten mit schwerer RA eine Remission gelingt. Trotzdem helfen diese zielgerichteten Therapien selbst in Kombination einigen Patienten nicht, und sie haben weiterhin eine hohe Krankheitsaktivität. Eine Möglichkeit für solche therapieresistenten Patienten könnte sein, in die Interaktion zwischen B- und T-Zellen einzugreifen.
Diesen Ansatz verfolgt das Fusionsprotein Abatacept, das zur Behandlung der RA zugelassen ist. Abatacept bindet mit höherer Affinität an CD80/86 als an CD28 und blockiert so CD28-abhängige T-Zell-Antworten. Die T-Zell-Aktivierung benötigt eine antigenspezifische Interaktion zwischen dem T-Zell-Rezeptor und dem MHC, ein zusätzliches kostimulatorisches Signal. Eines der wichtigsten kostimulatorischen Signale stellt die Interaktion zwischen CD28 auf den T-Zellen und CD80 oder CD86 auf den antigenpräsentierenden Zellen dar. Abatacept blockiert diese Interaktion.
Ein anderer Ansatz ist, die T-Zellen zu aktivieren, damit diese die B-Zellen zerstören, und zwar mittels bispezifischer Antikörper. Mit einem solchen Antikörper wurde jetzt eine Pilotstudie1 mit sechs Patienten durchgeführt. Die Rationale für den Ansatz: B-Zellen sind eng mit der Pathogenese der RA verbunden. Erstens sind bei den meisten Patienten Autoantikörper schon vor Ausbruch der Krankheit vorhanden, und sie sind mit einem schlechteren Verlauf assoziiert. Zweitens finden sich B-Zellen und Plasmazellen in großer Menge im entzündeten Synovialgewebe. Drittens lassen sich die B-Zellen mithilfe des Anti-CD20-Antikörpers Rituximab zerstören. Rituximab gehört seit Jahren zu den Standardmedikamenten bei RA, und zwar als Kombinationstherapie mit Methotrexat bei ungenügendem Ansprechen auf TNF-Hemmer. Doch es gibt immer wieder Patienten, bei denen Rituximab und andere krankheitsmodifizierende Medikamente nicht oder nicht ausreichend wirken.
T-Zellen aktivieren, um B-Zellen zu zerstören
Der neue bispezifische Antikörper heißt auf Englisch „bispecific T cell engager“ (BiTE). Er besteht aus zwei Immunglobulinketten: Antigen-erkennenden scFv-Fragmenten, die über eine Peptidbrücke verbunden sind. Ein Fragment bindet an den CD3-Rezeptor auf T-Zellen, das andere an CD19 auf den B-Zellen. Dadurch werden B- und T-Zellen immunologisch miteinander gekoppelt. Durch die Bindung werden die T-Zellen aktiviert und schütten zytotoxische Proteine wie Perforin aus. Die Zellmembran der B-Zellen wird geschädigt und die Zellen werden zerstört.
Der erste BiTE heißt Blinatumomab. Schon geringe Dosen reichen aus für seine Wirkung. Das liegt daran, dass T-Zellen sehr sensibel auf eine rezeptorvermittelte Aktivierung reagieren und eine einzige T-Zelle ausreicht, um serienweise B-Zellen zu töten. Das Prinzip wurde erfolgreich getestet bei Leukämie; Blinatumomab ist zugelassen zur Behandlung bestimmter akuter lymphatischer Leukämien. Ein Forscherteam aus Erlangen, Rom und Stockholm vermutete, dass dieses Prinzip – also die T-Zellen zu aktivieren, damit sie die B-Zellen zerstören – auch bei B-Zell-vermittelten Autoimmunkrankheiten wie der RA funktionieren könnte. Sie testeten in der Pilotstudie Blinatumomab bei drei Frauen und drei Männern mit schwerer RA, die gegen mehrere krankheitsmodifizierende Medikamente resistent waren.1 Die Patienten waren zwischen 31 und 60 Jahre alt und zwischen 3 und 27 Jahre an RA erkrankt. Der Krankheitsaktivitäts-Score DAS28 betrug zwischen 4,05 und 5,70; die Patienten hatten im Schnitt zuvor sechs krankheitsmodifizierende Medikamente erhalten. Blinatumomab wurde über fünf Tage stationär als kontinuierliche intravenöse Infusion verabreicht. Im Gegensatz zur onkologischen Indikation wurde mit einer geringeren Dosis und über einen kürzeren Zeitraum behandelt. Die RA-Patienten bekamen zunächst 9μg pro Tag, wie es auch bei akuter lymphoblastischer Leukämie empfohlen wird. Die Gesamtdosis bei der RA-Therapie betrug in den ersten fünf Tagen 38,5µg. Bei der akuten lymphoblastischen Leukämie (ALL) besteht ein einzelner Behandlungszyklus aus einer vierwöchigen Dauerinfusion (Tage 1–28). Die sechs Patienten mit RA erhielten fünf Tage eine Blinatumomab-Dauerinfusion, nach einer Woche Pause bekamen sie nochmals eine fünftägige Dauerinfusion. Drei Wochen vor Beginn der ersten Infusion wurde das zuletzt verabreichte (unwirksame) krankheitsmodifizierende Medikament gestoppt; Methotrexat wurde weiter gegeben.
Rasche Depletion der B-Zellen
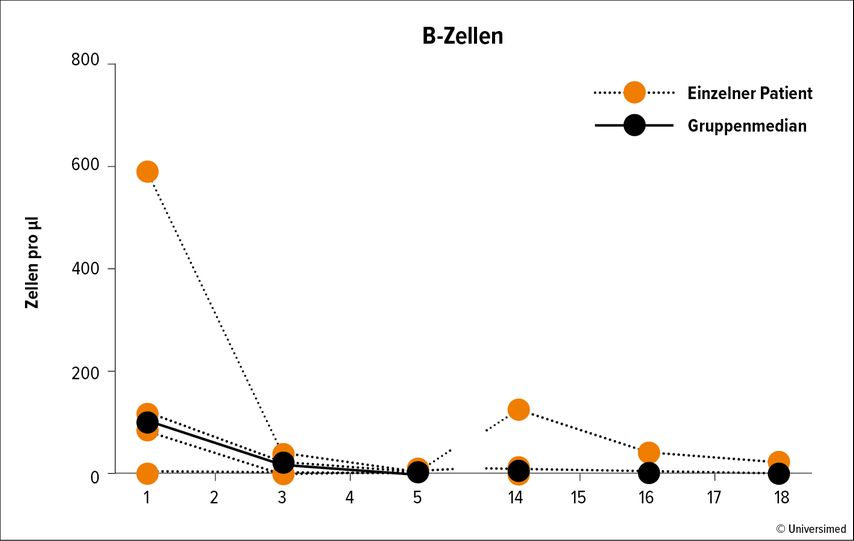
Alle Patienten vertrugen die Blinatumomab-Therapie gut; ernste Nebenwirkungen traten nicht auf. Vier Patienten erlitten Nebenwirkungen, die auf das Medikament zurückgeführt wurden, Zeichen für eine Neurotoxizität wurden nicht registriert. Die Infusion von Blinatumumab führte rasch zu einer Depletion der B-Zellen im peripheren Blut (Abb. 1). Der Antikörper führte zudem zu einer schnellen und deutlichen Reduktion der T-Zellen. Dies betraf mehr die CD8+-T-Zellen als die CD4+-Zellen, sodass sich konsequenterweise die CD4/CD8-Ratio erhöhte. Nach der Therapie normalisierte sie sich wieder. Die CD8+-T-Zellen sanken überraschenderweise auch bei dem Patienten, der keine zirkulierenden B-Zellen mehr hatte, weil sie zuvor mit Rituximab behandelt worden war. Dies lässt vermuten, dass die CD8+-T-Zellen mit übrig gebliebenen CD19+-B-Zellen in den Geweben interagierten. Die Behandlung mit Blinatumumab war effektiv: Die Zahl der geschwollenen Gelenke sank von im Schnitt 9 (Interquartilabstand 6–15) auf 0,5 (Interquartilabstand 0–2) nach zwölf Wochen. Auch die Krankheitsaktivität – gemessen mittels visueller Analogskala – bessserte sich deutlich von im Schnitt 60(Interquartilabstand 47–72,5) auf 10(Interquartilabstand 0–25). Der zusammengesetzte Krankheitsaktivitäts-Index DAS28-CRP sank von im Mittel 4,72 Einheiten auf 2,28 Einheiten nach drei Monaten, was einer Remission ähnelt.
Nach vier Monaten starteten fünf Patienten eine Behandlung mit Abatacept, ein Patient – in Remission mit einem DAS28 von 1,85 – führte die Methotrexat-Monotherapie fort. Bei einem der Patienten verschlechterten sich die Symptome vorübergehend zwischen dem dritten und vierten Monat vor der Abatacept-Behandlung. Nach sechs Monaten hielt der Effekt von Blinatumumab noch an. Die Patienten hatten kaum mehr geschwollene Gelenke, eine geringe globale Krankheitsaktivität und einen kombinierten DAS28-CRP-Index von 2,9. Auch in der Bildgebung zeigte sich eine Reduktion der Krankheitsaktivität, in der Histologie der Synovia bestätigte sich die Depletion der B-Zellen, und die Spiegel der Autoantikörper waren gesunken.
Keine zu großen Hoffnungen
In dieser Pilotstudie war der Ansatz erfolgreich, mithilfe des bispezifischen Antikörpers Blinatumomab die krankhaft reagierenden B-Zellen durch Aktivierung der T-Zellen zu töten. BiTE wie Blinatumomab, so die Autoren, könnten die klinischen Limitierungen der bisherigen B-Zell-Depletion überwinden. Allerdings wurden in dieser Studie nur sechs Patienten behandelt, und es gab keine Vergleichsgruppe mit Placebo oder mit einem anderen Medikament, welches die B-Zellen depletiert, wie Rituximab. Zum Nebenwirkungsprofil und zur Wirksamkeit von Blinatumomab lässt sich also noch kaum etwas sagen, auch wenn die sechs Patienten das Mittel vertrugen, es gut zu wirken schien und sich auch objektiv deutliche Verbesserungen der Krankheitsaktivität zeigten. Es bleibt spannend, ob der Ansatz den Weg in die Klinik finden wird. Auf www.clinicaltrials.gov findet sich bisher keine weitere Studie mit Blinatumomab bei rheumatoider Arthritis.
Quelle
1 Bucci L et al.: Nat Med 2024, online 26.4.2024. doi: 10.1038/s41591-024-02964-1
Das könnte Sie auch interessieren:
Bedeutung pulmonaler Symptome zum Zeitpunkt der Erstdiagnose
Bei der Erstdiagnose von entzündlich-rheumatischen Erkrankungen können bereits pulmonale Symptome vorliegen, dies muss jedoch nicht der Fall sein. Eine Studie des Rheumazentrums Jena hat ...
Betroffene effektiv behandeln und in hausärztliche Betreuung entlassen
Bei bestimmten Patientinnen und Patienten mit Gicht ist eine rheumatologisch-fachärztliche Betreuung sinnvoll. Eine im August 2024 veröffentlichte S3-Leitlinie zur Gicht macht deutlich, ...
Gezielte Therapien bei axSpA – und wie aus ihnen zu wählen ist
Nachdem 2003 der erste TNF-Blocker zugelassen wurde, existiert heute für die röntgenologische (r-axSpA) und die nichtröntgenologische axiale Spondyloarthritis (nr-axSpA) eine ganze Reihe ...