Thrombotisch-thrombozytopenische Purpura: neue Therapiekonzepte
Autor:
Univ.-Prof. Dr. Paul N. Knöbl
Klinische Abteilung für Hämatologie und Hämostaseologie
Universitätsklinik für Innere Medizin 1 Medizinische Universität Wien
E-Mail: paul.knoebl@meduniwien.ac.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die thrombotisch-thrombozytopenische Purpura (TTP) ist eine seltene, potenziell lebensbedrohliche thrombotische Mikroangiopathie, charakterisiert durch Thrombozytopenie, mikroangiopathische hämolytische Anämie und Zeichen von (diffusen) Organischämien. Ohne Behandlung betrug die Letalität historisch bis zu 90%, durch moderne Behandlungskonzepte konnte diese auf unter 1% gesenkt werden.
Pathophysiologie
Pathophysiologisch besteht bei der TTP ein schwerer Mangel des Enzyms ADAMTS13. Dieses reguliert die Multimergröße des Von-Willebrand-Faktors (VWF). Bei einem schweren ADAMTS13-Mangel akkumulieren ultralange VWF-Multimere, die Thrombozytenaggregation und Mikrothrombenbildung in kleinen Gefäßen fördern. Ein ADAMTS13-Mangel kann durch Autoantikörper, die dieses Enzym hemmen, verursacht werden (= immunmediierte TTP; iTTP), oder (sehr selten) durch homozygote oder gemischt heterozygote Mutationen im ADAMTS13-Gen (kongenitale TTP; cTTP; Upshaw-Schulman-Syndrom).
Diagnostik: Bestimmung der ADAMTS13-Aktivität essenziell
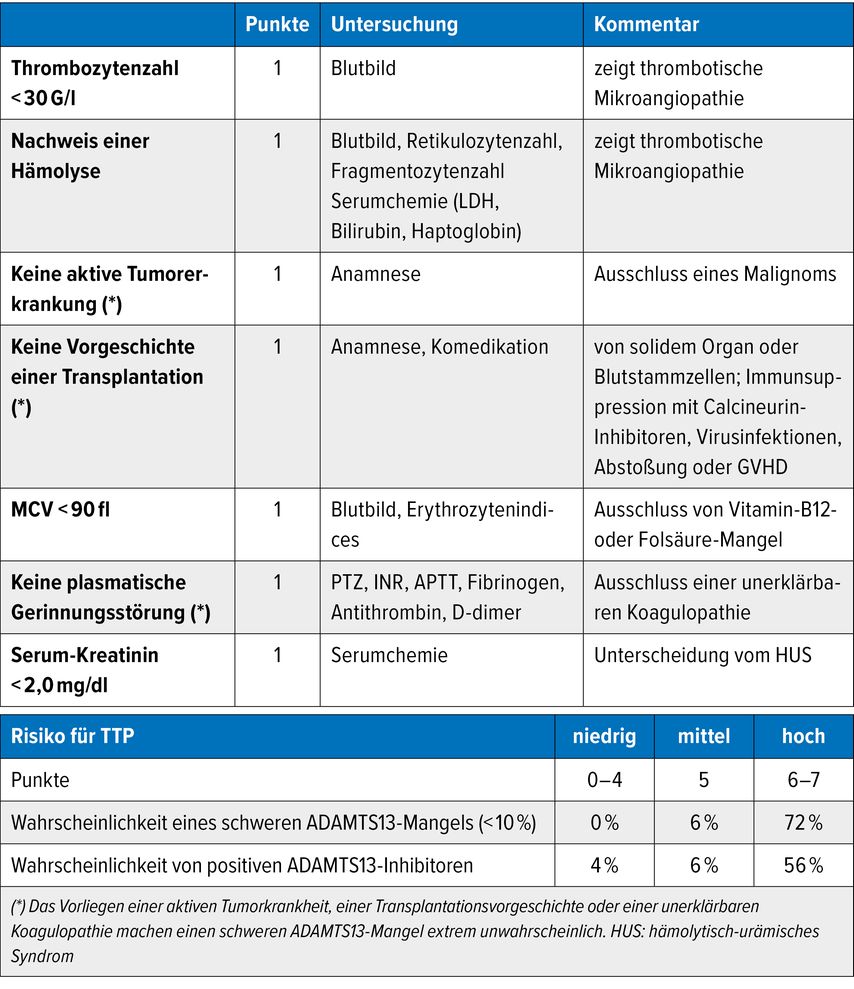
Die TTP ist eines von vielen klinisch ähnlichen Syndromen thrombotischer Mikroangiopathien, muss aber wegen der spezifischen modernen Therapiemöglichkeiten durch die sofortige Bestimmung der ADAMTS13-Aktivität eindeutig diagnostiziert werden. Dazu stehen mittlerweile in den größeren Behandlungszentren im deutschsprachigen Raum gute und schnelle Testsysteme zu Verfügung, die innerhalb weniger Stunden ein valides Ergebnis liefern. Bei stark erniedrigten ADAMTS13-Aktivitätswerten (<10%) kann dann auch mittels einer Verdünnungsreihe eine Quantifizierung des Inhibitortiters erfolgen. Periphere Häuser müssen jedoch eine Citratplasmaprobe zur Bestimmung versenden. Das darf jedoch niemals die sofortige Einleitung einer lebensrettenden Therapie verzögern. Die Wahrscheinlichkeit eines schweren ADAMTS13-Mangels kann mit klinischen Scoringsystemen (z.B. PLASMIC-Score, Tab.1) abgeschätzt werden. Das Vorliegen einer aktiven Tumorerkrankung, einer Organ- oder Stammzelltransplantation oder einer plasmatischen Gerinnungsstörung schließt einen schweren ADAMTS13-Mangel nahezu sicher aus. Ganz zu Beginn müssen alle Untersuchungen zur Beurteilung der Organfunktionen und zur Aufarbeitung der Differenzialdiagnosen durchgeführt werden.
Tab. 1: PLASMIC-Score zur Abschätzung der Wahrscheinlichkeit eines schweren ADAMTS13-Mangels (modifiziert)
TTP-Behandlung mit Caplacizumab
Die historische Behandlung der TTP stützt sich auf eine randomisierte Studie von 1991, bei der tägliche Plasmaaustauschbehandlungen einen Überlebensvorteil gebracht haben. Damals war jedoch die Pathophysiologie der TTP noch unbekannt, und es standen keine anderen Behandlungsmöglichkeiten zu Verfügung. Seither hat sich der sofortige Beginn mit Plasmaaustausch als notwendige Therapieform der TTP etabliert und wurde bis vor Kurzem auch konsequent eingesetzt. Durch die Fortschritte bei der Entdeckung der Pathophysiologie und der Entwicklung von gezielt wirksamen Managementstrategien konnte dieses historische Paradigma in den letzten Jahren zunehmend hinterfragt werden.
Die moderne TTP-Therapie stützt sich auf die möglichst frühzeitige Gabe von Caplacizumab (erste Dosis 10mg i.v., danach 1x tägl. 10mg sc.). Caplacizumab ist ein kleines Antikörperfragment, das die Bindung von Thrombozyten an den VWF verhindert. Es ist seit 2018 zur Behandlung der iTTP zugelassen. Sowohl die Zulassungsstudien als auch Real-World-Daten konnten zeigen, dass der sofortige Beginn dieser Therapie eindeutig von Vorteil ist.
Eine aktuelle große internationale Analyse mit mehr als 1000 Behandlungen (Capla 1000+Project, Coppo P et al., eClinicalMedicine 2025) konnte dies bestätigen. Die Thrombozytenzahlen normalisierten sich im Median drei Tage nach der ersten Caplacizumab-Gabe, die Mortalität lag <1%, und die Krankenhausaufenthaltsdauer sowie der Ressourcenverbrauch halbierten sich. Auch eine aktuelle Analyse von deutschen und österreichischen Daten (Kühne L et al., ISTH 2025) zeigt, dass die Raten des Ansprechens auf Caplacizumab bei >99% liegen. Einige Patient:innen (ca. 4%) zeigten ein leicht verzögertes Ansprechen, bei diesen liegt eine andere, nicht TTP-assoziierte Ursache zugrunde (Infektionen, Autoimmunerkrankungen etc.).
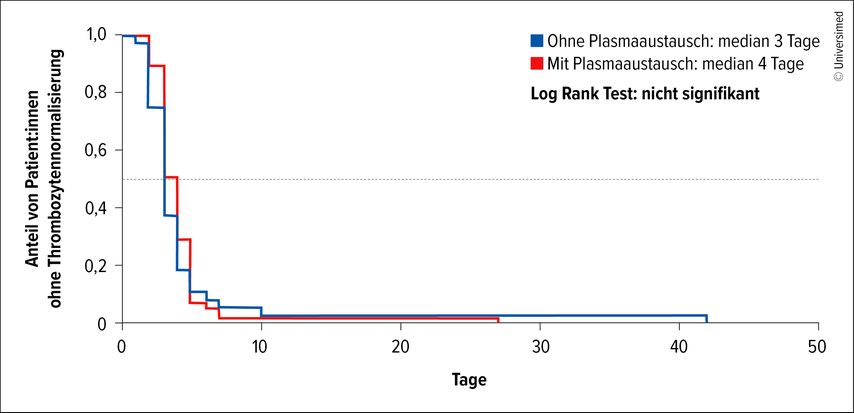
Diese hohe Erfolgsrate von Caplacizumab hat dazu geführt, dass die Notwendigkeit der Plasmaaustauschbehandlungen zunehmend hinterfragt wird. Mittlerweile wurden >100 iTTP-Patient:innen ohne Plasmaaustausch behandelt, wenn sich nach der ersten Gabe von Caplacizumab ein Anstieg der Thrombozytenzahlen als Zeichen eines Therapieansprechens zeigte. Die Patient:innen stammen vor allem aus retrospektiven Kohorten aus Deutschland und Österreich (Kühne L et al., 2024) sowie aus der prospektiven MAYARI-Studie, die heuer am ISTH-Kongress präsentiert wurde. Auch ohne Plasmaaustausch bestehen eine Ansprechrate >99%, eine Thrombozytennormalisierung innerhalb von drei Tagen (Abb.1), eine minimale Exazerbationsrate und eine Mortalität von 0%. Daher wird in Kompetenzzentren keine Plasmaaustauschtherapie mehr eingesetzt.
Abb. 1: Management der iTTP ohne Plasmaaustausch (mod. nach Kühne L et al.: Blood 2024; 144(14): 1486-95)
Caplacizumab beeinflusst jedoch nicht die ADAMTS13-Spiegel und muss weitergeführt werden, solange ADAMTS13 niedrig ist. Ein vorzeitiges Absetzen erhöht das Risiko für klinische Exazerbationen. Andererseits ist Caplacizumab teuer und kann bei längerer Anwendung auch das Risiko für Blutungen erhöhen, sodass eine möglichst kurze Therapiedauer angestrebt wird. Die Immunsuppression mit Rituximab ist mittlerweile fest etablierter Standard zur Elimination der Autoantikörper. Im Median zeigt sich nach 2–3 Wochen ein Anstieg der ADAMTS13-Aktivität und Caplacizumab kann beendet werden.
Therapie der kongenitalen TTP
Viele Patient:innen mit kongenitaler TTP (cTTP) benötigen eine prophylaktische ADAMTS13-Substitutionstherapie, um TTP-Schübe und Spätschäden zu verhindern. Dazu musste bislang alle 1–2 Wochen eine Infusion von ca. 15ml/kg Plasma (z.B. Octaplas®) erfolgen. Dies bedeutete für die Patient:innen jedes Mal einen großen zeitlichen Aufwand. Trotzdem kam es immer wieder zu Durchbruchsepisoden.
2024 wurde für die cTTP ein rekombinantes ADAMTS13-Konzentrat zugelassen, das eine wesentliche Verbesserung der Lebensqualität für die Betroffenen bewirkt hat. Mit dem neuen Konzentrat reduziert sich die Therapie auf die Injektion von ca. 10–15ml Präparat. Ähnlich wie bei der Hämophilie könnte dies auch durch die Patient:innen in Heim-/Selbsttherapie durchgeführt werden, was aber von den Kostenträgern derzeit nicht finanziert wird. Jedenfalls kann durch eine Substitution mit dem Konzentrat eine fünffach höhere Exposition erreicht werden, Durchbruchsschübe wurden in den Studien keine beobachtet.
Das ADAMTS13-Konzentrat wird derzeit auch für die iTTP untersucht, die bisher vorliegenden Daten sind jedoch noch zu heterogen, um eine Vorhersage zum zukünftigen Einsatz in dieser Indikation treffen zu können.
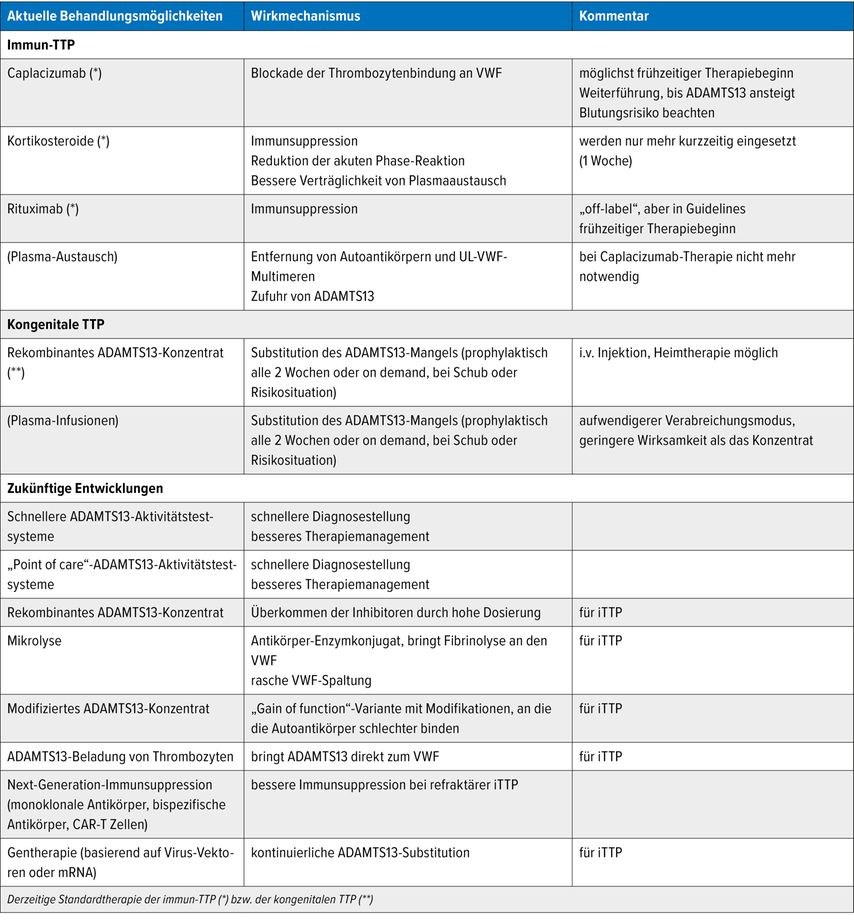
Derzeit laufen weitere Entwicklungen zum Management der TTP. Tabelle 2 gibt einen Überblick über die aktuellen Therapien und zukünftige Therapieoptionen. Doch sowohl bei der Diagnostik als auch bei der Therapie gibt es noch offene Fragen.
Fazit
Zusammenfassend kann gesagt werden, dass sich ein akuter TTP-Schub von einer akuten, lebensbedrohlichen Situation in eine recht einfach zu behandelnde Erkrankung gewandelt hat, sofern die TTP rechtzeitig diagnostiziert wird und eine sofortige Versorgung mit Caplacizumab sichergestellt ist. Auch sind schnelle ADAMTS13-Aktivitätstests für eine korrekte Betreuung von TTP-Patient:innen notwendig. Die Immunsuppression beruht zum Großteil auf Rituximab, muss aber konsequent eingesetzt und überwacht werden.
Literatur:
Literatur beim Verfasser
Das könnte Sie auch interessieren:
Früherkennung klonaler Mastzellerkrankungen durch Screening im peripheren Blut
Die Diagnose einer systemischen Mastozytose und anderer klonaler Mastzellerkrankungen erfolgt in der klinischen Praxis häufig verzögert. Unspezifische und heterogene Symptome sowie die ...
Erste Erfolge mit der Gentherapie bei der Hämophilie
Zur 70. Jahrestagung der Gesellschaft für Thrombose- und Hämostaseforschung (GTH) Mitte Februar 2026 kamen in Bonn über 1000 hämostaseologische Expertinnen und Experten zusammen. Das ...
Erfolg zielgerichteter und zeitlich begrenzter Therapien
Auf der Frühjahrstagung der OeGHO widmete sich eine spezielle Session zukunftsweisenden Entwicklungen in der Grundlagen- und klinischen Forschung auf dem Gebiet der Hämatologie. Im Fokus ...