Update atopisches Ekzem
Bericht:
Martha-Luise Storre
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
In den vergangenen Jahren haben sich das Verständnis des atopischen Ekzems (AE) sowie die therapeutischen Möglichkeiten deutlich weiterentwickelt. Und der Weg ist noch nicht zu Ende beschritten: So gibt es unter anderem neue Erkenntnisse zur möglichen Verlaufsvorhersage der Erkrankung und Bewegung bei der topischen und systemischen Therapie.
Keypoints
-
Die Suche nach Biomarkern für AD geht weiter. Als vielversprechend für eine Verlaufsvorhersage hat sich die Vernix caseosa erwiesen.
-
Rückfetten im frühen Kindesalter hat keinen präventiven Effekt. Es kann sich sogar nachteilig auf den TEWL auswirken.
-
Die verfügbaren Biologika und JAK-Inhibitoren ermöglichen eine individualisierte Therapieauswahl.
Wie in vielen anderen Indikationen werden auch beim AE mögliche Biomarker gesucht und erforscht. Eine potenzielle Quelle für prädiktive AE-Tests ist die Vernix caseosa, auch Käseschmiere genannt, berichtete Prof. Dr.med. Peter Schmid-Grendelmeier, Konsiliararzt für Allergologie und Dermatologie am Kantonsspital Zug sowie am MedizinCampus Davos, pensionierter Leiter der Allergiestation der Dermatologischen Klinik am Universitätsspital Zürich und Mitglied des multizentrischen Neurodermitis-Kohorten-Projekts ProRaD des Christine Kühne – Center for Allergy Research and Education (CK-CARE).
Die Vernix caseosa ist eine natürliche Substanz mit Funktionen in der fötalen Entwicklung sowie beim Neugeborenen. Es gibt Hinweise auf einen Zusammenhang zwischen mütterlicher Adipositas und der Pathogenese der atopischen Dermatitis (AD) in der Vernix caseosa:1 So zeigte sich eine verminderte Expression von Hautbarriere-Proteinen (Filaggrin, Loricrin) bei Kindern von übergewichtigen bzw. adipösen Müttern (BMI 25–29,9 bzw. ≥30). Ebenso konnten erhöhte proinflammatorische Biomarker (u.a. TSLP, IL-25 und IL-33) nachgewiesen werden. Zudem gab es eine negative Korrelation des BMI der Mutter zur Filaggrin-Expression in der Vernix caseosa und zur Staphylococcus-epidermidis-Besiedlung. Follow-up-Untersuchungen nach einem Jahr zeigten eine höhere Inzidenz von AD bei Nachkommen von Müttern mit Übergewicht und/oder Adipositas. Damit ist die Vernix caseosa ein möglicher Ansatz für vertiefende Studien zu Mechanismen, die beim Neugeborenen zum Risiko der Entstehung einer späteren AD beitragen.
Auf dem Weg zur personalisierten Medizin
Darüber hinaus sei man auf der Suche nach Endo- und Phänotypen des AE. «Wir sprechen noch immer vom atopischen Ekzem als Ganzem. Doch durch Untersuchungen von Speichel, Hautproben und Urin zeichnen sich einige Subtypen ab», meinte der Experte. Eine entsprechende Kategorisierung könnte dabei unterstützen, die jeweils optimale Therapie für die individuell betroffene Person auswählen zu können. Eine Studie bestimmte hierfür 143 Biomarker im Serum von 146 Patient:innen mit schwerer AD. Daraufhin konnten vier Serum-Biomarker-basierte Patientencluster identifiziert werden.2 So prädisponiert einer davon beispielsweise für zusätzliche Atemwegsallergien, während andere hier eher einen günstigeren Verlauf zeigen. «Es wird nicht den einen Biomarker für AD geben, sondern es wird eher eine Summe sein», führte Schmid-Grendelmeier aus. Durch moderne Methoden wie beispielsweise Proteomik lassen sich diese jedoch leichter identifizieren. In naher Zukunft könne man dann aller Voraussicht nach von Subtypen sprechen und vor allem bei Kindern den möglichen Verlauf des AE abschätzen.
Bei Verdacht auf Allergien und unklare Auslöser ermöglicht es die IgE-Messung mittels Chip-Technologien, neue Sensibilisierungsmuster zu erkennen.3 So lassen sich beispielsweise Rückschlüsse auf den Typ der AD ziehen. «Die Methoden sind sehr einfach anzuwenden und können sogar im Kapillarblut durchgeführt werden», erläuterte der Experte.
Waschen und Rückfetten – neue Erkenntnisse
Dass zu viel Hautpflege beim Kleinkind nicht nur wenig nützlich, sondern sogar schädlich sein kann, zeigen aktuell publizierte Daten. Die skandinavische Studie PreventADALL mit rund 2400 Säuglingen fand heraus, dass häufige Ölbäder die Hautbarrierefunktion verringern.4 Die Kinder wurden hierfür in vier Gruppen randomisiert: Gruppe 1 erhielt im Alter von 2 Wochen bis 8 Monaten mindestens 4x/Woche Ölbäder. In Gruppe 2 erfolgte eine Ernährungsbehandlung. Für die dritte Gruppe wurden die beiden vorgenannten Behandlungen kombiniert. Gruppe 4 blieb unbehandelt. Die Kinder wurden im Alter von 3, 6 und 12 Monaten untersucht. Es ergab sich kein Nachweis, dass die Interventionen in den Gruppen 1, 2 oder 3 im Säuglingsalter vor AD schützen. Ergänzende Untersuchungen ergaben, dass Ölbäder den transepidermalen Wasserverlust (TEWL) im Alter von drei Monaten sogar erhöhten.
Eine britische Forschungsgruppe untersuchte im Rahmen der BEEP(Barrier Enhancement for Eczema Prevention)-Studie rückfettende Massnahmen als AD-Prävention.5 Hierfür wurden 1394 Neugeborene mit hohem Risiko, ein Ekzem zu entwickeln, im ersten Lebensjahr entweder täglich mit Creme auf den gesamten Körper ausser der Kopfhaut behandelt oder nicht. Hinsichtlich der Ekzemrate zeigte sich nach zwei Jahren kein Unterschied (23% Behandlungsgruppe vs. 25% Kontrollgruppe). Die topischen Therapien mit wirkstofffreien Vehikeln erhöhten jedoch das Risiko von Hautinfektionen im frühen Säuglingsalter. «Das bedeutet nicht, dass Rückfetten und Hautpflege falsch sind, aber beides sollte in Massen erfolgen», meinte Schmid-Grendelmeier. Wichtig sind in diesem Zusammenhang edukative Massnahmen für Betroffene.
Therapeutische Aspekte bei AD
Zahlreiche Faktoren beeinflussen die Entstehung von AD: Neben einer Dysfunktion der Hautbarriere spielen Umwelteinflüsse eine wichtige Rolle. Hinzu kommen das Darm-Mikrobiom sowie die genetische Prädisposition.6 Die heute zur Verfügung stehenden Therapien adressieren laut Schmid-Grendelmeier zunehmend diese Punkte. Die Empfehlungen für die Behandlung des AE sehen einen vierstufigen Plan entsprechend des Schweregrades vor – von trockener Haut bis zu schwerem Ekzem. Am Anfang steht die rückfettende Basistherapie, die bis hin zur schweren Form ein wesentlicher Bestandteil der Behandlung bleibt (s. Abb.1).7 «Zudem sollten auf der Stufe eins Allergene vermieden werden, wenn entsprechende Allergien definiert sind», so Schmid-Grendelmeier. Hinzu kommen zu diesem Zeitpunkt bereits edukative Programme.
Bei milder AD sollten topische Kortikosteroide (TCS) oder Calcineurin-Inhibitoren (TCI) angewendet werden. Auf der dritten Stufe – moderate AD – ergänzt die Phototherapie das therapeutische Armamentarium. «Sehr wichtig ist hier oftmals die begleitende psychosomatische Betreuung der Betroffenen», hob Schmid-Grendelmeier hervor. Bei schweren Verlaufsformen greifen die Empfehlungen der Stufe vier, die den Einsatz von systemischen Therapeutika inklusive Biologika und JAK-Inhibitoren vorsehen. Systemische Steroide sollten nur ausnahmsweise und bei akuten Schüben eingesetzt werden. «Immunsuppressiva wie Azathioprin und MTX sind nicht zugelassen, es gibt aber zunehmend Studien, die zeigen, dass sie bei gezieltem Einsatz auch gut wirken. Sie sind deutlich günstiger als Biologika und JAK-Inhibitoren, haben aber ein heikleres Nebenwirkungsprofil», führte Schmid-Grendelmeier aus.
Volle Pipeline bei lokalen Therapien
«Es tut sich viel bei der topischen Therapie», so der Experte. So laufen unter anderem Studien zu Ruxolitinib sowie Delgocitinib, die sich laut Schmid-Grendelmeier als sehr wirksam bei lokalem Einsatz erweisen. Der topische Pan-JAK-Inhibitor Delgocitinib war zum Zeitpunkt des Referats in der Schweiz noch nicht zugelassen, stand jedoch im fortgeschrittenen Zulassungsverfahren. Seit 1. März 2025 ist er in der Schweiz zugelassen und erstattungsfähig. Delgocitinib inhibiert alle vier Januskinasen (JAK1, JAK2, JAK3 und TYK2) und wird daher ausschliesslich topisch eingesetzt werden, erklärte er. Systemisch seien zu viele Nebenwirkungen zu erwarten.
Eine aktuelle Netzwerk-Metaanalyse wertete Daten zur topischen Therapie von knapp 300 Studien mit insgesamt über 45000 AD-Patient:innen aus:8 Es zeigte sich, dass stark wirksame TCS, Tacrolimus 0,1% und JAK-Inhibitoren die wirksamsten topischen antiinflammatorischen Behandlungen sind. PDE-4-Inhibitoren wie Crisaborol, Roflumilast und Tapinarof (Letzteres ist in der EU nicht verfügbar) sind hingegen der Analyse zufolge wenig wirksam. «Topische Kortikosteroide haben nach wie vor ihren Platz in der Therapie», meinte Schmid-Grendelmeier.
Ein weiterer Aspekt bei der topischen Therapie ist die Beeinflussung des kutanen Mikrobioms. Eine Studie verglich die Auswirkungen einer Ekzemcreme mit 1% kolloidalem Hafer und einer Standard-Feuchtigkeitscreme auf das Hautmikrobiom und die Hautbarrierefunktion von Patient:innen mit leichtem bis mittelschwerem Ekzem (n=61).9 Nach 14 Tagen verringerte die Hafer-Ekzemcreme die mittleren Werte des Eczema Area Severity Index (EASI) um 51%. Im Gegensatz zur Behandlung mit der Standard-Feuchtigkeitscreme war die Behandlung in der Verum-Gruppe mit einer tendenziell geringeren Prävalenz von Staphylococcus-Spezies und einer höheren Mikrobiom-Diversität an den Läsionsstellen verbunden. Zudem verbesserten sich der pH-Wert der Haut, die Hautbarrierefunktion und die Hautfeuchtigkeit signifikant. «Bei der Beeinflussung des Hautmikrobioms ist noch vieles im Fluss», so Schmid-Grendelmeier.
Einsatz von Biologika und JAK-Inhibitoren
Auch bei den systemischen Therapien der schweren AD gab es grosse Fortschritte zu verzeichnen. «Wir sind sehr froh, dass sich hier das Spektrum mit Biologika und JAK-Inhibitoren erweitert hat», meinte der Experte. Aktuell stehen in der Schweiz mit Baricitinib, Upadacitinib und Abrocitinib drei JAK-Inhibitoren für die Behandlung der schweren AD zur Verfügung. Baricitinib zeigte sich auch bei anderen Indikationen wie Vitiligo und Alopecia areata als wirksam; Upadacitinib und Abrocitinib zeigen sich als sehr schnell wirksam. Das Nebenwirkungsprofil sei etwas heikler als bei den Biologika, berichtete Schmid-Grendelmeier.
Bei den Biologika ist bereits seit acht Jahren der IL-4-/IL-13-Inhibitor Dupilumab auf dem Markt, der inzwischen auch für die Therapie von Kindern ab 6 Monaten bei mittelschwerer bis schwerer AD zugelassen ist. Zudem ist in der Schweiz der gegen IL-13 gerichtete Antikörper Tralokinumab verfügbar; dazu wurde in diesen Monaten auch das ebenfalls gegen IL-13 gerichtete Lebrikizumab zugelassen. Noch keine Zulassung liegt für das gegen das Juckreiz-auslösende IL-31 wirkende Nemolizumab vor. Ein laut dem Experten interessanter Aspekt bei der Anwendung von Lebrikizumab sei der zu beobachtende lang anhaltende Therapieeffekt:10 Nach einer Induktionsphase mit zweiwöchiger Injektion erfolgt nach 16 Wochen eine monatliche Gabe, was auch bei Tralokinumab möglich ist. «Die Wirkung hält oft über den Einsatz hinaus sehr lange an», so Schmid-Grendelmeier.
Worin liegen die Hauptunterschiede in der Wirkweise von Biologika und JAK-Inhibitoren? Während Biologika ein oder zwei Interleukine bzw. deren Rezeptoren inhibieren, hemmen JAK-Inhibitoren eine breitere Palette immunologisch wirksamer Substanzen. Während die aktuell erhältlichen Biologika injiziert werden müssen, können JAK-Inhibitoren oral oder topisch angewendet werden.
Nebenwirkungen bei Dupilumab
Eine häufig unter der Therapie mit Dupilumab berichtete Nebenwirkung ist die Konjunktivitis. «Selten ist diese aber derart beeinträchtigend, dass die Behandlung abgebrochen werden muss», sagte Schmid-Grendelmeier. Sollte dennoch ein Therapiewechsel erwogen werden, zeigen Studiendaten u.a. ein gutes Ansprechen auf Tralokinumab.11 Weitere unter Dupilumab beobachtete Nebenwirkungen sind Blepharitis und Gesichtserytheme. Zudem gibt es Fallberichte von paradoxen Reaktionen wie Psoriasis.12 Auch das Aufflammen von Head-Neck-AD unter Dupilumab wurde beobachtet.13 Aus seiner eigenen klinischen Erfahrung berichtete der Experte, dass unter einer Dosisreduktion auf 300mg alle 4 Wochen eine Besserung des Gesichtserythems eintrat und die Wirkung auf das AE weiterhin bestehen blieb (n=3). Neue, laufende Studien deuten darauf hin, dass auch ein Wechsel auf JAK-Inhibitoren solche Reaktionen verringern kann.
Auswirkungen auf Schwangerschaft und Allergietests
Bislang gibt es keine Zulassung für den Einsatz von Dupilumab während einer Schwangerschaft. Die Applikation scheint zumindest in den frühen Phasen der Schwangerschaft nach bisherigen Daten weniger Fälle nicht kritisch zu sein.14 Wichtig ist es, die Zahl der Fehlgeburten und Frühgeburten unter Th2-gerichteter Therapie an ausreichend hohen Fallzahlen für eine belastbare Risikoabschätzung zu erfassen. Daher gibt es noch keine Empfehlungen in Positionspapieren und Leitlinien zur AD hinsichtlich eines bewussten Einsatzes von Dupilumab während einer Schwangerschaft. Derzeit laufen jedoch zwei prospektive Beobachtungsstudien zu dieser Thematik, deren Ergebnisse nicht vor 2026 bzw. 2027 zu erwarten sind.15
«Ein Thema, mit dem wir zunehmend konfrontiert sind, sind die Auswirkungen von Dupilumab auf Patchtest-Ergebnisse», berichtete Schmid-Grendelmeier. Hier ist sich die Literatur uneins: Während manche Studien zeigen, dass die Dupilumab-Einnahme keinen Einfluss auf den Patchtest hat,16 ergibt sich in anderen Untersuchungen eine reduzierte Sensitivität.17 Die Empfehlung laute daher, eine Epikutantestung – wenn möglich – vor Beginn der Dupilumab-Therapie zu veranlassen. Die Durchführung von Allergen-spezifischen Immuntherapien ist unter Biologika-Gabe möglich.18
Sicherheitsprofil von JAK-Inhibitoren
Im Vergleich zu therapeutischen Antikörpern treten unter JAK-Inhibitoren keine ophthalmologischen Nebenwirkungen, kein «Redface» sowie keine Arthritis auf. Jedoch kann es hier zu akneiformen Läsionen kommen, erläuterte der Experte. Bei Risikogruppen sei eine Infektanfälligkeit, insbesondere für Zoster, zu beobachten. In der Rheumatologie wurden kardiale Nebenwirkungen sowie ein erhöhtes Risiko für Thromboembolien berichtet. «Hier handelt es sich um eine abweichende Patientenpopulation sowie ein anderes Medikament. Da tut man den in der Dermatologie zugelassenen JAK-Inhibitoren wohl etwas unrecht», meinte Schmid-Grendelmeier. Nichtsdestotrotz sollte diese Substanzklasse bei Betroffenen mit einer entsprechenden Anamnese zurückhaltend eingesetzt werden.7
Im März 2023 wurde eine Black-Box-Warnung für JAK-Inhibitoren ausgesprochen:19 Es gebe mit dem JAK-Inhibitor Tofacitinib bei Patient:innen mit rheumatoider Arthritis ein erhöhtes Risiko für Malignome, schwerwiegende kardiovaskuläre Ereignisse (MACE), schwerwiegende Infektionen und Thrombosen sowie eine höhere Rate an Gesamtmortalität. Diese Risiken werden laut dem Schweizerischen Heilmittelinstitut als Klasseneffekte und relevant für alle für chronisch-entzündliche und dermatologische Erkrankungen zugelassenen JAK-Inhibitoren betrachtet. Schmid-Grendelmeier erwähnte in diesem Zusammenhang das Auftreten von nichtmelanozytärem Hautkrebs (NMSC): Dies sei in Zusammenhang mit den Substanzen, die in der Dermatologie eingesetzt werden, noch nicht belegt. Es gelte jedoch, dies zu beobachten.
Die Wahl der optimalen Therapie
Wie lässt sich nun für Patient:innen mit schwerer AD die individuell bestmögliche Behandlung gestalten? Schmid-Grendelmeier führte seine persönlichen Kriterien hierfür etwas aus. Zum einen können die verschiedenen Optionen mit dem Patienten/der Patientin besprochen werden («shared decision making»), zum anderen gibt es Kriterien, die für die eine oder andere Option sprechen. So empfehle sich beispielsweise beim Wunsch nach einer raschen Verbesserung sowie bei Spritzenangst ein (oraler) JAK-Inhibitor. Sind die Patient:innen >65 Jahre alt oder sind Komorbiditäten vorhanden, sollte bevorzugt ein Biologikum verordnet werden; für Kinder ab 6 Monaten ist lediglich Dupilumab zugelassen. Auch bei thromboembolischen oder kardiovaskulären Vorerkrankungen empfiehlt der Experte den Einsatz eines Biologikums. Ein Vorteil der bei AD einsetzbaren Biologika: Es sind im Gegensatz zu den JAK-Inhibitoren keine Laborkontrollen erforderlich. Dupilumab ist zudem für die Mitbehandlung verschiedener anderer Erkankungen, wie etwa Asthma bronchiale, geeignet. Zuletzt sollten auch die häufigsten Nebenwirkungen der jeweiligen Therapie in die individuelle Entscheidung miteinbezogen werden. Falls eine rasche Wirkung erwünscht ist oder nur ein vorübergehender Einsatz geplant wird, sind die JAK-Inhibitoren vorteilhafter – ebenso bei vorbestehenden konjunktivalen Erkrankungen. Zu beachten ist bei Letzteren ein korrekt erhobener Impfstatus, da unter JAK-Inhibitoren bestimmte Impfungen, etwa gegen Gelbfieber, nicht durchgeführt werden.
Für die Übernahme der Behandlungskosten durch die Krankenkassen sind Kostengutsprachen notwendig. Der Experte empfahl hierfür die Erhebung des Schweregrades des IGA (Investigator Global Assessment), der sich einfach und schnell im klinischen Alltag erfassen lasse.
Quelle:
Vortrag «Atopisches Ekzem» von Prof. Dr.med. Peter Schmid-Grendelmeier im Rahmen der Veranstaltung «Haus der Dermatologie» am 12. Dezember 2024 in Luzern
Literatur:
1 Cabalín C et al.: Vernix caseosa reveals mechanistic clues linking maternal obesity to atopic dermatitis pathogenesis. J Allergy Clin Immunol 2024; 153(3): 860-67.e1 2 Bakker D et al.: Biomarkers in atopic dermatitis. J Allergy Clin Immunol 2023; 151(5): 1163-8 3 Scala E et al.: A microarray-based IgE-molecular mimicry index (IgE-MMI): a biomarker for disease severity, clinical phenotypes, and therapeutic response in atopic dermatitis? Allergy 2024; 79(12): 3415-29 4 Rehbinder EM et al.: Frequent oil baths and skin barrier during infancy in the PreventADALL study. Br J Dermatol 2024; 191(1): 49-57 5 Bradshaw LE et al.: Emollient application from birth to prevent eczema in high-risk children: the BEEP RCT. Health Technol Assess 2024; 28(29): 1-116 6 Traidl-Hoffmann C et al.: Navigating the evolving landscape of atopic dermatitis: challenges and future opportunities: the 4th Davos declaration. Allergy 2024; 79(10): 2605-24 7 Wollenberg A et al.: Living EuroGuiDerm Guidelines for the systemic treatment of Atopic Eczema. European Dermatology Forum (EDF) 2025; verfügbar unter: https://www.guidelines.edf.one/guidelines/atopic-ezcema ; zuletzt aufgerufen am 19.3.2025 8 Lax SJ et al.: Topical anti-inflammatory treatments for eczema: network meta-analysis. Cochrane Database Syst Rev 2024; 8(8): CD015064 9 Capone K et al.: Effects of colloidal oatmeal topical atopic dermatitis cream on skin microbiome and skin barrier properties. J Drugs Dermatol 2020; 19(5): 524-31 10 Blauvelt A et al.: Efficacy and safety of lebrikizumab in moderate-to-severe atopic dermatitis: 52-week results of two randomized double-blinded placebo-controlled phase III trials. Br J Dermatol 2023; 188(6): 740-8 11 Achten R et al.: Switching from dupilumab to tralokinumab in atopic dermatitis patients with ocular surface disease: preliminary case series. Clin Exp Allergy 2023; 53(5): 586-9 12 Mirza FN et al.: Dupilumab-induced phenotype switch from atopic dermatitis to psoriasis is characterized by de novo interleukin-17A expression: a case report. Br J Dermatol 2021; 185(2): 432-4 13 Soria A et al.: Development or exacerbation of head and neck dermatitis in patients treated for atopic dermatitis with dupilumab. JAMA Dermatol 2019; 155(11): 1312-5 14 Avallone G et al.: Association between maternal dupilumab exposure and pregnancy outcomes in patients with moderate-to-severe atopic dermatitis: a nationwide retrospective cohort study. J Eur Acad Dermatol Venereol 2024; 38(9): 1799-808 15 vgl. aktuell laufende Studien zum Einsatz von Dupilumab während der Schwangerschaft, etwa https://clinicaltrials.gov/study/NCT04173442 und https://clinicaltrials.gov/study/NCT03936335 ; zuletzt aufgerufen am 12.3.2025 16 Bocquel S et al.: Impact of dupilumab on patch test results and allergic contact dermatitis: a prospective multicenter study. J Am Acad Dermatol 2024; 90(3): 512-20 17 Nedorost S et al.: To patch or not to patch on dupilumab: That is the question. J Am Acad Dermatol 2024; S0190-9622(24)03329-2 18 Yepes-Nuñez JJ et al.: Allergen immunotherapy for atopic dermatitis: systematic review and meta-analysis of benefits and harms. J Allergy Clin Immunol 2023; 151(1): 147-58 19 Schweizerisches Heilmittelinstitut swissmedic: DHPC – Januskinase (JAK)-Inhibitoren. Verfügbar unter https://www.swissmedic.ch/swissmedic/de/home/humanarzneimittel/marktueberwachung/health-professional-communication--hpc-/dhpc-januskinase-jak-inhibitoren.html , zuletzt aufgerufen am 12.3.2025
Das könnte Sie auch interessieren:
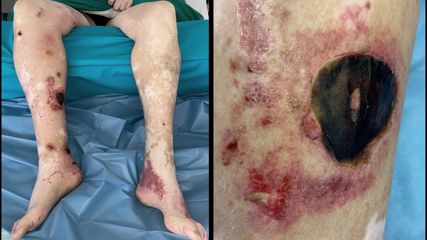
Hämorrhagische Läsionen nach Infekt: viele mögliche Differenzialdiagnosen
Eine 70-jährige Patientin stellt sich mit anhaltender Abgeschlagenheit, Rhinitis, Halsschmerzen und wiederkehrendem Schüttelfrost vor. Neu hinzugekommen sind schmerzhafte ...
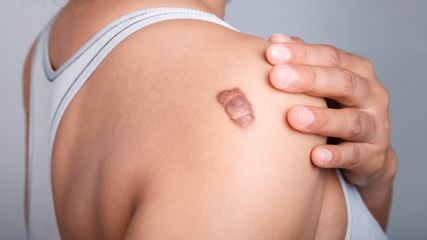
Narbenbehandlung ohne Devices
Für die Behandlung von Narben hat sich der Einsatz moderner Lasertechnologien als effektiv erwiesen. Doch wie kann man den Betroffenen helfen, wenn kein ablativer fraktionierter CO2- ...
Die menschliche Haut in der modernen Kunst
Dr. Ralph Ubl, Professor für neuere Kunstgeschichte an der Universität Basel, stellte sich der schwierigen Herausforderung, einem Raum voller erwartungsvoller Dermatologen das Organ Haut ...