Dysphagie bei der Huntington-Erkrankung
Autorin:
Beate Schumann-Werner, MSc
Lehr- und Forschungslogopädin
Klinik für Neurologie
Universitätsklinik RWTH Aachen
E-Mail: bschumann@ukaachen.de
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Neue Daten zeigen, dass neurogene Dysphagien bei der Huntington-Erkrankung anders als früher angenommen schon in frühen Stadien häufig vorkommen. Das klinische Muster und Bildgebungsdaten legen eine Störung vor allem der sensorischen Verarbeitung und der Koordination nahe. Welche Implikationen dies für Diagnostik und Therapie dieser lebensbedrohlichen Störung hat, skizziert der folgende Artikel.
Keypoints
-
Dysphagie bei der Huntington-Erkrankung ist kein rein motorisches Problem.
-
Stille Aspirationen sind häufig, auch in frühen Stadien.
-
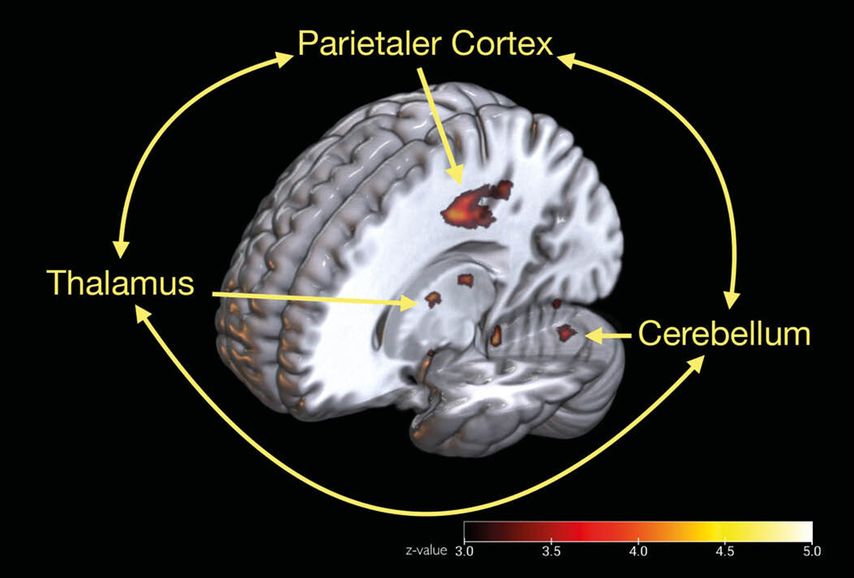
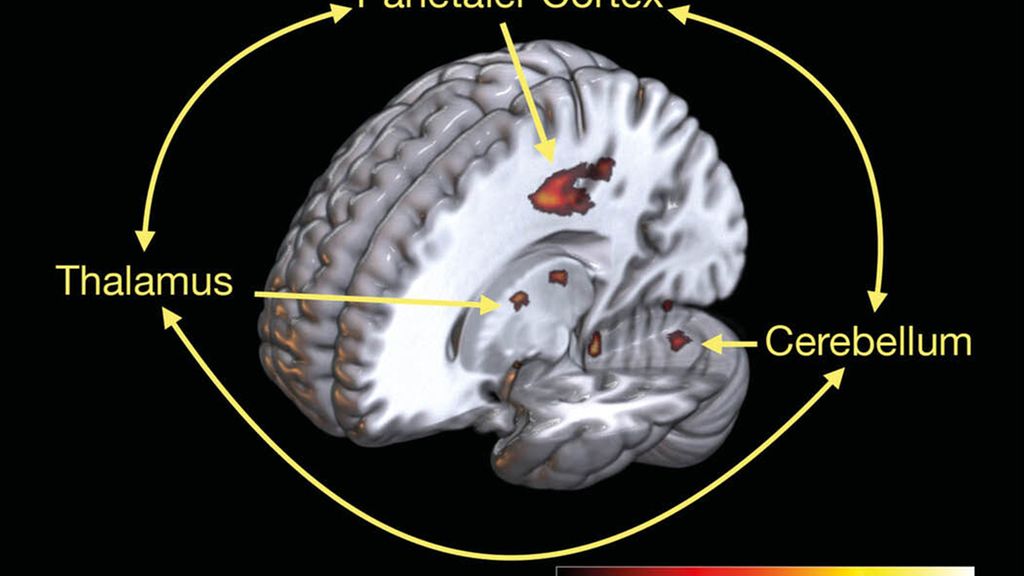
Atrophie in einem parieto-thalamo-zerebellären Netzwerk ist mit reduzierter Schlucksicherheit assoziiert.
-
Trotz hoher Prävalenz gibt es bisher keine evidenzbasierten Therapieverfahren.
Die Huntington-Erkrankung (engl. «Huntington’s disease», HD) ist eine autosomal-dominant vererbte neurodegenerative Erkrankung. Ursächlich für den Gendefekt ist eine CAG-Triplett-Repeatverlängerung im Huntington-Gen (HTT) auf Chromosom 4. Hierdurch kommt es zu einem progressiven Verlust von Nervenzellen in den Basalganglien (Striatum), Hirnrinde und Kleinhirn. Die Huntington-Erkrankung ist mit einer Prävalenz von ca. 5/100000 eine seltene Erkrankung, die sich typischerweise im mittleren Lebensalter manifestiert. Das klinische Bild ist sehr heterogen und äussert sich durch eine Trias aus motorischen, kognitiven und psychiatrischen Symptomen. Charakteristisch sind vor allem die choreatischen Bewegungen, jedoch kommen auch Depressionen und Affektstörungen bereits zu Beginn häufig vor. In der Spätphase der Erkrankung dominiert ein unterbeweglicher Phänotyp mit Rigor und Dystonie, zudem entwickeln die betroffenen Patienten eine Demenz. Die mittlere Überlebensdauer beträgt 15 Jahre.
Neurogene Dysphagien
Es ist bekannt, dass nahezu 100% der Patienten im Verlauf ihrer Erkrankung eine Dysphagie entwickeln. Die präzisen Mechanismen, die zur neurogenen Dysphagie bei der Huntington-Erkrankung führen, sind im Einzelnen noch unklar. Ein erhöhtes Aspirationsrisiko wird mit Sekundärkomplikationen wie Malnutrition, Dehydratation und Pneumonien in Verbindung gebracht. Letztere stellen neben Suizid die häufigste Todesursache bei der Erkrankung dar, auch Bolusereignisse treten auf. Trotz ihrer hohen Prävalenz gibt es bisher nur wenige Studien, die sich mit den Schluckstörungen bei der Huntington-Erkrankung befassen. Entsprechend fehlt es an evidenzbasierten Empfehlungen zu diagnostischen und therapeutischen Ansätzen.
Stand der Forschung
Bisher sind nur wenige Studien erschienen, die die Huntington-Dysphagie anhand einer grösseren Stichprobe und unter Einsatz apparativer Diagnostikverfahren wie z.B. der fiberoptischen endoskopischen Evaluation des Schluckens (FEES) oder der Videofluoroskopie des Schluckaktes (VFSS) untersuchten. Kagel & Leopold berichteten bereits 1992 retrospektiv anhand eines Kollektivs aus 35 mittels VFSS untersuchten Patienten, dass Auffälligkeiten in allen Phasen des Schluckaktes vorkommen.1 Hervorgehoben wurden u.a. eine choreatische Bewegungsstörung der Zunge, ein dyskoordinierter Schluckakt mit repetitivem Schlucken, eine prolongierte laryngeale Elevation, plötzliche Phasen der Einatmung und häufige Eruktationen. Eine aktuellere Studie von Keage et al. konnte an 49 Patienten retrospektiv ähnliche Pathomechanismen in der VFSS feststellen.3 Darüber hinaus berichteten sie von einem auffällig hohen Anteil stiller Aspirationen (32,7%). Bemerkenswert an dieser Studie ist, dass den Autoren von einigen Patienten (n=7) mehrere Verlaufsuntersuchungen vorlagen, aus denen kein klares Muster hinsichtlich einer Progredienz hervorging. Bei einigen Patienten blieb die Schluckfunktion trotz allgemeiner klinischer Verschlechterung stabil oder besserte sich sogar. Die Gründe hierfür bleiben noch unklar. Schindler et al. untersuchten 61 Patienten unterschiedlicher Krankheitsstadien mittels FEES und stellten fest, dass der durch die empfohlene Kostform definierte funktionelle Schluckstatus der Patienten, gemessen anhand der DOSS («dysphagia outcome severity scale»), signifikant mit den motorischen Beeinträchtigungen und der Erkrankungsdauer korrelierte.2 Eine Korrelation mit rein schluckphysiologischen Scores wie der validierten Penetrations-Aspirations-Skala (PAS) nach Rosenbek et al. wurde nicht untersucht.4
Während im Bereich der Diagnostik somit einige wenige Studien vorliegen, fällt dies im Bereich der Therapie deutlich reduzierter aus. In der bereits zitierten Arbeit von Kagel & Leopold wurde berichtet, dass in der VFSS angewandte kompensatorische und adaptive Verfahren zu einer gebesserten Schluckfunktion führten. Hinsichtlich rehabilitativer Therapieverfahren liegt bislang nur eine Studie von Reyes et al. vor, die den Effekt eines 4-monatigen respiratorischen Muskelkräftigungstrainings («respiratory muscle strength training») an 18 Huntington-Patienten randomisiert-kontrolliert untersuchten.5 Während sich die pulmonalen Funktionen in der experimentellen Gruppe gegenüber der Kontrollgruppe signifikant verbesserten, zeigten sich keine Effekte des Trainings auf die Schluckfunktion gemessen mittels eines Wassertests und eines Fragebogens, was methodisch eine deutliche Limitation darstellt. Ob die verbesserte Lungenfunktion protektiv gegen Pneumonien war, wurde nicht untersucht. Bedenkt man die in den diagnostischen Studien berichteten Pathomechanismen, insbesondere die gestörte Atem-Schluck-Koordination der Patienten, könnten sogenannte Skills-basierte therapeutische Ansätze (z.B. mittels sEMG-Biofeedback) in frühen Krankheitsstadien eine vielversprechende Therapiemassnahme gegenüber reinem Krafttraining darstellen. Untersuchungen hierzu stehen jedoch noch aus.
Bezüglich einer Pharmakotherapie existieren gar keine gesicherten Daten. Von anderen neurodegenerativen Erkrankungen, wie z.B. der Parkinson-Erkrankung oder den Demenzen, ist jedoch bekannt, dass Neuroleptika eine potenzielle Verschlechterung der Schluckfunktion bewirken können. Bei der Huntington-Erkrankung ist dies bislang nur anhand eines klinischen Schluckassessments untersucht worden.6 Hier zeigten sich keine systematischen Effekte. Ebenso ist unklar, inwieweit die bislang nur experimentell durchgeführte tiefe Hirnstimulation Auswirkungen auf die Schluckfunktion bei Huntington-Patienten hat. Eine sehr gute Übersicht zur aktuellen Studienlage bei der Huntington-Dysphagie bietet das kürzlich erschienene Review von Pizzorni et al., das in Ermangelung an publizierten Studien auch relevante Abstracts und Kongressbeiträge beinhaltet.7
Eigene Daten und klinische Erfahrungen
Im Rahmen einer prospektiven Beobachtungsstudie am Euregionalen Huntington-Zentrum der Uniklinik Aachen wurde die Prävalenz von Dysphagien bei Huntington-Patienten apparativ mittels FEES untersucht und in Bezug gesetzt zu validen Scores der Motorik, Kognition und Alltagsfunktion sowie MRT-Imagingparametern zur Hirnatrophie. Ziel war es, Prädiktoren für das Vorliegen einer Dysphagie sowie die dazugehörigen neuronalen Korrelate zu ermitteln. Anders als in früheren Studien wurden auch klinisch unauffällige Patienten untersucht. Insgesamt konnten 34 Patienten der Krankheitsstadien I–IV eingeschlossen werden, davon befanden sich 20 (58,9%) in einem frühen Stadium (≤II). Als Marker für eine reduzierte Schlucksicherheit wurde der PAS in der Adaptation nach Steele & Grace-Martin verwendet.8 Überraschenderweise zeigten 70,6% der Patienten eine Penetration oder Aspiration mindestens einer untersuchten Konsistenz. 29,4% zeigten eine Aspiration, die in 80% der Fälle still verlief. Dies ist ein bemerkenswert hoher Anteil gemessen an der Überzahl früh betroffener Patienten. Nach Korrektur für Quellen von Pseudokorrelationen zeigte sich in unserer Kohorte kein Zusammenhang der Schlucksicherheit mit motorischen, kognitiven oder funktionellen Scores. Auch ein Zusammenhang mit der verordneten Neuroleptika-Gesamtdosis konnte nicht beobachtet werden. Damit wird deutlich, dass das Vorliegen und die Schwere einer Dysphagie bei Huntington im frühen Stadium nicht ohne Weiteres aus klinischen Daten abgeleitet werden können. In späten Stadien, die bei uns unterrepräsentiert waren, muss gemäss vorliegender Literatur ohnehin vom Vorliegen einer relevanten Dysphagie ausgegangen werden.
Erstmals konnten wir zudem die neuronalen Grundlagen der Huntington-Dysphagie identifizieren: Patienten mit reduzierter Schlucksicherheit zeigten signifikante Hirnatrophie in einem parieto-thalamo-zerebellären Netzwerk (Abb.1). Diese Areale dienen vor allem sensorischen und koordinativen Aspekten der Schluckmotorik. Bemerkenswert hierbei ist, dass die für die Huntington-Erkrankung und ihre motorische Progression typische Atrophie im Nucleus caudatus hier keine Rolle zu spielen scheint. Diese Beobachtung zusammen mit dem hohen Anteil stiller Aspirationen in der FEES verdeutlicht, dass der Huntington-Dysphagie zumindest in frühen und mittleren Stadien keine dominierende motorische Komponente zugrunde liegt. Unsere klinische Erfahrung zeigt zudem, dass auch die Eigenwahrnehmung der Patienten in Bezug auf die Schluckstörung deutlich reduziert ist, was die Wertigkeit von Fragebögen und Selbst-Reports erheblich infrage stellt. Somit kommt der apparativen Dysphagiediagnostik, z.B. mittels FEES, in der Objektivierung und Graduierung der Dysphagie eine wichtige Rolle zu.
Weitere Studien zur prognostischen Relevanz, insbesondere longitudinaler Art, sind dringend notwendig, um den Patienten adäquate Empfehlungen und Behandlungsoptionen anzubieten.
Literatur:
1 Kagel MC, Leopold NA: Dysphagia in Huntington’s disease: a 16-year retrospective. Dysphagia 1992; 7: 106-14 2 Schindler A et al.: Fiberoptic endoscopic evaluation of swallowing in early-to-advanced stage Huntington’s disease. Sci Rep 2020; 10(1): 15242 3 Keage M et al.: Imaging and clinical data on swallowing function of individuals with Huntington’s disease and dysphagia. J Huntingtons Dis 2020; 9(2): 163-71 4 Rosenbek JC et al.: A penetration-aspiration scale. Dysphagia 1996; 11(2): 93-8 5 Reyes A et al.: Respiratory muscle strength training on pulmonary and swallowing function in patients with Huntington’s disease: a pilot randomized controlled trial. Clin Rehabil 2015; 29: 961-73 6 de Tomasso M et al.: Dysphagia in Huntington’s disease: correlation with clinical features. Eur Neurol 2015; 74: 49-53 7 Pizzorni N et al.: Management of dysphagia in Huntington’s disease: a descriptive review. Neurol Sci 2020; 41: 1405-17 8 Steele CM, Grace-Martin K: Reflections on clinical and statistical use of the penetration-aspiration scale. Dysphagie 2018; 32(5): 601-16
Das könnte Sie auch interessieren:
Chronische Diarrhö – so gelingt die Untersuchung
Die chronische Diarrhö ist Symptom verschiedener Erkrankungen. Wie nach dem Auslöser bestmöglich gesucht wird, erklärte Prof. Alain Schoepfer in seinem Referat am Jahreskongress der ...
Chirurgische Therapie: wie und für wen?
Für Patient:innen mit gastroösophagealer Refluxkrankheit (GERD) oder mit einer axialen Hiatushernie kann eine chirurgische Behandlung indiziert sein. Entscheidend ist dabei die richtige ...
Zöliakie: Stand der Entwicklung pharmakologischer Therapieoptionen
Viele Patienten mit Zöliakie haben trotz glutenfreier Diät weiterhin Beschwerden. Zurzeit befinden sich einige innovative therapeutische Ansätze in Entwicklung: u.a. ein Inhibitor der ...