CED: „First come, first served“ – Entscheidungshilfen bei der Therapiewahl
Autorin:
OÄ Dr. Sonja Heeren
Universitätsklinik für Innere Medizin I
Gastroenterologie-Hepatologie, Nephrologie, Stoffwechsel und Diabetologie
Uniklinikum Salzburg
E-Mail: s.heeren@salk.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Warum erscheint uns eine frühzeitige bzw. punktgenaue Therapie bei chronisch-enzündlichen Darmerkrankungen (CED) überhaupt wichtig? Eine unzureichend behandelte Inflammation führt mit der Zeit zu irreversiblen Gewebsschäden und häufig zur intestinalen Fibrose. Zu Beginn der Erkrankung herrschen noch eine hohe entzündliche Aktivität und kaum strukturelle Veränderungen vor. In diesem „window of opportunity“ erzielen die heutigen Therapiemöglichkeiten noch die größte Effektivität.
Keypoints
-
Ein frühzeitiger Therapiebeginn bei CED-Patienten ist wichtig, um die durch die aktive Inflammation verursachten strukturellen Schädigungen zu minimieren.
-
Vermutlich noch wichtiger als die Medikamentenwahl ist es, mithilfe der Stride-II-Kriterien die gewählte Therapie engmaschig zu überwachen, anzupassen und ggf. abzusetzen.
-
Alle CED-Patienten haben ihre eigene Krankheitsgeschichte und somit ist die Therapie individuell zu wählen.
-
Patienten sollen immer in Therapieentscheidungen so weit als möglich miteingebunden werden.
Stride-Kriterien
Bereits in der Vedolizumab-Zulassungsstudie GEMINI2 konnte rein für den Endpunkt klinische Remission eine Verdoppelung der Patientenzahl bei einem Krankheitsverlauf unter 3 Jahren im Vergleich mit Patienten, deren Krankheitsdauer über 7 Jahrebetrug, erzielt werden. Diese Erkenntnis hatnicht nur die Studienlandschaft hinsichtlich ihrer Endpunkte verändert, sondern auch unseren klinischen Alltag. In den Anti-TNF-Zulassungsstudien galt als primärer Endpunkt noch das klinische Ansprechen, in den rezenten Studien geht man bis zur Zielsetzung der histologischen Remission.
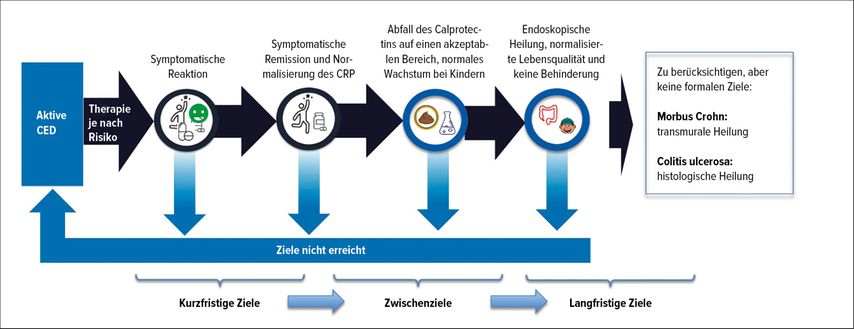
All dies spiegelt sich in den Stride-II-Kriterien (Abb. 1) wider, nach denen als langfristiges Ziel nicht nur die in der Routine schon fix eingeplante endoskopische Remission ein Langzeitkriterium ist, sondern auch die histologische Remission bei der Colitis ulcerosa (CU) in Erwägung gezogen werden sollte. Zwar konnten in den letzten Jahren neben den Anti-TNF-Therapien zahlreiche weitere Innovationen die Therapielandschaft bei chronisch-entzündlichen Darmerkrankungen (CED) erweitern, aber auch keiner dieser Substanzen gelang es bis dato, bei mehr als 50% der Patienten eine steroidfreie oder endoskopische Remission zu erzielen.
Abb. 1: Therapieziele in der Behandlung der Colitis ulcerosa und des Morbus Crohn (modifiziert nach Turner D et al.: Gastroenterology 2021; 160(5): 1570-83)
„First come, first served“
Zwar wachsen unsere Therapieziele, aber bis heute fehlen uns prädiktive Biomarker, die uns helfen, das richtige Medikament oder die richtige Medikamentenkombination für den richtigen Patienten zu finden. Bekannt ist, dass die erste Therapielinie die wirksamste ist und mit jeder weiteren Linie die Chance auf eine Remission sinkt. Somit liegt weiterhin die Verantwortung dieser Auswahl in den Händen der betreuenden Ärzte. Aber welche Entscheidungshilfen werden von uns angewendet?
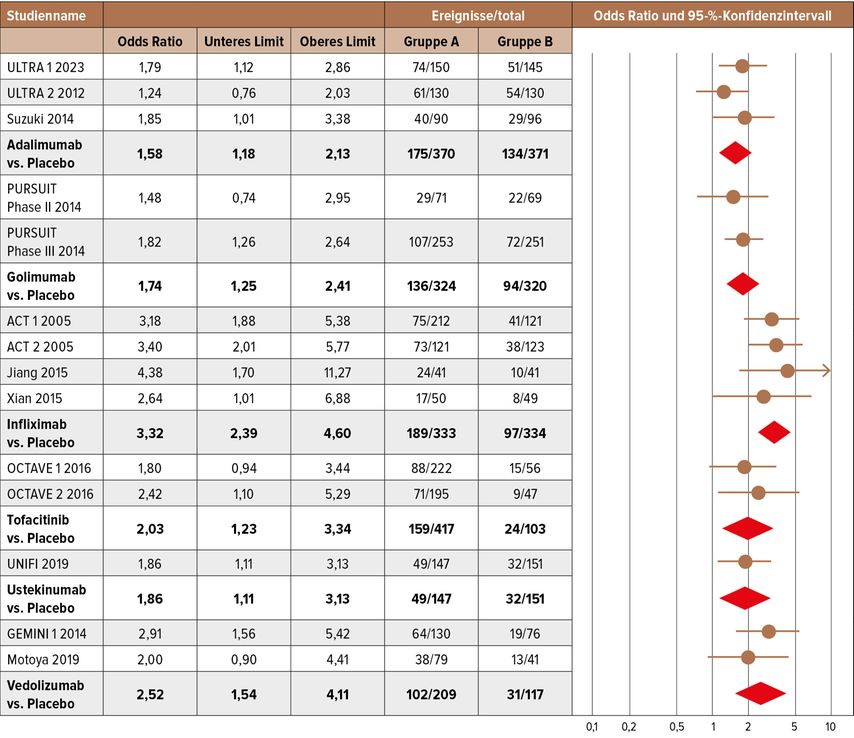
Denn Vergleiche der einzelnen Medikamente sind schwierig, da alle Zulassungsstudien nur darauf ausgerichtet sind, die Wirkung der einzelnen Substanz versus Placebo aufzuzeigen. Head-to-Head-Studiendesigns existieren nur in einem geringen Ausmaß und für die neuen Substanzklassen der „small molecules“ noch überhaupt nicht. Metaanalysen können uns eine Hilfestellung sein, aber es gilt zu beachten, dass jedes Studiensetting anders ist (Tab. 1).
Tab. 1: Metaanalyse: Wirksamkeit von Erst- und Zweitlinien-Pharmakotherapien bei Biologika-naiven Patienten mit mittelschwerer bis schwerer aktiver Colitis ulcerosa in Bezug auf die Induktion (A) einer klinischen Remission und (B) einer endoskopischen Verbesserung (modifiziert nach Singh S et al.: Clin Gastroenterol Hepatol 2020; 18(10): 2179-91.e6.)
Entscheidungshilfe 1: Wirkmechanismus des Medikamentes
Neben den bekannten Mechanismen der TNF-Blocker und den darmselektiven Integrin-Hemmern stehen uns nun auch die IL-23-Inhibitoren zur Verfügung, welche unter anderem die Ausreifung der Th17-Zellen beeinflussen oder auch die S1P-Modulatoren, die die Auswanderung der neu gebildeten Lymphozyten aus den Mukosa-Lymphknoten verhindern. Mit den Januskinase(JAK)-Inhibitoren, welche Einfluss auf die STAT-Signalwege in den Effektorzellen nehmen, erweitert eine weitere Substanzklasse unser Armamentarium.
Entscheidungshilfe 2: Medikamentencharakteristika
Spezifische zielgerichtete Biologika
-
Spezifische zielgerichtete Biologika (z.B. Adalimumab) werden i.v. oder s.c. verabreicht.
-
Die Wirksamkeit ist abhängig von ihrer Exposition im Körper und nicht rein dosisabhängig (z.B. führt Albuminmangel im schweren Schub zur verminderten Wirkung durch herabgesetzte Exposition).
-
Eine Dosissteigerung ändert nichts an ihrer Spezifität.
-
Bekannte Immunogenität
-
Es sind einige nicht zielgerichtete Nebeneffekte bekannt, welche unabhängig von Dosis und Exposition sind (z.B. durch Anti-TNF-Therapie induzierte Psoriasis).
Selektive „small molecules“
-
Selektive „small molecules“ sind orale Substanzen.
-
Ihre Effektivität ist abhängig von der relativen Inhibierung, Potenz, Dosis und Exposition.
-
Dies gilt auch für die Nebenwirkungen.
-
Steigt die Exposition, verändert sich das Inhibierungsprofil und somit wird auch das Nebenwirkungsspektrum breiter.
Entscheidungshilfe 3: Verabreichungsform
Dies ist sicherlich ein Kriterium, bei dem auch die Patientenentscheidung miteinfließen sollte. Laut der rezenten Umfragestudie ACCEPT-2 in Frankreich von Buisson et al. hat sich gezeigt, dass nach wie vor 65,8% aller Patienten eine orale Therapie bevorzugen würden und nur 12,8% eine i.v. Variante. Wobei die Akzeptanz stark abhängig von der Einnahmefrequenz und der Vortherapie ist. Subkutane Varianten mit langen Intervallen zwischen den Applikationen waren dann die am besten akzeptierten Verabreichungsformen. Jedoch ist auch hier immer eine individuelle Entscheidung zu treffen und auch mögliche Complianceprobleme bei oralen oder selbstständig durchgeführten subkutanen Regimes sind zu berücksichtigen.
Entscheidungshilfe 4: Wirkeintritt
Hier stellt sich immer die Frage, wie hoch tatsächlich die aktuelle Inflammation istund wie rasch das jeweilige Medikament seine Wirkung zeigenkann. Zu Zeiten der Anti-TNF war ein Bridging mit Steroiden meist notwendig. Mit Einführung der JAK-Inhibitoren stellt sich vermutlich ein neues Zeitalter ein. Bei einem klinischen Wirkeintritt dieser Medikamentengruppe innerhalb der ersten Woche wird ein Steroidverzicht möglich sein. In den Upadacitinib-Zulassungsstudien U-EXCEL und U-EXCEED für die CU konnte bereits zu Tag 6 eine signifikante Stuhlfrequenzreduktion unter 3 und eine Verbesserung des „abdominal pain scores“ ≤1 bei 23% aller Patienten erzielt werden.
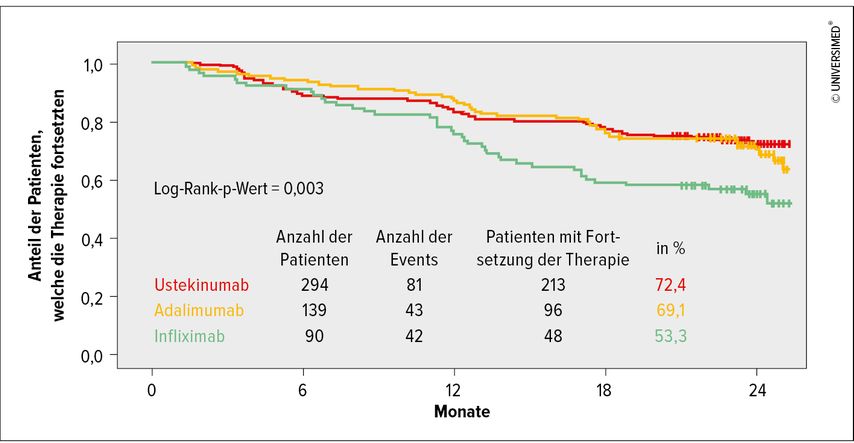
Nicht aus den Augen darf man aber trotzdem die Langzeiteffektivität der jeweiligen Therapie verlieren, da es sich bei der CED um eine lebenslange Erkrankung handelt. So konnte in Real-World-Daten der RUN-CD-Beobachtungsstudie von Bokemeyer et al. dargestellt werden, dass nach 24 Monaten nur mehr 53,3% aller Patienten auf der Infliximabtherapie sind vs. 69,1% bei Adalimumab und 72,4% bei Ustekinumab. Das anfängliche Ansprechen aller drei Therapien war ähnlich (Abb. 2).Die Gründe für die Therapieabbrüche sind vielfältig, jedoch im Vordergrund stehen hier sicher die Immunität und die verschiedenen Sicherheitsprofile.
Abb. 2: Behandlungspersistenz über 24 Monate in der prospektiven Beobachtungsstudie RUN-CD (modifiziert nach Bokemeyer et al.: Journal of Crohn’s and Colitis 2019; 13(1): S486)
Entscheidungshilfe 5: extraintestinale Manifestationen
Extraintestinale Manifestationen (EIM) treten bei 43% aller Morbus-Crohn(MC)- und 31% aller CU-Patienten auf, wobei ein Teil dieser Manifestationen – wie z.B. das Erythema nodosum – mit der Krankheitsaktivität assoziiert ist und z.B eine primär sklerosierende Cholangitis unabhängig von der Aktivität verläuft. Ein Teil dieser Patientengruppe weist nicht nur eine EIM auf, sondern gleich mehrere. In der rezent durchgeführten multizentrischen, retrospektiven EMOTIVE-Studie mit 99 Erwachsenen mit CED war mit 69,7% die Arthralgie und mit 21,2% die periphere Spondylarthropathie die häufigste EIM. Nach wie vor spielen hier die Anti-TNF-Therapien hinsichtlich ihres Wirkspektrums eine große Rolle, aber sicherlich profitieren diese Patienten auch von den Neuentwicklungen der JAK-Inhibitoren.
Hautmanifestationen treten bei einem Drittel aller Patienten auf, wobei hier sicherlich vor allem bei MC die Fissuren und die Stomatitis aphtosa am meisten verbreitet sind. Aber auch nicht zu vernachlässigen ist hier die Psoriasis, gelegentlich kombiniert mit einer Psoriasis-Arthritis. Hier steht uns mit den neuen IL-23- und Il-23/IL-12 Inhibitoren eine sehr effektive Substanzklasse zur Verfügung. Hinsichtlich ihrer Wirkung beim Erythema nodosum oder dem Pyoderma gangraenosum gibt es bis dato nur Fallberichte. Hier erscheint weiterhin die Anti-TNF-Therapie als bewährt und wirksam.
Die Multiple Sklerose gilt wohl eher als seltene Komorbidität der CED, aber man wird wohl zukünftig eher die Substanzklasse der S1P-Modulatoren wählen.
Entscheidungshilfe 6: Komplikationen der CED
Weit im Vordergrund rankt wohl die fistulierende Erkrankung. Rund 40% aller Crohn-Patienten entwickeln in ihrem Krankheitsverlauf mindestens eine Fistel, ca. 20% eine perianale Fistel. Lange galt der TNF-Blocker Infliximab als die vorherrschende Therapiemodalität. Aber auch hier konnte für die neueren Medikamente ein positiver Effekt gezeigt werden. In einer Post-hoc-Analyse der drei Upadacitinib-Zulassungsstudien U-EXCEL, U-ENDEED und U-ENDURE konnten 21,1% der Patienten mit Upadacitinib 30mg zu Woche 52 einen externen Verschluss der Fisteln erzielen. Diese ersten Daten geben uns Hinweise, dass auch neuere Substanzklassen in diesem Gebiet ihre Wirkung zeigen könnten. Detaillierte und vor allem für Fisteln gepowerte Studien fehlen allerdings bis dato noch. Zu beachten gilt es, dass gerade bei Fistelleiden eine höhere Dosis des Medikamentes notwendig ist.
Entscheidungshilfe 7: Sicherheitsprofil
Prinzipiell ist zu sagen, dass alle am Markt vorhandenen Medikamente ein entsprechendes Sicherheitsprofil aufweisen, sonst wäre ihnen wohl die Zulassung verwehrt geblieben. Angesichts des unterschiedlichen Entwicklungsstandes der einzelnen Substanzen ist es schwierig, diese zu vergleichen. Vielmehr muss man die individuellen Patientenspezifitäten betrachten. Je älter ein Patient ist, desto höher wird sein individuelles Risiko hinsichtlich z.B. kardiovaskulärer Ereignisse und Infektionen unabhängig von seiner Therapie sein. In dieser Gruppe wird man wohl eher auf Medikamente mit günstigem Nebenwirkungsprofil wie Vedolizumab, IL-23- und IL-23/Il-12-Inhibitoren zugreifen.
Aber bei allen Sicherheitsbedenken hinsichtlich möglicher Nebenwirkungen darf man das allerhöchste Risiko für sämtliche Komplikationen (Infektionen, Karzinom, venöse Thrombembolie etc.) – die aktive Inflammation – nicht vergessen. Somit wird man bei einer hohen Inflammationslast immer auf die möglichst potenteste Substanz mit Berücksichtigung der Kontraindikationen zugreifen.
Schlussfolgerung
Leider sind wir nach wie vor nicht in der Lage, das richtige Medikament für den richtigen Patienten unter Berücksichtigung seines Genoms, Mikrobioms, Immunoms und Exposoms herauszufiltern. Im Moment ist es vermutlich noch wichtiger, überhaupt frühzeitig mit einer Therapie zu beginnen und diese engmaschig hinsichtlich der angestrebten Endpunkte zu überwachen. Bei Nichterreichen dieser sollte das Therapieregime rasch intensiviert bzw. geändert werden. Um diese Ziele möglichst optimal zu erreichen, ist es immer wichtig, mit dem Patienten gemeinsam klare Therapieziele zu definieren und ihn soweit wie möglich in Therapieentscheidungen einzubeziehen.
Fest steht auch, dass alle unsere Patienten ihre individuellen Krankheitsgeschichten mitbringen und somit vorerst keine allgemeinen Empfehlungen für die Reihenfolge der Medikamente gegeben werden können.
Literatur:
bei der Verfasserin
Das könnte Sie auch interessieren:
Antirefluxbarriere des LES – ein Auslaufmodell?
Hauptursache für das Auftreten einer gastroösophagealen Refluxerkrankung ist ein Defekt der sogenannten Antirefluxbarriere, zu der der untere Ösophagussphinkter (LES) zählt. Moderne ...
Wenn die Magensonde nicht fördert: der seltene Fall eines Magenabszesses
Der vorliegende Fallbericht soll die Aufmerksamkeit auf die seltene Pathologie des Magenwandabszesses lenken, die mit einem eindrucksvollen Ausprägungsgrad initial eine falsche ...
Perioperative Ernährung bei gastrointestinalen Eingriffen
Im Bereich der perioperativen Ernährung bei geplanten Operationen am Magen-Darm-Trakt wurden in den letzten Jahren einige Dogmen über Bord geworfen – mit dem Ziel, den Patienten ...
_A.jpg)
