Immuntherapien in allen Krankheitsphasen des Melanoms
Bericht:
Dr. Ine Schmale
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Vor mehr als 10 Jahren begann die Erfolgsgeschichte der Checkpoint-Inhibitoren beim metastasierten Melanom. Nun rückt die Immuntherapie in die neoadjuvante Therapiephase vor, behält aber einen hohen Stellenwert auch für die metastasierte Situation. Laut Ergebnissen der SECOMBIT-Studie ist die doppelte Checkpoint-Blockade in der ersten Therapielinie gegenüber einer zielgerichteten Therapiekombination zu bevorzugen. Für spätere Therapielinien könnten auch tumorinfiltrierende Lymphozyten effektive Optionen sein. Welche weiteren Erkenntnisse der diesjährige ESMO-Kongress brachte, haben wir hier für Sie zusammengefasst.
Pembrolizumab-Therapie: je früher, desto besser
In der SWOG-S1801-Studie wurde der Frage nachgegangen, ob die neoadjuvante Immuncheckpoint-Blockade beim resektablen Melanom tatsächlich eine Antitumor-Immunantwort hervorruft oder ob die kurative Operation einfach nur verzögert oder sogar negativ beeinflusst wird.1 345 Patienten mit resektablem Melanom im Stadium IIIB–IV wurden in die Studie eingeschlossen und 313 Patienten erhielten randomisiert eine adjuvante Behandlung (18 Zyklen Pembrolizumab nach Resektion) oder eine perioperative Behandlung (3 Zyklen Pembrolizumab vor und 15 Zyklen nach Resektion). Primärer Endpunkt war das ereignisfreie Überleben (EFS). Als Ereignisse galten einerseits Progression oder Toxizität, die eine Operation verhinderten, andererseits der Umstand, dass eine adjuvante Therapie nicht innerhalb von 84 Tagen nach der Operation begonnen werden konnte oder ein Melanomrezidiv nach der Operation auftrat. Auch das Sterben des Patienten aufgrund jedweder Ursache wurde als Ereignis verzeichnet.
Zur Zeit der Auswertung waren noch 41 bzw. 43 Patienten unter adjuvanter Therapie, 40 bzw. 50 Patienten hatten die Studientherapie komplettiert, 71 bzw. 59 Patienten hatten die Therapie abgebrochen und 7 bzw. 2 Patienten hatten ihre Einwilligung entzogen. Das Alter der Patienten betrug median 62 bzw. 64,5 Jahre. Bei 24 bzw. 27% der Patienten lag ein bekannter positiver und bei jeweils 40% ein bekannter negativer BRAF-Status vor.
Mit dem neoadjuvanten Start der Therapie wurde ein signifikant längeres EFS erreicht im Vergleich zur rein adjuvanten Therapie (HR:0,58; 95% CI: 0,39–0,87; p=0,004). Nach 2 Jahren waren 49% der Patienten im adjuvanten Studienarm versus 72% im perioperativen Arm ohne Ereignis. Der Unterschied im Gesamtüberleben («overall survival», OS) erreichte die statistische Signifikanz, bei bisher nur 36 Todesfällen, nicht (HR:0,63; 95% CI: 0,32–1,24; p=0,18).
Nivolumab und Ipilimumab adjuvant im Stadium IV NED
In der prospektiven, randomisierten und placebokontrollierten IMMUNED-Studie wurde bei Melanompatienten im Stadium IV ohne erkennbare Erkrankung (NED) nach kompletter Resektion oder Radiatio eine adjuvante Therapie mit Nivolumab plus Ipilimumab versus Nivolumab versus Placebo gegeben. Es wurden 167 Patienten eingeschlossen und nach einer medianen Nachbeobachtungszeit von 27,4 Monaten ein signifikant verlängertes rezidivfreies Überleben (RFS) in den Verumarmen gegenüber Placebo publiziert. Mit nunmehr 49,2 Monaten medianer Nachbeobachtung wurden beim ESMO die finalen RFS-Daten sowie die ersten und finalen Ergebnisse zum OS präsentiert.2
Die in die IMMUNED-Studie eingeschlossenen Patienten waren 45–66 Jahre alt, mit einem Alters-Median von 52, 57 und 59 Jahren in den drei Studienarmen. 95–100% der Patienten wiesen <3 betroffene Organlokalisationen auf. Etwa die Hälfte der Patienten hatte eine PD-L1-Expression ≥5% und bei 40–48% der Patienten lag eine BRAF-Mutation vor. Zu einer frühzeitigen Beendigung der Therapie kam es bei 78,6% der Patienten im Nivolumab-plus-Ipilimumab-Arm, bei 59,3% der Patienten im Nivolumab-Arm und bei 78,8% der Patienten im Placeboarm. Nur im Studienarm mit der doppelten Immunblockade brachen Patienten die Therapie häufiger bereits nach einer Dosis (21,4 vs. 1,7 vs. 1,7%) oder zwei Dosen (28,6 vs. 1,7 vs. 1,9%) der Studienmedikation ab. Insgesamt erhielten die Patienten im Median 8 (5–17) Dosen der Kombinationstherapie, 18 (12–32) Dosen der Monotherapie sowie 19 (12–30) Dosen Placebo.
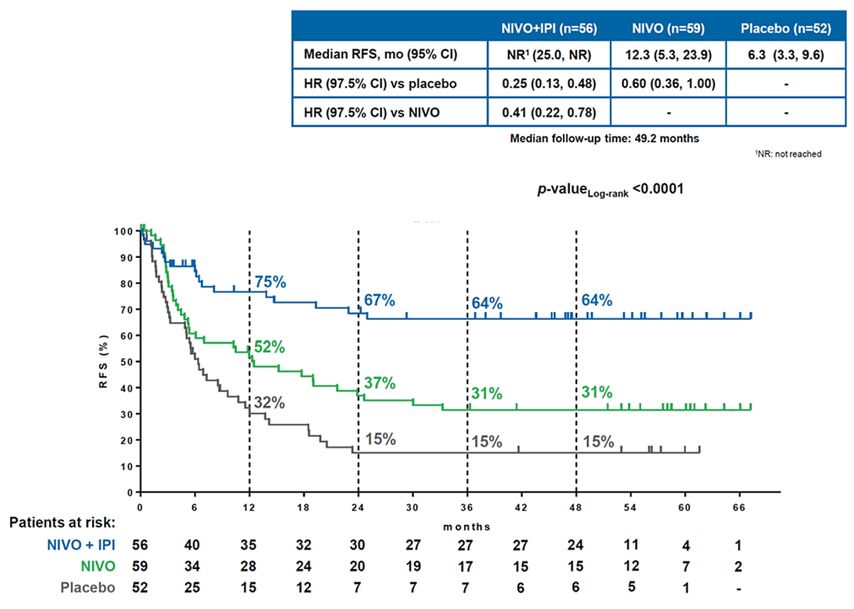
Die finalen Daten zum RFS zeigten ein signifikant verbessertes Ergebnis für die doppelte Immunblockade gegenüber Placebo (HR:0,25; 97,5% CI: 0,13–0,48; p<0,0001) sowie gegenüber der Nivolumab-Monotherapie (HR:0,41; 97,5% CI: 0,22–0,78; p<0,001). In den drei Studienarmen wurde das Erreichen eines Plateaus der RFS-Rate bei 64% vs. 31% vs. 15% beobachtet (Abb. 1). Der signifikante RFS-Vorteil übersetzte sich im Studienarm mit Nivolumab plus Ipilimumab gegenüber Placebo auch in einen klinisch relevanten OS-Vorteil (HR:0,41; 95% CI: 0,17–0,99; p=0,13). Im Vergleich von Nivolumab versus Placebo wurde das Risiko für ein Rezidiv um 40% (HR:0,60; 97,5% CI: 0,36–1,00; p=0,02) und für das Versterben um 25% (HR:0,75; 95% CI: 0,36–1,56) reduziert. Nach 48 Monaten lebten noch 84% versus 73% versus 63% der Patienten in den drei Studienarmen. Da Patienten des Placeboarms nach Krankheitsrückfall mehrheitlich mit einer anti-PD-1-basierten Therapie behandelt wurden, hatte dies wahrscheinlich einen Einfluss auf das OS-Ergebnis, insbesondere im Vergleich von Nivolumab versus Placebo.
Abb. 1: Rezidivfreies Überleben (RFS) bei Melanompatienten im Stadium IV NED unter adjuvanter Therapie mit Nivolumab + Ipilimumab vs. Nivolumab vs. Placebo (nach Schadendorf D et al. 2022)2
Wie bereits in anderen Studien beobachtet wurde, bestätigte sich auch in der IMMUNED-Studie die gute Wirksamkeit der immunonkologischen Therapie bei Patienten mit BRAF-Mutation. Die RFS-Rate nach 36 und 48 Monaten betrug für diese Patienten 78% im Nivolumab-plus-Ipilimumab-Arm, 40% im Nivolumab-Arm und 11% im Placeboarm. Das Risiko zu sterben war für Patienten mit BRAF-Mutation unter Nivolumab plus Ipilimumab gegenüber Placebo um 90% reduziert (HR:0,10; 95% CI: 0,01–0,76).
Immuntherapie in der Sequenz vor zielgerichteter Therapie
Die dreiarmige SECOMBIT-Studie untersuchte, wie immunonkologische und zielgerichtete Therapien zur Behandlung in der metastasierten Situation idealerweise angeordnet sein sollten.3 Patienten im Arm A erhielten in der ersten Therapielinie Encorafenib plus Binimetinib, nach Progress gefolgt von Ipilimumab plus Nivolumab. Patienten im Arm B wurden in der ersten Therapielinie mit Ipilimumab plus Nivolumab behandelt und erhielten nach Progress Encorafenib plus Binimetinib. In einem dritten Arm wurden über eine Dauer von 8 Wochen Encorafenib plus Binimetinib gegeben, danach Ipilimumab plus Nivolumab bis zum Tumorprogress und anschliessend wieder Encorafenib plus Binimetinib. Der primäre Studienendpunkt war das OS. Die beim ESMO präsentierte Analyse wurde mit einer medianen Nachbeobachtungszeit von 43 Monaten erhoben.
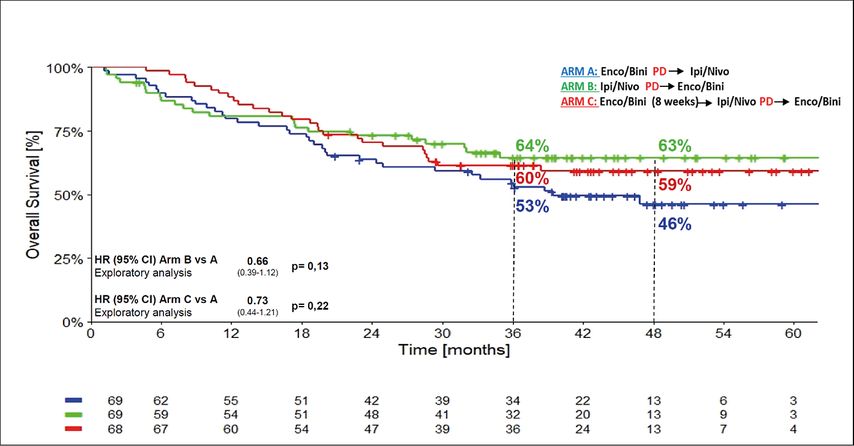
Insgesamt wurden 209 Patienten randomisiert und 68–69 Patienten pro Studienarm erhielten wenigstens eine Dosis der Studienmedikation. Nach vier Jahren waren 29% der Patienten im Arm A ohne Progress versus 55% bzw. 54% in den Studienarmen B und C. Das Risiko für einen Progress war zwischen Arm B versus A um 42% (HR:0,58; 95% CI: 0,37–0,91; p=0,01) und zwischen Arm C versus A um 40% (HR:0,60; 95% CI: 0,39–0,94; p=0,02) reduziert. Auch die OS-Daten bestätigten einen Vorteil für Arm B und Arm C gegenüber Arm A (HR:0,66; 95% CI: 0,39–1,12; p=0,13 bzw. HR:0,73; 95% CI: 0,44–1,21; p=0,22) (Abb. 2). Die 4-Jahres-OS-Rate betrug 63% unter Erstlinientherapie mit Ipilimumab plus Nivolumab (Arm B), 59% unter 8 Wochen Encorafenib/Binimetinib plus nachfolgend Ipilimumab/Nivolumab (Arm C) und 46% unter Erstlinientherapie mit Encorafenib plus Binimetinib.
Abb. 2: Gesamtüberleben (OS) im Vergleich diverser Sequenzen mit Ipilimumab plus Nivolumab und Encorafenib plus Binimetinib (nach Ascierto et al. 2022)3
Subgruppenanalysen spiegelten das bessere Ergebnis für Arm B für die meisten Patientengruppen wider. Patienten mit erhöhtem LDH-Wert zeigten das beste Ergebnis für progressionsfreies Überleben (PFS) und OS im Arm C: Nach 48 Monaten betrug die PFS-Rate 60% (Arm C) vs. 48% (Arm B) vs. 18% (Arm A) und die OS-Rate 65% (Arm C) vs. 53% (Arm B) vs. 42% (Arm A). Vorläufige Biomarkeranalysen weisen in den Studienarmen A und B auf bessere OS-Ergebnisse bei Patienten mit höherer Tumorlast hin, wohingegen in Arm C Patienten mit niedriger Tumorlast möglicherweise mehr profitierten. Patienten mit JAK-Mutation scheinen laut Subgruppenanalysen besonders gut von der Erstlinien-Immuntherapie (Arm B) zu profitieren, Patienten mit niedrigen IFN-γ-Zytokinen besser von der «Sandwich»-Therapie (Arm C).
Infiltrierende Lymphozyten zur Behandlung des fortgeschrittenen Melanoms
Melanompatienten, die in einem metastasierten Stadium diagnostiziert werden, versterben in etwa 50% der Fälle innerhalb von 5 Jahren trotz der hochwirksamen Immuncheckpoint-Inhibitoren. In einer Phase-III-Studie erhielten jeweils 84 Melanompatienten mit nicht resektablen Tumoren im Stadium IIIC und IV mit Progression nach maximal einer Therapielinie (Ipilimumab war ausgeschlossen) entweder tumorinfiltrierende Lymphozyten (TIL) oder Ipilimumab.4 Die Patienten waren im Median 59 bzw. 58 Jahre alt, häufiger Männer als Frauen, mit einem mehrheitlich (82–83%) sehr guten Allgemeinzustand (WHO PS 0). Bei 43–44% der Patienten wurde eine BRAFV600-Mutation identifiziert. Etwa 11–12% der Patienten waren bei Studieneinschluss noch nicht systemisch behandelt worden, 20 bzw. 27% hatten eine adjuvante und 67 bzw. 58% in der Erstlinie eine PD-1-gerichtete Therapie erhalten.
Im Ergebnis konnte das Risiko für einen Krankheitsprogress mit der TIL-Behandlung versus Ipilimumab um 50% reduziert werden (HR:0,50; 95% CI: 0,35–0,72; p<0,001). Das mediane PFS betrug 7,2 versus 3,1 Monate. Das beste Ansprechen war eine Komplettremission bei 20,2 versus 7,1% der Patienten, eine partielle Remission bei 28,6 versus 14,3% und eine stabile Erkrankung bei 19,1 versus 17,9% der Patienten. Das mediane OS betrug 25,8 Monate im TIL-Studienarm versus 18,9 Monate im Ipilimumab-Arm (HR:0,83; 95% CI: 0,54–1,27; p=0,39). Nach 2 Jahren lebten 54,3 versus 44,1% der Patienten.
Quelle:
ESMO-Kongress 2022, 9.–13. September 2022, Paris
Literatur:
1 Patel SP et al.: Neoadjuvant versus adjuvant pembrolizumab for resectable stage III-IV melanoma (SWOG S1801). ESMO 2022, Abstr. #LBA6 2 Schadendorf D et al.: The IMMUNED study. Adjuvant nivolumab alone or in combination with ipilimumab versus placebo in stage IV melanoma with no evidence of disease: Overall survival results of IMMUNED, a randomized, double-blind multi-center phase 2 DeCOG trial. ESMO 2022, Abstr. #784O 3 Ascierto PA et al.: Phase II study SECOMBIT (sequential combo immuno and targeted therapy study): 4-years OS data and preliminary biomarkers evaluation. ESMO 2022, Abstr. #LBA41 4 Haanen JBAG et al.: Treatment with tumor-infiltrating lymphocytes (TIL) versus ipilimumab for advanced melanoma: Results from a multicenter, randomized phase 3 trial. ESMO 2022, Abstr. #LBA3
Das könnte Sie auch interessieren:
Mikrotoning – sanfte Behandlung mit Effekt?
Erweiterte Kapillargefässe sind ein weitverbreitetes und kosmetisch störendes Phänomen. Manchmal sind sie schon mit blossem Auge sichtbar oder erweitern sich anfallsartig, wodurch eine ...
«Wir reden in der Medizin zu wenig über Sex»
Wer im Kontext von Haut und Sexualität primär an sexuell übertragbare Infektionen (STI) denkt, könnte überrascht werden. Denn das Thema Sexualität ist gesundheitlich aus ganz ...
Die menschliche Haut in der modernen Kunst
Dr. Ralph Ubl, Professor für neuere Kunstgeschichte an der Universität Basel, stellte sich der schwierigen Herausforderung, einem Raum voller erwartungsvoller Dermatologen das Organ Haut ...