Was man über den kardiovaskulären Risikofaktor Lipoprotein(a) wissen muss
Bericht:
Dr. med. Christine Adderson-Kisser, MPH
Medizinjournalistin
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Lipoprotein(a) ist längst eine feste Grösse unter den kardiovaskulären Risikofaktoren. Die therapeutischen Optionen zur Senkung erhöhter Werte sind bislang beschränkt. Noch, muss man sagen, denn neue Wirkstoffe sind auf dem Weg. Über die Risiken von erhöhten Lipoprotein(a)-Werten, aktuelle therapeutische Ansätze und zukünftige Therapien referierte Prof. Dr. med. Isabella Sudano am AGLA-Kurs für klinische Lipidologie in Zürich.
Keypoints
-
Der Lp(a)-Wert sollte einmal im Leben bestimmt werden (Nüchternzustand ist nicht notwendig).
-
Lp(a)-Konzentrationen >50mg/dl bzw. >125nmol/l sind mit einem erhöhten ASCVD-Risiko assoziiert.
-
Bei erhöhtem Lp(a) sollten die traditionellen kardiovaskulären Risikofaktoren frühzeitig therapiert und optimal eingestellt werden.
-
Ein Kaskadenscreening für hohe Lp(a)-Werte empfiehlt sich bei familiärer Hypercholesterinämie, familiärer Vorgeschichte von (sehr) hohem Lp(a) und persönlicher oder familiärer Vorgeschichte einer atherosklerotischen kardiovaskulären Erkrankung.
Lipoprotein(a) wurde 1963 erstmals beschrieben und wird seit 1974 mit der Entstehung einer koronaren Herzerkrankung assoziiert. Das in der Leber synthetisierte Lipoprotein(a) ähnelt zum Teil dem Low-Density-Lipoprotein (LDL), enthält also Cholesterin und ApoB, weist aber auch einige Besonderheiten auf. So enthält es einen hohen Anteil an oxidierten Phospholipiden sowie das über Disulfidbrücken an ApoB100 gebundene ApoA, ein Glykoprotein, das mit über 40 Isoformen eine grosse Heterogenität aufweist. Etwa 80% der Bevölkerung tragen zudem zwei unterschiedlich grosse ApoA-Isoformen, die jeweils von einem Elternteil geerbt wurden. Die Art der Isoform beeinflusst die Höhe der Serumkonzentration von Lp(a).1,2 Eine der Isoformen ähnelt strukturell dem Plasminogen, was bei einer hohen Anzahl an Kopien das Auftreten von Thrombosen begünstigt.3,4
Welche Faktoren beeinflussen die Höhe von Lp(a)?
Betrachtet man Menschen unterschiedlicher Ethnizität, fallen Unterschiede in der Häufigkeitsverteilung der Lp(a)-Serumkonzentration auf.2 Die höchsten Werte finden sich bei People of Colour (PoC), die niedrigsten in der kaukasischen Bevölkerung.3
Ein erhöhter Lp(a)-Wert (definiert als >125nmol/l bzw. >50mg/dl) findet sich in Afrika bei 30% der Bevölkerung, in Europa und Nordamerika bei 20% sowie in Ostasien bei 10%.5 Der Anteil der Bevölkerung mit 170nmol/l liegt bei Kaukasiern bei etwa 10%, bei PoC dagegen bei 17%.2 Je höher die Konzentration, desto höher ist auch das kardiovaskuläre (CV) Risiko, wie Daten einer deutschen Publikation zeigten.6 Während der grösste Teil der untersuchten kaukasischen Personen einen Wert von <75nmol/l aufwies und damit im kardiovaskulären Niedrigrisikobereich lag, kamen Konzentrationen von >430nmol/l, mit einem kardivaskulären Risiko im Bereich der familiären Hypercholesterinämie (HeFH), in diesem Kollektiv äusserst selten vor.6 Interessanterweise verläuft der Zusammenhang von Lp(a)-Konzentration und Lebenszeitrisiko für schwere kardiovaskuläre Ereignisse bei Kaukasiern sehr linear, während er bei PoC eine grosse Spannbreite aufweist.2
«Aber nicht nur die Gene, auch andere pathophysiologische Zustände können zu einer veränderten Lp(a)-Konzentration beitragen und möglicherweise eine erneute Lp(a)-Bestimmung rechtfertigen», betonte die Präsidentin der Arbeitsgruppe Lipide und Atherosklerose (AGLA), Prof. Dr. med. Isabella Sudano vom Universitären Herzzentrum in Zürich. «Die Höhe des Lp(a) wird zum Beispiel durch Ernährungsänderungen, Hyper- oder Hypothyreose und Schwangerschaft beeinflusst.» Eine chronische Nierenerkrankung wie ein nephrotisches Syndrom kann zu einer Erhöhung des Lp(a) um das 3- bis 5-Fache führen, während eine Nierentransplantation wieder zu einer Normalisierung führen kann.2 Die bei Lebererkrankungen eher erniedrigten Lp(a)-Werte gleichen sich nach einer Transplantation an die Werte des Spenders an. Eine Sepsis führt zu erniedrigten Lp(a)-Werten, weniger akute Entzündungszustände dagegen eher zu einer Erhöhung. «Auch Medikamente können einen Einfluss auf das Lipoprotein(a) haben», erklärte Sudano. So sei die Einnahme von Proteaseinhibitoren, älteren antiretroviralen Therapien und eine Behandlung mit Statinen mit einem Lp(a)-Anstieg verbunden.2
Je höher das Lp(a), desto höher das kardiovaskuläre Risiko
Das erhöhte kardiovaskuläre Risiko durch hohe Lp(a)-Werte lässt sich im Wesentlichen auf drei pathologische Eigenschaften von Lp(a) zurückführen: den proatherosklerotischen Effekt, der dem der anderen atherosklerotisch wirkenden Lipoproteine ähnelt, den proinflammatorischen Effekt, der auf die oxydierten Phospholipide zurückzuführen ist und u.a. zur Membrandysfunktion und Aktivierung von Immunzellen führt, sowie einen prokoagulierenden/antifibrinolytischen Effekt mit dem Risiko für die Entstehung von (arteriellen) Thromben.2
Die Daten einer Metaanalyse von 2009 mit 126635 Personen aus 36 prospektiven Studien bestätigten eine direkte Assoziation von erhöhten Lp(a)-Werten und dem Risiko für einen Myokardinfarkt.7 Eine Analyse der UK-Biodatenbank aus dem Jahr 2021 mit Daten von 460000 Erwachsenen konnte zudem zeigen, dass das Risiko für eine atherosklerotisch bedingte kardiovaskuläre Erkrankung (ASCVD) mit jeder Erhöhung des Lp(a) um 50nmol/l um 11% ansteigt.8
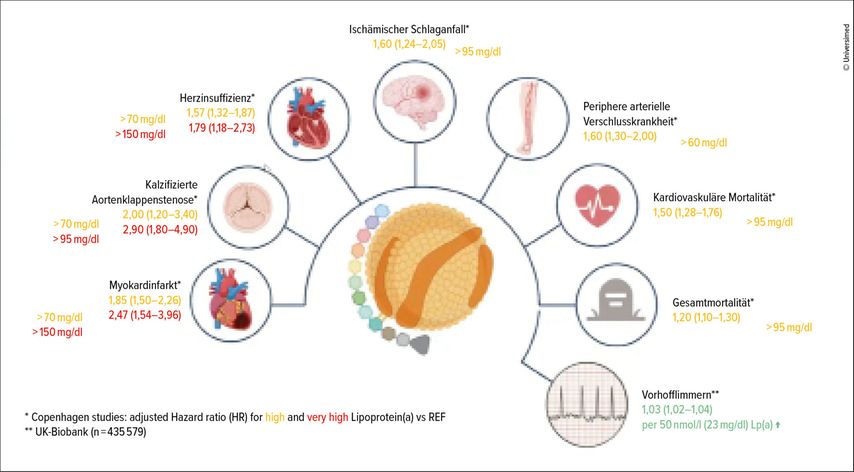
Die Morbidität und Mortalität durch erhöhte Lp(a)-Werte unterscheidet sich jedoch bei den unterschiedlichen kardiovaskulären Ereignissen. «Einen deutlichen und linearen Zusammenhang sehen wir beim Myokardinfarkt und der Aortenklappenstenose», so Sudano.3 Bei Personen mit sehr hohen Lp(a)-Werten (>90mg/dl bzw. >190nmol/l) ist das Risiko, an einem Myokardinfarkt oder einer Aortenklappenstenose zu sterben, um das 3-Fache erhöht. Die Morbidität und Mortalität infolge von Herzinsuffizienz, ischämischem Schlaganfall, peripherer arterieller Verschlusskrankheit (pAVK) oder kardiovaskulären Ursachen sind ebenfalls erhöht, wenn auch weniger deutlich (Abb.1). Relativ neu ist laut der Expertin die Erkenntnis, dass erhöhte Lp(a)-Level auch einen Risikofaktor für eine Aortenstenose darstellen.11 Die pathophysiologischen Mechanismen sind vielfältig, u.a. trägt ein hoher Anteil an oxidierten Phospholipiden im Lp(a) zu einer rascheren Kalzifizierung der Aortenklappe bei.4 Nicht erhöht sei hingegen das Risiko für die Entstehung venöser Thrombosen, wie neuere Studien zeigten.2
Abb. 1: Lipoprotein(a) hat sich zu einem der wichtigsten genetischen Determinanten für die Lebensdauer und Gesundheitsspanne des Menschen entwickelt.9 Diese Abbildung zeigt das kardiovaskuläre Morbiditäts- und Mortalitätsrisiko bei hohen und sehr hohen Lipoprotein(a)-Werten (modifiziert nach Arsenault BJ & Kamstrup PR 2022; Mohammadi-Shemirani P et al. 2022)9,10
Einschätzung des individuellen kardiovaskulären Risikos
Zur Risikoeinschätzung schlägt die European Atherosclerotic Society (EAS) in ihrem Consensus Statement folgende Einteilung vor:
-
Werte <30mg/dl bzw. <75nmol/l: «rule out» = normales Risiko
-
Werte >50mg/dl bzw. >125nmol/l: «rule in» = erhöhtes Risiko
-
Werte von 30–50mg/dl bzw. 75–125 nmol/l: leicht erhöhtes Risiko; additives Lp(a)-Risiko bei Vorliegen weiterer Risikofaktoren
«Je höher das vorbestehende kardiovaskuläre Risiko einer Person ist, desto mehr fallen bereits niedrigere Lp(a)-Konzentrationen ins Gewicht», erklärte die Spezialistin. Sehr hohe Lp(a)-Werte wiederum reichen aus, um das CV Risiko auch unabhängig vom Vorliegen weiterer CV Risikofaktoren stark zu erhöhen.
Vom Gesamtrisiko, bestehend aus dem Baselinerisiko für eine ASCVD und dem additiven Risiko durch das Lp(a), hängt ab, welche Interventionen für die Betroffenen infrage kommen.
Möglichkeiten der Lp(a)-Senkung – heute …
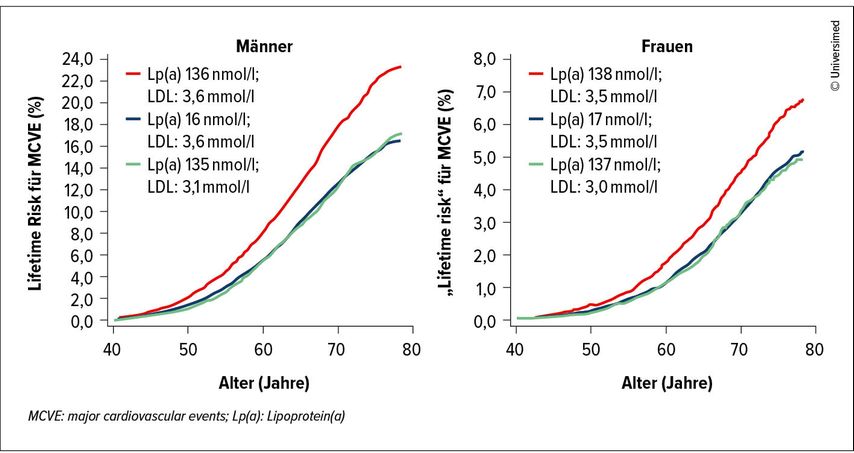
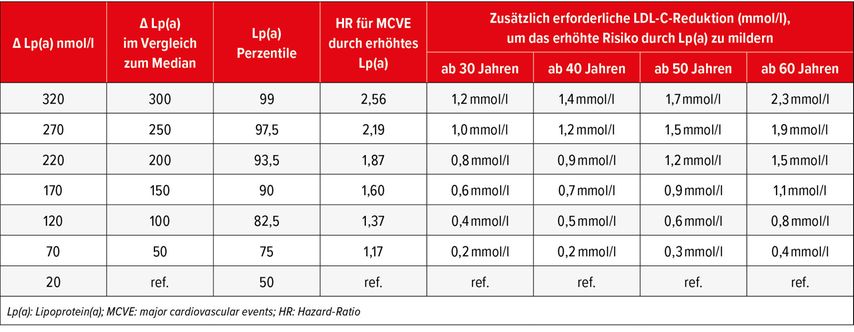
«Momentan können wir erhöhte Lp(a)-Werte noch nicht direkt medikamentös therapieren – das ändert sich aber bald», sagte Sudano. Bis dahin bestehe die Möglichkeit, das Risiko für kardiovaskuläre Komplikationen indirekt mittels LDL-Cholesterin(LDL-C)-Reduktion zu beeinflussen. Dabei kann ein erhöhtes CV Risiko durch eine um etwa 120nmol/l erhöhte Lp(a)-Lebenszeitexposition in allen Altersgruppen durch eine um circa 0,5mmol/l erniedrigte LDL-C-Lebenszeitexposition ausgeglichen werden (Abb.2). Das bedeutet: Je später im Leben die LDL-C-Senkung beginnt, desto intensiver muss sie ausfallen.2 «Reicht bei einem 30-Jährigen mit einem Lp(a)-Wert von 320nmol/l eine LDL-C-Senkung um 1,2mmol/l aus, muss sie bei einem Behandlungsbeginn im Alter von 60 Jahren schon bei 2,3mmol/l liegen, um das erhöhte CV Risiko im Vergleich zu Gleichaltrigen mit einem Lp(a)-Wert von 20nmol/l auszugleichen», erklärte Sudano (Tab.1).
Abb. 2: Das erhöhte Risiko für schwerwiegende kardiovaskuläre Ereignisse durch eine lebenslange Exposition gegenüber einem um etwa 120nmol/l höheren Lp(a)-Spiegel kann durch eine lebenslange Exposition gegenüber einem um etwa 0,5mmol/l niedrigeren LDL-C-Spiegel gemindert werden (modifiziert nach Kornenberg F et al. 2022)2
Tab. 1: Quantitative Schätzung der zusätzlich erforderlichen LDL-C-Reduktion, um das durch zunehmend höhere Lp(a)-Spiegel verursachte erhöhte Risiko für schwerwiegende kardiovaskuläre Ereignisse zu mindern (modifiziert nach Kornenberg F et al. 2022)2
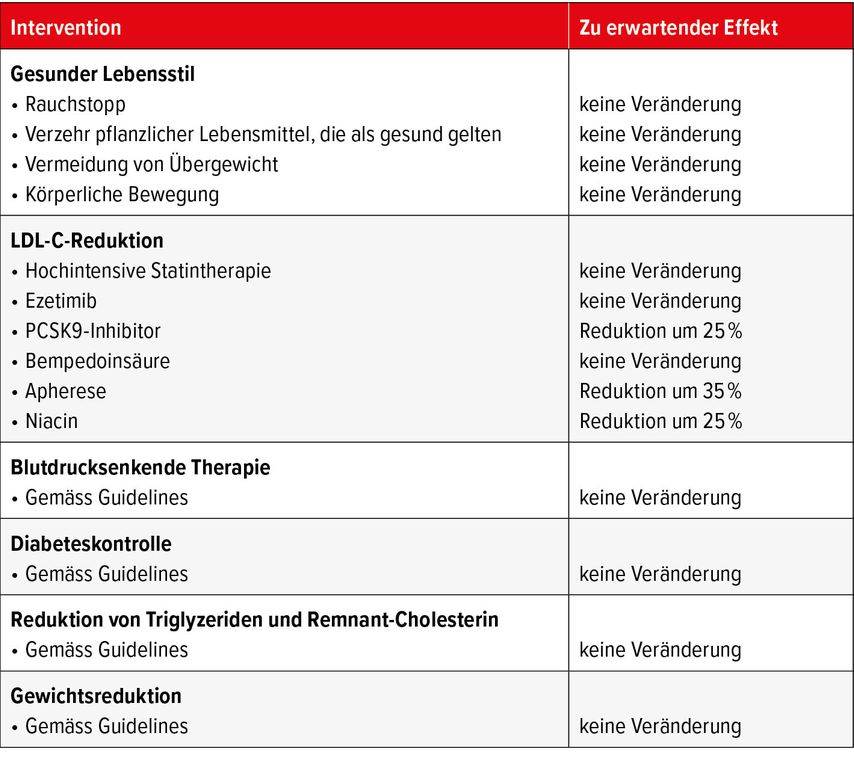
Ein direkter Lp(a)-senkender Effekt um circa 20–25% und ein günstiger Einfluss auf das CV Risiko wurden bislang nur für Niacin, die PCSK9-Inhibitoren Alirocumab und Evolocumab sowie die «small interfering RNA» (siRNA), Inclisirian, nachgewiesen.12–14 Bempedoinsäure, Ezetimib und Statine führen nicht zu einer Lp(a)-Reduktion, sondern können möglicherweise sogar einen leichten Anstieg verursachen (Tab. 2).3
Tab. 2: Spezifische Interventionen bei Personen mit hohen Lipoprotein(a)-Werten und deren Effekt auf das kardiovaskuläre Gesamtrisiko (modifiziert nach Nordestgaard BG et al. 2024)3
… und in Zukunft
Einen noch grösseren Lp(a)-senkenden Effekt sollen die derzeit noch in klinischen Studien befindlichen Antisense-Oligonukleotide (ASO) erzielen, wie Sudano erläuterte. Die Phase-III-Daten der HORIZON-Studie (NCT 04023552) zur Anwendung des ASO Pelacarsen, mit dem Lp(a) bis zu 80% gesenkt werden kann, werden für 2026 erwartet.15,16 Pelacarsen bindet gezielt apo(a)-mRNA in den Hepatozyten und verhindert so die Translation und Produktion von Lipoprotein(a). Den stärksten Effekt nach 6 Monaten Therapie hatte die Gabe von 20mg wöchentlich (−80%; p<0,001), worunter 98% der Behandelten einen Lp(a)-Wert ≤50mg/dl (125nmol/l) erreichen konnten. Ebenso gesenkt wurden die oxidierten Phospholipide OxPL-apoB und OxPL-apo(a), das LDL-C, ApoB und minimal auch das CRP.15 Die unerwünschten Wirkungen unter Pelacarsen befanden sich insgesamt etwa auf Placeboniveau und waren zum grössten Teil mild. Auch bei Thrombozytenzahl und Nierenfunktion zeigten sich keine auffälligen Signale.
In den Studienphasen II und III befinden sich zudem die siRNA Olpasiran, Zerlasiran und Lepodisiran, mit denen eine bis zu 100%ige Senkung des Lp(a) erreicht werden kann. Nach subkutaner Gabe gelangt die siRNA in die Leber und bindet an apo(a)-mRNA, was zu deren Abbau führt.13 Die Daten der Phase-III-Studie OCEAN(a) (NCT05581303) zu Olpasiran werden für Dezember 2026 erwartet.
Ebenfalls in der klinischen Prüfung befindet sich Obicetrapib, ein neuartiger, selektiver Cholesterylester-Transferprotein(CETP)-Hemmer.17 Dieser zeigte in einer Phase-II-Studie eine signifikante Reduktion des LDL-C (primärer Endpunkt), eine wirksame Senkung von ApoB, non-HDL-C und Lp(a) sowie eine signifikante Zunahme des HDL-C.18 Ein weiterer peroral zu verabreichender Wirkstoff, der aktuell in einer klinischen Phase-I-Studie untersucht wird, ist das «small molecule» Muvalaplin. Die zu erwartende Lp(a)-Reduktion unter dieser Therapie liegt bei circa 65%.3
«Auch wenn wir aktuell noch nicht so viel in der Hand haben, um das Lp(a) medikamentös zu senken, sollten wir den Wert einmal im Leben bestimmen, denn ein Wert ab 50mg/dl trägt zum kardiovaskulären Gesamtrisiko bei. Ist der Wert hoch, sind ein gesunder Lebensstil und die Optimierung der Behandlung aller anderen modifizierbaren Risikofaktoren wie Übergewicht, Rauchen, Diabetes oder Bluthochdruck umso wichtiger», resümierte Sudano.
Quelle:
AGLA-Kurs Klinische Lipidologie, 18. bis 19. Januar 2024, Zürich
Literatur:
1 Nordestgaard BG et al.: Lipoprotein(a) as a cardiovascular risk factor: current status. Eur Heart J 2010; 31: 2844-53 2 Kronenberg F et al.: Lipoprotein(a) in atherosclerotic cardiovascular disease and aortic stenosis: a European Atherosclerosis Society consensus statement. Eur Heart J 2022; 43: 3925-46 3 Nordestgaard BG et al.: Lipoprotein(a) and cardiovascular disease. Lancet 2024; 404: 1255-64 4 Tsimikas S: A test in context: lipoprotein(a): diagnosis, prognosis, controversies, and emerging Therapies. J Am Coll Cardiol 2017; 69: 692-711 5 Tsimikas S et al.: NHLBI working group recommendations to reduce lipoprotein(a)-mediated risk of cardiovascular disease and aortic stenosis. J Am Coll Cardiol 2018; 71: 177-92 6 Reuser A et al.: Lipoprotein(a). Dtsch Med Wochenschr 2022; 147: 1564-69 7 Erqou S et al.: Lipoprotein(a) concentration and the risk of coronary heart disease, stroke, and nonvascular mortality. JAMA 2009; 302: 412-23 8 Patel AP et al.: Lp(a) (lipoprotein(a)) concentrations and incident atherosclerotic cardiovascular disease: new insights from a large national biobank. Arterioscler Thromb Vasc Biol 2021; 41: 465-74 9 Arsenault BJ, Kamstrup PR: Lipoprotein(a) and cardiovascular and valvular diseases: A genetic epidemiological perspective. Atherosclerosis 2022; 349: 7-16 10 Mohammadi-Shemirani P et al.: Elevated lipoprotein(a) and risk of atrial fibrillation: an observational and mendelian randomization study. J Am Coll Cardiol 2022; 79: 1579-90 11 Thanassoulis G et al.: Genetic associations with valvular calcification and aortic stenosis. N Engl J Med 2013; 368: 503-12 12 Bittner VA et al.: Effect of alirocumab on lipoprotein(a) and cardiovascular risk after acute coronary syndrome. J Am Coll Cardiol 2020; 75: 133-44 13 O’Donoghue ML et al.: Lipoprotein(a), PCSK9 inhibition, and cardiovascular risk. Circulation 2019; 139: 1483-92 14 Ray KK et al.: Effect of an siRNA therapeutic targeting PCSK9 on atherogenic lipoproteins: prespecified secondary end points in ORION 1. Circulation 2018; 138: 1304-16 15 Tsimikas S et al.: Lipoprotein(a) reduction in persons with cardiovascular disease. N Engl J Med 2020; 382: 244-55 16 Cho L et al.: Design and rationale of Lp(a) HORIZON trial: Assessing the effect of lipoprotein(a) lowering with pelacarsen on major cardiovascular events in patients with CVD and elevated Lp(a). Am Heart J 2025; 287: 1-9 17 Kastelein JJP et al.: Obicetrapib: reversing the tide of CETP inhibitor disappointments. Current Atherosclerosis Reports 2024; 26: 35-44 18 Nicholls SJ et al.: Lipid lowering effects of the CETP inhibitor obicetrapib in combination with high-intensity statins: a randomized phase 2 trial. Nat Med 2022; 28: 1672-8
Das könnte Sie auch interessieren:
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
Inclisiran bei Patienten mit Statinintoleranz wirksam und sicher
Eine Analyse statinintoleranter Patienten aus dem Phase III Studienprogramm ORION zeigt, dass Inclisiran die LDL-Cholesterinspiegel kardiovaskulärer Hochrisikopatienten, die kein Statin ...