Vaccins contre le SARS-CoV-2
Compte-rendu:
Dr méd. Norbert Hasenöhrl
Journaliste médical
Review:
Prof. émérite Dr Franz X. Heinz
Zentrum für Virologie
Medizinische Universität Wien
E-mail: franz.x.heinz@meduniwien.ac.at
Les vaccins contre le SARS-CoV-2 peuvent fonctionner de manière très différente. Si, d’une part, des approches traditionnelles telles que les vaccins sous-unitaires sont en cours de développement, de nombreux fabricants se concentrent sur de nouvelles technologies, notamment les vaccins à ARNm et à adénovecteurs.
L’antigène clé
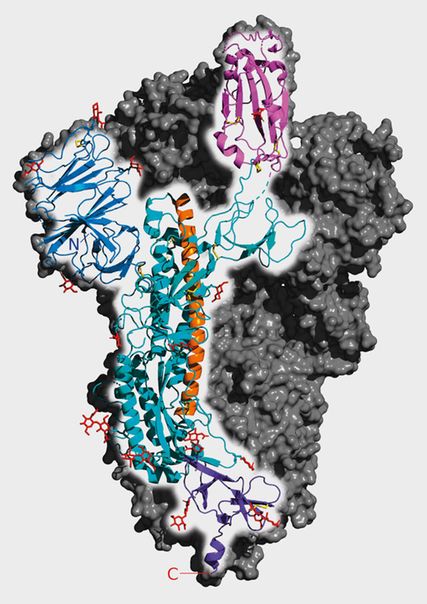
Fig. 1: Vue en 3D de la protéine S avec la région de liaison ACE2 en rose (source: 5-HT2AR: CC0; Wikimedia Commons)
«Tous les vaccins contre le SARS-CoV-2 qui existent aujourd’hui, et aussi la majorité de ceux qui sont encore en cours de développement, utilisent comme antigène la protéine de spicule (protéine S) virale», a expliqué le Prof. Franz X. Heinz, virologue et professeur émérite à la faculté de médecine de Vienne. Cette protéine prend la forme d’une pique à la surface de l’enveloppe virale et forme la «couronne» à laquelle le coronavirus doit son nom. Il s’agit d’une protéine relativement complexe composée de 1273 acides aminés (Fig. 1).
Cependant, contrairement aux représentations courantes, la totalité de la surface virale n’est pas occupée par les protéines S. Il y a environ 24 protéines S par virus. Ces protéines sont très mobiles, et leur surface est en mouvement dynamique constant. C’est le cas également du site de liaison du récepteur ACE2, qui doit être «déplié» par le virus pour pouvoir se lier aux cellules humaines et libérer ensuite son génome dans la cellule par endocytose.
Afin de générer une protection efficace contre le SARS-CoV-2, il est particulièrement important que des anticorps soient produits contre le domaine de liaison au récepteur afin d’empêcher le virus de pénétrer dans les cellules et de neutraliser ainsi le virus. Cependant, l’immunité contre le SARS-CoV-2 ne repose pas uniquement sur la formation d’anticorps neutralisants, mais également sur une immunité médiée par les lymphocytes T, ce qui signifie qu’en principe, il peut y avoir plusieurs «corrélats de la protection». Àl’heure actuelle, cependant, ce sont surtout les anticorps neutralisants qui sont utilisés pour évaluer la protection vaccinale. «La question est encore compliquée par le fait que différents vaccins induisent des réponses immunitaires différentes et qu’il faudrait donc les évaluer avec différents corrélats de protection», a déclaré le Prof. Heinz.
Les vaccins actuels
Les deux nouvelles technologies utilisées pour les vaccins contre le Covid sont les vaccins à ARN messager (ARNm) et les vaccins à adénovecteurs. Cependant, des technologies de vaccination conventionnelles sont également utilisées. Celles-ci comprennent les vaccins à virus entier inactivé, développés en Chine, mais également utilisés en Arabie saoudite, au Brésil ou en Turquie, par exemple. Il existe ensuite des vaccins sous-unitaires, dans lesquels seule la protéine S obtenue par génie génétique est utilisée comme antigène.
Vaccins à ARNm
Le principe de la vaccination par ARNm consiste à appliquer non pas la protéine S elle-même, mais l’ARNm qui la code. Parmi ces vaccins figurent ceux de Biontech/Pfizer et de Moderna.
L’ARNm administré via le vaccin pénètre dans les cellules musculaires ou immunitaires après l’injection, est transcrit dans leur cytoplasme (plutôt que dans le noyau de la cellule!), comme tout autre ARNm, pour former une protéine (dans ce cas précis, la protéine S du virus) qui est ensuite exprimée à la surface des cellules. L’organisme réagit alors à cette protéine virale produite par l’organisme lui-même avec une réponse immunitaire correspondante.
Afin d’éviter que l’ARNm ne soit dégradé avant de pénétrer dans les cellules ou que sa charge négative ne l’empêche de traverser la membrane cellulaire, également chargée négativement, l’acide nucléique a dû être entouré de liposomes, appelés nanoparticules lipidiques. Cependant, cela exige également de stocker les vaccins à des températures très basses. De plus, un ARN provenant de l’extérieur déclenche normalement un signal de danger dans la cellule. «Des recherches considérables ont été menées pour déterminer comment modifier l’ARNm afin de susciter une réponse immunitaire suffisante sans une ‹réponse immunitaire innée› excessive (associée à des effets secondaires)», a résumé le virologue.
Vaccins à adénovecteurs
Les vaccins à adénovecteurs transportent également l’information génétique de la protéine S, mais dans ce cas, elle est incorporée dans l’ADN d’un adénovirus inoffensif pour l’homme et modifié de manière à ne plus pouvoir se répliquer. Cependant, il peut encore servir de vecteur pour introduire dans les cellules l’information génétique de la protéine S virale. Ces vaccins comprennent ceux d’AstraZeneca, mais aussi le vaccin russe Sputnik, celui de Johnson & Johnson et d’autres encore, dont certains sont encore en cours de développement.
La pénétration des particules d’adénovirus du vaccin dans les cellules humaines se fait par l’intermédiaire de récepteurs spécifiques. Cependant, l’ADN contenu doit pénétrer dans le noyau pour y être transcrit en ARNm, ce qui mène à l’expression de la protéine S virale.
Pour garantir une immunogénicité appropriée, un tel vaccin doit contenir entre 50 et 100 milliards de particules de l’adénovirus génétiquement modifié par dose. Comme l’ARN des vaccins à ARNm, les particules d’adénovirus (bien qu’elles ne soient pas capables de se répliquer) déclenchent des signaux de danger, et il a fallu trouver le bon équilibre entre efficacité et réactions secondaires excessives. Ces vaccins ont l’avantage de pouvoir être conservés à des températures de réfrigération normales (4 °C).
L’immunité vectorielle – à savoir la présence ou le développement d’anticorps dirigés contre le vecteur viral – est un problème spécifique aux vaccins à vecteur. Cela peut atténuer la réponse immunitaire. «On a donc dû recourir à des adénovirus pour lesquels il n’existe que peu ou pas d’immunité humaine, comme un virus de chimpanzé», a expliqué le Professeur Heinz. Toutefois, la première vaccination avec un tel vecteur viral peut également déclencher une réaction immunitaire contre le vecteur, qui entraîne ensuite une réaction affaiblie lors des vaccinations suivantes.
Mutations et protection vaccinale
Les mutations de la protéine S peuvent être problématiques si elles interfèrent avec l’amarrage des anticorps protecteurs dirigés contre le SARS-CoV-2 induits par la vaccination ou une infection naturelle. Dans le cas de la variante britannique B1.1.7, ces changements sont mineurs et l’on peut donc supposer que les vaccins actuellement utilisés conservent un très bon effet protecteur. La variante sud-africaine B1.351 est nettement plus inquiétante à cet effet, car les changements au niveau du site de liaison pour les anticorps protecteurs sont bien plus importants que dans le cas de la variante britannique. Dans la variante brésilienne P1 il y a encore plus de mutations de ce type.
«La bonne nouvelle, cependant, c’est que les vaccins à ARNm et à adénovecteurs peuvent être adaptés à ces virus mutants relativement facilement et rapidement», a rassuré l’expert en virus.
Nouveaux développements
Parmi les développements récents, on note les tentatives de mise au point d’un vaccin intranasal contre le SARS-CoV-2 afin de renforcer l’immunité locale au niveau des muqueuses du nez et de la gorge, principal point d’entrée du virus. Il est possible que les vaccins à adénovecteurs soient particulièrement bien adaptés à cette fin puisque les adénovirus pénètrent également dans le corps humain par ces points d’entrée dans la nature.
Il existe également des innovations dans le développement des vaccins sous-unitaires, par exemple la tentative d’utiliser uniquement le domaine de liaison au récepteur comme antigène plutôt que la totalité de la protéine S. De nouveaux adjuvants sont également testés.
Un nouveau développement dans les vaccins à ARNm vise à administrer un ARNm auto-réplicatif. Celui-ci serait d’abord amplifié dans la cellule avant d’être soumis à la traduction. Cela permettrait d’avoir à utiliser des quantités beaucoup plus faibles d’ARNm par dose.
«Évidemment, de telles évolutions suscitent également de nouvelles questions, notamment en ce qui concerne les homologations», a conclu le Prof. Heinz. «Pour commencer, une fois que certains vaccins ont été approuvés, il n’est plus possible de mener des études contre placebo avec tous les autres vaccins, car cela serait tout simplement contraire à l’éthique. Il faudra donc concevoir des essais de non-infériorité, avec un vaccin homologué et un nouveau vaccin. De telles études sont beaucoup plus coûteuses que les études contrôlées par placebo. L’idéal serait de pouvoir définir de bons corrélats de protection in vitro, mais malheureusement nous n’en sommes pas encore là.»
Source:
«Impfstoffe gegen SARS-CoV-2 – welche Impfstoffe gibt es und wie unterscheiden sie sich?», (Vaccins contre le SARS-CoV-2 – quels vaccins sont disponibles et qu’est-ce qui les différencie?), conférence du Professeur émérite Dr Franz X. Heinz dans le cadre de la Journée (virtuelle) de la vaccination en Autriche, le 23 janvier 2021
Littérature:
cf. conférencier
Das könnte Sie auch interessieren:
Gérer les effets indésirables de manière ciblée: pratique selon les directives S3 et internationales
Les thérapies systémiques contre le cancer prolongent la survie et permettent de contrôler les maladies tumorales. Il est déterminant que les patient·es tolèrent bien le traitement. Cela ...
Mise à jour: comment éviter les transfusions?
Chez les patient·es à faible risqueatteint·es de syndromes myélodysplasiques (SMD), l’anémie nécessitant des transfusions constitue souvent le principal problème altérant la qualité de ...
La radiothérapie adjuvante à l’ère des thérapies systémiques modernes
La radiothérapie adjuvante demeure un élément central dans le traitement des tumeurs malignes cutanées, malgré les progrès réalisés avec les immunothérapies et les thérapies ciblées. ...