Thrombose veineuse profonde des membres inférieurs: diagnostic et traitement
Auteur:
Dr méd. Matthias Knittel
Klinik für Angiologie
Kantonspital Aarau AG
E-mail: matthias.knittel@ksa.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
La thrombose veineuse profonde des membres inférieurs est une maladie très répandue, dont l’incidence est estimée entre 88 et 112 événements pour 100000 personnes-année, soit environ 1 événement pour 1000 personnes par an.1 En raison de la possibilité de complications graves, telles que l’embolie pulmonaire, le syndrome post-thrombotique ou la survenue d’une insuffisance veineuse chronique, une prophylaxie de la thrombose adaptée au risque et un diagnostic approprié en cas de suspicion de thrombose sont essentiels.
Keypoints
-
Toute suspicion clinique de thrombose veineuse profonde doit faire rapidement l’objet d’un examen approprié pour qu’une décision thérapeutique puisse être prise.
-
La principale méthode de diagnostic est l’échographie de compression.
-
La thrombose veineuse profonde doit de préférence être traitée par des AOD. Ces derniers peuvent également être utilisés chez les patients atteints de tumeurs en l’absence de contre-indications.
-
Après 3 à 6 mois, il convient de réévaluer la nécessité de poursuivre l’anticoagulation et le traitement compressif.
Par définition, une thrombose veineuse profonde des membres inférieurs aiguë est une occlusion partielle ou totale des veines profondes par des thrombi. En l’absence de traitement ou si l’influence des facteurs procoagulants persiste, on observe dans de nombreux cas une croissance appositionnelle du thrombus avec extension proximale et/ou distale ultérieure.
Les directives allemandes de 2023 demandent donc que «toute suspicion clinique de thrombose veineuse fasse rapidement l’objet d’un examen approprié pour qu’une décision thérapeutique puisse être prise. L’anamnèse et l’examen physique seuls ne sont pas suffisants à cet égard».2
Facteurs de risque de thrombose veineuse profonde des membres inférieurs
Différents facteurs peuvent favoriser la survenue d’une thrombose veineuse profonde des membres inférieurs. On peut distinguer ici la prédisposition du patient (p.ex. en raison d’une thrombophilie) et les facteurs de risque d’exposition qui ont un impact sur les patients par le biais de leur environnement.
Chacun de ces facteurs doit être considéré en relation avec les différentes composantes de la triade de Virchow classique (lésion endothéliale, stase et hypercoagulabilité).
Il faut également faire la différence entre un facteur de risque transitoire et persistant. Le tableau 1 donne une vue d’ensemble des divers facteurs de risque avec différents degrés de sévérité.
Tab. 1: Facteurs de risque favorisant la survenue d’une thromboembolie veineuse (modifié selon Linnemann et al., 2023)2
L’âge avancé, en particulier, constitue un risque accru en soi. Il a ainsi été démontré que les patients âgés de plus de 80 ans présentent un risque de thromboembolie veineuse presque 8 fois plus élevé par rapport aux patients cinquantenaires.3
Les patients atteints de tumeurs présentent également un risque 7 fois plus élevé par rapport à ceux qui ne le sont pas. Selon le type de tumeur, le risque de thromboembolie veineuse peut atteindre 30% chez ces patients.
Diagnostic de la thrombose veineuse profonde des membres inférieurs
Tableau clinique
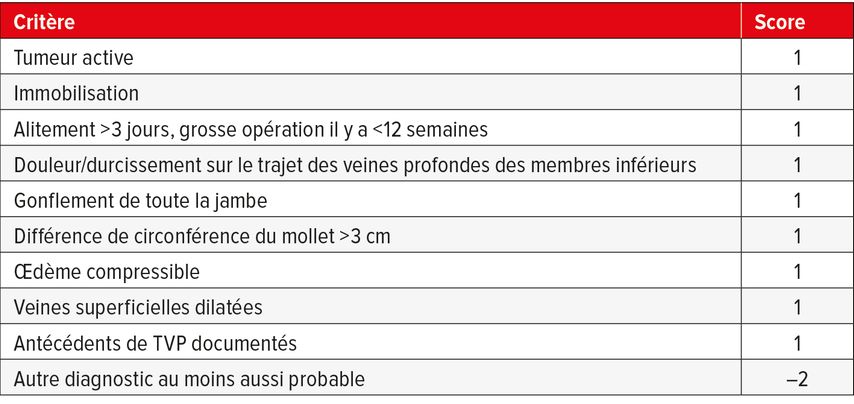
En présence de symptômes cliniques évocateurs d’une thrombose veineuse profonde des membres inférieurs, il convient en premier lieu d’évaluer la probabilité clinique à l’aide de scores établis, notamment le score de Wells4 (Tab. 2). Ce dernier consistait à l’origine en une classification à 3 niveaux (risque faible, modéré et élevé). La classification à 2 niveaux s’est toutefois établie dans la pratique clinique quotidienne, avec un risque élevé pour un score ≥2 points et faible pour un score ≤1 point. Cette classification est également utilisée dans les directives actuelles.
Tab. 2: Score de Wells pour déterminer la probabilité clinique d’une thrombose veineuse profonde des membres inférieurs (classification à 2 niveaux). Probabilité de TVP: forte: ≥2, faible: <2 points (modifié selon Wells et al., 2003)4
Imagerie
En cas de risque élevé (score de Wells ≥2 points), l’étape diagnostique suivante consiste à réaliser une échographie des veines profondes des membres inférieurs. Le cas échéant et selon l’expérience du médecin, un écho-doppler veineux de compression peut idéalement être réalisé. Il est toutefois possible d’effectuer une échographie proximale (limitée aux veines fémoro-poplitées) ou une échographie «point of care» (POCUS) en 2 points; en cas de résultat négatif, il convient cependant de procéder à un contrôle 4 à 7 jours plus tard.
L’échographie de compression complète permet de vérifier la compressibilité des veines profondes de la cuisse et du mollet ainsi que des veines musculaires du mollet, et de déduire également le profil de flux de la veine fémorale commune afin d’exclure un obstacle au flux sur le trajet de la veine iliaque. Selon le tableau clinique et les résultats, un examen complémentaire des veines iliaques ou des veines superficielles des membres inférieurs peut également s’avérer nécessaire. L’échographie de compression complète présente une spécificité et une sensibilité élevées de 97,3% et 94%, respectivement, comme l’a montré une revue systématique.5
L’échographie de compression limitée aux sections proximales des veines peut être réalisée par des médecins moins expérimentés et présente également une spécificité élevée de 98,5%, mais une sensibilité légèrement plus faible de 90,1%.
Dans environ 5 à 10% des cas confirmés de thrombose veineuse profonde des membres inférieurs au niveau d’une jambe symptomatique, des modifications thrombotiques sont également observées au niveau de l’autre jambe, de sorte qu’il est recommandé d’examiner également celle asymptomatique.
La phlébographie classique n’occupe plus une place importante dans le diagnostic actuel de la thrombose. Elle n’est plus disponible partout et de nombreux médecins manquent également d’expérience concernant le diagnostic avec cette méthode.
Elle a cependant encore une place dans le cadre du traitement interventionnel de la thrombose veineuse iliaque aiguë.
Les techniques d’imagerie complémentaire (phlébographie par résonance magnétique ou par tomodensitométrie) peuvent être utilisées pour déterminer l’étendue de la thrombose dans le cadre d’une thrombose veineuse iliaque.
Le phléboscanner, en particulier, peut également être combinée à un examen simultané des sections proximales des veines des membres inférieurs et des veines iliaques dans le cadre du diagnostic de l’embolie pulmonaire.
Importance du dosage des D-dimères
Si les résultats de l’échographie de compression ne sont pas clairs, il convient de procéder à un dosage complémentaire des D-dimères. Si les D-dimères sont normaux, une thrombose veineuse profonde des membres inférieurs peut être exclue avec une forte probabilité clinique. Si les D-dimères sont élevés, il est recommandé de contrôler l’évolution au moyen d’une échographie 4 à 7 jours plus tard ou, le cas échéant, d’établir un diagnostic par imagerie complémentaire, en particulier si la question se pose au niveau de la région iliaque.
La valeur limite généralement valable pour les D-dimères est <500µg/l. Chez les patients âgés de plus de 50 ans, la spécificité peut être augmentée en ajustant la valeur limite en fonction de l’âge (âge x 10µg/l), sans que la sensibilité ne diminue de manière significative.2 L’utilisation de valeurs limites ajustées en fonction de l’âge permet de réduire en conséquence le nombre d’échographies nécessaires.
Une suspicion de thrombose doit toujours être examinée rapidement, car une embolie pulmonaire peut être une complication engageant le pronostic vital. Si une échographie ne peut toutefois pas être réalisée dans les plus brefs délais (p.ex. en dehors des horaires d’ouverture normaux), il convient d’envisager une anticoagulation thérapeutique (uniquement en l’absence de contre-indications correspondantes), à condition que la probabilité clinique d’une thrombose veineuse profonde des membres inférieurs soit forte et/ou que les D-dimères soient élevés.
Traitement de la thrombose veineuse profonde des membres inférieurs
Auparavant, le traitement de la thrombose veineuse profonde des membres inférieurs se faisait généralement en milieu hospitalier et impliquait souvent une immobilisation du patient. Un changement s’est opéré au fil des décennies, de sorte qu’une grande partie des patients sont traités en ambulatoire de nos jours. Seuls les patients présentant des symptômes sévères, un risque élevé de complications ou des maladies concomitantes graves sont actuellement traités en milieu hospitalier. Une immobilisation n’est généralement pas nécessaire.
Dans le cadre du traitement de la thrombose veineuse profonde, différentes phases thérapeutiques doivent être prises en compte: la phase initiale (5 à 21 jours) est suivie d’une phase d’entretien (3 à 6 mois). Après cette période, il faut décider si une phase d’entretien prolongée avec poursuite du traitement est requise.
Les objectifs thérapeutiques dans le cadre du traitement d’une thrombose veineuse profonde des membres inférieurs sont la prévention de la progression du thrombus et des récidives, mais aussi celle des complications telles qu’un syndrome post-thrombotique ou une embolie pulmonaire.
Anticoagulation
Après confirmation du diagnostic, il convient d’instaurer immédiatement une anticoagulation à dose thérapeutique.
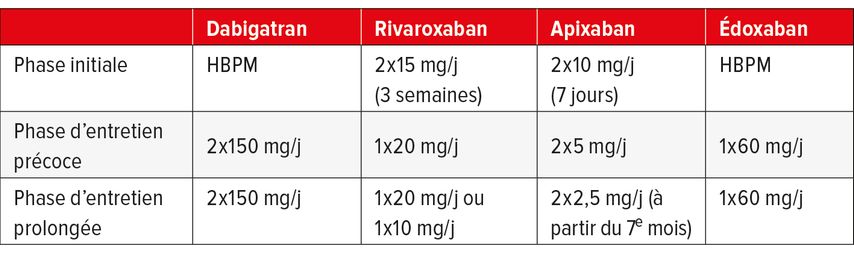
Plusieurs options sont disponibles à cet effet. Si l’on souhaite commencer immédiatement avec un anticoagulant oral direct (AOD), cela est possible avec l’apixaban ou le rivaroxaban, en tenant compte du fait qu’une dose plus élevée est nécessaire au cours de la phase initiale (pour la posologie individuelle, voir Tab. 3). Si un traitement par le dabigatran ou l’édoxaban est prévu, un traitement sous-cutané initial (p.ex. héparine de bas poids moléculaire [HBPM] à dose thérapeutique) est nécessaire pendant au moins 5 jours. Un traitement par des antagonistes de la vitamine K (AVK) avec anticoagulation parentérale superposée est sinon possible jusqu’à l’atteinte de l’INR cible (en général 2,0–3,0).
Tab. 3: Schémas posologiques des AOD sur la base des informations professionnelles actuellement en vigueur6–9 (le cas échéant, ajustement posologique en fonction de la fonction rénale)
Cependant, les directives actuelles recommandent clairement de donner la préférence aux AOD (en l’absence de contre-indications) plutôt qu’aux AVK dans le cas d’une efficacité égale ainsi que d’une meilleure sécurité et facilité d’utilisation.2
Au cours de la phase d’entretien, le traitement est poursuivi à la dose thérapeutique (Tab.3).
Il convient de tenir compte des interactions médicamenteuses correspondantes et, le cas échéant, des ajustements posologiques en cas d’insuffisance rénale.
En présence d’une thrombose veineuse profonde des membres inférieurs aiguë, les recommandations actuelles des directives préconisent un examen clinique dans les 1à 3 semaines suivant l’instauration du traitement afin de contrôler ce dernier (et d’évaluer les effets secondaires potentiels).2
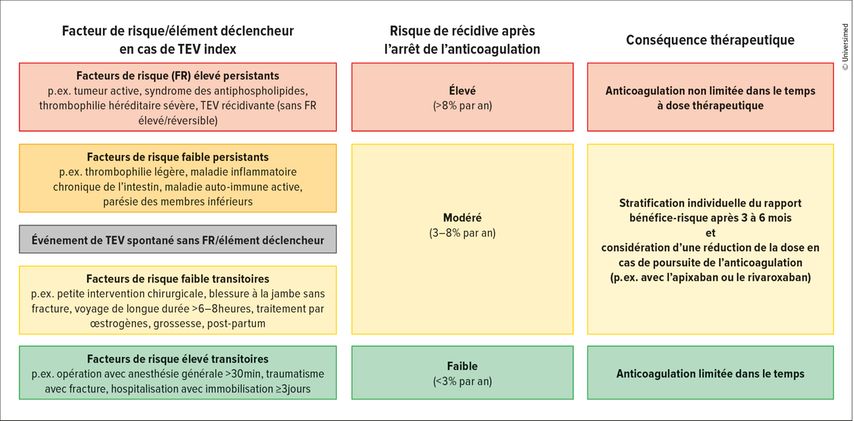
Après 3 à 6 mois, une stratification du risque doit être effectuée pour décider si l’anticoagulation peut être arrêtée ou doit être poursuivie (Fig. 1). En cas de facteurs de risque élevé persistants, l’anticoagulation doit être poursuivie à la dose thérapeutique. En cas de facteurs de risque faible persistants, de thrombose veineuse profonde des membres inférieurs idiopathique ou de facteurs de risque faible transitoires, les données des études EINSTEIN CHOICE10 et AMPLIFY-EXT11 indiquent qu’une anticoagulation par le rivaroxaban ou l’apixaban à dose réduite est également possible.
Fig. 1: Stratification du risque de récidive d’une thromboembolie veineuse (TEV) (modifié selon Linnemann et al., 2023)2
Les patients atteints de tumeurs malignes constituent un groupe particulier en ce qui concerne l’anticoagulation. D’une part, ils présentent un risque accru d’événements thromboemboliques et, d’autre part, ils doivent également faire l’objet d’une anticoagulation différenciée. Le traitement par l’HBPM était recommandé sur la base des données de l’étude CLOT12 dans des directives précédentes, mais, comme on dispose entre-temps d’un bon nombre d’études sur l’utilisation des AOD chez les patients atteints de tumeurs, leur utilisation est recommandée à la place de l’HBPM dans certaines conditions (aucun risque accru d’hémorragie, aucune tumeur intraluminale, absorption normale des médicaments). En fin de compte, le choix de l’anticoagulant chez ces patients reste une décision individuelle.
Les thromboembolies veineuses pendant la grossesse/le post-partum font partie des causes importantes de décès dans le cadre de la grossesse dans le monde occidental, c’est pourquoi une anticoagulation efficace s’avère également nécessaire dans ce cas. Elle se fait généralement par voie parentérale, car les AOD et les AVK sont contre-indiqués pendant la grossesse. L’HBPM constitue donc le traitement de première intention. En cas de contre-indications à l’utilisation de l’HBPM, le fondaparinux ou le danaparoïde peut être envisagé comme alternative.
Traitement compressif
Une autre mesure dans le traitement de la thrombose veineuse profonde des membres inférieurs est le traitement compressif, dont l’objectif est de réduire la douleur et le gonflement pendant la phase aiguë de la thrombose veineuse profonde ainsi que la fréquence et la sévérité du syndrome post-thrombotique (SPT) à long terme.
En présence de symptômes de stase veineuse, le traitement doit être instauré dans les 24 heures suivant la pose du diagnostic. En cas de gonflement sévère, il convient de mettre en place en premier lieu un traitement compressif avec des bandes de compression courts pour la décongestion, puis d’adapter des bas de contention de classe 2 au fur et à mesure de l’évolution. Dans ce cas, des bas de contention de la longueur du mollet sont généralement suffisants. En présence d’un gonflement de la cuisse, les bas cuisse sont toutefois à privilégier.
De la même manière que pour l’anticoagulation, il convient de réévaluer la nécessité de poursuivre le traitement compressif après 3 à 6 mois (en fonction du tableau clinique et du reflux veineux).
Mesures de recanalisation
Selon les directives actuelles, une recanalisation endovasculaire peut être envisagée en cas de thrombose proximale étendue avec atteinte des veines iliaques afin de réduire le risque de syndrome post-thrombotique. Cette recommandation s’applique en particulier aux patients présentant des symptômes sévères de stase veineuse en cas de thrombose ilio-fémorale descendante (les symptômes ne doivent pas persister plus de 14 jours et le risque d’hémorragie doit être faible).2
Diagnostic environnemental
En particulier chez les patients dont l’élément déclencheur de la thrombose ne peut être identifié avec certitude, il convient de poursuivre la recherche de la cause. Elle doit comprendre un dépistage des tumeurs adapté en fonction de l’âge et (si des conséquences thérapeutiques en découlent) un dépistage de la thrombophilie, le cas échéant. Les indications d’un dépistage de la thrombophilie sont par exemple les thromboembolies idiopathiques chez les patients âgés de <50ans, les événements récidivants, les fausses couches à répétition inexpliquées ou encore les thromboses de localisation atypique.
Littérature:
1 Chopard R et al.: Diagnosis and treatment of lower extremity venous thromboembolism: a review. JAMA 2020; 324: 1765-76 2 Linnemann B et al.: Diagnostik und Therapie der tiefen Venenthrombose und Lungenembolie – AWMF-S2k-Leitlinie. https://register.awmf.org/assets/guidelines/065-002l_S2k_Venenthrombose-Lungenembolie_2023-03.pdf ; zuletzt aufgerufen 5.6.2023 3 Wendelboe AM, Raskob GE: Global burden of thrombosis: epidemiologic aspects. Circ Res 2016; 118: 1340-7 4 Wells PS et al.: Evaluation of D-dimer in the diagnosis of suspected deep-vein thrombosis. N Engl J Med 2003; 349: 1227-35 5 Bhatt M et al.: Diagnosis of deep vein thrombosis of the lower extremity: a systematic review and meta-analysis of test accuracy. Blood Adv 2020; 4: 1250-64 6 Information professionnelle Pradaxa® (Dabigatran), mise à jour janvier 2022 7 Information professionnelle Xarelto® (Rivaroxaban), mise à jour décembre 2022 8 Information professionnelle Eliquis® (Apixaban), mise à jour février 2022 9 Information professionnelle Lixiana® (Edoxaban), mise à jour novembre 2020 10 Weitz JI et al.; EINSTEIN CHOICE Investigators: Rivaroxaban or aspirin for extended treatment of venous thromboembolism. N Engl J Med 2017; 376: 1211-22 11 Agnelli G et al.; AMPLIFY-EXT Investigators: Apixaban for extended treatment of venous thromboembolism. N Engl J Med 2013; 368: 699-708 12Lee AYet al.; CLOT Investigators: Low-molecular-weight heparin versus a coumarin for the prevention of recurrent venous thromboembolism in patients with cancer. N Engl J Med 2003; 349: 146-53
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...