Porteurs d’espoir ou source d’inquiétude? Les inhibiteurs JAK et la sécurité
Auteur:
Dr méd. Gregor Holak
Leiter Rheumaambulanz
5. Medizinische Abteilung
Klinik Ottakring
Wien
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Les Janus kinases (JAK) occupent une position clé dans l’homéostasie cellulaire, notamment dans la régulation de l’inflammation. Les inhibiteurs JAK sont des médicaments oraux dotés d’excellentes propriétés pour le traitement de différentes maladies à médiation inflammatoire, dont celles rhumatologiques et gastroentérologiques. Les conséquences des données de l’étude ORAL-SURVEILLANCE de 2022 limitent l’utilisation des inhibiteurs JAK et jettent une ombre sur l’utilisation future de cette classe de médicaments.
Keypoints
-
Les résultats de l’étude ORAL-SURVEILLANCE comparant l’inhibiteur JAK tofacitinib aux inhibiteurs du TNF adalimumab et étanercept ont été publiés en janvier 2022.
-
Le critère d’évaluation primaire était la nouvelle apparition de maladies malignes et d’événements cardiovasculaires.
-
Sur la base de ces données, la FDA ainsi que l’EMA ont émis des recommandations et des mises en garde pour tous les inhibiteurs JAK, qui ont entre-temps été appliquées par l’Association européenne de rhumatologie (EULAR).
-
Il n’est pas clair si les résultats de l’étude sont spécifiques au tofacitinib et à son mécanisme d’action ou si les mêmes conclusions doivent être tirées pour tous les autres inhibiteurs JAK.
Une classe de médicaments à fort potentiel
Lorsque Andrew F. Wilkes, du Ludwig Institute for Cancer Research, à Melbourne, a annoncé pour la première fois en 1989 l’identification de deux nouvelles tyrosines kinases, son équipe et lui n’avaient probablement pas conscience des conséquences de leur découverte. Le potentiel d’une manipulation pharmacologique de ces enzymes a toutefois été reconnu quelques années plus tard et le développement du premier inhibiteur JAK a commencé dès le tournant du millénaire.
Les JAK font partie de la voie de signalisation JAK/STAT («signal transducers and activators of transcription»), qui peut influencer diverses activités immunologiques.
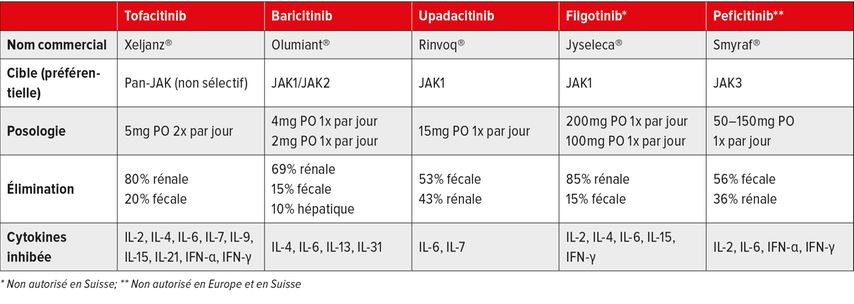
De nombreux messagers extracellulaires n’ayant aucune activité intrinsèque leur permettant d’agir directement dans le noyau cellulaire, ils font appel à différents systèmes de récepteurs qui agissent comme des transducteurs de signaux. Les JAK amplifient ainsi les signaux d’une trentaine de cytokines. Les interleukines IL-6, IL-12 et IL-23 sont particulièrement importantes en rhumatologie et en gastroentérologie, mais cette voie de signalisation est également utilisée par exemple par les cytokines de la famille IL-2, les interférons et divers facteurs de croissance, tels que l’érythropoïétine. En plus de 20 ans, une douzaine de principes actifs différents ont déjà pu être commercialisés, couvrant un large champ d’application, en particulier dans le spectre immunologique et hématologique. Dans le domaine de la rhumatologie, cinq substances sont actuellement disponibles sur le marché, dont quatre en Europe. Dans le domaine de la gastroentérologie, deux substances sont autorisées à ce jour pour les maladies inflammatoires chroniques de l’intestin. Une vue d’ensemble de leurs propriétés pharmacologiques est présentée dans le tableau 1.
Tab. 1: Différences pharmacologiques des inhibiteurs de Janus kinase (JAK) autorisés pour le traitement de la polyarthrite rhumatoïde
Dès le début, de grands espoirs ont été placés dans cette nouvelle classe de médicaments, qui se sont essentiellement positionnés comme une alternative administrée par voie orale aux anticorps monoclonaux (agents biologiques) administrés strictement par voie parentérale.
Des études comparatives montrent parfois des avantages par rapport aux inhibiteurs du TNF
Pour les quatre inhibiteurs JAK disponibles en Europe pour le traitement de la polyarthrite rhumatoïde (PR), il existe des études comparatives directes portant sur l’inhibiteur du facteur de nécrose tumorale (TNF) le plus utilisé actuellement (adalimumab). Étonnamment, les taux de réponse clinique sous inhibiteurs JAK ont tous été numériquement ou même significativement supérieurs à ceux sous adalimumab, et ont donc pu défier le «gold standard» établi pour le traitement de la PR ces vingt dernières années. Une réelle supériorité clinique ne peut pas être déduite de toutes ces études, mais il est possible de constater, sur la base des données disponibles, que les inhibiteurs JAK sont au moins aussi efficaces que ceux du TNF. Les avantages potentiels par rapport aux inhibiteurs du TNF sont par exemple une action plus rapide, ce qui permet d’espérer une diminution de l’utilisation de cortisone.
Chaque nouvelle classe de médicaments suscite non seulement des espoirs, mais aussi du scepticisme en ce qui concerne les effets secondaires et les conséquences – qui n’ont éventuellement pas été détectés lors de la procédure d’autorisation. Dans ce contexte, il est également important de noter que l’efficacité a toujours été le point central des études d’autorisation portant sur les inhibiteurs JAK, ce qui explique également la durée de suivi relativement courte. Les conclusions définitives sur la sécurité ne peuvent donc généralement être tirées qu’après des années d’utilisation de routine. La première substance autorisée pour la PR, le tofacitinib, a cependant montré des signaux de sécurité potentiels dès l’étude de phase III. Les autorités ont ainsi demandé au fabricant de réaliser une étude de sécurité après l’autorisation de mise sur le marché.
Risque accru démontré pour certains groupes de patients
Les résultats de l’étude ORAL-SURVEILLANCE, dont les conséquences potentielles avaient déjà fait l’objet d’un débat animé parmi les spécialistes, ont été publiés le 27 janvier 2022. Cette étude de sécurité de phase IIIb/IV, randomisée, multicentrique, ouverte a comparé le tofacitinib à deux inhibiteurs du TNF (adalimumab, étanercept) et avait pour critère d’évaluation primaire la combinaison de la nouvelle apparition d’affections malignes et de divers événements cardiovasculaires (MACE, «major adverse cardiovascular events»).
La population de l’étude était exclusivement composée de patients âgés de plus de 50 ans présentant un ou plusieurs facteurs de risque cardiovasculaire (CV) ainsi qu’une PR pas suffisamment contrôlée. Le tofacitinib devait démontrer sa non-infériorité par rapport aux comparateurs et aux principes thérapeutiques éprouvés de l’inhibition du TNF en termes de sécurité, ce qui n’a pas été le cas contre toute attente. En examinant les résultats de manière plus approfondie, on constate que le taux d’événements CV sous tofacitinib a été influencé par les hommes âgés >65 ans, les fumeurs actifs ainsi que les patients sous ASS. Un phénomène similaire a été observé lors de l’analyse des nouveaux cas de tumeurs malignes, dont le risque sous inhibiteurs JAK était également associé au sexe masculin, à un âge >65 ans et à des antécédents de tabagisme. En chiffres absolus, cela signifie qu’il faut traiter 567 et 319 patients à une dose de respectivement 5mg et 10mg de tofacitinib BID pendant >1an pour observer un événement CV supplémentaire par rapport à un traitement par des inhibiteurs du TNF. En ce qui concerne les tumeurs malignes, il faudrait traiter 276 et 275 patients à une dose de respectivement 5mg et 10mg de tofacitinib BID pendant >1an pour observer une tumeur supplémentaire par rapport à un traitement par des inhibiteurs du TNF. On ignore dans quelle mesure le risque CV concomitant a été traité avant l’étude ou combien de cigarettes ont été fumées quotidiennement. Comme il est bien connu qu’une maladie rhumatologique sous-jacente pas suffisamment contrôlée entraîne un risque nettement accru aussi bien de maladies CV secondaires que de cancers, il est également important de mentionner que plus de la moitié des patients avaient besoin d’un traitement concomitant par des stéroïdes au début de l’étude.
Il n’est pas clair à l’heure actuelle si les résultats de cette étude sont spécifiques au tofacitinib et doivent être clarifiés quant à son mécanisme d’action ou si les mêmes conclusions doivent être tirées pour tous les autres inhibiteurs JAK. On se demande également si les inhibiteurs du TNF ont un effet potentiellement positif, par exemple sur l’apparition de lésions CV tardives, et si les mauvais résultats du tofacitinib ne font donc que refléter un comportement neutre, mais ne constituent pas un effet nocif en soi. Des signaux similaires, autres que ceux observés dans l’étude ORAL-SURVEILLANCE, n’ont pas encore été confirmés tels quels dans les observations à long terme de tous les inhibiteurs JAK, y compris pour le tofacitinib. Au contraire, les substances ne semblent pas être significativement moins efficaces que les agents biologiques, y compris les inhibiteurs du TNF, notamment en ce qui concerne les tumeurs malignes et les événements CV.
Malgré cela, les autorités compétentes américaine (FDA) et européenne (EMA) ont émis des recommandations ainsi que des mises en garde pour tous les inhibiteurs JAK, qui ont entre-temps été mises en œuvre par l’EULAR et sont présentées en détail dans le tableau 2.
Mise en œuvre des directives dans la pratique quotidienne
Transposé dans la pratique quotidienne, cela signifie notamment que la première utilisation d’un inhibiteur JAK dans le groupe à risque correspondant descend dans la hiérarchie des options. Il n’est pas clairement défini si cela signifie que toutes les alternatives disponibles doivent avoir été essayées avant de pouvoir recourir à un inhibiteur JAK, ou peut-être seulement un représentant de chaque classe de principes actifs (donc pas tous les inhibiteurs du TNF disponibles, par exemple), cela relève de l’expertise du praticien.
Fig.: Les inhibiteurs JAK ont également fait leur entrée dans le traitement des maladies inflammatoires chroniques de l’intestin
Il est actuellement plus difficile de décider si et quand il convient de changer un traitement en cours par un inhibiteur JAK (pour les patients présentant les facteurs de risque mentionnés), si celui-ci a par exemple été commencé avant la publication de l’étude ORAL-SURVEILLANCE. Si l’activité de la maladie n’est de toute façon pas suffisamment contrôlée à l’heure actuelle, la décision en faveur d’un autre mécanisme d’action sera sans doute plutôt facile à prendre. Arrêter un schéma thérapeutique bien établi uniquement pour changer de mode d’action au détriment d’un inhibiteur JAK et au risque d’aggraver le contrôle de la maladie est cependant mal accepté par de nombreux patients. Il faut ici faire preuve de tact et fournir une bonne explication – une décision doit toujours être prise par consensus.
Conclusion
En résumé, l’utilisation de la classe de principes actifs des inhibiteurs JAK, qui était jusqu’alors large et peu réfléchie, a été limitée en 2022 et n’est plus recommandée de la même manière. Cette classe de principes actifs, qui possède des propriétés immunologiques remarquables dans de nombreuses indications et constitue toujours un complément précieux dans l’arsenal thérapeutique inflammatoire, ne doit toutefois pas être exclue à l’avenir pour les patients qui n’appartiennent pas au groupe à risque.
Littérature:
•Alten R et al.: Janus kinase inhibitors: State of the art in clinical use and future perspectives. Z Rheumatol 2020; 79: 241-54 • Charles-Shoeman C et al.: Risk of major adverse cardiovascular events with tofacitinib versus tumour necrosis factor inhibitors in patients with rheumatoid arthritis with or without a history of atherosclerotic cardiovascular disease: a post hoc analysis from ORAL Surveillance. Ann Rheum Dis 2023; 82: 119-29 • Kotyla PJ: Are Janus kinase inhibitors superior over classic biologic agents in RA patients? Biomed Res Int 2018; 2018: 7492904 • Rubbert-Roth A: ORAL SURVEILLANCE: Was hat sich an der Risikobeurteilung von JAK-Inhibitoren geändert? Z Rheumatol 2022; 81: 780-1 • Smolen JS et al.: EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2022 update. Ann Rheum Dis 2023; 82: 3-18 • Wilkes AF: Two putative protein-tyrosine kinases identified by application of the polymerase chain reaction. Proc Natl Acad Sci USA 1989; 86: 1603-7 • Winthrop KL et al.: Oral surveillance and JAK inhibitor safety: the theory of relativity. Nat Rev Rheumatol 2022; 18(5): 301-4 • Ytterberg SR et al.: Cardiovascular and cancer risk with Tofacitinib in rheumatoid arthritis. N Engl J Med 2022; 386: 316-26
Das könnte Sie auch interessieren:
Gérer les effets indésirables de manière ciblée: pratique selon les directives S3 et internationales
Les thérapies systémiques contre le cancer prolongent la survie et permettent de contrôler les maladies tumorales. Il est déterminant que les patient·es tolèrent bien le traitement. Cela ...
Mise à jour: comment éviter les transfusions?
Chez les patient·es à faible risqueatteint·es de syndromes myélodysplasiques (SMD), l’anémie nécessitant des transfusions constitue souvent le principal problème altérant la qualité de ...
La radiothérapie adjuvante à l’ère des thérapies systémiques modernes
La radiothérapie adjuvante demeure un élément central dans le traitement des tumeurs malignes cutanées, malgré les progrès réalisés avec les immunothérapies et les thérapies ciblées. ...