Malformation congénitale de l’intestin grêle et ses conséquences à l’âge adulte
Auteur:
Dr méd. Philipp Alexander Pimingstorfer
Universitätsklinik für Innere Medizin II
Kepler Universitätsklinikum Linz
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
L’œsophage de Barrett (métaplasie intestinale) est un diagnostic relativement fréquent. Au plan de la pathogénèse, de nombreux facteurs typiques de la société occidentale, tels que l’obésité, le tabagisme et la consommation d’alcool, interagissent. Chez les jeunes patients ne présentant aucun facteur de risque classique, il convient toutefois de rester vigilant et d’orienter l’évaluation vers des causes secondaires. Il est également essentiel de connaître la surveillance correcte et les stratégies thérapeutiques possibles.
Keypoints
-
Un endoscope haute résolution, une chromoendoscopie virtuelle et une chromoendoscopie avec coloration à l’acide acétique sont nécessaires à la surveillance adéquate de l’œsophage de Barrett.
-
Outre les indications établies de traitement par ablation, la prise en charge de l’œsophage de Barrett non dysplasique long doit être individualisée.
Gastroscopie préventive
En août 2020, un homme de 23 ans a été envoyé pour une gastroscopie préventive. Il ne présentait aucun symptôme, était en bonne santé et athlétique. Un adénocarcinome (T2N0M0) sur œsophage de Barrett avait été diagnostiqué depuis peu chez son père âgé de 53 ans.
Les données relatives au bénéfice médical et à la rentabilité d’une gastroscopie préventive sont actuellement limitées. Quelques indications sont toutefois établies:
-
antécédents familiaux positifs de carcinome, 10 années de vie avant le premier diagnostic,
-
reflux gastro-œsophagien (RGO) depuis plusieurs années,
-
œsophage de Barret connu,
-
gastrite auto-immune connue ou atrophie/métaplasie touchant l’antre et le corps gastrique
Aux Pays-Bas, une gastroscopie unique est proposée depuis quelques années à titre préventif à l’âge de 60 ans. En Autriche, certains experts considèrent qu’une «gastroscopie préventive légère» est pertinente. On entend par là la réalisation d’une endoscopie digestive haute dans le cadre de la première coloscopie préventive, sous la même sédation. Cependant, aucune déclaration officielle correspondante n’a encore été faite.
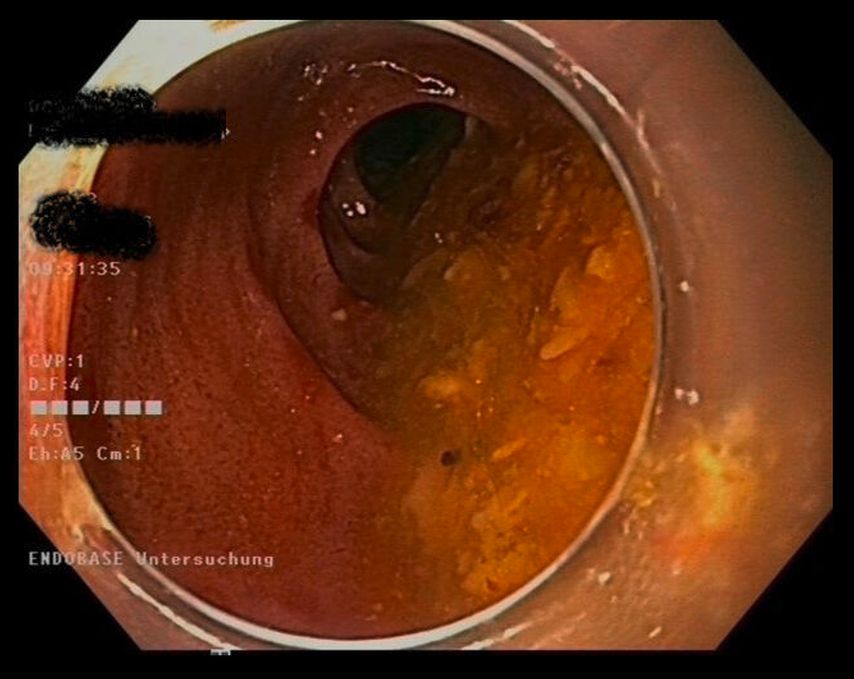
Chez le patient mentionné, la gastroscopie a été réalisée à titre préventif. Elle a révélé une œsophagite de reflux marquée avec des érosions allongées et non confluentes, ce qui correspond au grade B de la classification de Los Angeles. Elle a également mis en évidence un œsophage de Barrett circonférentiel et long de 9 cm, ce qui correspond à C9M9 selon la classification de Prague. La muqueuse de Barrett présentait des lésions inflammatoires évidentes. Le duodénum était de plus nettement distendu, l’endoscope pouvait être retourné sans danger, et une quantité importante de résidus alimentaires était présente (Fig. 1). Ces résultats nous ont permis de poser le diagnostic de suspicion d’occlusion de l’intestin grêle.
Fig. 1: Duodénum nettement distendu avec une quantité importante de résidus alimentaires
Surveillance de l’œsophage de Barrett
Pour permettre une endoscopie de surveillance adéquate en cas d’œsophage de Barrett (les lésions muqueuses et vasculaires ne peuvent pas être détectées de manière appropriée dans les zones inflammatoires), le patient a reçu un traitement par des inhibiteurs de la pompe à protons à fortes doses pendant 8 semaines.
Une nouvelle gastroscopie avec chromoendoscopie virtuelle et chromoendoscopie avec coloration à l’acide acétique 3% a ensuite été réalisée. Elle n’a révélé aucune lésion visible et les biopsies prélevées selon le protocole de Seattle n’ont montré aucun signe de dysplasie, même sur le plan histopathologique.
L’œsophage de Barrett est une maladie précancéreuse dont le risque de dégénérescence est d’environ 0,3% par année de vie.1 Ce risque est toutefois corrélé à la longueur de la muqueuse de Barrett et à la présence de dysplasies («low grade» ou «high grade»), lesquels augmentent considérablement le risque. Le diagnostic ne doit être posé que si un épithélium cylindrique est visible sur un centimètre du côté oral des plis gastriques et l’histologie révèle une métaplasie intestinale spécialisée avec cellules caliciformes. Les sociétés spécialisées concernées donnent des directives sur les intervalles de contrôle auxquels une gastroscopie de surveillance est recommandée. Il convient ainsi de contrôler tout œsophage de Barrett un an après le premier diagnostic. Par la suite, l’intervalle s’oriente sur la longueur de l’œsophage de Barrett:
-
1–3cm: tous les 5 ans
-
3–10cm: tous les 3 ans
-
>10cm: prise en charge dans un centre spécialisé
Dans le cadre de la surveillance, il s’agit de rechercher des lésions visibles. La chromoendoscopie virtuelle est utile à cet égard, car elle permet de mieux visualiser l’anatomie vasculaire. La chromoendoscopie avec coloration à l’acide acétique 3% est également un outil fiable, car les zones dysplasiques ne se colorent pas en blanc, mais restent rougeâtres. Les deux méthodes ont été comparées dans le cadre d’études randomisées et se sont avérées équivalentes.2
Pertinence de l’occlusion de l’intestin grêle
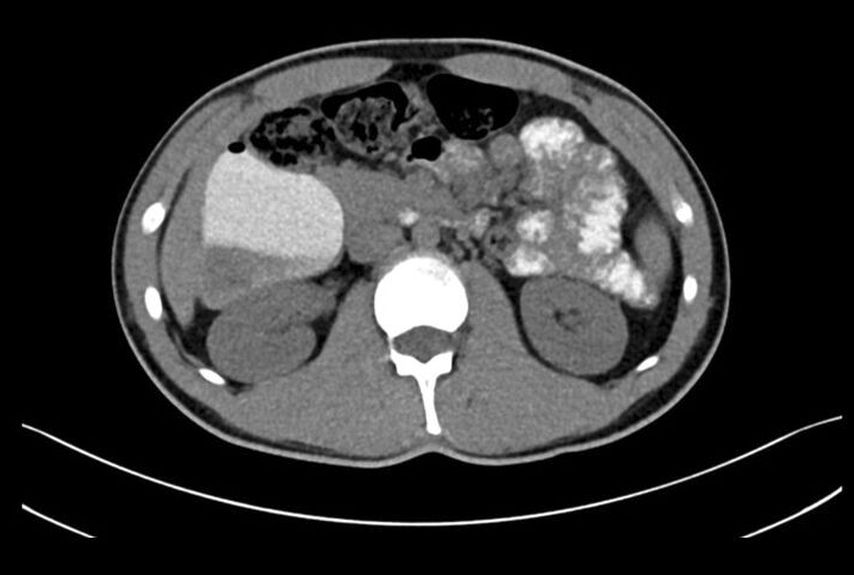
Une entérographie par résonance magnétique a été réalisée pour clarifier la suspicion d’occlusion de l’intestin grêle. Elle a révélé une dilatation du duodénum ainsi qu’un saut de calibre au niveau de la racine du mésentère. Aucune autre pathologie n’était visible sur le reste de l’intestin grêle. L’imagerie par résonance magnétique ayant été réalisée sans angiographie, il n’a pas été possible de se prononcer sur les relations vasculaires. C’est pourquoi une tomodensitométrie avec angiographie des vaisseaux mésentériques et produit de contraste oral (gastrografine) a été réalisée en complément (Fig. 2). Elle a révélé une sténose filiforme du duodénum d’environ 4cm de long au niveau du passage entre l’Aorta abdominalis et l’Arteria mesenterica superior. L’angle formé par l’Aorta et l’Arteria mesenterica superior était de 32°, de sorte que le diagnostic différentiel d’un syndrome de Wilkie a été envisagé.
Fig. 2: TDM avec angiographie des vaisseaux mésentériques et produit de contraste oral: sténose filiforme du duodénum d’environ 4cm de long au niveau du passage entre l’Aorta abdominalis et A. mesenterica superior
L’indication d’une laparotomie exploratrice a été posée et celle-ci a été réalisée par un chirurgien viscéral expérimenté en collaboration avec un chirurgien pédiatrique. En peropératoire, le duodénum présentait des lésions fibrotiques au niveau du passage entre l’Arteria mesenterica superior et l’Aorta abdominalis, avec une réduction significative de la lumière. Le diagnostic opératoire d’une sténose duodénale incomplète a été posé. Le patient a subi une duodénojéjunostomie latérale pour contourner la sténose sans résection partielle de l’intestin grêle. Il n’y a eu aucune complication en postopératoire.
Les atrésies duodénales complètes ont une prévalence de 1:10000 naissances vivantes et se divisent en trois sous-types.3 Elles sont symptomatiques aiguës au cours des premiers jours de vie. Aucune donnée épidémiologique sur les sténoses duodénales incomplètes n’est disponible. Dans 30% des cas, les patients sont atteints d’autres malformations (cardiaques, rénales) ou de trisomie 21, les autres cas étant sporadiques.4
Traitement par ablation de l’œsophage de Barrett
Compte tenu d’un reflux biliaire dû à une sténose duodénale incomplète avec œsophage de Barrett long chez un patient de 23 ans, l’indication d’une ablation de la muqueuse de Barrett a été envisagée. Le risque de dégénérescence d’un œsophage de Barrett d’environ dix centimètres de long doit être estimé à peu près au même niveau que celui d’un œsophage de Barrett court avec dysplasie de bas grade.5,6 Ce dernier constitue une indication claire pour l’ablation par radiofréquence ou la mucosectomie endoscopique en cas de lésion visible.7
Pour évaluer en postopératoire si le reflux sous-jacent a été éliminé grâce à l’intervention chirurgicale, le patient a été reconvoqué pour une pH-impédancemétrie de 24 heures. Aucun reflux cliniquement significatif n’a été démontré. La manométrie œsophagienne haute résolution a également révélé un résultat normal.
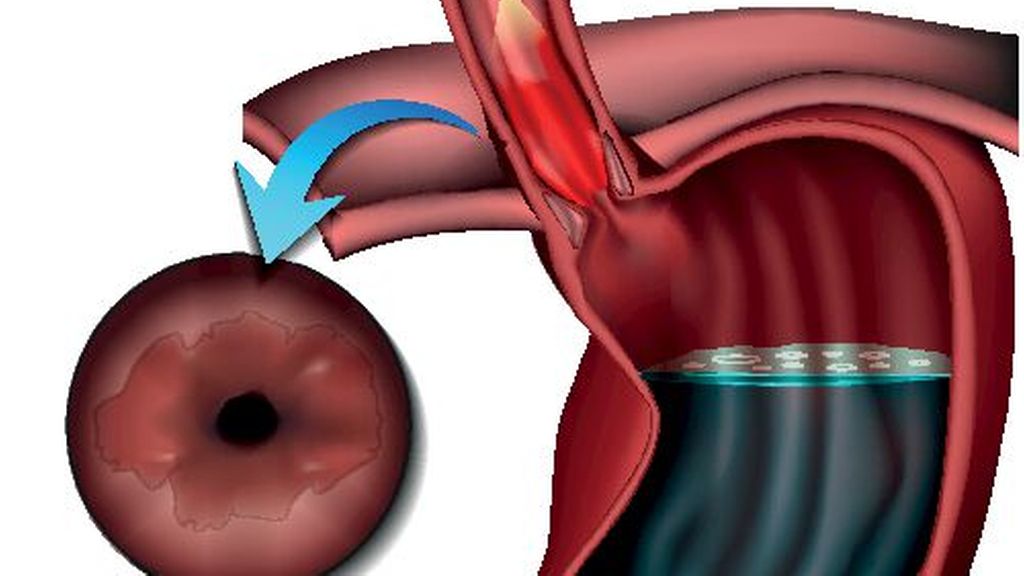
En raison du jeune âge du patient et du fait que le problème de reflux était dû à une malformation congénitale, désormais traitée chirurgicalement, l’indication d’une ablation par radiofréquence de l’œsophage de Barrett non dysplasique, mais long, a été posée. Cette dernière a été réalisée en une seule séance à l’aide d’un système de cathéter à ballonnet établi. Le suivi visant à évaluer le succès du traitement d’éradication est actuellement encore en suspens.
Littérature:
1 Desai TK et al.: The incidence of oesophageal adenocarcinoma in non-dysplastic Barrett’s oesophagus: a meta-analysis. Gut 2012; 61: 970-9 2 Pohl J et al.: Comparison of computed virtual chromoendoscopy and conventional chromoendoscopy with acetic acid for detection of neoplasia in Barrett’s esophagus. Endoscopy 2007; 39: 594-8 3 Best KE et al.: Epidemiology of small intestinal atresia in Europe: a register-based study. Arch Dis Child Fetal Neonatal Ed 2012; 97: 353-8 4 Bethell GS et al.: BAPS-CASS. Congenital duodenal obstruction in the UK: a population-based study. Arch Dis Child Fetal Neonatal Ed 2020; 105: 178-83 5 Duits LC et al.: Barrett’s oesophagus patients with low-grade dysplasia can be accurately risk-stratified after histological review by an expert pathology panel. Gut 2015; 64: 700-6 6 Pohl H et al.: Length of Barrett’s oesophagus and cancer risk: implications from a large sample of patients with early oesophageal adenocarcinoma. Gut 2016; 65: 196-201 7 Weusten B et al.: Endoscopic management of Barrett’s esophagus: European Society of Gastrointestinal Endoscopy (ESGE) Position Statement. Endoscopy 2017; 49: 191-8
Das könnte Sie auch interessieren:
Gérer les effets indésirables de manière ciblée: pratique selon les directives S3 et internationales
Les thérapies systémiques contre le cancer prolongent la survie et permettent de contrôler les maladies tumorales. Il est déterminant que les patient·es tolèrent bien le traitement. Cela ...
Mise à jour: comment éviter les transfusions?
Chez les patient·es à faible risqueatteint·es de syndromes myélodysplasiques (SMD), l’anémie nécessitant des transfusions constitue souvent le principal problème altérant la qualité de ...
La radiothérapie adjuvante à l’ère des thérapies systémiques modernes
La radiothérapie adjuvante demeure un élément central dans le traitement des tumeurs malignes cutanées, malgré les progrès réalisés avec les immunothérapies et les thérapies ciblées. ...