Les implications cliniques de la recherche sur le microbiome
Auteur: Dr méd. Christoph Stein-Thoeringer
Abteilung Mikrobiom und Krebs
Deutsches Krebsforschungszentrum
Heidelberg
Nationales Centrum für Tumorerkrankungen
Heidelberg
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Le microbiome du tractus gastro-intestinal est un écosystème très complexe. Lorsqu’il est déséquilibré, les effets ne se limitent pas au tractus gastro-intestinal, mais touchent l’ensemble de l’organisme. Ceci a une grande pertinence clinique, notamment dans le contexte des antibiothérapies qui sont l’une des principales causes d’altérations du microbiome. Une gestion responsable de la prescription d’antibiotiques contribue donc également à prévenir les dommages au niveau du microbiome qui peuvent, à leur tour, influer négativement sur les processus pathologiques et les autres traitements.
Informations de base sur le microbiome
Le corps humain adulte abrite environ 1013 bactéries, ce qui correspond à peu près au nombre de cellules humaines.1 Cet écosystème microbien, communément appelé microbiome, est composé non seulement de bactéries, mais aussi d’eucaryotes (champignons et protozoaires), de virus et de procaryotes2 et est impliqué dans un large éventail de processus physiologiques et pathologiques chez l’homme. La diversité génétique du microbiome est 100 fois supérieure et les gènes codant pour divers mécanismes et compétences métaboliques peuvent influer sur sa propre niche microbienne, sur l’homéostasie de l’hôte et sur la pathologie.3,4 La majorité des bactéries commensales colonisent le tractus gastro-intestinal (principalement le côlon); mais d’autres régions anatomiques, telles que la bouche, les voies respiratoires, le tractus urogénital, la peau ou même les tissus, dont les tumeurs, sont également colonisées par des bactéries commensales. Globalement, l’hôte et le microbiome coexistent en tant que méta-organisme, dans des conditions physiologiques en formant un équilibre symbiotique, l’hôte fournissant un environnement riche en nutriments dans le tractus gastro-intestinal en échange du rôle actif des micro-organismes favorisant les processus digestifs et métaboliques. À titre d’exemple, le microbiome en tant que tel synthétise les vitamines et dégrade les aliments en nutriments absorbables tels que les glucides, les acides gras à chaîne courte et longue ou d’autres métabolites qui, à leur tour, sont bénéfiques à l’homme pour son métabolisme ou la régulation de son immunité.5
De nombreuses études épidémiologiques ont démontré que les différences en termes de localisation géographique, d’appartenance ethnique et socio-économique et d’habitudes alimentaires entraînent une grande variabilité du microbiome humain entre les individus et au sein de ceux-ci.6,7 Des analyses indépendantes ont en outre mis en évidence le fait que l’âge, le sexe, l’IMC (en particulier le surpoids), la fonction rénale (mesurée par le DFG), la consommation d’alcool et divers facteurs diététiques sont les facteurs physiologiques qui ont l’impact le plus important sur la composition du microbiote intestinal chez les adultes en bonne santé.6,8
Microbiome et processus pathologiques
Au cours des vingt dernières années, une large communauté scientifique a manifesté un intérêt considérable pour le microbiome qui est devenu un domaine de recherche à part entière, principalement en raison de la conception et de la disponibilité pratique de méthodes de séquençage à haut débit (séquençage de nouvelle génération) du microbiome, notamment le séquençage du gène de l’ARNr 16S et la mise en œuvre d’algorithmes bio-informatiques permettant l’analyse standardisée du microbiome. De plus, de grandes études de cohorte et des consortiums tels que le Human Microbiome Project 1/2 (États-Unis), l’American Gut Project (États-Unis), MetaHIT (UE) ou le projet IHMS (UE) ont été créés afin d’analyser systématiquement et à l’échelle de la population le microbiome, ses facteurs d’influence intrinsèques et extrinsèques et son rôle dans les processus pathologiques. Toutes les études menées à ce jour sur les altérations du microbiome et la pathogenèse ont révélé de nombreux liens avec les maladies cardiovasculaires,9 les maladies inflammatoires de l’intestin,10 le diabète,11 les maladies cardiométaboliques,12 les hépatopathies,13 les troubles du développement neurologique14 et en particulier les cancers15 comportant des modifications du microbiome intestinal ou des interactions microbes-hôte, appelées dysbiose. Les mécanismes des interactions microbiome-hôte impliqués dans la pathogenèse qui ont été étudiés jusqu’à présent suggèrent un rôle direct des bactéries commensales, en tant que microbes potentiellement pathogènes, qui peuvent par exemple influer de manière décisive sur le développement de l’auto-immunité16 par l’intermédiaire de protéines bactériennes sécrétées, telles que le lipopolysaccharide (LPS), ou sur la cancérogenèse gastro-intestinale par le biais de la génotoxicité de la colibactine.17 D’autres mécanismes reposent sur la métabolisation des composants alimentaires. À titre d’exemple, la consommation de viande rouge et de L-carnitine favorise ainsi la production de métabolites microbiens en tant que précurseurs du N-oxyde de triméthylamine, qui peut renforcer la formation de l’athérosclérose chez l’homme.18 De surcroît, il existe de nombreux autres exemples physiopathologiques d’interaction microbiome-hôte, bien que le spectre n’ait pas encore été entièrement exploré ni scientifiquement validé.
L’utilisation d’antibiotiques: un facteur cliniquement pertinent de la dysbiose du microbiome
Le traitement antibiotique est l’une des principales causes d’altération du microbiome intestinal humain. Les modifications de la composition microbienne dépendent de la posologie, de la durée du traitement, de la forme d’administration et de la classe d’antibiotiques (AB). Les effets à court et à long terme sur le microbiome intestinal pendant et après un traitement antibiotique ont été examinés dans le cadre de plusieurs études. Une diminution de la diversité alpha du microbiome était le phénomène le plus fréquemment observé. À titre d’exemple, il a été ainsi démontré que l’administration à court terme de la quinolone ciprofloxacine ou du méropénème associé à la vancomycine chez des sujets sains peut altérer la diversité du microbiome pendant une période allant jusqu’à 6 mois.19,20 Une autre étude a en outre permis de constater que l’administration de mélanges de probiotiques après l’administration de l’AB ciprofloxacine associé au métronidazole chez des volontaires sains ne peut pas accélérer la restauration de la diversité du microbiome, mais au contraire la retarder davantage et aggraver la dysbiose microbienne dans le tractus gastro-intestinal.21 L’alimentation a été identifiée comme un autre facteur d’altération de la récupération après un stress antibiotique et il a été constaté qu’une alimentation sans fibres prolonge la dysbiose du microbiome intestinal induite par les AB et altère également le micro-environnement intestinal et le métabolome.22
Du point de vue clinique, des liens épidémiologiques ont été établis entre le recours aux antibiothérapies pendant la petite enfance et le risque accru d’asthme, impliquant des liens significatifs avec une diversité alpha altérée au cours des premières années de la vie.23 De la même manière, l’antibiothérapie administrée durant la petite enfance prédispose à l’apparition de surpoids plus tard dans la vie,24 ce qui, dans le cadre des expériences précliniques, a été attribué à une dysbiose du microbiome intestinal et parallèlement à des troubles métaboliques.25 À l’âge adulte, l’administration d’AB entraîne également des dommages collatéraux liés au microbiome, allant des maladies infectieuses à la cancérologie. À titre d’exemple, les antibiothérapies peuvent réduire la résistance à la colonisation du micro-environnement intestinal et favoriser les infections à Clostridioides difficile, Klebsiella pneumoniae ou E. coli.26,27 À l’autre extrémité du spectre, on trouve les immunothérapies à base de lymphocytes T contre les cancers à tumeurs solides. Dans ce contexte, il a été décrit à plusieurs reprises que l’administration d’AB à large spectre à des patients cancéreux porte atteinte au microbiome intestinal et que des liens significatifs associés à une efficacité réduite de l’immunothérapie et à une mortalité accrue ont été constatés.28 Des corrélations similaires ont été observées pour la greffe de cellules souches (GCS) allogéniques ou pour les thérapies par cellules CAR-T anti-CD19 contre les tumeurs hématologiques malignes.29,30 D’un point de vue physiopathologique, on tente d’expliquer ces liens par le fait que les antibiothérapies éradiquent un certain nombre de bactéries intestinales commensales, par exemple les espèces Bifidobacterium ou Clostridium, qui produisent des métabolites microbiens tels que l’adénosine ou les acides gras à chaîne courte dans l’intestin, et qui sont essentiels à la fonction antitumorale des lymphocytesT humains.31,32
Le microbiome intestinal en tant que structure effectrice («druggable target») dans le contexte clinique
L’administration d’AB est inévitable dans la grande majorité des situations cliniques nécessitant le traitement d’infections ou la prévention de complications infectieuses après une intervention chirurgicale ou une greffe (GSC allogénique). Afin de limiter les dommages collatéraux sur le microbiome, différentes stratégies sont actuellement à l’étude. Bien qu’elles soient encore controversées, il existe des données probantes sérieuses selon lesquelles les traitements probiotiques ne favorisent pas la récupération du microbiome après un stress antibiotique et même la réduisent.21,33 En revanche, une transplantation de microbiome fécal (TMF) autologue avec du matériel fécal contenant du microbiome intestinal recueilli, traité et stocké avant l’antibiothérapie entraîne une récupération complète et rapide du microbiome spécifique du patient après les antibiothérapies.21,34 D’autres stratégies alternatives, actuellement testées dans le cadre d’études cliniques de phase II/III, consistent à neutraliser les AB dans l’intestin par le biais de nanoparticules activées35 ou de bêta-lactamases36, ce qui permet de réduire les dommages causés au niveau du microbiome tout en conservant l’efficacité systémique des AB.
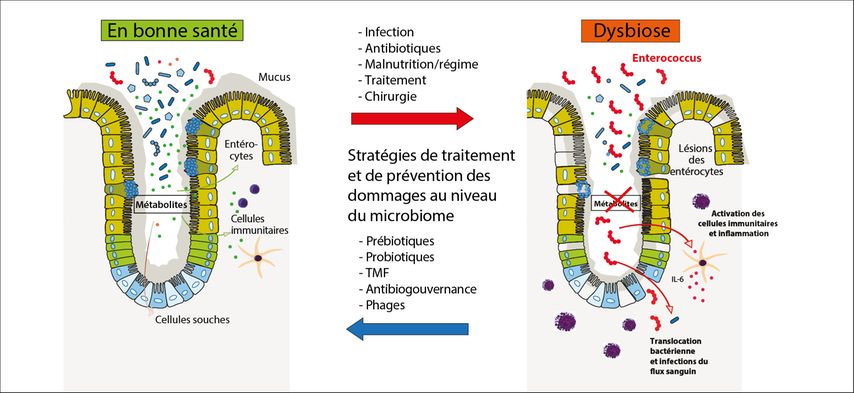
La TMF en soi a été testée en tant que l’une des stratégies d’intervention les plus importantes dans la recherche clinique et translationnelle sur le microbiome dans de nombreuses indications et met en évidence une très bonne efficacité pouvant être reproduite notamment pour les maladies infectieuses et inflammatoires de l’intestin telles que l’infection à Clostridioides difficile (ICD), la colite ulcéreuse et la réaction du greffon intestinal contre l’hôte après une GSC allogénique.37–39 L’étude de phase I/II a également montré que même l’efficacité des traitements par un inhibiteur de point de contrôle immunitaire peut être augmentée par la TMF de matériel fécal contenant du microbiome intestinal provenant de répondeurs à l’immunothérapie.40,41 Non seulement les concepts microbiens complexes comme la TMF, mais aussi les probiotiques tels que les bifidobactéries, dont l’administration orale a augmenté de manière significative l’effet du nivolumab associé à l’ipilimumab sur la survie sans progression de patients atteints de carcinome rénal, présentent un effet clinique en immunothérapie.42 Cependant, de manière générale, l’incertitude règne jusqu’à aujourd’hui quant à l’effet effecteur de la TMF, qu’il s’agisse de microbes viables capables de se multiplier ou de leurs métabolites, étant donné que des études pilotes ont démontré que des filtrats stériles de TMF contenant des métabolites microbiens ou des bactériophages sont tout aussi efficaces contre l’ICD ou l’entérocolite nécrosante.43,44 La Figure 1 présente un résumé des stratégies d’intervention cliniquement pertinentes dans la recherche translationnelle sur le microbiome.
Fig. 1: Stratégies d’intervention cliniquement pertinentes dans la recherche translationnelle sur le microbiome
Fig. 2: Le corps humain adulte abrite environ 1013 bactéries, ce qui correspond à peu près au nombre de cellules humaines
Résumé
Bien que nous n’en soyons qu’au début des recherches sur l’interaction entre le microbiome et l’homme, on peut déjà constater que le microbiome est impliqué dans de nombreuses maladies et que l’efficacité des traitements cliniquement établis dépend également de l’homéostasie du microbiome. Dans ce contexte, il convient d’attirer l’attention sur les pratiques de prescription d’AB, étant donné que d’un point de vue clinique, il ne faut pas seulement tenir compte de l’aspect de l’antibiogouvernance. C’est bien plus en raison de l’importance clinique croissante du microbiome humain, qu’il faut aussi prendre en considération le fait que les AB, en particulier les AB à large spectre, induisent des dommages au niveau du microbiome et de l’interaction microbe-hôte qui peuvent avoir un effet négatif sur les processus pathologiques ou les traitements cliniques, de sorte que l’on peut également parler dans ce contexte de «gouvernance du microbiome».
Littérature:
1 Sender R et al.: PLoS Biol 2016; 14: e1002533 2 Kern L et al.: Curr Opin Microbiol 2021; 63: 158-71 3 Ansaldo E et al.: Annu Rev Immunol 2021; 39: 449-79 4 Koh A, Backhed F: Mol Cell 2020; 78: 584-96 5 Lin W et al.: Curr Opin Microbiol 2021; 63: 150-7 6 Vujkovic-Cvijin I et al.: Nature 2020; 587: 448-54 7 Gacesa R et al.: Nature 2022; 604: 732-9 8 Byrd, AL et al.: J Exp Med 2021; 218: e20200606 9 Fromentin S et al.: Nat Med 2022; 28: 303-14 10 Lloyd-Price J et al.: Nature 2019; 569: 655-62 11 Vatanen T et al.: Nature 2018; 562: 589-94 12 Koeth RA et al.:J Clin Invest 2019; 129: 373-87 13 Wang R et al.: Cell Mol Immunol 2021; 18: 4-17 14 Morais LH et al.: Nat Rev Microbiol 2021; 19: 241-55 15 Cullin N et al.:Cancer Cell 2021; 39: 1317-41 16 Vatanen T et al.: Cell 2016; 165: 842-53 17 Pleguezuelos-Manzano C et al.: Nature 2020; 580: 269-73 18 Koeth RA et al.: Nat Med 2013; 19: 576-85 19 Dethlefsen L, Relman DA: Proc Natl Acad Sci U S A 2011; 108 Suppl 1: 4554-61 20 Palleja A et al.: Nat Microbiol 2018; 3: 1255-65 21 Suez J et al.: Cell 2018; 174: 1406-23 22 Tanes C et al.: Cell Host Microbe 2021; 29: 394-407 23 Patrick DM et al.: Lancet Respir Med 2020; 8: 1094-105 24 Leong KSW et al.: JAMA Netw Open 2020; 3: e1919681 25 Mahana D et al.: Genome Med 2016; 8: 48 26 Sorbara MT et al.: J Exp Med 2019; 216: 84-98 27 Buffie CG et al.: Nature 2015; 517: 205-08 28 Pinato DJ et al.: JAMA Oncol 2019; 5: 1774-8 29 Shono Y et al.: Sci Transl Med 2016; 8: 339ra371 30 Jenq RR et al.: Biol Blood Marrow Transplant 2015; 21: 1373-83 31 Mager LF et al.: Science 2020; 369: 1481-9 32 Docampo MD et al.: Blood 2022; 139: 2392-405 33 Montassier E et al.: Nat Microbiol 2021; 6: 1043-54 34 Taur Y et al.: RSci Transl Med 2018; 10: eaap9489 35 de Gunzburg J et al.: J Infect Dis 2018; 217: 628-36 36 Kokai-Kun JF et al.: Lancet Infect Dis 2019; 19: 487-96 37 van Nood E et al.: N Engl J Med 2013; 368: 407-15 38 Costello SP et al.: JAMA 2019; 321: 156-64 39 Goeser F et al.: Eur J Haematol 2021; 107: 229-45 40 Baruch EN et al.: Science 2021; 371: 602-9 41 Davar D et al.: Science 2021; 371: 595-602 42 Dizman N et al.: Nat Med 2022; 28: 704-12 43 Ott SJ et al.: Gastroenterology 2017; 152: 799-811 44 Brunse A et al.: ISME J 2022; 16: 686-94
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...