Le potentiel d’analyses de routine du métagénome microbien des voies respiratoires de la mucoviscidose
Auteurs:
Marie-Madlen Pust, MSc
Prof. Dr méd. Dr rer. nat. Burkhard Tümmler
Klinik für pädiatrische Pneumologie, Allergologie und Neonatologie
Medizinische Hochschule Hannover
E-mail: pust.marie-madlen@mh-hannover.de
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Les agents pathogènes bactériens jouent un rôle non négligeable dans la colonisation des voies respiratoires. Une diversité bactérienne fortement réduite, accompagnée d’une présence accrue d’un ou plusieurs agents pathogènes, est considérée comme typique du microbiome pulmonaire de la mucoviscidose. Des analyses de routine du métagénome des voies respiratoires, ainsi que l’établissement de valeurs seuils, pourraient contribuer de manière significative au succès du traitement des patients atteints de mucoviscidose.
Keypoints
Les méthodes de séquençage permettent de détecter rapidement les bactéries abondantes et rares et leurs déterminants de résistance aux antibiotiques à partir d’un échantillon de patient.
Le suivi longitudinal de l’ADN spécifique des agents pathogènes pourrait contribuer à prévenir les infections respiratoires bactériennes et le développement d’une signature irréversible du microbiome de la mucoviscidose.
L’évaluation de la dynamique de croissance d’une population d’agents pathogènes dans les voies respiratoires permet de suivre en continu le taux de division bactérienne.
L’absence de directives standard empêche actuellement l’introduction d’analyses de routine du métagénome des voies respiratoires de la mucoviscidose dans les diagnostics cliniques.
Bien que la mucoviscidose (ou fibrose kystique) soit une maladie multisystémique, la morbidité accrue et la mortalité prématurée des patients s’expliquent principalement par les infections chroniques et les inflammations des voies respiratoires inférieures. Les agents pathogènes bactériens et leurs déterminants de résistance aux antibiotiques sont couramment mesurés par des méthodes dépendantes de la culture. Étant donné qu’il y a souvent un délai de 48 à 72 heures entre le prélèvement de l’échantillon et le diagnostic, l’instauration d’un traitement par des antibiotiques spécifiques à l’agent pathogène peut être retardée.1 Pendant ce temps, l’antibiothérapie empirique à large spectre déstabilise l’ensemble du microbiome pulmonaire et favorise la croissance sans concurrence de germes résistants.2 De plus, la charge bactérienne de l’agent pathogène doit être ≥103–105UFC/ml pour que la croissance dans le milieu de culture microbiologique soit couronnée de succès.1 L’apparition de ce modèle de microbiome pulmonaire, avec une diversité bactérienne fortement réduite et la présence accrue d’un ou plusieurs agents pathogènes, a été décrite dans la littérature comme typique de la mucoviscidose et comme une signature irréversible du microbiome dans la progression avancée de la maladie.3
La métagénomiquerespiratoire
Dans la métagénomique des voies respiratoires, l’ensemble du matériel génétique humain et microbien présent dans l’échantillon du patient est isolé et séquencé, p.ex. à partir du frottis nasopharyngé profond, du lavage broncho-alvéolaire ou de l’expectoration induite. Les fragments d’ADN sont ensuite mis en correspondance avec une base de données contenant les séquences de référence des chromosomes humains, des bactéries, des virus à ADN, des phages et des champignons. Grâce au procédé de séquençage sensible à haut débit, il est possible de déterminer la taxonomie des micro-organismes d’un seul échantillon de patient en quelques heures.1, 3, 4 Il est également possible d’analyser les gènes associés à la virulence et à la résistance aux antibiotiques des micro-organismes de l’échantillon du patient.1, 5
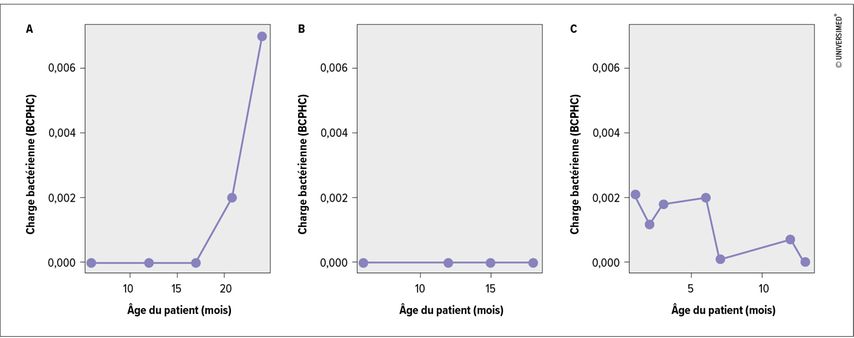
Dans une récente étude longitudinale de métagénomique des voies respiratoires, nous avons démontré que de petites quantités d’ADN de l’agent pathogène de la mucoviscidose Pseudomonas aeruginosa peuvent être présentes dans les voies respiratoires inférieures des nouveau-nés et bébés atteints de mucoviscidose avant que l’agent pathogène ne soit détectable en culture. À cet égard, les trois modèles de survenance de P. aeruginosa suivants ont été mis en évidence chez les enfants (Fig.1):
Fig. 1: Les trois modèles de survenance de P. aeruginosa dans l’enfance. (A) Le mode classique de la mucoviscidose avec une colonisation pathogène des voies respiratoires inférieures. (B) Aucune détection d’ADN spécifique de P. aeruginosa. (C) Détection stochastique de l’ADN spécifique de P.aeruginosa sans preuve de persistance bactérienne dans les voies respiratoires. BCPHC: «bacterial cell per human cell»3
-
Le mode de la mucoviscidose classique (rare chez le bébé) avec une colonisation aiguë puis chronique des voies respiratoires inférieures, attestée par la méthode de séquençage indépendante de la culture et la méthode de diagnostic dépendante de la culture (Fig. 1A).
-
Aucune détection d’ADN spécifique de P. aeruginosa (Fig. 1B).
-
La détection stochastique d’ADN spécifique de P. aeruginosa sans preuve de persistance bactérienne dans les voies respiratoires. Dans ce cas, P. aeruginosa a été détecté exclusivement par la méthode de séquençage (Fig. 1C).
Fait intéressant: le modèle de survenance 3 de P. aeruginosa (Fig. 1C) n’était pas associé à la maladie. L’agent pathogène a également pu être attesté de manière stochastique chez des bébés en bonne santé, avec un taux de détection similaire. Étant donné que P.aeruginosa est largement répandu dans l’environnement, nous considérons que même les bébés en bonne santé entrent régulièrement en contact avec de petites quantités de l’agent pathogène et qu’il peut être bénéfique de développer une réponse immunitaire spécifique qui protège contre les infections respiratoires ultérieures à P. aeruginosa. Un dépistage de routine du métagénome pulmonaire avec un suivi longitudinal de l’ADN spécifique des agents pathogènes pourrait contribuer à prévenir les infections respiratoires bactériennes et éviter le développement d’une signature irréversible du microbiome de la mucoviscidose au cours de l’évolution ultérieure de la maladie.
Calcul de la dynamique de croissance d’une population d’agents pathogènes
Outre la détermination taxonomique des micro-organismes présents dans un échantillon, d’autres informations importantes peuvent être glanées à partir des données de séquençage. Les bactéries des voies respiratoires les plus fréquentes ont un génome circulaire et se divisent de manière bidirectionnelle; la réplication commence à l’origine de la réplication et se termine à l’endroit où les deux fourches de réplication se rencontrent (terminaison). Dans la phase de croissance exponentielle, les cycles de réplication commencent avant que les précédents ne soient terminés. Si l’on séquence l’ADN d’une population d’agents pathogènes à division rapide et que l’on cartographie les fragments par rapport au génome de référence associé, on obtient un gradient de fragments le long du génome avec un nombre accru de fragments à l’origine de la réplication et un nombre réduit à la terminaison.6 L’étendue du gradient peut être déterminée quantitativement pour calculer la dynamique de croissance de la population d’agents pathogènes ou le taux de division de l’agent pathogène dans la communauté microbienne. Des analyses de routine du métagénome des voies respiratoires de la mucoviscidose permettraient de distinguer les agents pathogènes à activité réduite dans le poumon de la mucoviscidose des agents pathogènes en phase de croissance exponentielle précoce ou tardive. En outre, l’effet des facteurs environnementaux sur la population pathogène pourrait être évalué de manière longitudinale, p.ex. au début d’une intervention médicale ou d’un changement de traitement.
Limitations
La qualité et la reproductibilité des résultats du séquençage sont influencées par le type d’échantillon, la qualité du prélèvement d’échantillon, la procédure de laboratoire et de bioinformatique choisie, ainsi que la propreté de l’environnement clinique et de laboratoire.7, 8 À ce jour, il n’existe pas de directives standard pour le traitement des échantillons, les procédures de séquençage ou les bases de données de référence à utiliser. De même, nos connaissances actuelles sur un microbiome pulmonaire sain sont limitées. Notre récente découverte que l’agent pathogène de la mucoviscidose P. aeruginosa peut apparaître à de faibles niveaux dans le microbiome pulmonaire sain de jeunes enfants sans nécessiter d’intervention médicale, souligne l’importance d’établir des seuils cliniquement pertinents. En attendant la mise en place de ces directives et valeurs seuils standard, le diagnostic dépendant de la culture reste une méthode irremplaçable pour distinguer l’apparition inoffensive et non persistante de faibles niveaux de pathogènes de la colonisation pathologique des voies respiratoires inférieures.
Littérature:
1 Charalampous T et al.: Nat Biotechnol 2019; 37: 783-92 2 Langdon A et al.: Genome Med 2016; 8: 39 3 Losada PM et al.: ERJ 2019; 2: 00096-2015 4 Pienkowska K et al.: Microbes Infect 2018; 20: 536-42 5 Bacci G et al.: Int J Mol Sci 2017; 18: 1654 6 Pienkowska K et al.: J Cyst Fibros 2019; 18: 653-56 7 Glassing A et al.: Gut Pathog 2016; 8: 24 8 Salter SJ et al.: BMC Biol 2014; 12: 87
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...