Immunothérapie du carcinome hépatocellulaire
Auteur:
Ap. Prof. PD Dr Matthias Pinter, PhD
Abteilung für Gastroenterologie & Hepatologie
Universitätsklinik für Innere Medizin III
Medizinische Universität Wien
E-mail: matthias.pinter@meduniwien.ac.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
L’inhibiteur de tyrosine kinase (ITK) sorafénib a été pendant environ une décennie la seule option de traitement systémique efficace pour les patients atteints de carcinome hépatocellulaire (CHC) avancé. Ce n’est qu’au cours des quatre dernières années que d’autres substances ont été ajoutées à l’algorithme de traitement du CHC, notamment les ITK tels que le lenvatinib en première intention et le régorafénib ou le cabozantinib en deuxième intention, mais aussi le ramucirumab, un anticorps monoclonal dirigé contre le VEGFR-2 («vascular endothelial growth factor receptor 2»).
Keypoints
-
Alors que la monothérapie par les inhibiteurs des points de contrôle immunitaire n’a jusqu’ici pas encore été couronnée de succès dans le cadre des études de phase III sur le CHC, l’association de l’atézolizumab et du bévacizumab est parvenue à s’imposer par rapport au sorafénib et représente donc le nouveau standard de référence dans le traitement systémique de première intention du CHC.
-
Actuellement, les inhibiteurs des points de contrôle immunitaire sont également évalués dans le cadre d’études cliniques à des stades tumoraux plus précoces, par exemple en association avec la TACE ou comme traitement adjuvant après résection ou ablation locale.
L’immunothérapie par des inhibiteurs des points de contrôle immunitaire (ICI) constitue désormais un pilier de traitement important pour un grand nombre de maladies oncologiques. Les ICI font également l’objet d’évaluations approfondies dans le cadre d’études cliniques chez des patients atteints de carcinome hépatocellulaire (CHC).1,2 Les développements les plus récents sont résumés ci-après.
Les inhibiteurs des points de contrôle immunitaire dans le traitement du CHC
Sur la base de données d’efficacité prometteuses issues d’études de phase II, les ICI nivolumab et pembrolizumab, mais aussi l’association nivolumab/ipilimumab ont été autorisés aux États-Unis (mais pas en Europe) pour le traitement des patients prétraités par le sorafénib. L’autorisation présupposait que ces traitements soient ensuite évalués dans le cadre d’études de phase III.1
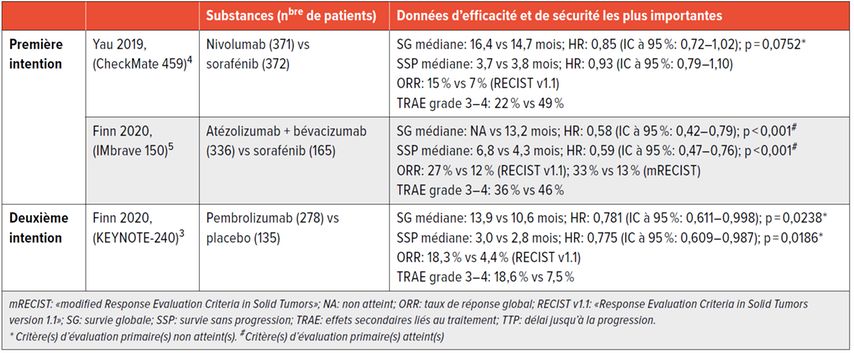
Alors que l’étude de phase III portant sur le nivolumab associé à l’ipilimumab recrute encore des patients (NCT04039607), des résultats des études de phase III sont déjà disponibles pour les deux autres substances. Le nivolumab a été testé en traitement de première intention par rapport au sorafénib et le pembrolizumab a été comparé à un placebo en traitement de deuxième intention (à l’issue d’un traitement préalable par le sorafénib). Les taux de réponse radiologique et les données de sécurité observés lors des études de phase II ont certes pu être confirmés tant pour le nivolumab que pour le pembrolizumab, mais les critères d’évaluation primaires concernant la survie n’ont pas pu être atteints, de sorte que les deux études doivent être formellement considérées comme étant négatives (Tab. 1).3,4
Tab. 1: Études randomisées de phase III évaluant les inhibiteurs des points de contrôle immunitaire dans le traitement du carcinome hépatocellulaire avancé
Outre l’association des ICI entre eux, les ICI sont également associés à d’autres classes de substances. Les traitements qui bloquent la voie de signalisation du VEGF sont notamment bien étayés. En effet, le VEGF n’est pas seulement un facteur d’angiogenèse important; il favorise également un microenvironnement tumoral immunosuppresseur qui stimule la croissance tumorale. Le traitement anti-VEGF vise à reprogrammer cet environnement immunosuppresseur, de sorte que l’efficacité de l’immunothérapie puisse être encore améliorée.1
Ce concept fonctionne dans le cas du CHC comme l’a démontré l’étude IMbrave-150 de manière impressionnante. Dans le cadre de cette étude de phase III, l’association atézolizumab/bévacizumab a été testée vs sorafénib chez des patients non prétraités par voie systémique. Outre une prolongation significative des deux critères d’évaluation primaires que sont la survie globale et la survie sans progression, l’association d’atézolizumab et de bévacizumab a induit une réponse complète ou partielle chez environ un tiers des patients. Le profil d’effets secondaires était également satisfaisant et le délai jusqu’à la détérioration de la qualité de vie a pu être nettement prolongé grâce au traitement en association (Tab. 1).5
Par conséquent, l’atézolizumab associé au bévacizumab a convaincu à tous les niveaux et représente à juste titre le nouveau standard de référence dans le traitement de première intention du CHC.2,6
Développements futurs
Actuellement, les ICI ne sont pas seulement testés chez des patients atteints de CHC avancé, mais aussi à des stades tumoraux plus précoces, en monothérapie ou en association. Ainsi, plusieurs études de phase III sont en cours; elles évaluent les ICI en association avec la chimioembolisation transartérielle (TACE) chez des patients à un stade tumoral intermédiaire (CHC multifocal intrahépatique) (p.ex. NCT03778957, NCT04340193). Les ICI sont également utilisés actuellement dans le cadre d’études cliniques en traitement adjuvant après résection ou ablation locale (p.ex. NCT03847428, NCT04102098).
L’avenir nous dira quels traitements en association s’imposeront ou dans quels contextes l’immunothérapie s’établira dans la prise en charge du CHC au cours des prochaines années.
Littérature:
1 Pinter M et al.: JAMA Oncol 2021; 7: 113-23 2 Gordan JD et al.: J Clin Oncol 2020; 38: 4317-45 3 Finn RS et al.: JClin Oncol 2020; 38: 193-202 4 Yau T et al.: Ann Oncol 2019; 30(Suppl 5): v874-5 5 Finn RS et al.: N Engl J Med 2020; 382: 1894-905 6 Pinter M et al.: Gut 2021; 70: 204-14
Das könnte Sie auch interessieren:
L’obésité et ses conséquences sur les reins
L’obésité est devenue l’un des principaux problèmes de santé dans le monde. Elle a des conséquences directes et indirectes sur les reins. Outre le risque de glomérulopathie et l’ ...
Une perte de poids précoce peut favoriser la rémission du diabète de type 2
De nouveaux concepts physiopathologiques remettent en question la compréhension actuelle du diabète de type 2 (DT2). L’accent n’est plus mis sur l’augmentation de la glycémie, mais sur ...
Suivi à long terme après un cancer de l’enfant ou de l’adolescent: points pertinents pour les internistes et les médecins de famille
En raison de l’augmentation de la survie globale après un cancer de l’enfant ou de l’adolescent, la population de patients ayant survécu à un cancer de l’enfant ne cesse de croître et de ...