Endocardite infectieuse: pathologie redoutable avec diagnostic difficile
Auteur:
PD Dr méd. Hajo Müller
Médecin adjoint agrégé, chargé de cours
Service de cardiologie
Unité d’échocardiographie
Hôpitaux universitaires de Genève
E-mail: hajo.muller@hcuge.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
L’endocardite infectieuse est une pathologie redoutable avec une mortalité et morbidité toujours très élevées. Le diagnostic reste difficile et se base sur des hémocultures et la documentation d’une atteinte cardiaque comme critères majeurs. L’implication du cardiologue se fait dans la démarche diagnostique ainsi que la prise en charge dans le contexte d’une approche multidisciplinaire («team endocardite»). L’imagerie cardiaque de premier choix reste l’échocardiographie avec les modalités transthoraciques et transœsophagiennes qui sont complémentaires.
Keypoints
-
L’endocardite infectieuse est une pathologie redoutable avec une mortalité et morbidité toujours très élevées.
-
Devant tout état fébrile avec valve artificielle, accident vasculaire cérébral ischémique ou insuffisance valvulaire ou cardiaque nouvelle, il faut penser à une endocardite.
-
Le diagnostic peut être difficile et il se base sur le tableau clinique, les hémocultures et la documentation d’une atteinte cardiaque par imagerie.
-
Vu le défi diagnostique et la complexité du tableau clinique, une évaluation des patients dans un groupe multidisciplinaire (team endocardite) est fortement recommandée.
Classifications et définitions
On peut classifier l’endocardite de plusieurs manières, par exemple selon la localisation de l’infection et l’absence ou présence de matériel intracardiaque prothétique, ou selon le mode d’acquisition.
On distingue une endocardite des valves du cœur gauche et une endocardite des valves du cœur droit. Par ailleurs, on fait la différence entre une endocardite sur valve native et une endocardite de prothèse valvulaire. Ceci est pertinent car la morbi-mortalité intra-hospitalière d’une endocardite sur valve prothétique est plus élevée que celle d’une endocardite sur valve native et nécessite souvent un traitement chirurgical pour éradiquer le foyer infectieux de manière durable ou en raison de complications. L’infection de prothèse peut être précoce (<1 année par rapport à l’intervention avec probable acquisition peropératoire) ou tardive (>1 année avec probable acquisition communautaire) expliquant la différence dans la distribution des germes en cause. Une catégorie particulière est l’endocardite sur matériel prothétique de type stimulateur cardiaque ou défibrillateur interne. En effet, il s’agit d’une catégorie avec diagnostic difficile nécessitant souvent l’emploi de moyens d’imagerie supplémentaires p.ex. scanner (CT) cardiaque ou tomographie par émission de positrons (TEP/CT).1
Concernant le mode d’acquisition, on fait la différence entre une endocardite acquise en communauté et une endocardite acquise dans un contexte de soins médicaux ambulatoires ou institutionnels. À l’intérieur de cette dernière catégorie on peut faire la différence entre une endocardite nosocomiale et non nosocomiale en fonction de la durée d’hospitalisation avant le diagnostic (>48h vs <48h).2 Une autre catégorie d’acquisition est l’endocardite dans un contexte de toxicomanie intraveineuse, avec souvent une atteinte des valves du cœur droit, mais il faut garder à l’esprit que les valves gauches sont également fréquemment atteintes dans ce contexte.
Épidémiologie et pathogénèse
La fréquence de l’endocardite infectieuse est en augmentation. On assiste à un changement épidémiologique avec une prédominance du staphylocoque par rapport au streptocoque et une augmentation des cas d’endocardite acquis dans un contexte de soins médicaux avec plus d’endocardites à staphylocoque et des patients plus âgés qu’auparavant.3−5 Les endocardites sur prothèse valvulaire mécanique ou biologique représentent environ 10 à 30% des cas et on trouve fréquemment des staphylocoques ou des champignons comme agents infectieux.2,3 Les valves percutanées sont également concernées avec surtout des staphylocoques et des entérocoques comme agents infectieux en cause.3,6,7 En général, le processus pathogénique est favorisé par une lésion de l’endocarde avec dépôt de plaquettes et de fibrine à l’origine de «pseudo végétations» et initié par un traumatisme des muqueuses ou de la peau permettant une bactériémie et par la suite une adhérence et colonisation résultant en des végétations infectieuses. À noter que le staphylocoque doré est capable de causer des infections sans lésion de l’endocarde au préalable, ce qui explique probablement son caractère agressif2,8 et la fréquence élevée d’atteintes cardiaques en cas de bactériémie avec ce germe.9 L’atteinte au niveau du cœur gauche est de loin plus fréquente et probablement due à des gradients de pression plus élevés au niveau du cœur gauche.
Manifestations cliniques, complications majeures et pronostic
L’endocardite infectieuse est une maladie grave et donc une urgence en raison d’un taux de mortalité élevé. Celle-ci avoisine en intra-hospitalier les 15 à 30% de toutes endocardites confondues5,10,11 et semble plus élevée (20 à 40%) en cas d’endocardite de prothèse valvulaire.2,3 Une place particulière revient à l’endocardite à staphylocoque doré plus fréquemment à l’origine de complications locales graves (abcès ou pseudo-anévrisme et dysfonction valvulaire sévère à l’origine d’un tableau d’insuffisance cardiaque sévère voire état de choc) avec une mortalité qui peut atteindre un taux de 80%.2,12 L’autre raison de considérer le caractère urgent de cette pathologie est le taux élevé de complications emboliques responsables d’une morbidité augmentée. Les embolies cérébrales et spléniques sont les plus fréquentes. Des embolies cliniquement manifestes sont décrites dans environ 30% des cas13 mais des lésions silencieuses sont fréquentes. On peut trouver dans certaines séries des lésions cérébrales chez 50 à 80% des patients.14−16 Le tableau clinique est donc dominé par les complications locales et emboliques. Le pronostic est influencé par les caractéristiques du patient, le type de germes, le type de complication et les trouvailles à l’échocardiographie. Des marqueurs échocardiographiques de mauvais pronostic sont par exemple une diminution sévère de la fraction d’éjection ventriculaire gauche et des signes d’une augmentation importante des pressions de remplissage ventriculaire gauche ou pulmonaires. Les trois complications majeures qui représentent une indication pour une chirurgie cardiaque précoce voire urgente sont l’insuffisance cardiaque dans le contexte d’une dysfonction valvulaire sévère, une infection non contrôlée soit localement soit selon le type de germe soit en cas de non réponse aux antibiotiques ainsi que la prévention d’embolisations artérielles en prévention secondaire ou primaire.2,3 À noter l’importance de la localisation, la mobilité et la taille (>10mm)13 des végétations pour la stratification du risque embolique. La taille des végétations semble également prédictive de la mortalité avec une valeur >15mm comme valeur seuil.13 La majorité des accidents vasculaires cérébraux sont ischémiques et la mortalité d’endocardite est plus élevée en cas d’embolisation. Il existe une association avec le type de germe notamment le staphylocoque doré.15−17 Les embolisations diminuent après le début de l’antibiothérapie et notamment après la deuxième semaine.18 Environ 50% des patients avec endocardite infectieuse seront opérés.19 Une chirurgie précoce semble pouvoir prévenir des embolisations chez des patients hémodynamiquement stables à bas risque opératoire mais avec dysfonction valvulaire sévère et des végétations >10mm selon la seule étude randomisée actuellement à disposition.20 Un autre avantage d’une chirurgie précoce est la possibilité de conserver la fonction valvulaire par réparation plutôt que de devoir remplacer la valve par une prothèse en cas de destruction avancée.21
Diagnostic
L’endocardite est difficile à diagnostiquer. La présentation clinique est variable et le diagnostic est plus facile à évoquer face à un tableau clinique aigu avec bactériémie à staphylocoque doré. Mais la situation est parfois moins claire, p.ex. chez un patient hospitalisé pour bronchopneumonie22 ou avec une clinique décapitée par un traitement antibiotique au préalable. Le diagnostic est également plus difficile face à un tableau subaigu chronique chez un patient afébrile avec baisse de l’état général et perte de poids comme symptômes prédominants. Les patients âgés et/ou immunosupprimés se présentent souvent avec un tableau clinique atypique.23 À noter qu’il y a des endocardites sans élévation de marqueurs d’inflammation de type protéine C réactive.
En général, l’état fébrile (90%), l’apparition d’un souffle cardiaque à l’auscultation (85%) ainsi que des manifestations cliniques d’embolisation (25 à 30%) doivent alerter le clinicien. Étant donné la présence fréquente d’embolies silencieuses au niveau cérébral et splénique, une imagerie systématique en cas de suspicion clinique d’endocardite infectieuse est proposée. Devant tout état fébrile avec valve artificielle, accident vasculaire cérébral ischémique, insuffisance valvulaire ou cardiaque nouvelle, il faut penser à une endocardite. On peut également être face à une présentation comme fièvre d’origine indéterminée ou des arthrites septiques multiples. Enfin, des troubles de la conduction nouvelle de type BAV (bloc auriculo-ventriculaire) peuvent être le signe d’un abcès avec atteinte des voies de conduction. Des lésions périphériques d’endocardite de type phénomène vasculaire et immunologique sont à rechercher. Finalement, le type de germe retrouvé dans les hémocultures oriente le diagnostic et la probabilité d’endocardite infectieuse (p.ex. groupe HACEK).
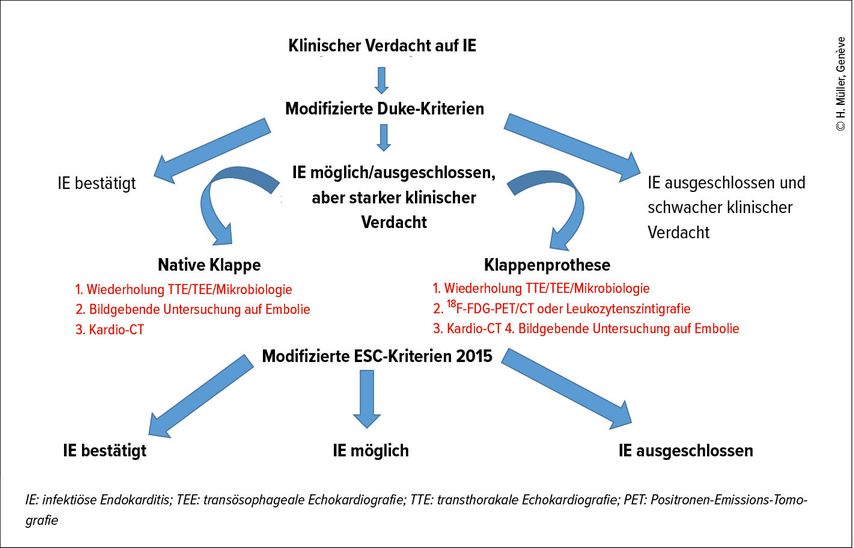
Classiquement, le diagnostic se base sur les critères de Duke avec 2 critères majeurs (hémocultures et imagerie cardiaque) et plusieurs critères mineurs2,24 qui sont néanmoins nettement moins performants dans certains sous-groupes, comme les patients avec hémocultures négatives ou chez les patients avec valve et matériel cardiaque prothétique. Pour augmenter la performance diagnostique de ces critères, la société Européenne de cardiologie a proposé en 2015 des critères modifiés en ajoutant des critères majeurs d’imagerie par CT cardiaque et/ou TEP/CT et comme nouveau critère mineur la mise en évidence de phénomènes d’embolisation même asymptomatiques par imagerie (Fig. 1).3 Ceci permet de réduire le nombre de cas classifiés comme possible endocardite notamment chez les patients avec matériel cardiaque prothétique.25
Imagerie
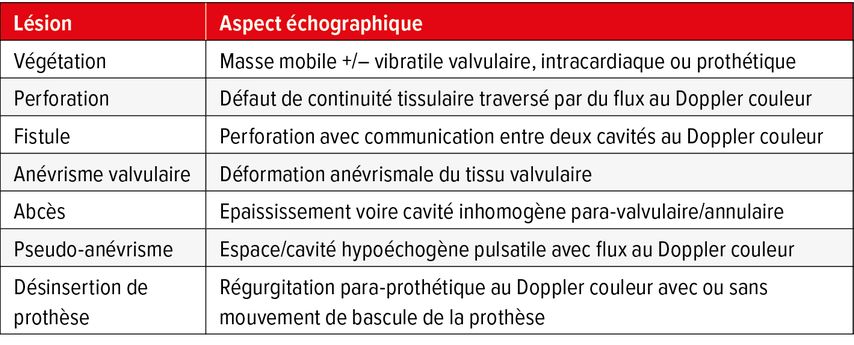
L’imagerie cardiaque initiale de premier choix reste néanmoins l’échocardiographie avec ses modalités transthoracique et transœsophagienne qui sont complémentaires.2,3,26 Les critères principaux majeurs échocardiographiques pour une endocardite infectieuse sont des atteintes valvulaires avec présence de végétations, perforation ou anévrisme, des atteintes paravalvulaires de type abcès, fistule ou pseudo-anévrisme ainsi qu’une désinsertion de prothèse avec régurgitation paraprothétique nouvelle2,21,26,27 (Tab. 1, Fig. 2). Globalement, on admet une sensibilité de 70% pour l’échographie transthoracique et de 96% pour l’échographie transœsophagienne pour le diagnostic d’endocardite sur valve native.3 La performance diagnostique est moindre surtout en ce qui concerne l’examen transthoracique chez les patients porteurs de prothèses et matériel intracardiaque avec une sensibilité de 50% et 92% respectivement.3 Il peut y avoir des faux positifs car le diagnostic différentiel de végétation infectieuse à l’échocardiographie est large avec masse thrombotique, végétation non bactérienne, rupture de cordage et tumeur valvulaire. Il faut donc toujours intégrer le contexte clinique dans l’interprétation des images et comparer celles-ci avec des examens antérieurs si disponibles.
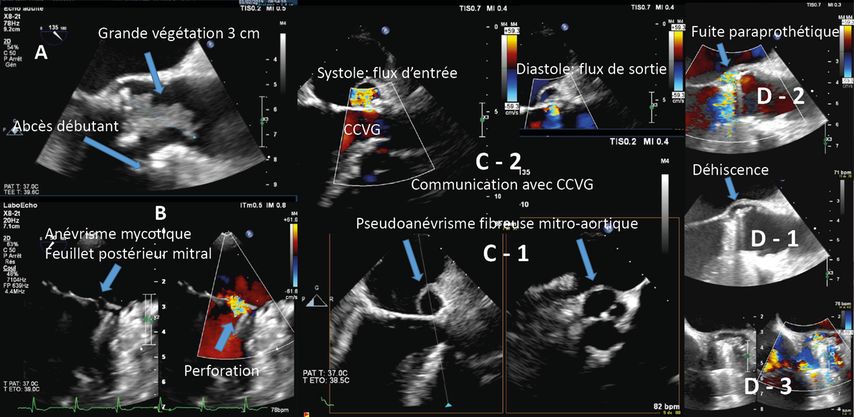
Fig. 2: Images d’échocardiographie d’endocardite. A): grande végétation de 3cm sur bioprothèse aortique avec abcès débutant périprothétique au niveau de la paroi antérieure de la racine aortique. B): anévrisme mycotique au niveau du segment P1 du feuillet postérieur de la valve mitrale avec perforation (flux traversant au Doppler couleur). C): pseudoanévrisme de la région fibreuse mitro-aortique (C-1) communicant avec la chambre de chasse ventriculaire gauche (CCVG) avec remplissage en systole et vidange en diastole (C2) au Doppler couleur. D): déhiscence de prothèse aortique mécanique (D-1) avec régurgitation paraprothétique(D-2) au niveau postérieur. Vue court axe (D-3)
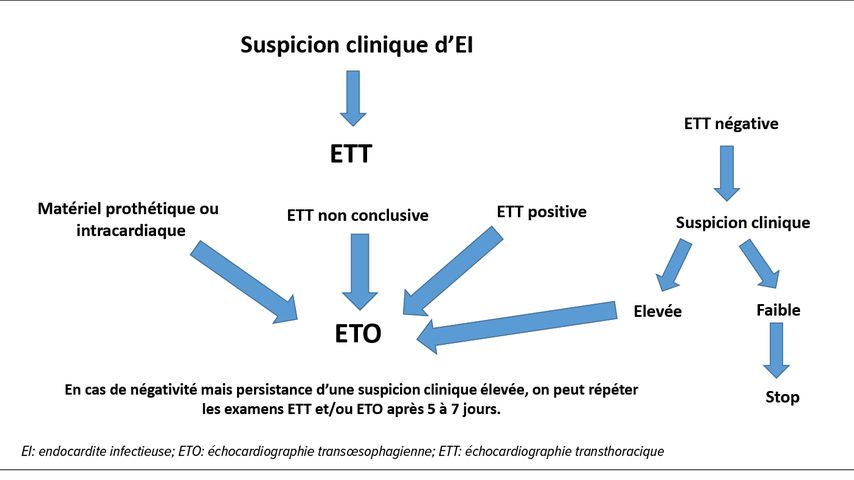
Selon la suspicion clinique et le résultat de l’examen transthoracique initial, on complète avec un examen transœsophagien ou on rejette le diagnostic. En cas de trouvaille positive à l’examen transthoracique, examen non conclusif, ou présence de matériel soit prothétique soit intracardiaque, on procède à un examen transœsophagien. En cas de négativité mais persistance d’une suspicion clinique élevée, on devrait répéter un examen après 5à 7 jours (Fig. 3). Dans le cas particulier d’une endocardite des valves droites qui sont de localisation antérieure, on peut parfois se contenter d’une échographie transthoracique seule en raison de la bonne visualisation des valves droites par cette approche. Néanmoins il faut garder à l’esprit la possibilité d’une atteinte des valves gauches concomitante qui doit être recherchée lors de la moindre suspicion.
Fig. 3: Suspicion d’endocardite – Indications de l’échocardiographie (adapté selon Habib et al., 2009 et Habib et al., 2015)2, 3
Le diagnostic de complication paravalvulaire, surtout celui d’abcès débutant autour de prothèses valvulaires peut être difficile et c’est donc ici qu’une imagerie complémentaire de type CT cardiaque est proposée3,28,29 même si la supériorité par rapport à l’examen transœsophagien n’est pas certaine.30 Il faut aussi considérer la toxicité du produit de contraste ainsi que l’exposition rayonnante. Cet examen donnera par contre des informations complémentaires pour le chirurgien cardiovasculaire en cas de nécessité d’intervention. Un autre moyen diagnostique est le TEP/CT ou la scintigraphie marquée aux leucocytes à la recherche d’un foyer d’inflammation péri-prothétique ou extracardiaque.1,3 Examen limité par sa disponibilité mais très utile à la recherche d’abcès débutant péri-prothétique avec échocardiographie transœsophagienne négative ou suspicion d’infection de boîtier chez les patients porteurs de stimulateur cardiaque. À noter qu’il peut y avoir des faux positifs du TEP/CT notamment dans la période inflammatoire post-opératoire.1,3
Team endocardite
Vu le défi diagnostique et la complexité du tableau clinique, une évaluation des patients dans un groupe multidisciplinaire (team endocardite) est fortement recommandée. Un tel groupe devrait être composé d’un infectiologue, cardiologue et chirurgien cardiovasculaire expérimentés dans le domaine, complété au besoin par un neurologue. En effet, la littérature suggère qu’une telle prise en charge systématique est bénéfique en termes de mortalité pour ces patients complexes.31,32
Littérature:
1 Bruun NE et al.: Cardiac imaging in infectious endocarditis. Eur Heart J 2014; 35: 624-32 2 Habib G et al.: Guidelines on the prevention, diagnosis, and treatment of infective endocarditis (new version 2009): the Task Force on the Prevention, Diagnosis, and Treatment of Infective Endocarditis of the European Society of Cardiology (ESC). Endorsed by the European Society of Clinical Microbiology and Infectious Diseases (ESCMID) and the International Society of Chemotherapy (ISC) for Infection and Cancer. Eur Heart J 2009; 30: 2369-413 3 Habib G et al.: 2015 ESC Guidelines for the management of infective endocarditis: The Task Force for the Management of Infective Endocarditis of the European Society of Cardiology (ESC). Endorsed by: European Association for Cardio-Thoracic Surgery (EACTS), the European Association of Nuclear Medicine (EANM). Eur Heart J 2015; 36: 3075-128 4 Fernández-Hidalgo N et al.: Contemporary epidemiology and prognosis of health care-associated infective endocarditis. Clin Infect Dis 2008; 47: 1287-97 5 Slipczuk L et al.: Infective endocarditis epidemiology over five decades: a systematic review. PLoS One 2013; 8: e82665 6 Khan A et al.: Infective endocarditis post-transcatheter aortic valve implantation (TAVI), microbiological profile and clinical outcomes: A systematic review. PLoS One 2020; 15: e0225077 7Amat-Santos IJ et al.: Infective endocarditis after transcatheter aortic valve implantation: results from a large multicenter registry. Circulation 2015; 131: 1566-74 8 Que YA et al.: Fibrinogen and fibronectin binding cooperate for valve infection and invasion in Staphylococcus aureus experimental endocarditis. J Exp Med 2005; 201: 1627-35 9 Rasmussen RV et al.: Prevalence of infective endocarditis in patients with Staphylococcus aureus bacteraemia: the value of screening with echocardiography. Eur J Echocardiogr 2011; 12: 414-20 10 Cahill TJ, Prendergast BD: Infective endocarditis. Lancet 2016; 387: 882-93 11 Murdoch DR et al.: Clinical presentation, etiology, and outcome of infective endocarditis in the 21st century: the International Collaboration on Endocarditis-Prospective Cohort Study. Arch Intern Med 2009; 169: 463-73 12 San Román JA et al.: Prognostic stratification of patients with left-sided endocarditis determined at admission. Am J Med 2007; 120: 369.e1-7 13 Thuny F et al.: Risk of embolism and death in infective endocarditis: prognostic value of echocardiography: a prospective multicenter study. Circulation 2005; 112: 69-75 14 Snygg-Martin U et al.: Cerebrovascular complications in patients with left-sided infective endocarditis are common: a prospective study using magnetic resonance imaging and neurochemical brain damage markers. Clin Infect Dis 2008; 47: 23-30 15 Cooper HA et al.: Subclinical brain embolization in left-sided infective endocarditis: results from the evaluation by MRI of the brains of patients with left-sided intracardiac solid masses (EMBOLISM) pilot study. Circulation 2009; 120: 585-91 16 Iung B et al.: Determinants of cerebral lesions in endocarditis on systematic cerebral magnetic resonance imaging: a prospective study. Stroke 2013; 44: 3056-62 17 Lebowitz D et al.: Disseminated emboli caused by a large Vegetation in Staphylococcus aureus Endocarditis. Am J Clin Microbiol Antimicrob 2018; 1: 1021 18 Dickerman SA et al.: The relationship between the initiation of antimicrobial therapy and the incidence of stroke in infective endocarditis: an analysis from the ICE Prospective Cohort Study (ICE-PCS). Am Heart J 2007; 154: 1086-94 19 Tornos P et al.: Infective endocarditis in Europe: lessons from the Euro heart survey. Heart 2005; 91: 571-5 20 Kang DH et al.: Early surgery versus conventional treatment for infective endocarditis. N Engl J Med 2012; 366: 2466-73 21 Müller H et al.: Mitral valve repair in acute extensive infectious endocarditis. Arch Cardiovasc Dis 2009; 102: 667-8 22 Mossaz L et al.: What seemed to be a typical pneumonia. Cardiovascular Medicine 2014; 16: 171 23 Pérez de Isla L et al.: Negative blood culture infective endocarditis in the elderly: long-term follow-up. Gerontology 2007; 53: 245-9 24 Li JS et al.: Proposed modifications to the Duke criteria for the diagnosis of infective endocarditis. Clin Infect Dis 2000; 30: 633-8 25 Saby L et al.: Positron emission tomography/computed tomography for diagnosis of prosthetic valve endocarditis: increased valvular 18F-fluorodeoxyglucose uptake as a novel major criterion. J Am Coll Cardiol 2013; 61: 2374-82 26 Habib G et al.: Recommendations for the practice of echocardiography in infective endocarditis. Eur J Echocardiogr 2010; 11: 202-19 27 Müller H et al.: Subaortic aneurysm caused by Paecilomyces lilacinus endocarditis. Arch Cardiovasc Dis 2008; 101: 803-4 28 Feuchtner GM et al.: Multislice computed tomography in infective endocarditis: comparison with transesophageal echocardiography and intraoperative findings. J Am Coll Cardiol 2009; 53: 436-44 29 Fagman E et al.: ECG-gated computed tomography: a new role for patients with suspected aortic prosthetic valve endocarditis. Eur Radiol 2012; 22: 2407-14 30 Sifaoui I et al.: Diagnostic performance of transesophageal echocardiography and cardiac computed tomography in infective endocarditis. J Am Soc Echocardiogr 2020; 33: 1442-53 31 Chirillo F et al.: Impact of a multidisciplinary management strategy on the outcome of patients with native valve infective endocarditis. Am J Cardiol 2013; 112: 1171-6 32 Botelho-Nevers E et al.: Dramatic reduction in infective endocarditis-related mortality with a management-based approach. Arch Intern Med 2009; 169: 1290-8
Das könnte Sie auch interessieren:
Nouvelle option thérapeutique: zanubrutinib plus obinutuzumab
Le traitement combiné par zanubrutinib plus obinutuzumab promet de bons résultats dans le traitement du lymphome folliculaire. Il a fait l’objet de l’étude ROSEWOOD, qui est présentée ...
Points forts du congrès de l’ASH sur la LMA: les inhibiteurs de la ménine sont prometteurs
Lors du dernier congrès annuel de l’American Society of Hematology (ASH), d’innombrables données d’études passionnantes et porteuses d’espoir sur la leucémie myéloïde aiguë (LMA) ont été ...
Mise à jour lors de l’APCCC 2024
Depuis 2015, la Prof. Dre méd. Silke Gillessen et le PD Dr méd. Aurelius Omlin organisent tous les deux ans une conférence de consensus sur le cancer de la prostate avancé (APCCC) en ...